定制型颞下颌关节-下颌骨联合假体的临床初步应用
2020-11-30郑吉驷焦子先张善勇陈敏洁姜闻博
郑吉驷, 焦子先, 白 果, 张善勇, 陈敏洁, 姜闻博, 杨 驰
1.上海交通大学医学院附属第九人民医院·口腔医学院口腔外科,国家口腔疾病临床医学研究中心,上海市口腔医学重点实验室,上海市口腔医学研究所,上海200011;2.上海交通大学医学院附属第九人民医院3D 打印医学转化中心,上海200011
颞下颌关节(temporomandibular joint, TMJ)位于耳屏前,向上毗邻颅底,向下延伸至下颌升支和下颌体,是人体唯一的双侧联动关节,其结构精细、功能复杂,作用至关重要[1-2]。TMJ 疾病是一种常见病、多发病,多为TMJ 紊乱病、强直、骨折、关节肿瘤及类肿瘤等[3]。部分病变仅涉及TMJ,但范围大时也会累及下颌升支和下颌体[4-5]。与此同时,诸如下颌骨良恶性肿瘤、骨纤维性结构不良及类肿瘤病变等多种颌骨疾病,在造成下颌骨严重的骨质破坏的同时,也往往累及TMJ,进而导致TMJ 及颌骨严重的组织缺损和功能障碍[6-8]。对于上述2 种类型的患者,治疗时往往需彻底切除病变,从而造成大范围TMJ-下颌骨联合缺损,导致患者严重的咀嚼、语言、吞咽、呼吸等功能障碍及面部畸形,甚至危及生命。因此,对于大范围TMJ-下颌骨联合缺损的治疗重点,不仅要恢复下颌骨的连续性及面部外形,更重要的是重建病变的TMJ 和建立后期牙列修复的解剖基础。
对大范围TMJ-下颌骨联合缺损,目前修复重建主要有2 种方案—自体骨移植和假体重建,而前者是目前应用较多的方式。对于自体骨移植修复大范围TMJ-下颌骨联合缺损,目前主流方法多采用血管化或非血管化的髂骨、腓骨等进行修复[9-10]。该方法的主要优点在于技术已完备和成熟、手术操作相对固定。但其也存在诸多不可避免的劣势。其一,自体骨重建取骨量大、手术区多、创伤大;其二,充当髁突头的腓骨端不稳定,易脱位,导致面部和牙列的偏斜[11-12];其三,自体骨移植往往存在术后牙列修复骨量不足、垂直高度过低等劣势[13-15]。因此,假体重建相比自体骨移植创伤更小、疗效更稳定,是国际公认的发展趋势。其中,定制型假体根据个体不同的骨骼外形设计,具有术中无需大量磨骨、手术快捷、创伤小且精准等优点[16-20],逐步成为修复大范围TMJ-下颌骨联合缺损的发展趋势。目前对于TMJ-下颌骨联合假体,国内外几乎同时提出了TMJ-下颌骨延伸或联合假体设计概念,主要代表为TMJ Concepts 公司和上海交通大学医学院附属第九人民医院TMJ 团队[21-23]。TMJ Concepts 公司设计的TMJ-下颌骨延伸假体,可恢复下颌骨外形和连续性、TMJ 结构和功能,但无法进行后期牙列修复[21]。基于目前亟待解决的临床问题、丰富的颅颌面假体设计应用经验及可靠的前期力学试验基础,本团队设计研发了一款新型TMJ-下颌骨联合假体,除了能够有效恢复下颌骨外形和连续性、TMJ 结构和功能,假体内侧还配合自体骨移植,为后续的牙列修复提供了足够的骨组织基础[22-23]。
基于此,本研究初步总结自行研发的3D 打印定制型TMJ-下颌骨联合假体的设计制造过程,同时评估其临床初步应用的安全性、有效性和精准性。
1 资料与方法
1.1 病例资料
选择2016 年10 月—2019 年10 月就诊于上海交通大学医学院附属第九人民医院口腔外科的TMJ-下颌骨联合病变患者为临床试验对 象。排除标准:①对钛合金、钴铬钼合金以及超高分子聚乙烯内植物过敏者。②急性感染、严重感染或慢性感染处于急性发作期者。③ 合并心、肺、脑、肾等重要脏器原发性疾病未控制者。④妊娠、哺乳期女性。⑤中晚期恶性肿瘤、肿瘤远处转移、肿瘤复发患者。⑥严重免疫功能不全的患者[22-23]。
所有患者均告知需切除TMJ 和部分下颌骨,均同意使用3D 打印定制型TMJ-下颌骨联合假体,并签署临床试验知情同意书。研究经上海交通大学医学院附属第九人民医院伦理委员会批准(沪九院伦审[2015]18 号)。
1.2 TMJ-下颌骨联合假体的设计

图1 定制型TMJ-下颌骨联合假体设计Fig 1 Design of custom-made TMJ-mandible combined prosthesis
获取颌面部、髂骨或腓骨CT 影像,将数据导入Mimics 18.0 软件中,重建颅颌面三维模型(图1A);切除病变的髁突和下颌骨,必要时需切除部分关节结节(图1B);对于需切除部分牙列者,按照自体骨移植原则,模拟重建髂骨或腓骨修复下颌体部或部分升支(图1C);利用3-matic Medical 9.0 软件设计定制型TMJ-下颌骨联合假体,其主要包括关节窝假体、关节头假体和下颌假体(图1D)。关节窝假体能与颧弓外侧和关节窝个性化贴合,其上有5 ~7 个钉孔用于固定;关节窝假体和关节头假体形成关节运动功能面,用于恢复关节运动功能;下颌假体又分为升支部和体部,分别用于恢复下颌升支和体部的完整性和连续性,其内侧能与移植的自体骨(髂骨或腓骨)个性化贴合,体部前端与正常下颌骨下端表面个性化贴合,其上有6 ~10 个钉孔用于固定[22-23]。
1.3 TMJ-下颌骨联合假体的制作
TMJ-下颌骨联合假体各部件所选的医用材料主要包括钛合金(Ti6Al4V alloy,GB/T13810)、超高分子聚乙烯(UHMWP,GB/T19701.2)和钴铬钼合金(Co-Cr-Mo alloy,YY0117.3)。关节窝假体选用UHMWP,关节头假体选用Co-Cr-Mo 合金,两者均利用五轴精加工机器(DMU60,DGM,德国)制作而成;下颌假体选用Ti6Al4V 合金,通过金属3D 打印机器(Arcam A1,MÖlnda,瑞典)加工而成。关节头假体和下颌假体通过莫氏锥度牢固结合(图2A)。下颌假体与骨接触的内侧面利用喷砂技术进行表面粗糙化处理,利于假体和骨形成良好的骨整合。完成联合假体制作后,对假体进行静态力学、疲劳和磨损试验,其需满足以下条件:①静态力学测试 中最大受力不低于2 500 N。②磨损测试中负载497 ~0 N,12 Hz 为周期,循环1 000 万次,在荧光透视中未见明显 失败和裂隙,经荧光渗透检验下表面不得有不连续缺陷。③磨损测试中在牛血清中以持续9 kg 负载循环500万圈,其平均渗透性和体积磨损率每100 万圈分别不低于0.01 mm。力学检测合格后需要在头模上试装,观察假体就位是否顺利、与骨贴合是否紧密,关节窝和关节头相对位置是否正确以及固定是否牢固(图2B)。试装成功后,将假体各部件进行消毒和包装,其UHMWP 的关节窝假体利用环氧乙烷消毒;Co-Cr-Mo 合金的关节头假体和Ti6Al4V 合金的下颌假体选用高温高压消毒,并通过生物检测合格后备用[22-23]。

图2 定制型TMJ-下颌骨联合假体的制造和试装Fig 2 Manufacture of TMJ-mandible combined prosthesis and simulation in skull model
1.4 手术方法
患者常规鼻腔插管全身麻醉,采用改良耳前、颌后、颌下切口入路,分别显露关节、下颌升支及下颌体。利用导板定位截骨,完成肿瘤、关节及部分下颌骨的完整切除;若病变为良性,可进行分块切除,保留下牙槽神经血管束(图3)。病变完整切除后,封闭切口进行口内颌间结扎。重新消毒、铺巾,植入关节窝假体,使其稳定地贴合关节窝和颧弓的骨性解剖结构,并以5 ~6 枚钛钉固定(图4A)。再放入下颌假体,当下颌假体内侧面稳定地贴合在下颌体下端表面,关节头假体位于关节窝假体的后中位置,以及关节头和关节窝假体形成良好且稳定的接触,以5 ~6 枚钛钉固定下颌假体(图4B)。取髂骨或腓骨,分块贴合移植于联合假体内侧面,并以2 ~3 枚钛钉/块固定移植骨(若为带蒂骨瓣,还需吻合血管)(图4C)。取颊脂垫或腹部脂肪,填塞假体周围死腔(图4D)。打开颌间结扎并检查咬合关系良好后,重新消毒、铺巾,严密分层缝合口内外创面,留置负压[22-23]。
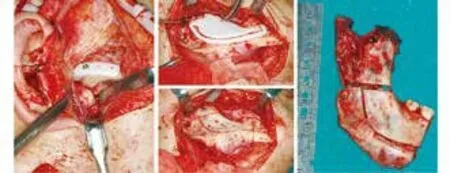
图3 TMJ-下颌骨联合切除步骤Fig 3 Surgical procedure of TMJ-mandible combined resection
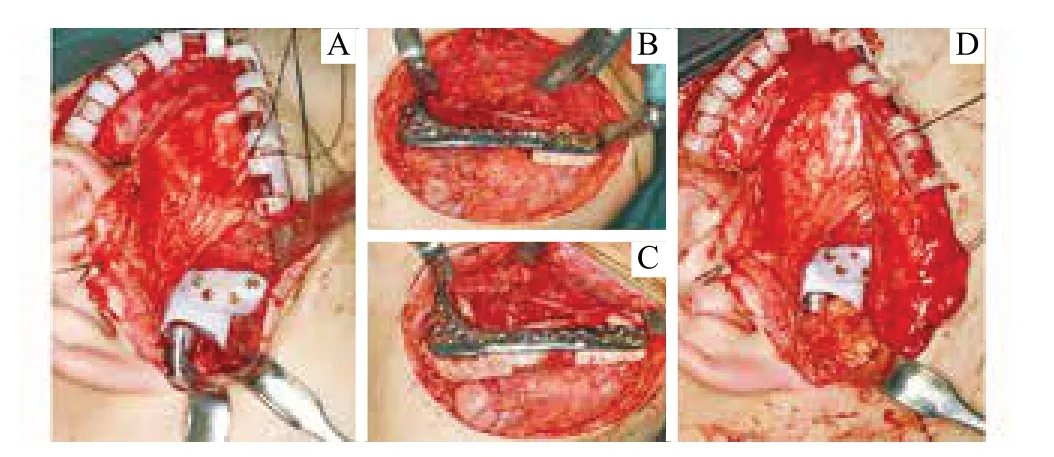
图4 TMJ-下颌骨联合假体的安装步骤Fig 4 Surgical procedure of TMJ-mandible combined fixation
1.5 效果评价
术中观察假体能否顺利就位及与骨面贴合情况。术后采用视觉模拟评分法(visual analogue scale, VAS)评价张口度、疼痛、饮食及下颌运动功能等指标[22]。术后拍摄X线片(全景片,正侧位片)观察假体是否移位、松动、断裂,关节周围是否有异位骨化、关节强直等不良反应发生。术后拍摄颌面部CT,数据导入Mimics 18.0 软件后,分离关节头、关节窝和下颌假体,再次导入关节窝假体,利用固位螺钉的位置,确定关节窝假体的术后位置,分别匹配并拟合术后实际和术前设计的关节头、关节窝和下颌假体位置,对各部件进行色谱分析,计算其植入的平均误 差[22-23]。
1.6 统计学分析
采用SPSS 17.0 软件进行统计学分析。所有数据均测量2 次。定量资料以x±s 表示。数据比较采用配对t 检验,P<0.05 表示差异具有统计学意义。
2 结果
2.1 患者基本情况
共计入组6 例患者,男、女各3 例,平均年龄(34.3±13.9)岁;2 例右侧病变,4 例左侧病变;2 例为成釉细胞瘤,1 例为髁突软骨肉瘤,1 例为滑膜软骨瘤病,1 例为骨性强直术后,1 例为巨细胞病变;平均随访(22.5±17.9)个月(其中最长48 个月,最短8 个月)。患者基本信息见表1。

表1 患者基本信息 Tab 1 Basic information of the patients
2.2 手术情况
6 例患者中,1 例截骨至对侧颏部和颏孔间、2 例至同侧下颌角和颏孔间、3 例至同侧下颌孔和下颌角间。2例涉及牙列缺损,同期利用游离髂骨和带蒂腓骨肌皮瓣修复(表1)。除1 例软骨肉瘤未保存下牙槽神经血管束外,其余5 例均得到有效保存。术中假体均就位顺利,且与关节窝、颧弓、移植骨、下颌骨下端骨面均贴合良好。关节头假体均位于关节窝假体的后中部,且接触良好。术后X线片均未见异位骨化、关节强直表现,未见假体移位、松动、断裂。术中和术后咬合关系均稳定(图5)。
2.3 临床效果评价
6例患者术前疼痛VAS评分为7.3±1.8,术后为1.7± 0.8 术前张口度为(13.3±9.1)mm,术后为(31.0± 6.8)mm 术前下颌运动功能评分为6.3±2.1,术后为2.3± 1.4;术前饮食评分为7.2±1.9,术后为2.7±1.4。上述指标术前与术后的差异均有统计学意义(均P=0.000)。

图5 术前和术后面型对比及术后X-ray 和CT 重建Fig 5 Comparison of pre and post clinical examinations and postoperative X-ray and CT reconstruction
2.4 影像学评价
术前设计和术后实际效果拟合结果显示,关节窝假体植入的平均误差为(0.891±0.127)mm,下颌假体植入的平均误差为(1.240±0.246)mm,总体平均误差为(1.122±0.198)mm(图6)。

图6 联合假体植入位置精度分析Fig 6 Accuracy analysis of TMJ-mandible combined prosthesis
3 讨论
定制型人工关节假体,需按照骨骼结构和运动特征进行个性化设计,是目前骨和关节重建的主要趋势。定制型TMJ 假体最早由美国TMJ Concepts 公司推出,并得到国际认可和应用[17]。上海交通大学医学院附属第九人民医院TMJ 团队自2009 年开始研发TMJ 假体,目前拥有了较成熟的定制型TMJ 假体产品,临床初步应用获得良好的效果[22-23]。但对TMJ 和下颌骨大范围病变,常规定制型TMJ假体无法对其进行修复[21]。针对这一问题,TMJ Concepts公司和上海交通大学医学院附属第九人民医院TMJ 团队几乎同时设计制造了TMJ-下颌骨延伸或联合假体,为TMJ、下颌升支、下颌体,甚至涉及对侧的TMJ-下颌骨联合病变提供了一种新的治疗方案。
TMJ Concepts 公司和上海交通大学医学院附属第九人民医院TMJ 团队设计的TMJ-下颌骨延伸或联合假体有显著的差异。在设计理念上,前者关节窝假体由钛网和超高分子聚乙烯共同连接而成,后者为纯超高分子聚乙烯材质[17];前者下颌假体内侧面不结合自体骨,对涉及牙列缺损的病例,无法进行后期种植牙列修复;后者下颌假体内侧让出自体骨空间,且能与自体骨个性化贴合和固定,使后期种植修复成为可能。在制作方法上,前者利用五轴精加工和锻造技术制作假体各部件[17,21];后者对于不同部件采用不同加工方法,对于关节窝和关节头假体利用五轴精加工,下颌假体采用增材制造技术,缩短假体制作时间,节省假体制备材料。在手术方法上,前者切除病变后,植入假体即完成手术[17];后者必要时还要制备自体骨并进行移植,且术后还需进行种植牙列修复,手术步骤稍复杂,但能同期恢复TMJ 结构和功能,保证下颌骨连续性及牙列完整性,达到关节-颌骨-咬合联合治疗的目的。
对于临床应用效果,TMJ Concepts 公司的TMJ-下颌骨延伸假体仅为案例报道,无完整的随访数据。上海交通大学医学院附属第九人民医院研发的TMJ-下颌骨联合假体连续应用6 例患者,并对其假体设计、制造、手术方案、临床安全性和有效性、假体植入精确度进行了系统性评价。从随访结果可以看出,该假体对大范围TMJ-下颌骨联合缺损的修复具有较好的治疗效果,术后的疼痛、张口度、饮食、下颌运动功能得到明显改善,术后面型、咬合关系等得到有效保持,同时假体植入精度仅在1.122 mm 左右。可见,通过数字医学、3D 打印等新技术,结合精准医学、关节-颌骨-咬合联合重建等新理念,可达到颅颌面骨及关节的高效修复和精准重建。本研究后续将扩大样本量和延长随访时间,进一步验证TMJ-下颌骨联合假体临床应用的可行性[22]。
综上所述,该3D 打印定制型TMJ-下颌骨联合假体设计上与国外同类的产品有明显的区别,在加工方面结合新型的3D 打印技术,在治疗方面达到关节-颌骨-咬合联合重建的目的,临床应用安全、有效、精准,为后期国内大范围应用和推广奠定基础。
参·考·文·献
[1] Guarda-Nardini L, Manfredini D, Ferronato G. Temporomandibular joint total replacement prosthesis: current knowledge and considerations for the future[J]. Int J Oral Maxillofac Surg, 2008, 37(2): 103-110.
[2] Sidebottom AJ. Guidelines for the replacement of temporomandibular joints in the United Kingdom[J]. Br J Oral Maxillofac Surg, 2008, 46(2): 146-147.
[3] Shen Y, Ma CY, Wang L, et al. Surgical management of giant cell tumors in temporomandibular joint region involving lateral skull base: a multidisciplinary approach[J]. J Oral Maxillofac Surg, 2016, 74(11): 2295-2311.
[4] Oukabli M, Chibani M, Ennouali H, et al. Pseudotumeurs et tumeurs primitives de l'articulation temporomandibulaire[J]. Revue De Stomatol De Chir Maxillo - Faciale et De Chir Orale, 2013, 114(1): 9-14.
[5] Tiftikcioglu YO, Gur E, Bilkay U. Simultaneous autologus mandible and temporomandibular joint reconstruction[J]. J Craniofac Surg, 2017, 28(4): e374-e376.
[6] Ruiz Valero CA, Duran-Rodriguez G, Solano-Parra N, et al. Immediate total temporomandibular joint replacement with TMJ concepts prosthesis as an alternative for ameloblastoma cases[J]. J Oral Maxillofac Surg, 2014, 72(3): 646.e1-646.e12.
[7] Kumar BP, Venkatesh V, Kumar KAJ, et al. Mandibular reconstruction: overview[J]. J Maxillofac Oral Surg, 2016, 15(4): 425-441.
[8] Johnson NR, Roberts MJ, Doi SA, et al. Total temporomandibular joint replacement prostheses: a systematic review and bias-adjusted meta-analysis[J]. Int J Oral Maxillofac Surg, 2017, 46(1): 86-92.
[9] Vittayakittipong P, Jarudejkajon J, Kirirat P, et al. Feasibility of the vascularized fibula bone graft for reconstruction of the mandible: a cadaveric study[J]. Int J Oral Maxillofac Surg, 2016, 45(8): 960-963.
[10] Ghassemi A, Schreiber L, Prescher A, et al. Regions of ilium and fibula providing clinically usable bone for mandible reconstruction: “a different approach to bone comparison”[J]. Clin Anat, 2016, 29(6): 773-778.
[11] Wang W, Shan XF, Liang J, et al. Changes in condylar position after mandibular reconstruction with condylar head preservation by computed tomography[J]. J Oral Maxillofac Surg, 2019, 77(6): 1286-1292.
[12] Kang SH, Lee S, Nam W. Condyle dislocation following mandibular reconstruction using a fibula free flap: complication cases[J]. Maxillofac Plast Reconstr Surg, 2019, 41(1): 1-10.
[13] Ferri J, Piot B, Ruhin B, et al. Advantages and limitations of the fibula free flap in mandibular reconstruction[J]. J Oral Maxillofacial Surgery, 1997, 55(5): 440-448.
[14] Ishii N, Shimizu Y, Ihara J, et al. Analysis of fibular single graft and fibular double-barrel graft for mandibular reconstruction[J]. Plast Reconstr Surg Glob Open, 2016, 4(8): e1018.
[15] Wang W, Zhu J, Xu B, et al. Reconstruction of mandibular defects using vascularized fibular osteomyocutaneous flap combined with nonvascularized fibular flap[J]. Med Oral Patol Oral Cir Bucal, 2019, 24(5): e691-e697.
[16] Westermark A. Total reconstruction of the temporomandibular joint. Up to 8 years of follow-up of patients treated with Biomet®total joint prostheses[J]. Int J Oral Maxillofac Surg, 2010, 39(10): 951-955.
[17] Mercuri LG. Alloplastic temporomandibular joint replacement: rationale for the use of custom devices[J]. Int J Oral Maxillofac Surg, 2012, 41(9): 1033-1040.
[18] Zhang SY, Liu H, Yang C, et al. Modified surgical techniques for total alloplastic temporomandibular joint replacement: one institution's experience[J]. J Cranio-Maxillo-Facial Surg, 2015, 43(6): 934-939.
[19] Bai G, He DM, Yang C, et al. Application of digital templates to guide total alloplastic joint replacement surgery with biomet standard replacement system[J]. J Oral Maxillofac Surg, 2014, 72(12): 2440-2452.
[20] Onoriobe U, Miloro M, Sukotjo C, et al. How many temporomandibular joint total joint alloplastic implants will be placed in the United States in 2030?[J]. J Oral Maxillofac Surg, 2016, 74(8): 1531-1538.
[21] Elledge R, Mercuri LG, Speculand B. Extended total temporomandibular joint replacements: a classification system[J]. Br J Oral Maxillofac Surg, 2018, 56(7): 578-581.
[22] Zheng JS, Chen XZ, Jiang WB, et al. An innovative total temporomandibular joint prosthesis with customized design and 3D printing additive fabrication: a prospective clinical study[J]. J Transl Med, 2019, 17(1): 4.
[23] Zheng JS, Liu XH, Chen XZ, et al. Customized skull base-temporomandibular joint combined prosthesis with 3D-printing fabrication for craniomaxillofacial reconstruction: a preliminary study[J]. Int J Oral Maxillofac Surg, 2019, 48(11): 1440-1447.
