西妥昔单抗与FOLFIRI化疗联合治疗晚期结肠癌的效果
2020-11-25宋延海
宋延海
(丹东市第一医院肿瘤内科,辽宁 丹东 118000)
结肠癌是结肠部位常见的恶性肿瘤,多见于乙状结肠与直肠的交汇处,其发病率在胃肠系统肿瘤中居第三位,包括未分化癌、黏液腺癌、腺癌,形态呈溃疡型与息肉状[1]。由于早期结肠癌的症状表现不具备典型性,多数患者就诊时已是中晚期,早已错失治疗的最佳时机,主要采用化疗方案杀灭癌细胞,延长生存周期[2]。然而,部分研究发现,单纯化疗治疗晚期结肠癌的疗效有所欠缺,加之化疗周期长、不良反应强,进一步影响了患者的生存质量[3-4]。因此,探寻一种疗效可靠且安全性佳的药物联合化疗强化整体治疗效果,对于晚期结肠癌患者而言具有十分重要的意义。西妥昔单抗是一种新型的生物靶向药物,属于表皮生长因子受体抑制剂,对于表达表皮生长因子的恶性肿瘤细胞具有阻断作用。2015年1月至2017年12月,我院为45例晚期结肠癌患者在常规FOLFIRI[伊立替康(irinotecan,CPT-11)+5-氟尿嘧啶(5-fluorouracil,5-FU)+亚叶酸钙(leucovorin,LV)]化疗的基础上应用了西妥昔单抗治疗,对其治疗效果进行研究,报道如下。
1 资料与方法
1.1 一般资料 90例晚期结肠癌患者均于丹东市第一医院接受治疗,时机为2015年1月至2017年12月。90例研究对象以随机数表法划分为对照组(n=45)与研究组(n=45)。对照组:男性、女性患者分别为27例、18例;年龄最小32岁,最大75岁,平均年龄(53.5±4.8)岁;Dukes分期为C期15例,D期30例;病理类型为中分化腺癌25例,高分化腺癌10例,低分化腺癌8例,黏液腺癌2例。研究组:男性、女性患者分别为28例、17例;年龄最小35岁,最大74岁,平均年龄(53.8±4.5)岁;Dukes分期为C期17例,D期28例;病理类型为中分化腺癌24例,高分化腺癌11例,低分化腺癌7例,黏液腺癌3例。两组患者性别、年龄、Dukes分期、病理类型等一般资料经SPSS20.0统计软件比较,两组无明显差异(P>0.05),具有可比性。
1.2 纳入与排除标准 纳入标准:经病理检查证实为结肠癌;V-Kiras2鼠Kirsten肉瘤病毒致癌基因同源物(KRAS)基因突变阴性者;Dukes分期为C期(其中C1期为存在区域淋巴结转移,但未见肠系膜血管淋巴结转移;C2期为存在肠系膜血管旁淋巴结转移)与D期(有腹腔转移或远处转移,或广泛浸润不能切除者);预计生存期>3个月;Karnofsky功能状态评分标准≥60分;患者具有良好的沟通与认知能力;患者及其家属已了解本次研究方案,签署了知情同意书。排除标准:血液系统与免疫系统疾病者;其他脏器功能严重障碍或异常者;意识障碍或伴有精神疾病史者。
1.3 方法 两组患者均采取FOLFIRI化疗方法治疗,具体方案:第1天静脉滴注180 mg/m2伊立替康(由海南锦瑞制药有限公司名生产,国药准字H20143125),400 mg/m2的5氟尿嘧啶(上海旭东海普药业有限公司生产国药准字H31020593),200 mg/m2亚叶酸钙(山东罗欣药业集团股份有限公司,国药准字H20054300);之后400 mg/m2的5氟尿嘧啶持续泵入46 h。在此基础上,研究组患者应用西妥昔单抗(由德国默克里昂制药公司生产,国药准字S20130004)治疗,具体方案:用药前0.5 h肌内注射25 mg盐酸异丙嗪,静脉推注5 mg的地塞米松,首次静脉滴注400 mg/m2西妥昔单抗,时间为120 min,之后降至每周使用量为250 mg/m2,时间为60 min,治疗期间密切给予心电监护。1个化疗周期为14 d。
1.4 观察指标 ①根据实体瘤疗效标准(RECIST)1.1版对比两组患者的化疗治疗效果。②比较两组患者治疗期间的不良反应情况,观察指标包括白细胞减少、血小板减少、恶心呕吐、皮疹、肝功能损伤。
1.5 统计学处理 研究中涉及的数据资料均以SPSS20.0软件进行处理,其中临床疗效、不良反应计数资料以例数(n)、百分率(%)表示,结果行χ2检验;检验水准α=0.05。
2 结果
2.1 两组晚期结肠癌患者的临床疗效比较 两组晚期结肠癌患者的临床疗效比较中,研究组总有效率为53.33%,比对照组的31.11%更高,结果比较差异具有统计学意义(P<0.05)。见表1。
2.2 两组晚期结肠癌患者治疗期间的不良反应比较 两组晚期结肠癌患者治疗期间白细胞减少、血小板减少、恶心呕吐、皮疹、肝功能损伤的发生率对比差异无统计学意义(P>0.05)。见表2。
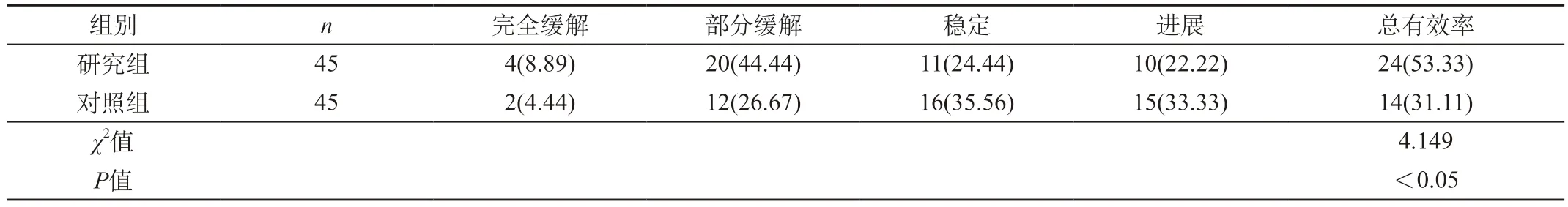
表1 两组晚期结肠癌患者的临床疗效比较[n(%)]
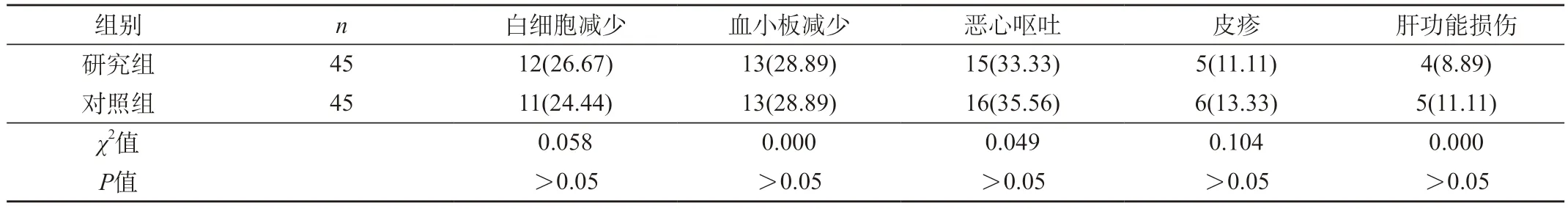
表2 两组晚期结肠癌患者治疗期间的不良反应比较[n(%)]
3 讨论
近年来,结肠癌的发病率也不断攀升,且向年轻化群体扩增,与人们生活方式与饮食结构的变化息息相关[5]。由于早期结肠癌缺乏典型性的症状表现,所以多数患者就诊时已步入晚期,此时主要以化疗方案进行治疗,然而一旦治疗不及时、无效便会影响患者的生存时间[6]。FOLFIRI化疗是治疗晚期结肠癌的常用方案之一,但因该方案不良反应多,加之化疗药物耐药性不断增加等原因,致使整体收效不够理想[7]。
部分研究发现,约75.00%的晚期结肠癌患者表皮生长因子呈高水平表达,表皮生长因子是人表皮受体家族中的重要组成部分,与癌细胞的扩散、侵袭、肿瘤血生成等因素具有密切的相关性,其水平升高往往提示预后不良[8]。因此,采取有效的药物阻断表皮生长因子与相关信号传导通路,有效抑制癌细胞侵袭、增殖、播散与新生血管形成十分必要。目前,表皮生长因子是成为肿瘤治疗的重要靶点,西妥昔单抗作为表皮生长因子特异性抑制剂,现已被美国国立综合癌症网络指南纳入到晚期结肠癌的一线治疗药物中[9]。西妥昔单抗可单独使用,也可以与化疗方案联合使用,该药能够结合于体内正常细胞、多种癌细胞人表皮生长因子胞外激酶,对表皮生长因子与相关配体进行竞争性抑制,继而阻断受体有关的激酶磷酸化作用,切断细胞内部信息传递,控制癌细胞增长,并使其凋亡,最终达到理想的治疗效果[10]。本文研究结果显示,两组晚期结肠癌患者的临床疗效比较中,研究组总有效率比对照组更高(P<0.05)。可见,在常规FOLFIRI化疗的基础上应用西妥昔单抗,能够有效提高患者的临床疗效,是治疗晚期结肠癌的新突破。从药物安全性来看,西妥昔单抗在国内属于推广阶段,其药物安全性备受临床机构的关注。一些报道发现,该药所致的不良反应不具有特异性,通常为腹泻、白细胞减少、发热等,偶尔可见过敏反应,但症状较为轻微[11-12]。本文中两组晚期结肠癌患者治疗期间白细胞减少、血小板减少、恶心呕吐、皮疹、肝功能损伤的发生率对比差异无统计学意义(P>0.05)。结果说明,联合应用西妥昔单抗并未增加治疗的不良反应,安全性尚可。
总之,西妥昔单抗与FOLFIRI化疗联合治疗晚期结肠癌疗效确切,且不会增加不良反应,值得临床推广。
