替诺福韦与恩替卡韦治疗HBeAg阳性初治慢性乙型肝炎患者的临床效果
2020-11-25王增伟
王增伟
(新沂市人民医院,江苏 新沂 221400)
人体在感染乙型肝炎病毒后可引起乙型肝炎,若不能快速且彻底地将乙型肝炎病毒清除,随着时间的延长可发展为慢性乙型肝炎。慢性乙型肝炎是目前临床最常见的传染性疾病,如果不能快速控制病情,随着病情的发展会进一步恶化为肝硬化或者肝癌。目前,临床主要采取抗病毒方法治疗慢性乙型肝炎,抗病毒药物可及时将乙型肝炎病毒清除,进而消除病毒大量繁殖对肝功能造成的影响[1]。替诺福韦、恩替卡韦均属于抗病毒治疗药物。临床关于上述两种药物对慢性乙型肝炎治疗的相关研究较少。本研究旨在探讨替诺福韦与恩替卡韦治疗乙型肝炎e抗原(HBeAg)阳性初治慢性乙型肝炎患者的临床效果。
1 资料与方法
1.1 一般资料 研究对象为2016年2月至2019年1月新沂市人民医院收治的60例HBeAg阳性初治慢性乙型肝炎患者,根据入院先后顺序分为对照组与观察组,每组30例。观察组男性21例,女性9例;年龄25~73岁,平均(45.92±5.04)岁;入院时HBV-DNA为(7.51±0.87)IgIU/mL,丙氨酸氨基转移酶(ALT)为(164.96±125.01)U/L。对照组男性19例,女性11例;年龄22~75岁,平均(45.90±5.06)岁;入院时HBVDNA为(7.45±0.89)IgIU/mL,ALT为(169.06±125.24)U/L。两组上述一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经经医院伦理委员会批准通过。
1.2 纳入标准与排除标准 纳入标准:①根据中国病毒性肝炎及肝病学术会议制定的《中国慢性乙型病毒性肝炎防治指南》中慢性乙型肝炎肝炎的诊断标准确诊[2];②有完整的随访资料;③有良好的用药依从性;④HBeAg阳性持续时间>6个月;⑤HBV-DNA定量检查显示超过20 IU/mL;⑥血清ALT存在异常升高;⑦患者知情并签署知情同意书。排除标准:①慢性乙型肝炎已经进展为肝硬化或者肝癌者;②严重心、肺、肾功能不全者;③合并多种肝炎病毒感染类型者;④认知功能障碍或者精神异常者;⑤妊娠期、哺乳期妇女;⑥合并高血压、糖尿病等基础疾病者。
1.3 方法 对所有患者实施常规保肝治疗、对症支持治疗。在此基础上,对照组予以恩替卡韦(中美上海施贵宝制药有限公司,国药准字H20052237)治疗,每次0.5 mg,每日1次,连续用药3个月。观察组予以替诺福韦酯(成都市倍特药业有限公司,国药准字H20163436)治疗,每次300 mg,每日1次,连续治疗3个月。所有患者在治疗期间均做好健康指导与护理指导。在患者治疗后1、3个月测定乙型肝炎功能以及乙型肝炎病毒相关指标,并做好数据记录。
1.4 观察指标 ①比较治疗后1、3个月两组患者的HBV-DNA转阴率,HBV-DNA检测下限为1×103copies/mL,以<500 copies/mL为阴性;②比较治疗后1、3个月两组患者的血清HBV-DNA水平;③比较治疗后1、3个月两组患者的ALT复常情况,ALT复常的标准是ALT≤40 IU/L;④比较治疗后1、3个月两组患者的HBeAg血清学应答率,HBeAg血清学应答的标准是S/CO≥1为阳性;⑤统计两组患者的用药不良反应。
1.5 统计学方法 采用SPSS 21.0统计学软件对数据进行分析。血清HBV-DNA水平、ALT复常情况等计量资料采用()表示,组间比较行t检验;HBV-DNA转阴率、HBeAg血清学应答率等计数资料采用[n(%)]表示,组间比较行χ2检验;P<0.05表示差异有统计学意义。
2 结果
2.1 不同时间段两组患者的HBV-DNA转阴率比较 治疗后1个月,观察组HBV-DNA转阴率为10.00%(3/30),对照组HBV-DNA转阴率为6.67%(2/30),组间差异无统计学意义(χ2=0.218,P=0.640)。治疗后3个月,观察组HBV-DNA转阴率为40.00%(12/30),对照组HBVDNA转阴率为16.67%(5/30),组间差异有统计学意义(χ2=4.021,P=0.044)。
2.2 不同时间段两组患者的血清HBV-DNA水平比较 与治疗前相比,两组患者治疗后1、3个月的血清HBV-DNA水平均明显下降,差异均有统计学意义(均P<0.05);在治疗后1、3个月,观察组血清HBVDNA水平低于对照组,差异均有统计学意义(均P<0.05)。见表1。
表1 不同时间两组患者的血清HBV-DNA水平比较(IgIU/mL,)
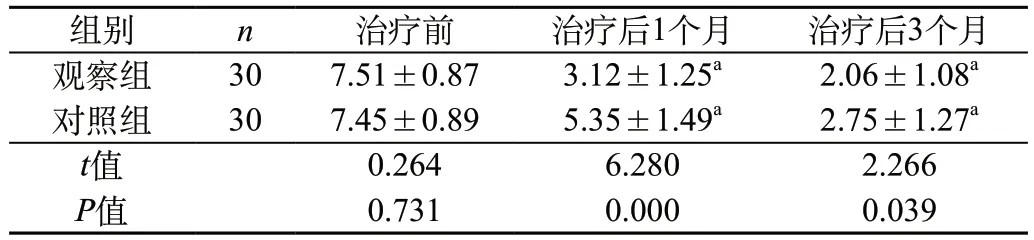
表1 不同时间两组患者的血清HBV-DNA水平比较(IgIU/mL,)
注:a表示治疗前后比较,P<0.05。
2.3 不同时间段两组患者ALT复常情况比较 与治疗前相比,两组患者治疗后1、3个月的血清ALT水平明显下降,且观察组ALT水平低于对照组,差异均有统计学意义(均P<0.05)。见表2。
表2 不同时间段两组患者ALT复常情况比较(U/L,)
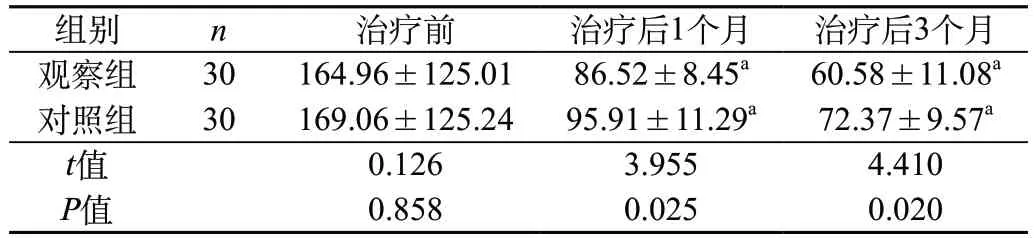
表2 不同时间段两组患者ALT复常情况比较(U/L,)
注:a表示治疗前后比较,P<0.05。
2.4 不同时间段两组患者HBeAg血清学应答率比较 两组患者治疗后1、3个月的HBeAg血清学应答率比较,差异无统计学意义(P>0.05)。见表3。
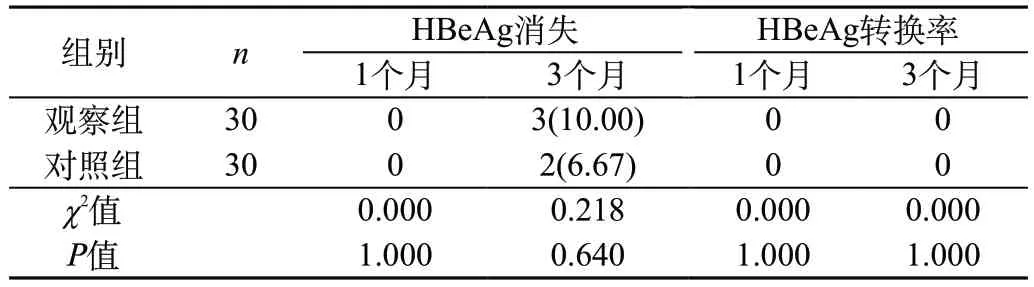
表3 不同时间段两组患者HBeAg血清学应答率比较[n(%)]
2.5 两组治疗期间不良反应发生情况 两组患者均严格遵医嘱用药,配合有效护理干预,治疗期间均无不良反应发生,总体治疗安全性较高。
3 讨 论
慢性乙型肝炎属于临床常见的传染性疾病,也是严重危害公众健康的疾病之一。随着社会公共卫生事业的不断发展与科教宣传的普及,人们逐渐了解乙型肝炎的传染途径,并养成了良好的卫生习惯。此外,通过接种乙型肝炎疫苗也能够预防乙型肝炎[3]。虽然采取了较多的乙型肝炎防控措施,但是我国每年因为慢性乙型肝炎引起的肝硬化、肝癌患者仍然较多,因此重视慢性乙型肝炎患者的初治研究对延缓病情发展、避免疾病的传播具有重要意义。
由于乙型肝炎病毒是引起乙型慢性肝炎的主要原因,故临床主要采取抗病毒的治疗方法。通过抗病毒治疗抑制患者体内乙型肝炎病毒的持续繁殖,消除乙型肝炎病毒对患者肝脏功能与结构的影响,进而帮助患者控制病情[4]。目前,临床治疗慢性乙型肝炎患者的一线抗病毒药物主要有替诺福韦与恩替卡韦。恩替卡韦为核苷类抗病毒药物,其总体抗病毒作用较强,且耐药性较低,患者长时间用药的安全性较高,因而在慢性乙型肝炎治疗中的应用较多。有研究指出,恩替卡韦有助于改善患者的肝功能指标,避免乙型肝炎病毒对肝功能造成更大的影响[5]。替诺福韦属于新型核苷酸类逆转录酶抑制剂,现代医学研究显示,该药物能够对多种病毒发挥作用,通过对病毒逆转录酶活性的抑制达到抑制病毒复制的作用,在多种病毒感染疾病治疗中均有应用,同时适用于慢性乙型肝炎的治疗[6]。
本研究结果显示,治疗后3个月,研究组HBV-DNA转阴率高于对照组(P<0.05),表明替诺福韦能够促进HBV-DNA转阴,有效抑制乙型肝炎病毒毒性,减少疾病的传播,且可减轻病毒对肝功能的影响;治疗后1、3个月,观察组血清HBV-DNA水平低于对照组(均P<0.05),提示替诺福韦对乙型肝炎病毒的抑制效果更明显[7]。ALT属于存在肝细胞中的一种酶,当肝细胞出现损害后会引起血液中ALT水平升高,因而通过测定ALT水平可评估患者的肝功能损伤情况。两组患者采用不同药物治疗后1、3个月,观察组ALT水平低于对照组(均P<0.05),说明替诺福韦对慢性乙型肝炎的治疗效果更明显,能够抑制病毒对肝功能造成的损伤。两组患者在治疗期间的HBeAg血清学应答率比较,差异无统计学意义(P>0.05),考虑可能与随访时间较短有关[8]。此外,两组患者治疗期间均无不良反应发生,显示出两种药物在抗病毒方面均有良好的安全性。相关研究亦指出,恩替卡韦较替诺福韦对乙型肝炎肝硬化治疗效果更好,能够帮助患者改善肝功能[9]。由此可见,替诺福韦较恩替卡韦对HBeAg阳性初治慢性乙型肝炎患者的治疗效果更好,能够较好的抑制乙型肝炎病毒[10]。
综上所述,替诺福韦与恩替卡韦都可用于HBeAg阳性初治慢性乙型肝炎患者的临床治疗中,但替诺福韦能够兼顾用药有效性与安全性,可作为首选治疗药物。
