奥曲肽联合凝血酶治疗肝硬化合并上消化道出血患者的临床疗效
2020-11-25邢凤媛
邢凤媛
(沈阳市红十字会医院,辽宁 沈阳 110003)
上消化道出血和肝硬化都是临床常见的疾病,而肝硬化患者由于肝功能的衰退,门静脉高压也逐渐减退,因此极易并发上消化道出血,若不及时接受治疗,患者会出现缺血休克,甚至导致死亡,严重影响患者的生命健康和生存质量[1]。本研究探讨对我院2017年5月至2019年5月收治的54例肝硬化合并上消化道出血患者使用奥曲肽联合凝血酶治疗的临床疗效。报道如下。
1 资料与方法
1.1 一般资料 选择我院2017年5月至2019年5月收治的54例肝硬化合并上消化道出血的患者,随机分为研究组和对照组,各27例。研究组患者中女性12例,男性15例;年龄40~75岁,平均年龄(60.36±14.18)岁;出血量500~1500 mL,平均出血量(896.68±256.84)mL;病程12~24个月,平均病程(19.64±2.15)个月。对照组患者中女性16例,男性11例;年龄40~80岁,平均年龄(62.08±14.99)岁;出血量500~1500 mL,平均出血量(908.64±2.64)mL;病程12~24个月,平均病程(20.27±2.35)个月。两组患者的性别、年龄、出血量、病程等一般资料比较差异无统计学意义(P>0.05)。本次研究中的所有患者及其家属均已经签署了知情同意书,我院的伦理委员会也批准了本次试验。
1.2 纳入和排除标准 纳入标准:所有患者均符合肝硬化合并上消化道出血的诊断标准,大便的潜血试验结果为阳性,并配合本次研究[2]。排除标准:存在药物过敏史,肝肾等器官严重功能障碍,凝血功能障碍,恶性肿瘤,严重精神性疾病,不配合本次研究[3]。
1.3 方法 所有患者均接受常规基础治疗,包括:建立静脉通道,给予基础抗感染、输血补血等治疗。
1.3.1 研究组 在此基础上使用奥曲肽联合凝血酶治疗[4]。静脉滴注奥曲肽(北京百奥药业有限责任公司,国药准字H20061309),最适剂量为每日0.2~0.3 mg,最大剂量≤每日1.5 mg,可用0.9%氯化钠溶液或葡萄糖溶液稀释,若生长激素浓度未下降、临床症状未改善,则应考虑停药。口服或局部灌注凝血酶(上海长城药业有限公司,国药准字H 31022822),用0.9%氯化钠溶液或温开水(≤37 ℃)溶解成每毫升10~100单位的溶液,也可根据出血部位及程度增减浓度、次数。
1.3.2 对照组 在此基础上使用奥曲肽治疗。静脉滴注奥曲肽(北京百奥药业有限责任公司,国药准字H20061309),最适剂量为每日0.2~0.3 mg,最大剂量≤每日1.5 mg,可用0.9%氯化钠溶液或葡萄糖溶液稀释,若生长激素浓度未下降、临床症状未改善,则应考虑停药。
1.4 观察指标及判定标准
1.4.1 临床疗效 疗效判定标准[5]:显效:患者经治疗后临床症状消失,大便的潜血试验结果为阴性,血常规恢复正常,其他临床指标也恢复正常;改善:患者经治疗后临床症状改善,大便的潜血试验结果为阴性,血常规得到改善,其他临床指标也得到改善;无效:患者经治疗后临床症状未改变甚至加重,大便的潜血试验结果为阳性,血常规未恢复,其他临床指标也未改变甚至加重。
1.4.2 治疗后肝功能指标 包括天冬氨酸转氨酶(aspartate aminotransferase,AST)、丙氨酸转氨酶(alanine aminotransferase,ALT)、碱性磷酸酶(alkaline phosphatase,ALP)、谷氨酞转移酶(gamma glutamyl transpeptidase,GGT)、血清总蛋白(total protein,TP)、白蛋白(albumin,ALB)、总胆红素(total bilirubin,TBiL)、直接胆红素(direct bilirubin,DBiL)。
1.4.3 临床指标 包括住院时间、输血量、止血时间,出血停止判定标准为:胃管无出血的现象,黑便症状基本消失,大便的潜血试验结果为阴性;
1.4.4 不良反应发生情况 包括过敏、恶心呕吐、头痛头晕、腹部胀气[6]。
1.5 统计学方法 本研究应用SPSS20.0进行统计学分析,肝功能指标、住院时间、输血量、止血时间等计量资料采用()表示,组间比较行t检验;临床疗效、不良反应等计数资料采用[n(%)]表示,组间比较行χ2检验。P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者临床疗效的比较 研究组患者的治疗总有效率高于对照组(P<0.05)。见表1。

表1 两组患者临床疗效的比较[n(%)]
2.2 两组患者治疗后肝功能指标的比较 研究组患者治疗后的AST、ALT、ALP、GGT、TBiL、DBiL水平低于对照组,TP、ALB水平高于对照组(P<0.05)。见表2。
表2 两组患者治疗后肝功能指标的比较()
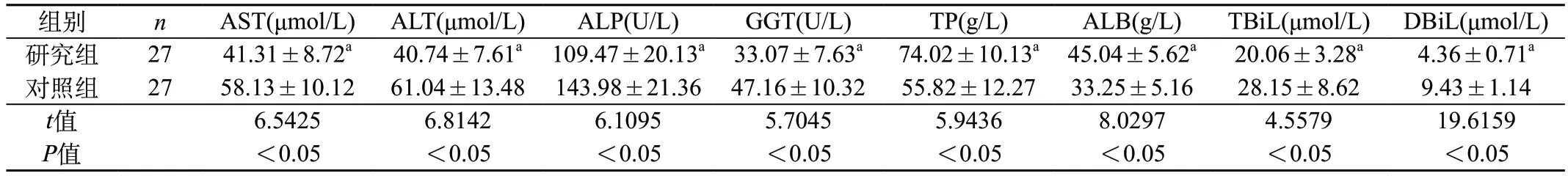
表2 两组患者治疗后肝功能指标的比较()
注:与对照组比较aP<0.05。
2.3 两组患者临床指标的比较 研究组患者住院时间(7.43±2.11)d、输血量(284.65±68.39)mL、止血时间(26.57±5.86)h均优于对照组的(11.58±3.86)d、(374.26±70.68)mL、(37.94±8.04)h(t=4.9020、4.7344、5.9384,P<0.05)。
2.4 两组患者不良反应发生情况的比较 研究组患者发生过敏2例(7.41%)、恶心呕吐1例(3.70%)、头痛头晕1例(3.70%)、腹部胀气0例,总不良反应4例(14.81%);对照组患者发生过敏3例(11.11%)、恶心呕吐4例(14.81%)、头痛头晕3例(11.11%)、腹部胀气1例(3.70%),总不良反应11例(40.74%)。研究组患者不良反应发生率低于对照组(χ2=4.5231,P<0.05)。
3 讨 论
肝硬化主要是由于慢性肝部疾病引起的弥漫性肝损伤,主要表现为门静脉高压、肝功能障碍等[7]。上消化道出血是肝硬化的一种并发症,临床主要表现为疼痛、呕吐、黑便等,主要发病原因为大量酗酒、不规律饮食、不健康饮食、滥用非甾体类药物等。若不及时进行治疗会引起肝功能障碍、出血性休克等,甚至会引发死亡,因此对于肝硬化合并上消化道出血患者要及时实施治疗。
本次研究中,使用奥曲肽联合凝血酶治疗的观察组患者的临床疗效明显,不良反应发生率较低,住院时间、止血时间较短,输血量较少,并且肝功能指标得到明显改善。奥曲肽是一种人工合成的天然抑素,属于八肽环状化合物,具有抑制生长激素、促甲状腺素的作用,对胃酸、胃蛋白酶、胃泌素分泌过多具有显著的抑制作用,可降低门脉压力和胃部的运动[8]。凝血酶是一种具有抗凝和促凝作用的生物活性蛋白,主要作用于人体循环的凝血因子细胞。当凝血酶与其接触时,会聚集并激活伤口组织中的血小板,加速纤维蛋白原转化为纤维蛋白酶[9],使血液可以迅速形成固体凝块,加速血液凝聚[10],可以有效地止血,改善出血症状,并且两种药物合用,还能起到协同作用,保护消化道黏膜,患者输血量减少,住院时间缩短,不良反应少,痛苦减轻,康复速度较快。
综上所述,肝硬化合并上消化道出血患者使用奥曲肽联合凝血酶治疗的临床疗效显著,可以降低炎性反应,缩短止血时间,减少输血量,有效改善患者的肝功能指标,促进患者康复,缩短住院时间,并且不良反应少,更为安全可靠。
