替吉奥联合奥沙利铂治疗中晚期原发性肝癌的疗效及安全性评价
2020-11-25阚庆生
刘 静 阚庆生
安徽医科大学附属宿州医院肿瘤内科 (安徽 宿州, 234000)
原发性肝癌(HCC)是常见的恶性肿瘤,其发病率排名第六,病死率位居第二[1,2]。手术是早中期HCC患者的主要治疗手段,但HCC确诊时多已失去手术时机。化疗是无法切除HCC患者的重要治疗手段[3,4]。传统抗肿瘤药物如多柔比星(ADM)和氟尿嘧啶(5-FU)等的疗效均不理想,且毒副作用明显。EACH研究证实,与阿霉素相比,奥沙利铂(L-OHP)联合5-氟尿嘧啶(FOLFOX4)方案可以明显改善总缓解率(ORR)、疾病控制率(DCR)、无进展生存期(PFS)和总生存期(OS)[5]。因此,FOLFOX4已成为中晚期HCC患者的标准治疗方案。但临床应用中发现该方案不良反应较大,患者耐受性差,因此寻找安全、有效的治疗方案是中晚期HCC患者治疗中急需解决的问题。
替吉奥(S-1)是一种新型的氟尿嘧啶衍生物,口服可取得与5-FU持续静脉滴注相似的疗效,且毒副作用轻微。但能否以S-1替代5-FU静滴联合奥沙利铂治疗中晚期HCC尚缺乏相关的临床证据。本研究旨在探讨SOX方案治疗中晚期HCC的疗效及安全性。
1 资料与方法
1.1 一般资料 收集2015年1月至2016年12月于宿州市立医院肿瘤内科接受系统性化疗的中晚期HCC患者56例,按照随机数字表法分为观察组(SOX方案)和对照组(FOLFOX4方案),每组28例,所有HCC患者均经组织病理学或细胞学检查确诊,按照2010年美国癌症联合会TNM分期标准(第七版)进行分期[6],其中Ⅲ期患者9例,Ⅳ期患者47例。两组患者性别、年龄、肝炎病史、肝硬化病史、Child-Pugh分级、肿瘤大小、临床分期、ECOG评分和既往治疗等资料比较,差异均无统计学意义(P>0.05)。见表1。
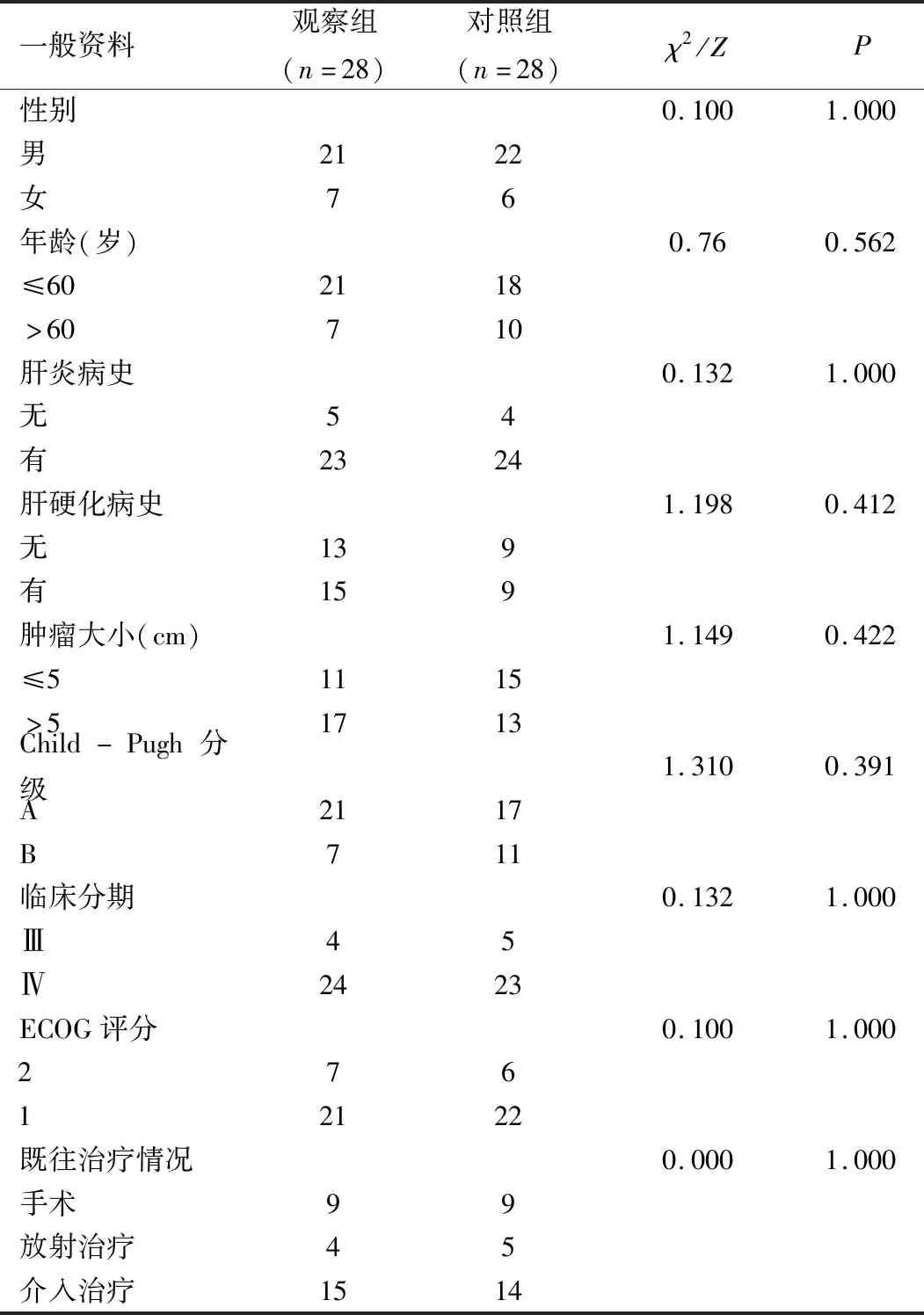
表1 两组患者一般资料比较(例)
1.2 纳入标准 ①年龄18~70岁者;②经组织病理学确诊为中晚期肝细胞肝癌者;③不符合或不愿意接受局部治疗的患者(如化学栓塞、射频消融);④6个月内未接受放疗或化疗者(包括使用奥沙利铂或S-1者);⑤至少有1个符合实体肿瘤疗效评价标准(RECIST)的可测量病灶者[7];⑥美国东部肿瘤协作组体力状态评分(ECOG;https://ecog-acrin.org/resources/ecog-performance-status)≤2分者;⑦有足够的器官和骨髓功能,无化疗禁忌证者;⑧预计生存期3个月以上者。
1.3 排除标准 ①诊断不明确者;②不愿接受化疗或存在化疗禁忌证者;③合并中枢神经系统转移、胃肠道梗阻、出血或Ⅱ度以上感觉神经障碍的患者;④合并严重心肺功能不全等基础疾病或骨髓功能不全者;⑤对本研究使用的化疗药物过敏者;⑥不能评价疗效者;⑦研究期间化疗方案变更者,或在指定方案中联合其它治疗方案者。所有患者治疗前均签署知情同意书。
1.4 方法 观察组患者给予L-OHP(江苏恒瑞医药股份有限公司,批准文号:H20000337)联合S-1胶囊(山东新时代药业有限公司,批准文号:H20080802)治疗,每21天重复;对照组患者使用L-OHP联合5-FU(天津金耀氨基酸有限公司,批准文号:H12020959)化疗,每28天重复。观察组患者用药方案:第1天给予L-OHP 135 mg/m2静脉滴注,并且每日2剂服用S-1,具体剂量为给药体表面积≥1.5 m2者口服60 mg,体表面积1.25~1.5 m2者口服50 mg,体表面积≤1.25 m2者口服40 mg,连服14d停7 d为一个治疗周期。对照组患者用药方案:第1、14天给予L-OHP 85 mg/m2静脉滴注;第1、14天5-FU 400 mg/m2静脉注射,并分别于第1、2、14、15天持续22 h泵注600 mg/m25-FU;第1、2、14、15天同时给予亚叶酸钙200 mg/m2静脉滴注;每4周为1个周期。记录所有可能与治疗相关的不良反应及合并用药情况,直至患者疾病进展或出现不可耐受的毒性反应。每2个治疗周期进行1次疗效及安全性评价。
1.5 疗效及安全性分析 按照WHO实体瘤RECIST疗效评价标准评价疗效[7],分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。治疗2个周期观察客观有效率(ORR)、疾病控制率(DCR)、无进展生存时间(PFS)和总生存时间(OS)。其中,ORR=CR+PR,DCR=CR+PR+SD。按照NCI-CTC V3.0标准评价治疗相关毒副反应(0~Ⅳ)[8]。
2 结果
2.1 两组患者近期疗效及生存预后情况 所有入组患者均可进行疗效评价,中位随访时间为12.0个月(95%CI,9.97~14.03个月)。观察组PR 6例,SD 11例,PD 11例;对照组PR 7例,SD 11例,PD 10例。两组患者的ORR、DCR以及中位PFS、OS均无统计学差异。见表2、图1。

表2 两组患者疗效比较

图1 观察组与对照组患者OS和PFS比较
2.2 两组患者不良反应情况 见表3。

表3 两组患者不良反应情况比较(例)
3 讨论
EACH研究奠定了FOLFOX4方案在中晚期HCC系统性化疗中的地位[5],但该方案毒性明显,晚期患者往往因不能耐受毒副作用而中断治疗。靶向治疗在中晚期HCC中占有重要地位,索拉非尼是第一个被证明能够延长中晚期HCC患者生存期的药物,但其OS的延长也仅仅只有2.8个月[9],且价格昂贵、副作用明显。所以寻找安全、更有效的治疗方案具有重要的临床意义。
S-1是一种新型的口服5-FU类似物,它是由替加氟(一种5-FU的活性代谢前药)和吉美嘧啶、奥替拉西钾两种5-FU生化调节剂构成[10]。目前,S-1应用于治疗中晚期HCC患者的疗效和安全性的数据十分有限,但S-1的抗肿瘤作用已在多种瘤种中得到证实[11]。理论上,以S-1代替FOLFOX4方案中的5-FU不仅可以增强抗肿瘤作用,而且可以减少毒副作用。研究表明[12,13],S-1联合奥沙利铂治疗晚期结直肠癌的疗效并不劣于FOLFOX4,表明以S-1口服代替5-FU持续静脉滴注是一种可行的方案。程晓梅等[14]比较SOX和FOLFOX4方案一线治疗老年晚期结直肠癌的疗效,发现观察组与对照组的RR、DCR、1年生存率和中位肿瘤进展时间均无差异,但SOX方案组患者的白细胞减少、消化道反应发生率均明显降低,差异有统计学意义(P<0.05)。上述结果表明,SOX方案不仅有效,而且安全性较高值得临床进一步研究推广。
近年在HCC系统性化疗的研究中发现[5,15],FOLFOX4方案治疗中晚期HCC可以取得较高的RR,并能显著延长患者的PFS,对OS也有一定的提高。但对于能否使用SOX方案代替FOLFOX4方案治疗中晚期HCC的报道相对较少。刘淑红[16]使用SOX方案治疗42例晚期原发性肝癌,RR为19%,DCR达48%,超过50%的患者临床症状得到明显改善,且不良反应发生率低。但蒋永丰等[17]研究发现,与FOLFOX4方案相比,SOX方案患者的临床疗效较高,但不良反应的发生率也较高,差异有统计学意义(P<0.05)。本研究发现,SOX方案治疗中晚期HCC患者在ORR、DCR、OS和PFS等方面均不劣于FOLFOX4方案。而SOX组患者Ⅰ~Ⅱ级和Ⅲ~Ⅳ级血液学毒性的发生率分别为25.00%和3.57%,低于FOLFOX4组患者的53.57%和10.71%,差异有统计学意义(P<0.05)。而消化道反应、肝功能异常、神经系统毒性以及皮症瘙痒等不良反应无统计学差异(P>0.05)。
综上所述,SOX方案治疗中晚期HCC可取得与FOLFOX4方案相似的疗效,但不良反应的发生率更低,是一种安全有效的治疗策略。本研究亦存在一定的局限性:①本研究为单中心、小样本量研究,SOX方案应用于中晚期HCC的数据十分有限,研究结果可能存在一定偏倚,后续仍需进一步扩大样本量进行研究以验证本研究结果;②本研究为回顾性病例对照研究,患者的选择偏倚要大于前瞻性随机对照研究。总之,本研究有待进一步进行大样本量的前瞻性随机对照研究。
