抗骨质疏松症药物预防绝经后骨质疏松性骨折有效性与安全性的网状Meta分析
2020-11-23户光刘梓晗李灿曾明
户光 刘梓晗 李灿 曾明
1.中公网医疗信息技术有限公司,北京 100028 2.解放军总医院第七医学中心药理科,北京 100700
骨质疏松症已经成为绝经后女性面临的主要健康威胁之一,据国家卫生健康委员会于2018年发布的首个中国骨质疏松症流行病学调查结果显示,50岁以上女性骨质疏松症患病率为32.1%,65岁以上女性患病率则达51.6%[1]。并且老年患者的骨折治疗费用高昂,患者单次平均住院费用高达27 561.27元[2],仅2010年中国卫生系统为此支出的医疗费用就超过100亿美元,这一数字预计在2050年将达到254亿美元[3]。绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)一般发生在女性绝经后5~10年内,由于体内的雌激素缺乏,促使骨微组织结构发生变化,骨量减少,增加脆性。PMOP早期症状不明显,容易忽视,若任由其发展,可导致骨折,临床上常以驼背、脆性骨折、呼吸功能降低、腰背疼痛等为主诉就医。目前,用于治疗PMOP及预防脆性骨折的药物除已广泛用于临床的维生素D及钙片、双膦酸盐类、激素替代疗法、雷洛昔芬、雷奈酸锶等,还有近年来在中国获批的特立帕肽和地舒单抗,以及未在国内上市但已经处于研发或申报阶段的新药:巴多昔芬、阿巴帕肽、米诺膦酸和romosozumab。
通过查询国内外相关文献发现,目前尚无研究将所有国内处于研发阶段的待上市药物纳入比较。新药的获批为高骨折风险的人群带来了新的治疗选择,也为不适用于已有药物治疗的患者带来了新的希望。因此,本研究通过网状Meta分析对16种包括最新批准的以及临床常用的抗骨质疏松症药物预防绝经后骨质疏松性骨折进行有效性及安全性评价,以期为无法通过现行疗法获益的患者提供临床用药参考,为预防绝经后骨质疏松性骨折提供最新证据支持。
1 资料与方法
1.1 纳入与排除标准
1.1.1研究类型:随机对照试验(randomized controlled trials,RCTs)。
1.1.2研究对象:经临床确诊的绝经后骨质疏松症患者(采用WHO推荐的诊断标准)。
1.1.3干预措施:包括双膦酸盐、选择性雌激素受体调节剂、核因子kappa-B受体活化因子配体(RANKL)抑制剂、甲状旁腺激素类似物、雷奈酸锶、romosozumab、安慰剂等,研究至少包含一组所列药物的两两对比。
1.1.4结局指标:①新发椎体骨折;②非椎体骨折;③髋部骨折;④总不良反应;⑤药物相关不良反应;⑥严重不良反应。
1.1.5排除标准:非RCT研究、综述、重复报道等;排除患有其他影响骨代谢的疾病及长期服用糖皮质激素等药物的患者。
1.2 检索策略
计算机检索以下数据库:PubMed、Embase、Cochrane Central Register of Controlled Trials (CENTRAL)、临床试验注册网、中国生物医学文献数据库、中国期刊全文数据库及万方数据库,检索时限均从建库至2019 年3月15日。检索词包括:绝经后骨质疏松、双膦酸盐、阿巴帕肽、地舒单抗、随机对照试验、postmenopausal、osteoporosis、romosozumab、teriparatide、randomized controlled trial等。
1.3 质量评价
由2名评价员独立评价纳入研究的偏倚风险,并交叉核对结果。采用Cochrane系统评价员手册5.1.0推荐的RCT偏倚风险评估工具对每篇纳入的文献进行质量评价。
1.4 统计学分析
使用R Studio软件基于马尔科夫链-蒙特卡洛方法进行贝叶斯网状Meta分析,以3条马尔科夫链进行模拟,20 000次预迭代及75 000次迭代。Stata14绘制网状关系图,RevMan 5.3.5进行文献偏倚风险评估。计数资料采用比值比(odds ratio,OR)为效应指标,各效应量均给出其点估计值和95%CI。使用节点分析模型进行一致性检验,若结果无显著性差异(P>0.05),提示直接比较与间接比较结果一致。采用χ2检验进行异质性分析(检验水准为=0.1),同时利用I2判断异质性大小。若同质,用固定效应模型;若有异质性时(I2>50%或P≤0.05),则进一步分析异质性来源,在排除明显临床异质性的影响后,采用随机效应模型进行Meta分析。不同干预措施的疗效排序可通过计算累积排序曲线下面积(surface under the cumulative ranking,SUCRA)得到。
2 结果
2.1 文献检索结果
数据库检出11 817篇相关文献,经初筛和复筛,最终纳入38篇文献,共37个RCT研究,文献筛选流程见图1。
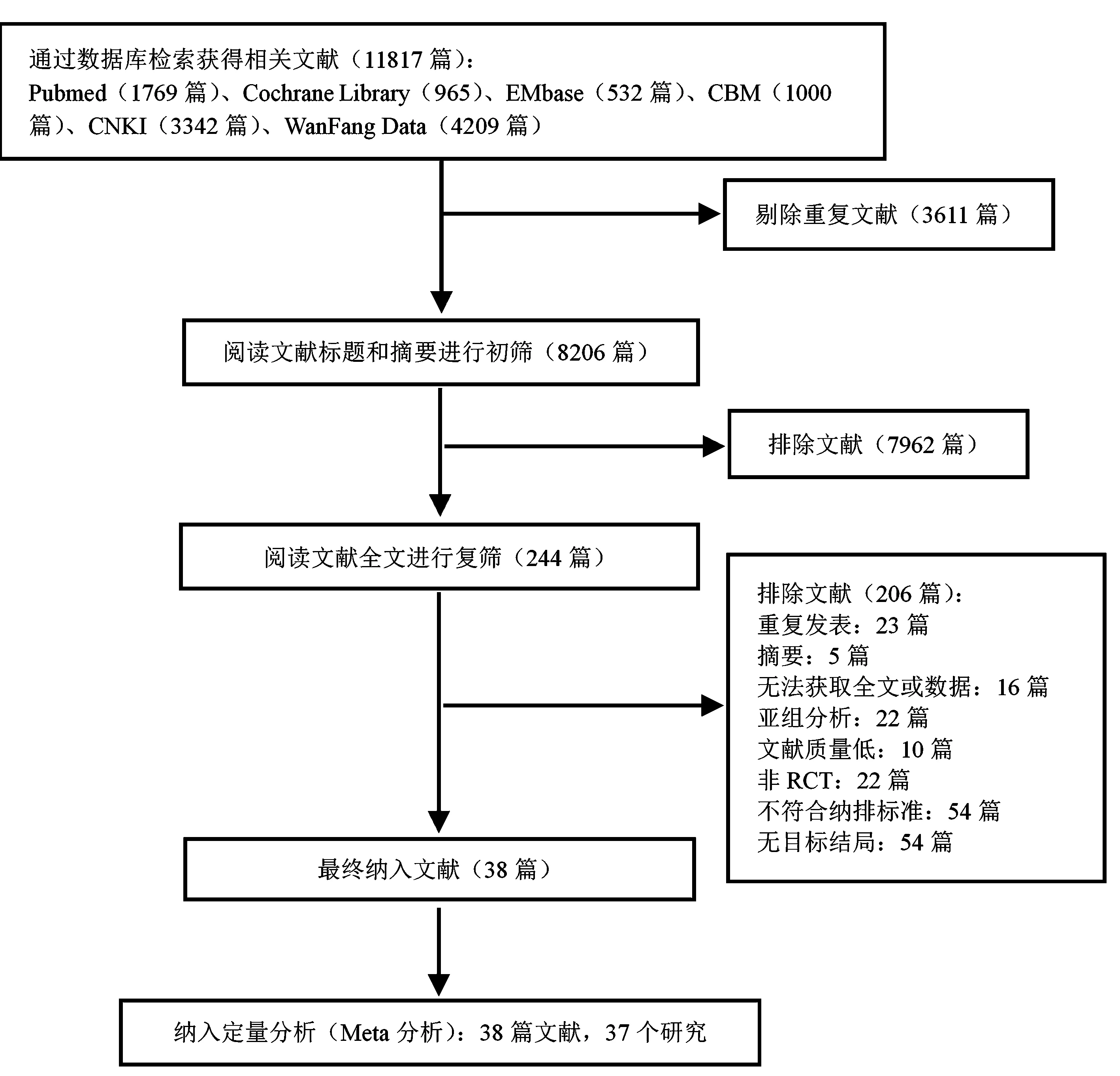
图1 文献筛选流程图Fig.1 Flow chart of the study selection
2.2 纳入文献基本特征与偏倚风险评价结果
纳入的37个RCT共计83 907例患者,共涉及16种干预措施,包括阿巴帕肽(abaloparatide)、阿仑膦酸钠(alendronate)、特立帕肽(teriparatide)、利塞膦酸钠(risedronate)、米诺磷酸(minodronic acid)、伊班膦酸钠(ibandronate)、替勃龙(tibolone)、地舒单抗(denosumab)、雷奈酸锶(strontium ranelate)、唑来膦酸(zoledronic acid)、雷洛昔芬(raloxifene)、巴多昔芬(bazedoxifene)、romosozumab、rhPTH(1-84)、rhPTH(1-31)、安慰剂(placebo)。3个三臂试验,其余均为两臂试验;纳入研究的一般情况及基线特征见表1,偏倚风险评价结果见图2。
2.3 网状关系图
各结局指标网状关系见图3,图中圆点大小代表干预措施被研究次数,直线连接的两个干预措施存在直接比较,线越粗表示比较次数越多。
2.4 Meta分析结果
2.4.1新发椎体骨折:24项RCT研究[5-6, 8, 10-14, 16, 20-22, 25-28, 30, 32-34, 36-39, 41](共661 947例患者)报告了新发椎体骨折。节点分析模型结果提示一致性良好(P>0.05),异质性检验显示伊班膦酸钠与安慰剂组内研究间异质性较大(I2=86.2%,P=0.007 ),其他研究间均无异质性。网状Meta分析结果显示:各干预措施新发椎体骨折发生率均低于安慰剂,且差异具有统计学意义。其中,阿巴帕肽(OR=0.12,95%CI:0.04~0.35)、特立帕肽(OR=0.24,95%CI:0.16~0.35)、唑来膦酸(OR=0.28,95%CI:0.18~0.43)以及romosozumab(OR=0.30,95%CI:0.19~0.45)预防椎体骨折效果最为显著,见图4。
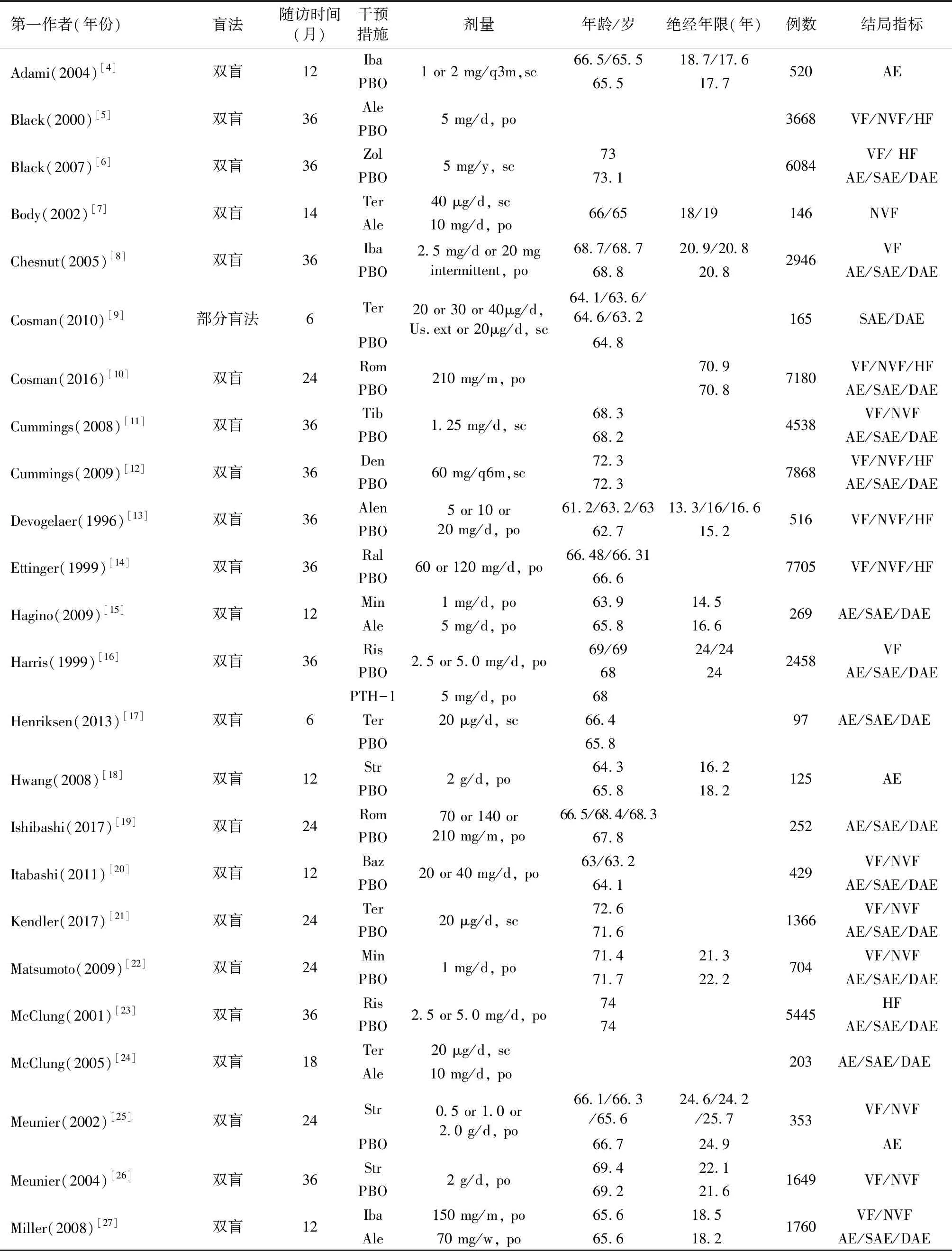
表1 纳入研究基本特征Table 1 Characteristics of the included studies
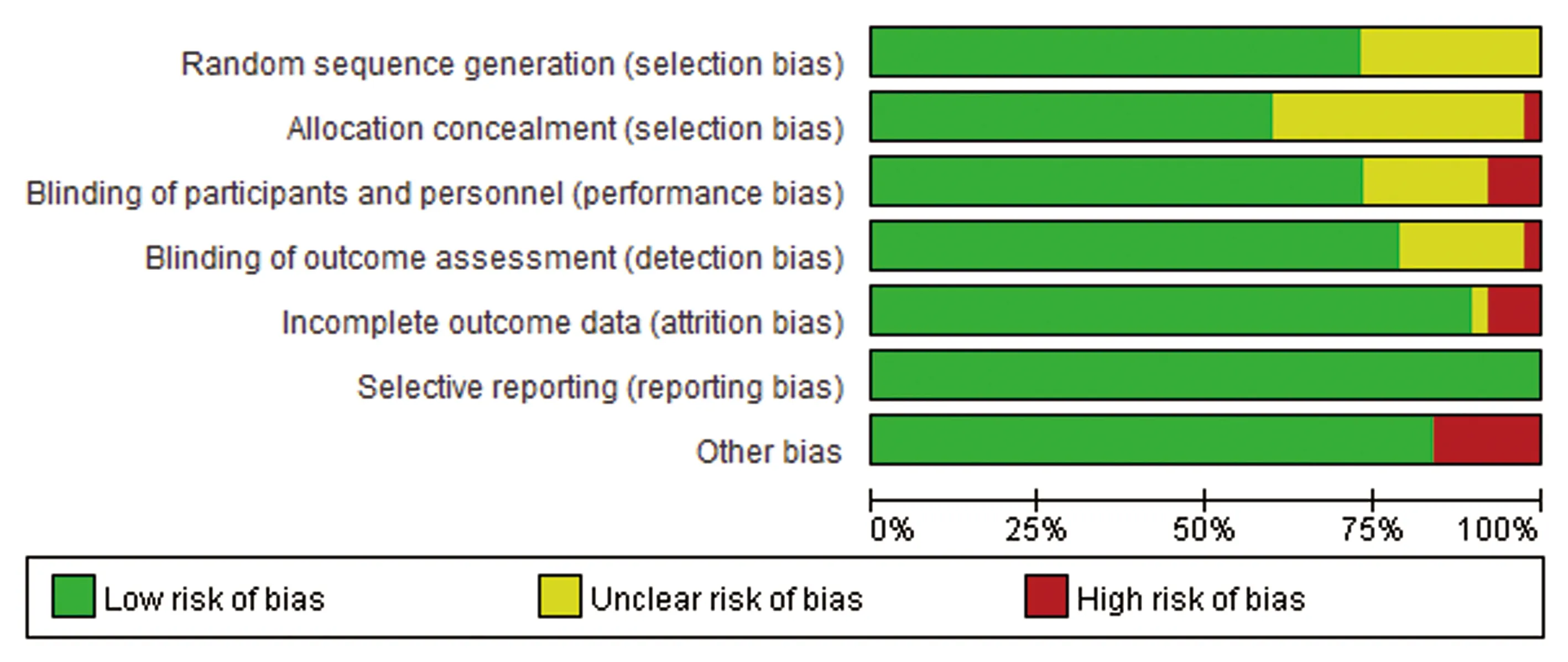
图2 纳入研究的偏倚风险评价Fig.2 Assessment of the risk of bias of the included studies
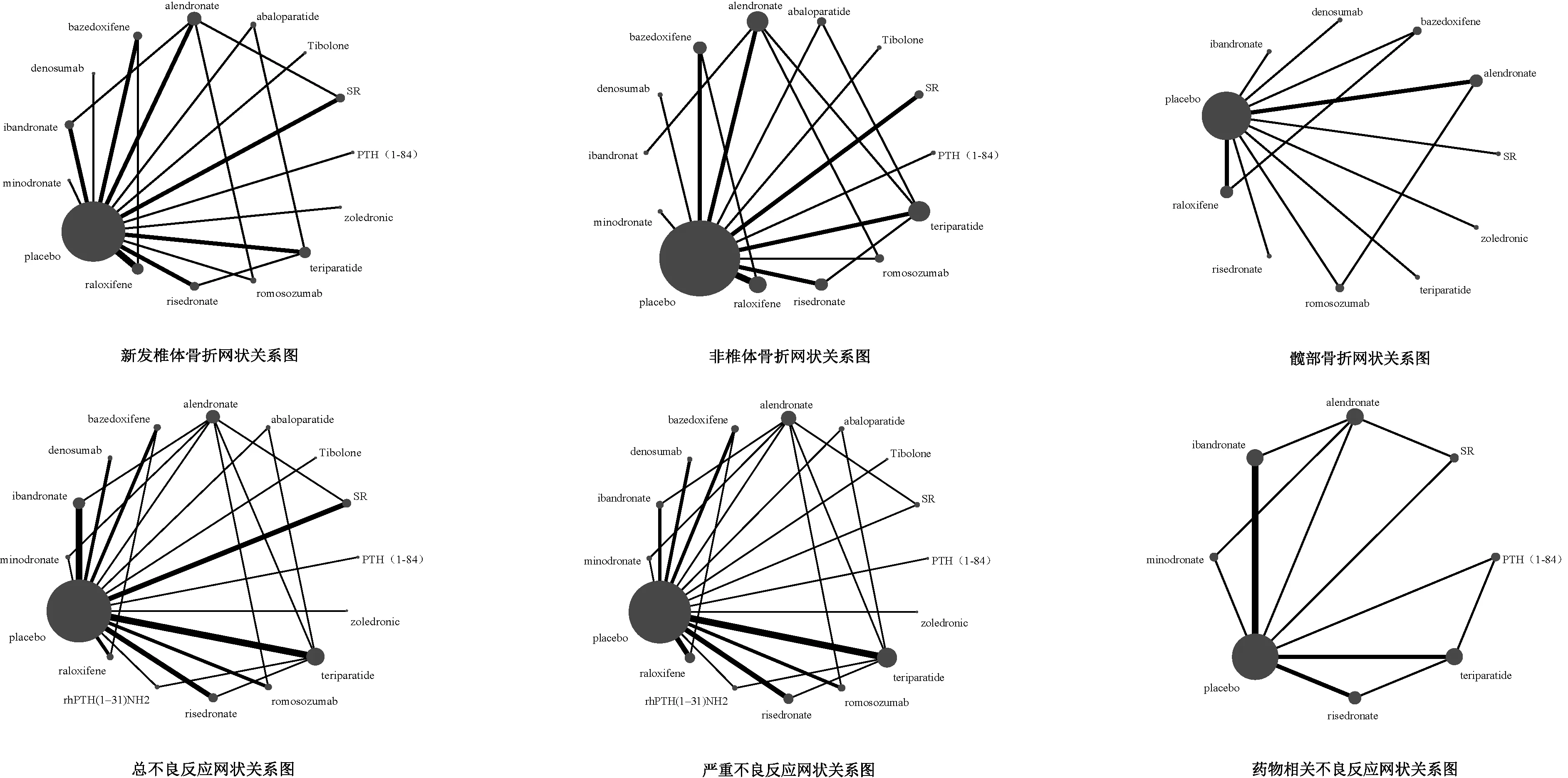
图3 各干预措施网状关系图Fig.3 Network plots of the intervening measures
2.4.2非椎体骨折:21项RCT研究[5,7,10-14,16,20-22,26-28,30,32,34-35,37-39, 41](共63107例患者)报告了非椎体骨折。节点分析模型结果提示一致性良好(P>0.05),且研究间均无异质性。网状Meta分析结果显示:阿巴帕肽(OR=0.46,95%CI:0.21~0.97)、特立帕肽(OR=0.54,95%CI:0.39~0.75)、romosozumab(OR=0.62,95%CI:0.44~0.90)、利塞膦酸钠(OR=0.70,95%CI:0.50~0.97)干预措施组非椎体骨折发生风险低于安慰剂组,且特立帕肽组非椎体骨折发生风险低于巴多昔芬(OR=0.62,95%CI:0.39~0.97)、rhPTH(1-84)(OR=0.56,95%CI:0.32~0.98)、雷洛昔芬(OR=0.61,95%CI:0.41~0.94)和雷奈酸锶(OR=0.63,95%CI:0.41~0.95),差异均具有统计学意义,见图4。
2.4.3髋部骨折:12项RCT研究[5-6,10,12-14,23,32-33,35,37-38,41](共59891例患者)报告了髋部骨折。节点分析模型结果提示一致性良好(P>0.05),且研究间均无异质性。网状Meta分析结果显示:各干预措施对降低髋部骨折发生风险均无统计学差异,见图4。
2.4.4不良反应:32项RCT研究[4,6,8,10-25,27-29,31-41](共83529例患者)报告了总体不良反应。一致性差异无统计学意义(P>0.05),异质性检验显示各干预组内研究间统计学异质性均较小(P>0.10,I2<50%)。网状Meta分析结果显示:除rhPTH(1-31)外,各干预措施间不良反应发生率与安慰剂相比均无统计学差异,安全性良好。14项RCT研究[4,8,13,15-18,21-22,27,29,33-34,36,41](共14675例患者)报告了药物相关不良反应。一致性差异无统计学意义(P>0.05)。异质性检验显示伊班膦酸钠与安慰剂组内研究间统计学有异质性(I2=77.2%,P=0.015),其他研究间均无异质性。网状Meta分析结果显示:伊班膦酸钠(OR=1.39,95%CI:1.00~1.95)和rhPTH(1-84)(OR=2.98,95%CI:1.07~8.24)药物相关的不良反应发生率高于安慰剂,并且rhPTH(1-84)(OR=2.98,95%CI:1.05~8.6)药物相关的不良反应发生率高于利塞膦酸钠。其他各干预措施间药物相关不良反应发生率无统计学差异,见图4。

图4 网状Meta分析结果Fig.4 Results of the network meta-analysis注:字体加粗代表差异具有统计学意义。
2.5 SUCRA值与排序结果
各干预措施对不同部位骨折预防的疗效排序见表2,SUCRA值越大提示干预措施越好。
3 讨论
骨质疏松症最严重的后果就是骨质疏松性骨折,其常见部位为椎体、髋部和腕部。骨质疏松性骨折导致的致残率和致死率显著增加,预计到2050年,一半的髋部骨折将发生在以中国为主的亚洲国家[42-43]。目前,抗骨质疏松症药物主要分为骨吸收抑制剂、骨形成促进剂、其他机制类药物及中药制剂。阿巴帕肽和romosozumab是近年来新获批上市的两种抗骨质疏松症药物,阿巴帕肽为甲状旁腺激素相关蛋白类似物,于2017年4月在美国批准上市,该药是一种人工合成的34个氨基酸多肽,通过选择性激活PTH1型受体的信号通道,起到调节代谢、促进骨骼形成的作用[44]。Romosozumab为单克隆抗体药物,该药作为全球首个骨硬化蛋白(sclerostin)靶点药物于2019年分别在日本、美国获批上市,其可抑制骨硬化蛋白的活性,从而加速骨形成减少骨吸收。
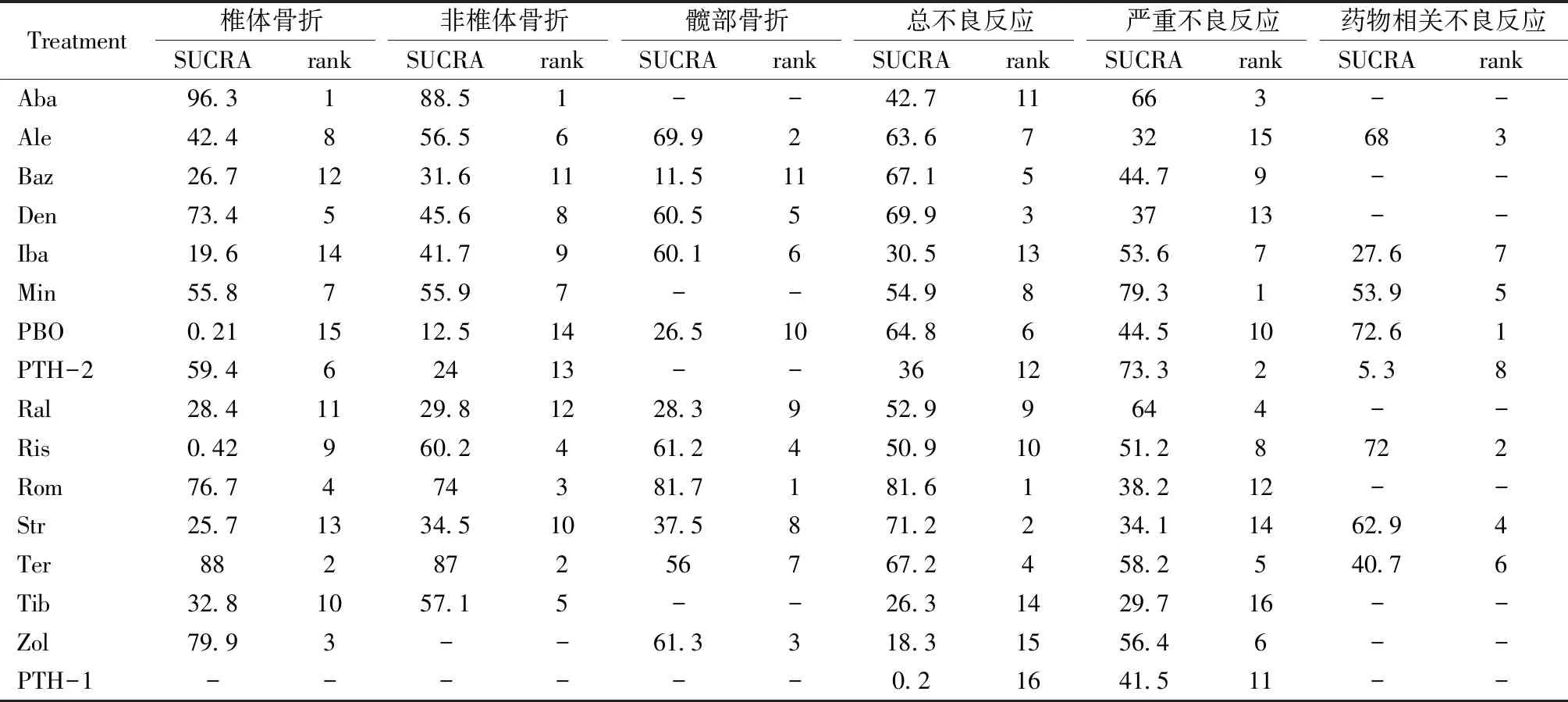
表2 网状Meta分析SUCRA值和排序 Table 2 SUCRAs and the rankings of SUCRAs in network meta-analyses
本研究在纳入我国指南推荐的临床常用药物的同时还将国外上市的药物如romosozumab、阿巴帕肽、巴多昔芬、米诺膦酸等也纳入研究。共纳入37个RCT,包括16种干预措施,共计83 907例患者。网状Meta分析结果显示:各干预措施对椎体骨折的预防均优于安慰剂,差异具有统计学意义;其中,阿巴帕肽、特立帕肽、唑来膦酸以及romosozumab的效果最为显著;对于非椎体骨折的预防,阿巴帕肽、特立帕肽、romosozumab、利塞膦酸钠的疗效均优于安慰剂;除rhPTH(1-31)外,各干预措施间不良反应发生率与安慰剂相比差异均无统计学意义,安全性良好。
本研究仍存在一些局限性:①本研究纳入的文献均为英文文献,并未纳入其他语言的文献,可能存在潜在的选择性偏倚;②纳入研究均为已发表文献,未能纳入灰色文献、增刊、会议论文等,可能存在发表偏倚。③伊班膦酸钠和安慰剂组内研究间存在较大异质性,经分析判断可能是因为Chesunt-2005[13]和Recker-2004[38]两个研究试验组的给药方式及剂量不同导致的异质性,又由于只纳入两个研究,未能进行敏感性分析,因此,结果仍需更多相关研究数据的支持。④本次研究试图对国内外已上市的所有抗骨质疏松症药物进行有效性与安全性分析,但由于相关研究少、研究较久远、不符合纳入排除标准等原因,本次网状Meta分析未对依替膦酸钠、氯膦酸二钠以及帕米膦酸二钠、降钙素进行评价。
综上所述,阿巴帕肽、特立帕肽、romosozumab和唑来膦酸相比其他抗骨质疏松症药物对绝经后骨质疏松性骨折的预防效果更加安全有效;并且阿巴帕肽对预防椎体骨折和非椎体骨折效果最佳,romosozumab对预防髋部骨折效果最佳。
