玻璃体腔注射雷珠单抗联合视网膜光凝治疗糖尿病性黄斑水肿的效果
2020-11-20王皎皎
张 丹 王皎皎
中国人民武装警察部队重庆市总队医院眼科,重庆 400061
近年来随着人们生活方式的改变,糖尿病的发病率与日俱增,随之而来的糖尿病并发症也逐渐增多,其中糖尿病视网膜病变(diabetic retinopathy,DR)是引起患者视力下降、生活质量降低的常见并发症。DR是由于患者长期高血糖导致的视网膜微血管病变,临床上主要表现为糖尿病性黄斑水肿(diabetic macular edema,DME),有关文献报道我国DME发病率达35.6%[1],DME 治疗棘手,易反复,长期持续的DME 可引起永久性黄斑变性或者黄斑裂孔[2],导致不可逆转的视功能丧失,甚至失明,应积极治疗。治疗DME 的传统方法是视网膜激光光凝[3],采用黄斑格栅样光凝或局灶光凝,可以适当延缓DME 引起的视力下降,但有局限性,DME 严重时激光治疗困难且需高能量激光,治疗后DME 仍反复发作。目前,有文献报道[4]DME 患者玻璃体内血管内皮生长因子(vascular endothelial growth factor,VEGF)明显升高且高于血管内水平,并深入证实VEGF 可增加血管通透性,破坏血-视网膜屏障,引起液体渗漏,导致DME 形成,因此抗VEGF 药物治疗DME 已成为临床上较为有效的治疗方法[5],但抗VEGF 药物作用时间短,药效消退后DME 可再次出现。由此本研究设想将传统的激光光凝和抗VEGF 药物联合治疗以观察能否产生更为理想的临床效果,旨在探讨玻璃体腔注射雷珠单抗联合激光光凝治疗DME 的效果,以期为DME 的治疗提供临床依据,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2017年1月~2018年1月在我院确诊的90 例(91 眼)DME 患者的临床资料,根据不同的治疗方式,将玻璃体腔注射雷珠单抗联合黄斑格栅样光凝或局灶光凝治疗的45 例(46 眼)设为治疗组,玻璃体腔注射雷珠单抗治疗的45 例(45 眼)设为对照组。治疗组中,男22 例(22 眼),女23 例(24 眼);年龄52~73 岁,平均(64±5)岁;糖尿病病程5~10年,平均(7.7±1.4)年。对照组中,男22 例(22 眼),女23 例(23 眼);年龄54~75 岁,平均(64±6)岁;糖尿病病程5~10年,平均(7.6±1.4)年。两组患者的性别、年龄、糖尿病病程等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核批准。
纳入标准:①已确诊为2 型糖尿病;②经眼底血管造影(fundus fluorescein angiography,FFA)检查确诊为DR;③根据美国糖尿病视网膜病变早期治疗研究组(early treatment diabetic retinopathy study,ETDRS)标准诊断为有临床意义的DME[6];④全身情况良好能够配合治疗。排除标准:①进行过眼底激光、球内注射或眼底手术者;②由其他疾病引起的黄斑水肿,如视网膜静脉阻塞、年龄相关性黄斑变性、视网膜血管炎等眼底病;③存在大面积的玻璃体积血及视网膜脱离需手术治疗者; ④屈光介质混浊影响眼底观察和治疗;⑤妊娠期或哺乳期妇女、严重过敏体质者或有严重全身疾病不能配合治疗者。
1.2 治疗方法
两组患者玻璃体腔注射雷珠单抗注射液(瑞Novartis Pharma Stein AG,注册证号:S20170003,生产批号:SR195)治疗方法相同。治疗前3 d 患眼采用盐酸左氧氟沙星滴眼液滴眼(珠海联邦制药股份有限公司中山分公司,国药准字H20020327,生产批号:77062103)4 次/d;玻璃体内注射在眼科手术室内完成:常规消毒铺巾,盐酸奥布卡因滴眼液(参天制药株式会社,国药准字J20160094,生产批号:B2045)表面麻醉,用0.5%聚维酮碘溶液常规洗眼,在颞下方角膜缘后3.5~4.0 mm 处进针,采用30 号针头沿球心方向刺入眼内,进针深度约4 mm,确保针尖位于玻璃体腔后缓慢注射雷珠单抗(0.5 mg/0.05 ml),出针后对穿刺点进行1 min 的压迫,无菌敷料包扎患眼,术后2 h、术后1 d 检测眼压、眼部情况,术后24 h 打开敷料,给予溴芬酸钠滴眼液(辰欣佛都药业有限公司,国药准字H20150022,生产批号:17100531022)2 次/d,妥布霉素地塞米松滴眼液(比利时S.A. Alcon Couvreur N.V.,国药准字H20080661,生产批号:17F25KA)4 次/d、妥布霉素地塞米松眼膏(比利时S.A. Alcon Couvreur N.V.,国药准字H20160337,生产批号:7KEE1A)每晚1 次,治疗1 周停药。治疗组患者联合视网膜激光光凝,玻璃体腔注射雷珠单抗1 周后局部黄斑区水肿采用视网膜局部光凝,弥漫性黄斑水肿采用格栅样激光光凝,在FFA 指导下,采用532 nm 氩绿激光,激光参数:光斑能量110~130 mW,光斑直径50~100 μm,时间0.10~0.15 s,光斑的间距约为1 个光斑直径,每次治疗200~500 点。所有治疗均由同一名眼科专科医师完成。
1.3 观察指标
①最佳矫正视力:采用国际标准对数视力表于治疗前及治疗后1、3 个月进行最佳矫正视力测量,其中治疗后最佳矫正视力提高两行及以上为提高;提高一行、下降一行或无变化为稳定;下降两行及以上为下降。②黄斑部中心凹区域视网膜厚度:治疗前和治疗后1、3 个月均采用光学相干断层扫描(optical coherence tomography,OCT)仪检测黄斑中心凹区域视网膜厚度。③黄斑部渗漏情况:治疗后3 个月采用FFA 技术检查以黄斑中心凹区域为中心2 个视盘(PD)直径范围内视网膜渗漏情况。④不良反应发生情况:观察治疗期间有无角膜损伤、炎症反应、高眼压、玻璃体积血、视网膜出血及视网膜脱离等眼部及全身不良反应发生。
1.4 统计学方法
采用SPSS 17.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用t检验; 计数资料采用率表示,组间比较采用χ2检验;等级资料采用秩和检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗后1、3 个月最佳矫正视力变化的比较
两组患者治疗后1 个月的最佳矫正视力比较,差异无统计学意义(P>0.05);治疗组患者治疗后3 个月的最佳矫正视力优于对照组,差异有统计学意义(P<0.05); 治疗组患者治疗后3 个月的最佳矫正视力与本组治疗后1 个月比较,差异无统计学意义(P>0.05); 对照组患者治疗后3 个月的最佳矫正视力低于本组治疗后1 个月,差异有统计学意义(P<0.05)(表1)。
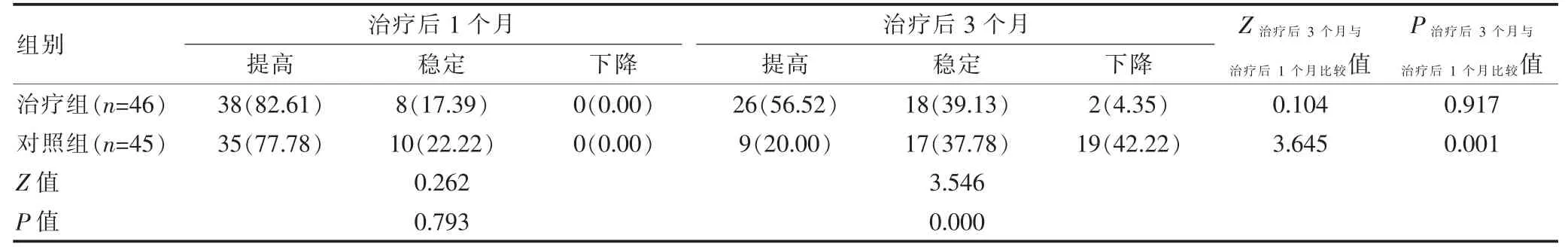
表1 两组患者治疗后1、3 个月最佳矫正视力变化的比较[n(%)]
2.2 两组患者治疗前后黄斑中心凹区域视网膜厚度的比较
两组患者治疗前的黄斑中心凹区域视网膜厚度比较,差异无统计学意义(P>0.05);两组患者治疗后1、3 个月的黄斑中心凹区域视网膜厚度低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后1、3个月的黄斑中心凹区域视网膜厚度低于对照组,差异有统计学意义(P<0.05);治疗组患者治疗后3 个月的黄斑中心凹区域视网膜厚度与本组治疗后1 个月比较,差异无统计学意义(P>0.05);治疗后3 个月,对照组患者的黄斑中心凹区域视网膜再次出现水肿,厚度增加,高于本组治疗后1 个月,差异有统计学意义(P<0.05)(图1~2,封三、表2)。

图1 治疗组患者治疗前后黄斑中心凹区域视网膜厚度的比较(n=46)

图2 对照组患者治疗前后黄斑中心凹区域视网膜厚度的比较(n=45)
2.3 两组患者治疗后3 个月以黄斑中心凹区域为中心2 个PD 直径范围内视网膜渗漏的比较
治疗后3 个月复查FFA,观察以黄斑中心凹区域为中心2 个PD 直径范围内视网膜渗漏情况,治疗组渗漏3 眼(6.52%),对照组渗漏18 眼(40.00%),两组比较,差异有统计学意义(P<0.05)。
2.4 两组患者的不良反应发生情况
观察治疗期间,所有患者均未发现角膜损伤、炎症反应、高眼压、玻璃体积血、视网膜出血及视网膜脱离等眼部和全身不良反应。
3 讨论
糖尿病是一组终身性疾病,随之而来的并发症亦不可避免,病程越长出现并发症的风险就越高[7],DR便是其中不可忽略且较为严重的微血管病变,而DME 则可发生于DR 任何时期,一旦出现DME 则提示视网膜微循环功能出现障碍,血-视网膜屏障出现异常,毛细血管通透性升高,水分进入视网膜组织内引起视网膜水肿增厚。此外,DR 还可以出现微血管瘤、硬性渗出、软性渗出、异常新生血管、玻璃体积血等较多眼底改变[8],但在诸多改变中,DME 更容易引起患者视力下降,影响生活质量,DME 进展可能比较缓慢,但多数患者往往缺乏正确认识,错过最佳治疗时机,导致不可逆性的视力损害。DME 主要累及黄斑中心2 个PD 直径内的视网膜,病理生理研究发现[9]DME 异常渗出的液体主要聚集在视网膜外丛状层、内核层,也可表现为视网膜细胞外间隙扩张以及黄斑区细胞内水肿,最终引起视网膜增厚。DME 是多因素参与的复杂病理生理过程,对其发病机制的研究也在不断深入与发展,近几年国内外大量基础实验[10-11]提示VEGF 在DR 和DME 的发生和发展中起着十分重要的作用,DR 时视网膜出现微循环障碍引起组织缺血缺氧,从而激活VEGF 的表达,VEGF 作为始动因素可触发一系列炎症反应过程,加重视网膜组织结构、功能及微环境改变,导致DME 或异常新生血管出现,持久的DME 可引起黄斑区视网膜功能结构永久性损害和不可逆性的视功能丧失。有学者研究[12]证实DME 患者玻璃体内VEGF 水平明显高于正常眼,且与DME 严重程度成正相关,这些研究为抗VEGF 药物应用于临床治疗DME 提供了理论基础。
表2 两组患者治疗前后黄斑中心凹区域视网膜厚度的比较(μm,±s)

表2 两组患者治疗前后黄斑中心凹区域视网膜厚度的比较(μm,±s)
?
2012年,美国食品药品管理局批准雷珠单抗用于湿性老年性黄斑病变以及DME 的治疗,雷珠单抗是一种新型的抗新生血管生成靶向治疗药物,同时也是一种人源化的重组单克隆抗体片段(Fab),作用位点广,可靶向抑制人VEGF 所有亚型的表达[13]。与以往药物相比,雷珠单抗分子量小,玻璃体腔内注射雷珠单抗后,其对视网膜组织穿透力及渗透性更强,生物利用度高,有研究报道其可达50%~60%[14],能有效抑制VEGF 的表达,降低血管通透性,改善血-视网膜屏障功能,减少水分进入视网膜组织内,亦能促进视网膜内渗液吸收,改善黄斑水肿。目前,已有相关临床研究[15]表明玻璃体腔注射雷珠单抗能有效减轻DME并改善视力。本研究中,治疗组与对照组均采用了玻璃体腔注射雷珠单抗,故治疗后1 个月,两组患者黄斑部视网膜厚度均降低,与治疗前比较,差异有统计学意义(P<0.05),验证了雷珠单抗可降低血管通透性,减轻因血管渗漏导致的组织水肿、从而改善视力。但雷珠单抗在玻璃体内的平均消除半衰期约为9 d,雷珠单抗治疗的作用时间短暂,对照组治疗后3 个月,患者最佳矫正视力下降,黄斑部再次出现水肿,所以仅单独使用玻璃体腔注射雷珠单抗治疗,DME 容易复发,雷珠单抗仅通过阻止VEGF 与其特异性受体结合,抑制新生血管生成和降低血管通透性,从而减少血管渗漏消除组织水肿,但雷珠单抗不能改善DR引起的视网膜组织缺氧,视网膜组织缺氧持续存在,必然会引起VEGF 上调,视网膜血管通透性增高,再次出现视网膜血管的渗漏,引起DME。因此,本研究中治疗组联合视网膜局部光凝或格栅样光凝,结果显示,治疗后3 个月,治疗组在稳定最佳矫正视力和减轻黄斑水肿渗漏方面更具优势,治疗DME 效果稳定持久,与对照组比较,差异有统计学意义(P<0.05),分析原因在于雷珠单抗联合激光光凝治疗在减轻DME中产生了协同作用。视网膜激光光凝是DME 治疗的传统常用方法,文献报道其治疗原理可归纳为以下3个方面[16-18]:①激光利用热能直接破坏需氧高且代谢旺盛的光感受器复合体,形成低耗氧量的胶原瘢痕组织,降低视网膜厚度,光凝后外层视网膜耗氧量降低,而内层缺氧的视网膜可通过脉络膜毛细血管直接供氧,缓解缺氧状态,改善视网膜血管通透性,促进视网膜内屏障修复,减少血管内液体外渗至视网膜组织,减轻黄斑水肿;②激光光凝至视网膜色素上皮(retinal pigment epithelium,RPE)层损伤,光凝后促进产生更具活力的、新的RPE,RPE 转运功能增强,帮助血管内皮细胞修复,有助于视网膜内外屏障的修复进而减轻黄斑水肿;③激光光凝在黄斑区周围可产生“屏障保护”,防止和减少黄斑区外视网膜各层间渗液渗透与聚集于黄斑无血管区。两者协同作用在于,雷珠单抗降低DME 引起的视网膜增厚,恢复视网膜透明度,有助于眼内激光治疗并减少对高激光能量的需求,而激光治疗可以降低视网膜耗氧量,抑制VEGF 上调,减少雷珠单抗注射次数,两者相辅相成。因此,当玻璃体腔注射雷珠单抗联合激光光凝治疗时,可降低DME复发率,有效稳定患者视力、恢复视网膜功能。视网膜激光光凝和玻璃体内注射雷珠单抗都属于有创治疗,两者联合治疗可降低激光所用的能量、减少玻璃体内注射次数,从而降低有创治疗风险,有重要临床意义,但本次研究选取病例数偏少,不能以点带全,期待更大样本及更深入的研究,更期待新的有效无创治疗方法应用于临床。
综上所述,与玻璃体腔注射雷珠单抗单独治疗相比,雷珠单抗联合视网膜光凝治疗DME 在改善视力、恢复视网膜功能方面效果更佳,且具有良好的安全性。
