肉桂精油/海藻酸钠/膨润土复合凝胶微球的制备及缓释研究
2020-11-18侯聪颖张诗韵孙建安中国海洋大学食品科学与工程学院山东青岛266003海南热带海洋学院食品科学与工程学院海南三亚572022
侯聪颖,张诗韵,孙建安,*,王 卉(.中国海洋大学食品科学与工程学院,山东青岛 266003;2.海南热带海洋学院食品科学与工程学院,海南三亚 572022)
近年来,食源性疾病的爆发日趋严重,因此寻找有效无毒的抗菌剂十分重要。植物精油作为天然提取物,安全性高,抗菌性能优良,因而备受青睐[1]。其中肉桂精油具有强烈的抑菌特性,可作为天然防腐剂用于食品行业[2-3],但因其具有较强的挥发性而在一定程度上限制了其应用,若将其制成凝胶微球则可有效的控制其挥发。
海藻酸钠是制备凝胶微球的一种常用材料,无毒,易降解,成本低,与Ca2+等二价金属阳离子相互作用,可制得凝胶微球,被广泛应用于药物装载领域[4-6]。但是海藻酸钠制成的凝胶微球机械强度低,遇水易溶胀,突释现象严重[7],为了解决这些问题,可采用不同的物理化学方法对海藻酸钠进行改性[8-10]。在海藻酸钠中加入低成本的无机材料是克服海藻酸钠凝胶微球缺陷的较佳方式,膨润土的主要成分是蒙脱石,蒙脱石具有独特的空间结构和阳离子交换特性,且具有高的弹性模量,可以增强聚合物的机械强度和稳定性[11-12]。同时,膨润土安全性高,对人体无害,其有效成分蒙脱石可作为药物及药物缓释载体使用,例如卢建华等[13]的研究表明双歧三联活菌片结合蒙脱石散可以治疗儿童腹泻,提高机体免疫力。Kawase等[14]研究表明蒙脱石可以保护质粒DNA不受胃内酸性环境和肠内DNA降解酶的影响,成功将其送入到小肠细胞。例如Zhao等[15]设计了基于蒙脱石的聚合物纳米颗粒,可以用来局部给药治疗青光眼,可递送足够浓度的药物,且对绒毛膜尿囊膜的刺激性非常小。将其与海藻酸钠共混改性制成的凝胶微球,机械性能更佳,能够更好的控制药物的释放[15-17]。
目前,研究人员对海藻酸钠和膨润土共混改性主要应用于农业,工业领域,例如周红军等[18]将改性膨润土和海藻酸钠复合制作成的凝胶微球可以有效提高毒死蜱的释放性能。Shawky[19]以蒙脱石和海藻酸钠为材料制作而成的珠粒用来除去水溶液中的铅,从而改善水质等。但是对于其在食品领域尤其是针对挥发性精油的缓释控制研究较少。因此,在本研究中,将海藻酸钠中加入膨润土进行混合改性,包封肉桂精油,优化得到复合凝胶微球的最佳制备条件,然后在不同的条件进行肉桂精油的释放实验,最后用零级,一级,Higuchi,Ritger-Peppas,Noyes-Whitney以及Hixson-Crowell动力学模型对释放曲线进行拟合[20-25],以期扩大肉桂精油在今后食品领域的应用,并提供一定的理论指导。
1 材料与方法
1.1 材料与仪器
海藻酸钠、硝酸钾、氯化钙、硝酸钾、氯化钠、溴化钾 均为国产分析纯,国药集团化学试剂有限公司;膨润土 含量>80%,浙江丰虹新材料有限公司;肉桂精油 食品级,上海麦克林生化科技有限公司;无水乙醇 分析纯,西陇科学股份有限公司。
JY99-IIDN高速分散机 宁波新芝生物科技股份有限公司;HWS-26超级水浴锅 金力永磁坛市仪器制造有限公司;LT-DBXF精密可编程热风循环鼓风干燥箱 立德泰勀(上海)科学仪器有限公司。
1.2 实验方法
1.2.1 海藻酸钠/膨润土(SA/BT)凝胶微球的制备 于55 ℃配制2%海藻酸钠溶液,在其中加入1%(w/v)的膨润土,8000 r/min分散5 min,超声20 min,放置3 h使膨润土进行充分溶胀,加入肉桂精油(与载体的比例为2∶1)以及0.2%的tween-80,再将混合液8000 r/min分散5 min,形成均匀的乳白色液体后,用注射器以距离液面30 cm的距离滴入1.5%的CaCl2溶液中,静置45 min,用蒸馏水反复清洗3~5次,于40 ℃干燥箱中干燥5 h至重量无明显变化。
1.2.2 单因素实验
1.2.2.1 海藻酸钠浓度对包封率的影响 保持膨润土添加量1%(w/v)、肉桂精油与载体的比例为2∶1、CaCl2浓度为1.5%、tween-80浓度为0.2%,分别配制0.5%、1%、2%、3%、4%海藻酸钠溶液,制备凝胶微球并测定其包封率。
1.2.2.2 膨润土添加量对包封率的影响 保持海藻酸钠的浓度为2%、肉桂精油与载体的比例为2∶1、CaCl2浓度为1.5%、tween-80浓度为0.2%,分别添加0.5%、1.0%、1.5%、2.0%、2.5%(w/v)膨润土,制备凝胶微球并测定其包封率。
1.2.2.3 肉桂精油与载体的比例对包封率的影响 保持海藻酸钠的浓度为2%、膨润土添加量为1%、CaCl2浓度为1.5%、tween-80浓度为0.2%,保持肉桂精油与载体的比例分别为0.5∶1、1∶1、2∶1、3∶1、3.5∶1,制备凝胶微球并测定其包封率。
1.2.2.4 CaCl2浓度对包封率的影响 保持海藻酸钠的浓度为2%、膨润土添加量为1%、肉桂精油与载体的比例为2∶1、tween-80浓度为0.2%,分别配制CaCl2浓度为0.5%、1.5%、2.5%、3%、3.5%,制备凝胶微球并测定其包封率。
1.2.2.5 tween-80浓度对包封率的影响 保持海藻酸钠的浓度为2%、膨润土添加量为1%、肉桂精油与载体的比例为2∶1、CaCl2浓度为1.5%,分别配制浓度为0.50%、0.10%、0.15%、0.20%、0.25%的tween-80水溶液,制备凝胶微球并测定其包封率。
1.2.3 响应面试验 根据各个因素对包封率的影响,选取海藻酸钠浓度、肉桂精油与载体比例、膨润土添加量三个因素进行响应面实验,优化得到最佳的制备条件以及相应的参数及方程。用Design-Expert软件进行试验设计[26],因素与水平表如表1所示。
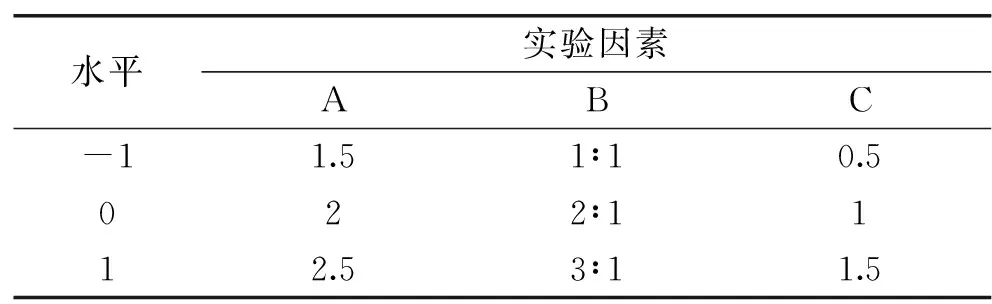
表1 试验因素与水平表Table 1 Experimental factors and level table
1.2.4.1 测定波长的选择 取0.5 mL肉桂精油加入到50 mL的容量瓶中并用无水乙醇定容,取该定容好的溶液0.5 mL于50 mL容量瓶并定容,再取第二次定容好的溶液1.0 mL定容至50 mL。以无水乙醇作为空白溶液对照,取最终定容好的溶液在240~350 nm下进行波长扫描,得到肉桂精油的最大吸收波长为287 nm[27-28]。
1.2.4.2 肉桂精油标准曲线的制作 分别取上述第二次定容好的溶液0.5、0.75、1.0、1.25、1.5 mL,并在50 mL容量瓶定容,测定最大吸收波长下的吸光度值,得到肉桂精油浓度与吸光度值的关系[27-28],即标准曲线,(R2=0.999)。
1.2.4.3 肉桂精油含量及包封率的计算 凝胶微球中肉桂精油含量测定方法:称取0.05 g凝胶微球,加入一定量的无水乙醇,研磨至完全破碎,然后超声功率360 W条件下超声15 min,使其完全破壁溶解。过滤,将滤液定容至50 mL,取一定量定容后的溶液稀释至合适的倍数,在最大吸收波长下测定其吸光度,并根据标准曲线计算凝胶微球中肉桂精油含量[27-28]。并按照下式计算包封率:

1.2.5 不同温度缓释实验 响应面试验优化后得到最佳制备条件下制备海藻酸钠/膨润土(SA/BT)包封肉桂精油的凝胶微球,同时以单一海藻酸钠(SA)包封肉桂精油的凝胶微球为对照比较两者的释放性能。分别取称取干燥后的两种凝胶微球0.05 g若干份置于玻璃平皿中,放置在室温(25 ℃)和温度分别为40、60、80 ℃的鼓风干燥箱中模拟凝胶微球在不同温度下的释放[29],每隔一段时间后测量凝胶微球中肉桂精油的含量,按照下式计算肉桂精油的累积释放量,以横坐标为释放时间,纵坐标为累积释放量,绘制释放动力学曲线。
累积释放量(%)=(1-某一测量时刻每份凝胶微球中肉桂精油含量/每份凝胶微球原始肉桂精油含量)×100
1.2.6 不同湿度缓释实验 配制饱和的溴化钠(模拟相对湿度为55%环境)、氯化钠(模拟相对湿度为75%环境)、硫酸钾(模拟相对湿度为90%环境)放入干燥器底部,称取0.05 g凝胶微球若干份放入玻璃平皿中,并将玻璃平皿置于干燥器中,密封[30]。每隔一段时间测定每份凝胶微球中肉桂精油的含量。计算累积释放量,绘制释放动力学曲线。
1.2.7 释放模型拟合 分别用零级,一级,Higuchi,Ritger-Peppas,Noyes-Whitney以及Hixson-Crowell动力学模型进行拟合,得到拟合方程和决定系数[31-33]。
1.3 数据处理
实验数据为三次平行实验测定结果,采用SPSS 22软件进行显著性分析,采用Origin 9.1软件拟合释放曲线并进行分析,Origin 9.1软件绘图。
2 结果与分析
2.1 各因素对凝胶微球包封率的影响
2.1.1 海藻酸钠浓度对凝胶微球包封率的影响 图1为海藻酸钠浓度对凝胶微球包封率的影响。当海藻酸钠滴入Ca2+溶液中时,海藻酸钠分子与Ca2+作用形成凝胶微球。海藻酸钠的粘度直接决定凝胶微球的质量,海藻酸钠的粘度随着其浓度的增加而加大。当海藻酸钠浓度足够高时,生成的凝胶微球才能保持好的球形。当浓度较低时,微球受两相接触碰撞影响较大,会影响其质量[32]。因此海藻酸钠浓度的选择至关重要。由图1可知,作为载体材料之一的海藻酸钠,对包封率的影响较大,随着海藻酸钠的浓度的增加,包封率呈现先增加后减小的趋势。当浓度达到2%时,包封率达到最高,为79.64%。原因是海藻酸钠浓度较低时,形成的网络结构比较松散,不稳定,导致成型效果不佳,包封率也很低。海藻酸钠浓度过高时,形成致密坚硬的网络结构,海藻酸钠微球可提供给肉桂精油的空间有限,一定程度上减少了对肉桂精油的包封率。同时,海藻酸钠各个浓度对包封率的影响差异性显著(P<0.05)。
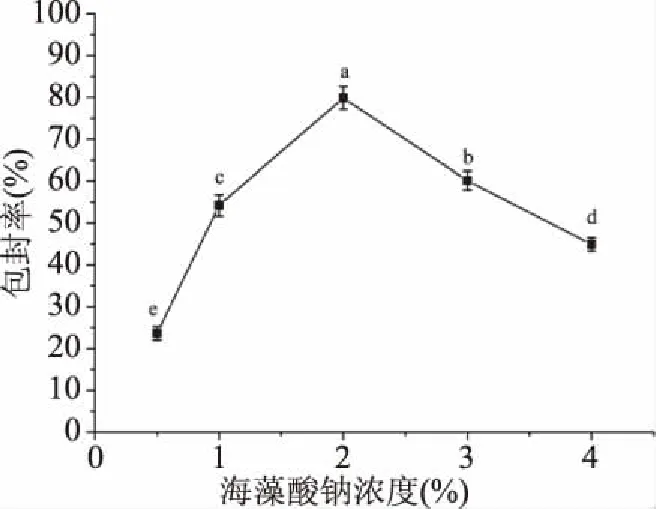
图1 海藻酸钠浓度对凝胶微球包封率的影响Fig.1 Effect of sodium alginate concentration on encapsulation efficiency of gel microspheres注:不同小写字母表示显著性差异(P<0.05);图2~图5同。
2.1.2 膨润土添加量对凝胶微球包封率的影响 由图2可知,随着膨润土添加量的加大,包封率先增加后降低,在添加量为1.0%时达到最高,为79.64%。由于膨润土具有吸附性较好,具有较高的弹性模量,可增强凝胶微球的机械强度和对肉桂精油的包封率[35-36]。所以随着膨润土添加量的增加,会增大凝胶微球的包封率,在添加量为1.0%时效果最佳。膨润土中含有大量的羟基,可以与海藻酸钠相互作用形成氢键,但是当膨润土添加的量继续增加时,会造成膨润土的团聚,与海藻酸钠氢键作用力的减少,使复合载体产生缺陷,导致包封率的下降[18,36]。在膨润土的添加量为1.0%时,凝胶微球的包封率为79.64%,同时各个添加量之间的差异性显著(P<0.05)。
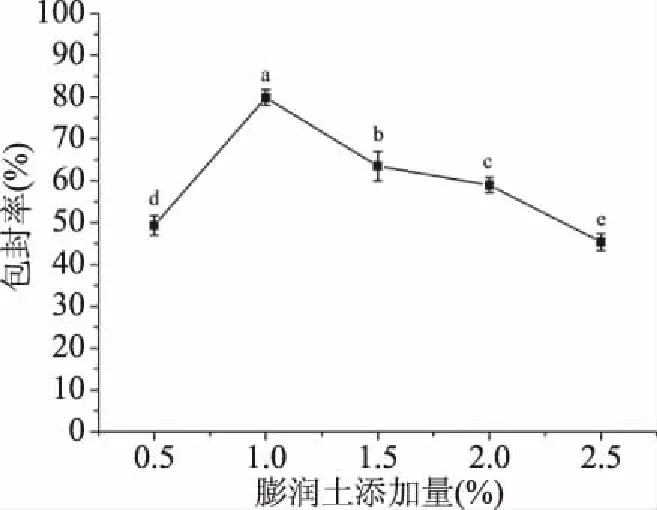
图2 膨润土添加量对凝胶微球包封率的影响Fig.2 Effect of the addition amount of bentonite on the encapsulation efficiency of gel microspheres
2.1.3 肉桂精油与载体比例对凝胶微球包封率的影响 肉桂精油与载体的比例对微球的包封率影响如图3所示。随着两者比例的增加,包封率先增加后降低,两者比例达到2.0∶1的时候包封率达到最高。理论上,两者比例越大,肉桂精油被包封进去的可能性就越大,所以刚开始随着两者比例的增加,包封率呈现上升趋势。同时,凝胶微球颜色较透明,这是因为肉桂精油添加量较少,使得载体的颜色相对比较明显。随着两者比例的增大,凝胶微球乳白色加深。当两者的比例大于2.0∶1时,由于载体有一定的包封能力,因此增加肉桂精油量过多会使其没有办法全部被包封,容易造成其流出,部分没有被包封的肉桂精油漂浮在CaCl2溶液中,造成精油浪费,包封率下降[27-28]。在两者比例为2.0∶1时,包封率最高,为79%,且各个比例之间的差异性显著(P<0.05)。
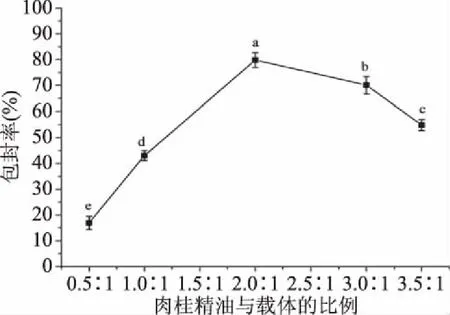
图3 肉桂精油与载体的比例对凝胶微球包封率的影响Fig.3 Effect of the ratio of cinnamon oil to carrier on the encapsulation efficiency of gel microspheres
2.1.4 CaCl2浓度对凝胶微球包封率的影响 CaCl2作为凝胶微球成型的重要阳离子供体,它的浓度也会影响凝胶微球的包封率。随着CaCl2的浓度增加,被交联的海藻酸钠增多,形成更多的三维网络结构,包封率也随之上升,在1.5%时达到最高,为79.68%,当CaCl2的浓度继续增加,凝胶微球表面硬度增加,包封率也呈下降趋势。其原因是当CaCl2的浓度过大时,凝胶微球的外层会首先形成致密的网状结构,外层迅速凝固,对CaCl2进入内层有了一定的阻碍作用,不利于凝胶微球的形成,造成了包封率的降低[6],同时,不同CaCl2浓度之间的差异性显著(P<0.05)。
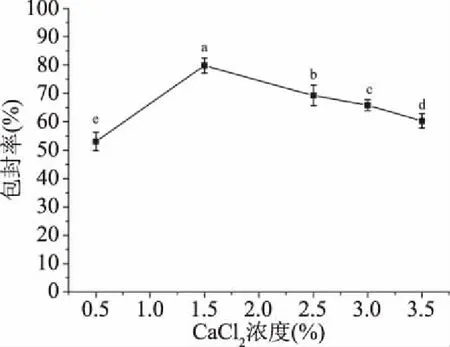
图4 CaCl2浓度对凝胶微球包封率的影响Fig.4 Effect of CaCl2 concentration on the encapsulation efficiency of gel microspheres
2.1.5 tween-80浓度对凝胶微球包封率的影响 tween-80作为乳化剂,起到乳化载体与肉桂精油的作用,由图5可知,其对凝胶微球的包封率的影响较小,随着tween-80浓度的增加包封率先增加后减小,在浓度为0.2%的时候微球包封率达到最高,在79.27%。乳化剂浓度较低时,乳化力不足,乳化效果和乳液稳定性不佳,精油不能完全被乳化剂分子乳化,会造成包封率的达不到最大值,但是乳化剂的过多使用也会造成包封率有一定的下降,这可能与乳化剂过多使用破坏乳液稳定性,从而导致凝胶微球包封率的下降[37-39]。同时,tween-80浓度在0.05%和0.25%差异性不显著(P>0.05),其他浓度差异性显著(P<0.05),说明乳化剂浓度过高或者过低均会造成凝胶微球的包封率的降低。
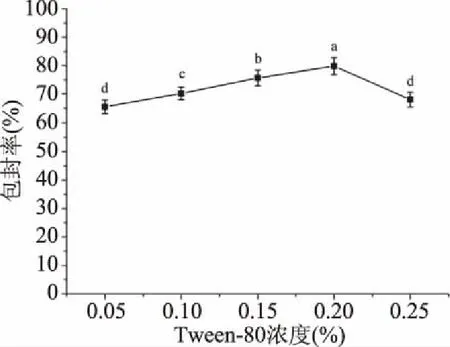
图5 Tween-80浓度对包封率的影响Fig.5 Effect of tween-80 concentration on encapsulation efficiency of gel microspheres
2.2 响应面试验
通过对表2的实验数据进行多元化回归方程分析,得到包封率的回归方程为:
包封率(%)=-230.55+230.11A+65.59B+16.38C-1.65AB-0.86AC-1.63BC-55.78A2-14.51B2-4.00C2
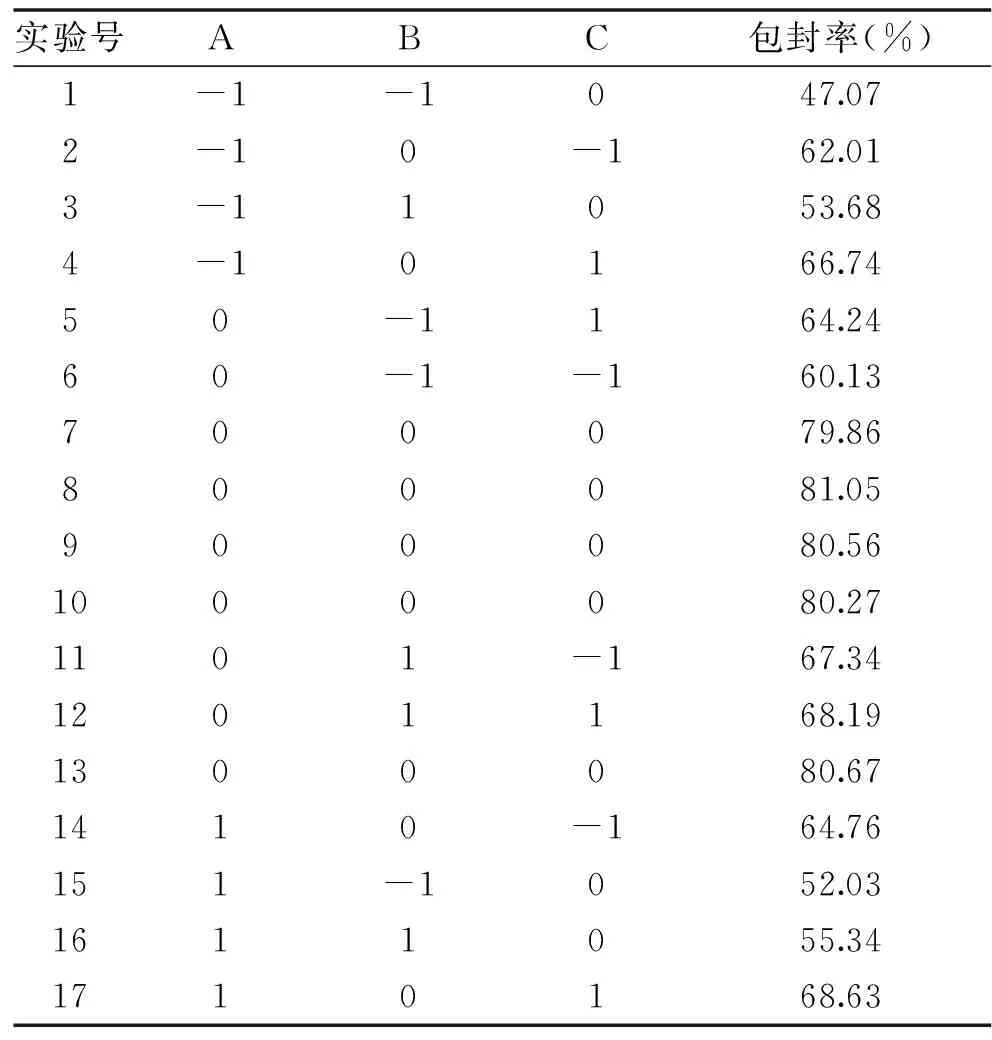
表2 试验设计结果Table 2 Experimental design results
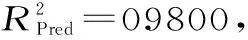
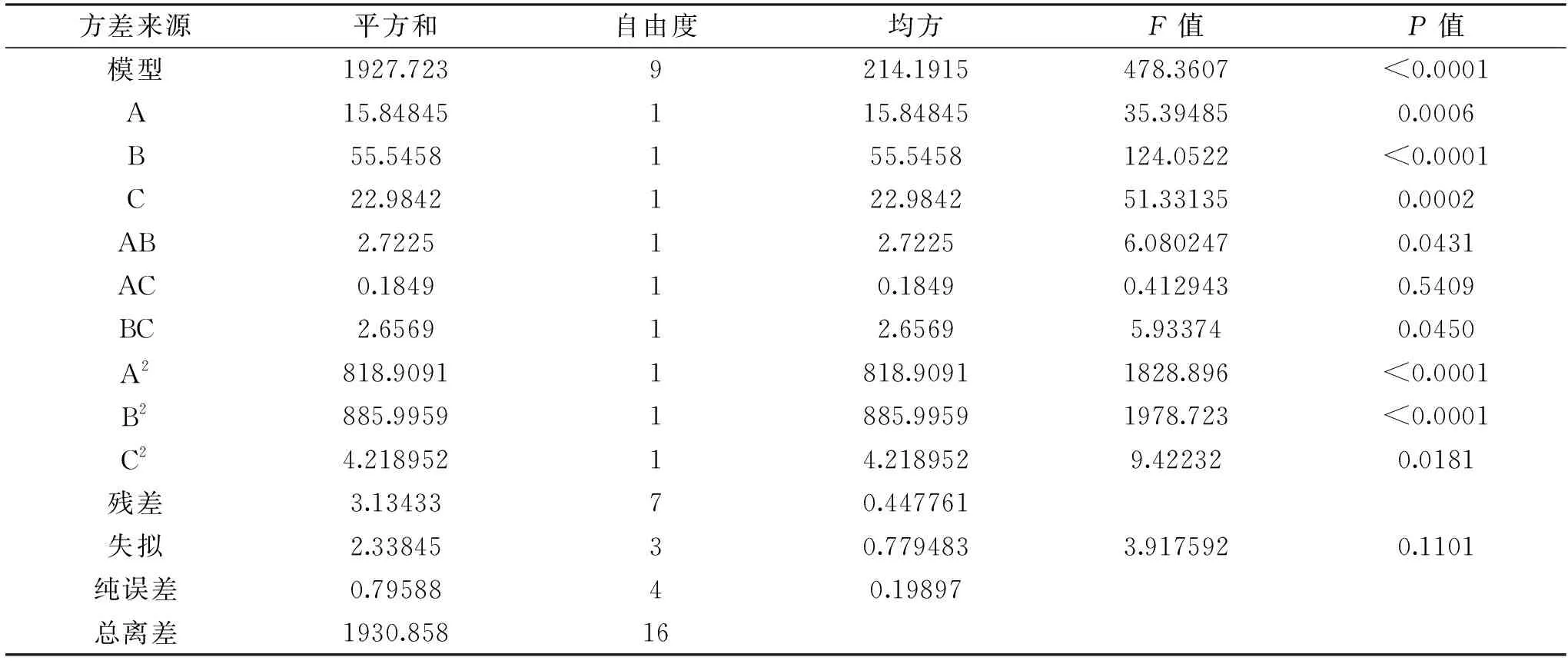
表3 包封率回归模型方差分析表Table 3 Encapsulation rate regression model analysis of variance
通过响应面试验分析,软件预测的最佳制备条件为海藻酸钠浓度2.02%,肉桂精油与载体的比例2.07∶1,膨润土的添加量1.1%,包封率为80.92%,考虑到实际实验条件,将条件调整为海藻酸钠浓度2%,肉桂精油与载体的比例2.1∶1,膨润土添加量为1.1%,在此条件下验证实验得到的包封率为80.74%,与预测值相差较小,模型可靠。
2.3 缓释实验结果
2.3.1 不同温度下的缓释动力学曲线 图6为25、40、60、80 ℃不同温度下的释放动力学曲线,以累积释放量来表示凝胶微球的释放效果。由图6可知,在各个温度下SA/BT的释放量均低于SA一组,表示膨润土的添加确有利于控制肉桂精油的释放。其中,SA和SA/BT的凝胶微球在25 ℃的条件下,84 d时累积释放量分别为31.61%和20.55%;40 ℃的条件下,78 d时累积释放量分别为34.1%和27.84%;60 ℃的条件下,48 d时累积释放量分别为45.83%和38.21%;80 ℃的条件下,在120 h时累积释放量分别为56.71%和42.71%。肉桂精油通过载体材料的微孔进行扩散,且随着温度的增加这种扩散作用增大,因此温度的升高,肉桂精油的挥发性增强,且其挥发释放过程呈现前期较快,后期较慢的趋势,在前期释放较快的过程中,由图6可知,SA/BT凝胶微球释放速率低于SA凝胶微球,因此膨润土的添加在一定程度上改善了单一的SA微球的突释现象,减慢了肉桂精油释放。
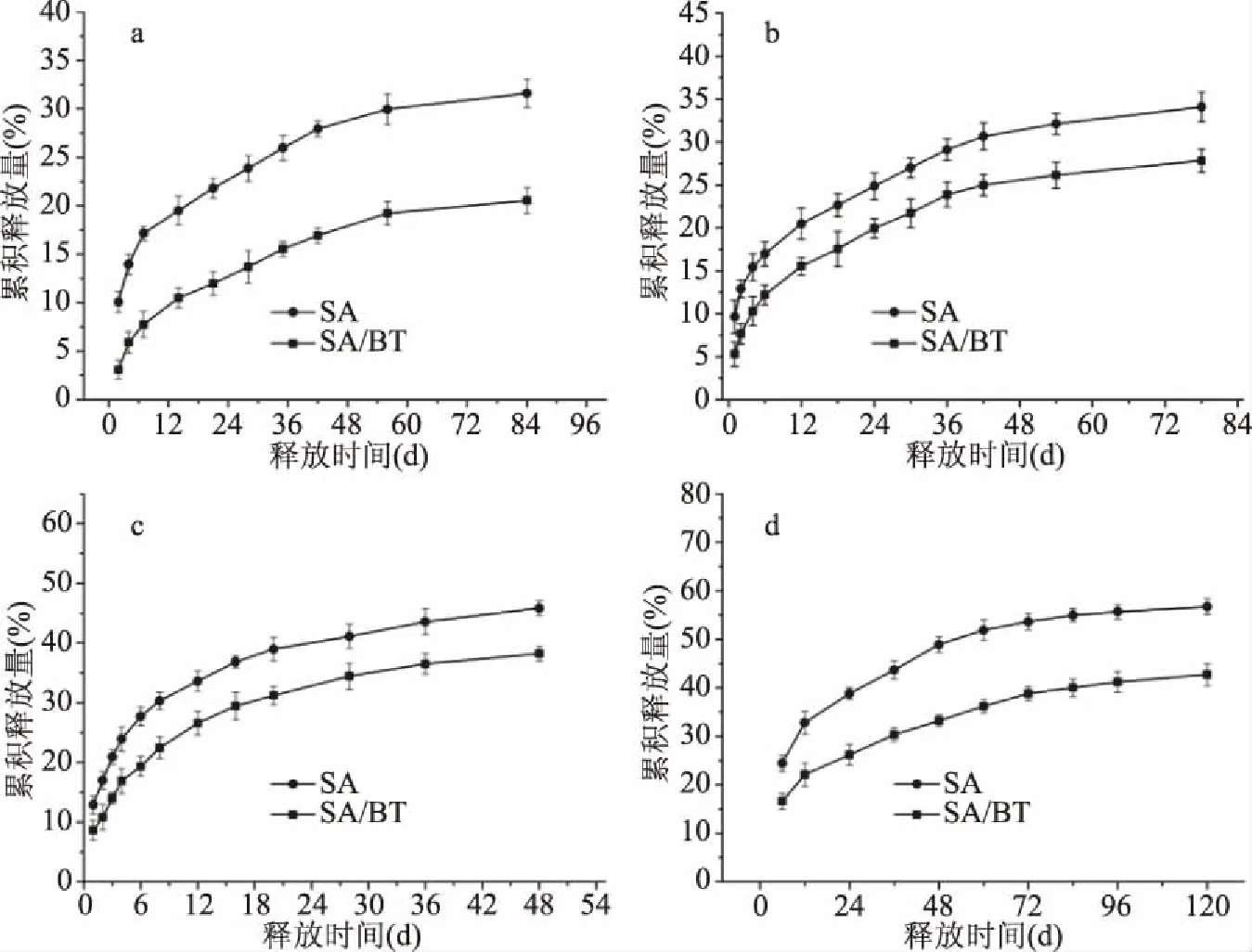
图6 不同温度释放动力学曲线Fig.6 Release kinetics curve at different temperatures 注:a:25 ℃;b:40 ℃;c:60 ℃;d:80 ℃。
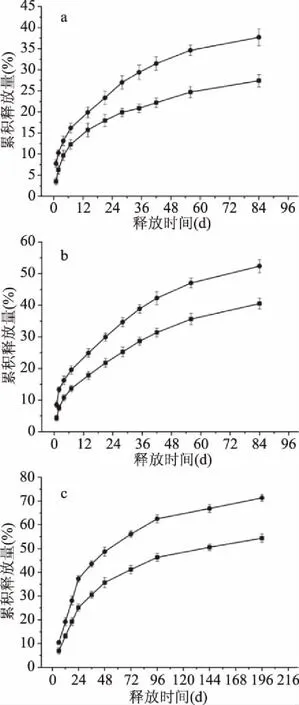
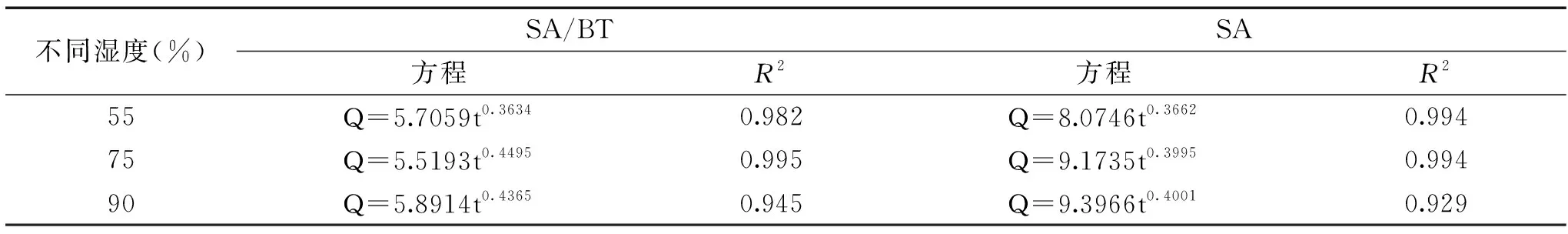
2.3.2 不同温度下缓释动力学模型拟合 将不同温度下的释放动力学曲线用零级,一级,Higuchi,Ritger-Peppas,Noyes-Whitney以及Hixson-Crowell动力学模型进行拟合后,发现Ritger-Peppas的决定系数R2的值高于其它的模型,所以Ritger-Peppas模型能更好的反应肉桂精油从凝胶微球中的释放。表4分别代表凝胶微球SA/BT和SA凝胶微球在25、40、60、80 ℃下Ritger-Peppas模型拟合之后的方程与决定系数(R2)。如表4所示。其中,释放机制与Ritger-Peppas释放模型中的释放因子n有关系,其中,在25 ℃时,SA/BT和SA凝胶微球的n值分别为0.4246,0.2844均小于0.45;40 ℃时两者的n值分别为0.4089,0.3017;60 ℃时两者的n值分别为0.3252,0.2983;80 ℃时两者的n值分别为0.3107,0.2655。当n≤0.45,药物释放机制为Fick自由扩散;当0.45 表4 不同温度下Ritger-Peppas释放动力学模型拟合结果Table 4 Fitting results of Ritger-Peppas release kinetic model at different temperatures 2.3.3 不同湿度下的缓释动力学曲线 图7为55%、75%、90%相对湿度下的释放动力学曲线。影响肉桂精油凝胶微球释放的因素除了环境温度外,环境湿度也是一个重要的因素。图7中分别为在相对湿度为55%,75%和90%的相对湿度下SA和SA/BT凝胶微球的释放动力学曲线。随着相对湿度的增加,释放速率同时呈现增加的趋势。 图7 不同相对湿度下释放动力学曲线Fig.7 Release kinetics curves at different relative humidity注:a:55%;b:75%;c:90%。 其中,SA和SA/BT凝胶微球在55%的相对湿度下,84 d时的累积释放量分别为37.71%和27.41%;在75%的相对湿度下,84 d时累积释放量分别为52.37%和40.52%;在90%的相对湿度下,192 h(8 d)时累积释放量分别为71.31%和45.63%。其过程均可以分为第一阶段的快速释放和第二阶段的缓慢释放,其中SA/BT凝胶微球的释放速率明显低于SA凝胶微球,对单一SA凝胶微球的突释现象有一定改善作用。随着湿度的增加,释放速率加快,可能是由于部分亲水性的聚合物溶胀导致了肉桂精油扩散距离缩短,导致其释放速率的增加。 2.3.4 不同湿度下缓释动力学模型拟合 同样将不同湿度下的释放动力学曲线用零级,一级,Higuchi,Ritger-Peppas,Noyes-Whitney以及Hixson-Crowell动力学模型进行拟合后,发现Ritger-Peppas动力学模型的决定系数R2值最高,拟合性最佳,所以Ritger-Peppas模型能更好的反应肉桂精油在不同的湿度下从凝胶微球中的释放。表5为SA/BT凝胶微球和SA凝胶微球在相对湿度为55%,75%,90%下不同释放动力学模型的拟合结果,拟合方程与决定系数R2如表格所示。其中,在55%相对湿度下,SA/BT和SA凝胶微球的n值分别为0.3634,0.3662;75%相对湿度下两者的n值分别为0.4495,0.3995;90%相对湿度下两者的n值分别为0.4365,0.4001;n值均小于0.45,说明肉桂精油的释放以Fick自由扩散为主。 表5 55%相对湿度下不同释放动力学模型拟合Table 5 Fitting of different release kinetic models at 55% relative humidity 通过单因素和响应面实验分析,得到了海藻酸钠/膨润土复合凝胶微球包封肉桂精油的最佳制备条件:海藻酸钠浓度2%,肉桂精油与载体的比例2.1∶1,膨润土添加量为1.1%,CaCl2浓度1.5%,tween-80浓度0.2%,包封率可达80.74%。同时,海藻酸钠/膨润土凝胶微球相对于单一海藻酸钠包封肉桂精油后在不同的温度和湿度条件下均能够更好的控制肉桂精油的挥发性,使其能够更长久的发挥作用,为肉桂精油在食品领域尤其是防腐保鲜方面的应用提供了一定的理论指导,但是需要对其应用的具体食品种类以及保鲜方式进行进一步的深入探究。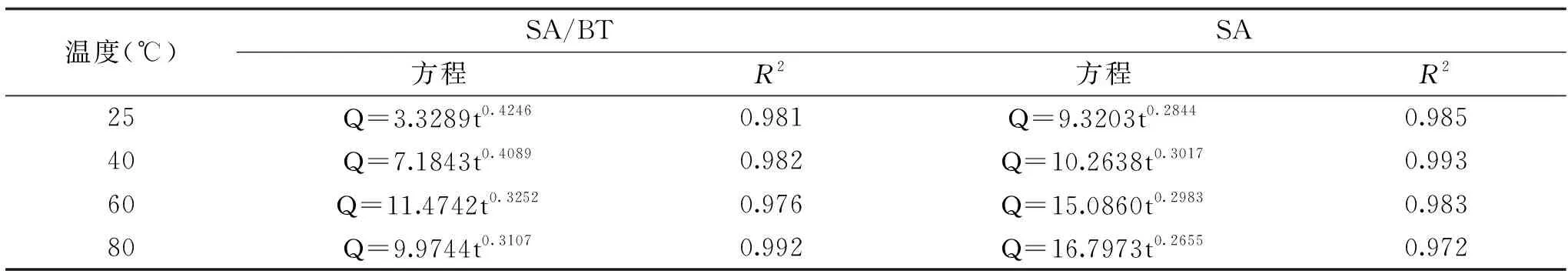
3 结论
