活性氧敏感型有机共价聚合物的制备及药物释放研究
2020-11-17丁谦,陈鹏,曹明
丁 谦,陈 鹏,曹 明
(安徽大学 化学化工学院,安徽 合肥 230601)
共价有机聚合物(covalent organic polymers,简称COPs)是一类共价有机分子组成的交联结合多孔网络结构,其具有比表面积大、组成与结构可控、易于修饰等特点,广泛应用于气体储存与分离、多相催化及光电转换等领域[1].近年来,通过网络结构中特有的纳米孔洞可高效负载抗肿瘤药物,在药物输送领域显示出巨大的优势.例如,Bai等[2]制备了一种孔径可控的共价有机聚合物,并负载不同种类的药物,结果显示该共价有机聚合物具有载药量高、生物相容性好和可控的药物释放等特点.Wang等[3]通过氨基与丙烯酸酯间的点击反应,设计合成了一种光敏感的共价有机聚合物,并负载了化疗药物阿霉素(DOX).体内研究结果显示COPs显著延长了DOX的血液循环时间,提高了DOX在肿瘤部位的富集.将化疗与光动力治疗结合,获得了优异的肿瘤抑制效率[3].Zhang等[4]制备了一种可降解且具有适宜尺寸的COPs,通过硅烷偶联剂稳定后可实现抗癌药物DOX的高效负载,并将PEG修饰姜黄素实现对其载药材料亲水性的修饰及荧光示踪.小鼠活体实验结果显示,在静脉注射后该纳米载体能有效在裸鼠肿瘤部位富集,显著增强抑瘤效果[4].
理想的药物载体是在血液循环过程中具有良好的稳定性并且有效地在肿瘤部位富集,而到达肿瘤组织后能将负载药物有效释放并到达作用靶点[5].如何解决这一对矛盾的要求是获得高效治疗的关键因素之一.近年来,在载体内引入光刺激响应性的官能团是一种有效的策略,可以增强药物在肿瘤细胞内释放的同时,降低药物在血液循环过程的泄露.目前,常见的刺激信号主要为内源性(酸度、氧化还原性和酶等)和外源性(光、声、磁场等)信号[6].其中,以光作为刺激响应信号,具有在特定时间和位置精确可控等优势,尤其是近红外光具有更深的组织穿透特点[7].因此,基于光刺激响应型纳米载体的构建并用于肿瘤的治疗,近年来得到了科研工作者的广泛关注.例如,Gurusamy等[8]制备了一种单线态氧敏感的乙烯基二硫醚的两亲嵌段共聚物的胶束,并包埋化疗药物和光敏剂.在可见光刺激下,单线态氧的生成不仅破坏了聚合物胶束增强化疗药物的释放,而且将光动力治疗与化疗相结合,显著增强肿瘤的治疗效果[8].Liu等[9]将化疗药物吉西他滨和光敏剂卟啉通过单线态氧敏感的硫缩酮键进行连接,实现了光刺激药物释放的化学疗法与光动力疗法的有机结合.Jin等[10]制备了一种具有光触发裂解的活性氧响应纳米药物,尺寸由大到小的转变有效增强药物在肿瘤内部的渗透性,并在胞内高效释放出化疗药物.
笔者通过光敏剂卟啉(TCPP)与乙烯基二硫化衍生物间的酯化反应,制备了一类光激发活性氧敏感型的共价有机聚合物(COPs),在其表面引入聚乙二醇以改善其水溶性,并物理包埋化疗药物DOX(图1).一方面,在光照条件下,基于光敏剂产生的活性氧破坏共价有机聚合物的结构,从而释放出内部包埋的化疗药物DOX,实现药物在光响应下的可控释放;另一方面,基于光敏剂产生的活性氧和化疗药物的协同作用,有望提高肿瘤的治疗效果.
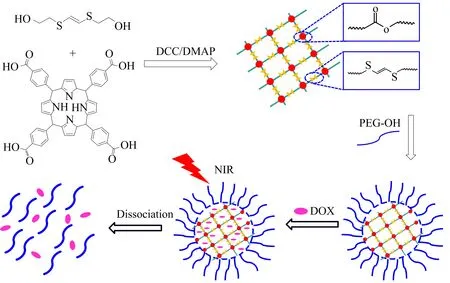
图1 COPs的合成、DOX负载及药物释放流程图
1 实验部分
1.1 实验试剂
聚乙二醇单甲醚2000(PEG2000)、2-巯基乙醇和顺1-2-二氯乙烯购自梯希爱(上海)化成工业发展有限公司;N,N-二甲基甲酰胺(DMF)、4-二甲氨基吡啶(DMAP)、N,N-二环己基碳酰亚胺(DCC)、二甲基亚砜(DMSO)、无水乙醚、磷酸二氢钠、磷酸氢二钠、三乙胺购自Aladdin;盐酸阿霉素,纯度为98%,购自安耐吉化学试剂有限公司;荧光探针(DCFH-DA)购自碧云天生物试剂公司;5,10,15,20-四(4-羧基苯基)卟啉购自北京华威锐科化工有限公司.
1.2 测试与表征
核磁共振氢谱(1H-NMR)AVANCE Ⅲ-400Hz型,德国Bruker,采用四甲基硅烷为化学位移的内标, 溶剂为氘代氯仿或氘代二甲基亚砜; 动态光散射(DLS)Zetasizer Nano ZS90型,英国Malvern,测量温度设为25 ℃,以二次水作为分散介质,平衡2 min, 测试前通过0.22 μm过滤器除尘处理,平行测量3次;傅里叶红外光谱仪(FTIR) iS50,美国Nicolet公司;荧光分光光度计F-2500型,日本Hitachi公司;紫外可见光谱(UV-Vis)UV-3600型,上海元析仪器有限公司;扫描电子显微镜(SEM) S-4800型,日本Hitachi公司,对样品表面喷金20 s后在加速电压5 kV下进行观测;透射电子显微镜(TEM) JEM-2100型,日本Hitachi公司,将样品溶液滴加到铜网表面,待烘干后在200 kV电压下观察.
1.3 实验步骤
1.3.1 2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇的合成
参照文献[8]合成2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇:将2-巯基乙醇(1.5 g,19.195 mmol)和NaOH固体(0.77 g,19.195 mmol)溶解在7.5 mL乙醇中,放入0 ℃冰浴中搅拌30 min,在N2保护氛围下,向上述溶液中缓慢滴加预先溶解的顺-1,2-二氯乙烯(0.93 g,9.6 mmol)乙醇溶液,80 ℃冷凝回流反应18 h(图2).然后,将溶液冷却至室温,先用饱和食盐水(20 mL)稀释,再用无水乙醚(3×10 mL)洗涤萃取.将合并的乙醚溶液用二次水(3×15 mL)洗涤,加入无水MgSO4干燥,通过旋转蒸发仪浓缩得到粗产物.通过柱色谱法纯化粗产物,洗脱剂使用乙酸乙酯/石油醚(70∶30)的混合物,所收集的产物溶液经旋干、真空干燥后,得到最终产物(Z)- 2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇,产率约70%.
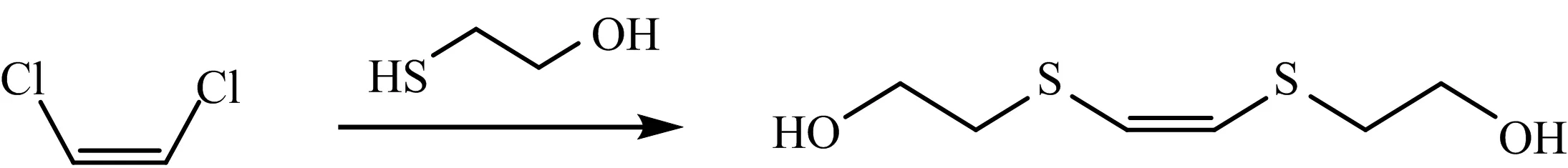
图2 2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇的合成示意图
1.3.2 共价有机聚合物(COPs)的合成
0.1 g 2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇与0.24 g TCPP溶解在10 mL N,N-二甲基甲酰胺(DMF)中(n-COOH∶n-OH=1.1∶1),随后向上述溶液中加入0.30 g DCC和0.089 g DMAP,40 ℃搅拌反应24 h.最后,向反应溶液中加入1.2 g的聚乙二醇单甲醚2000 (PEG-2000),将所得溶液转移到透析袋中,采用透析法除去未反应的单体和过量的PEG,透析液放入冷冻干燥机中冻干处理48 h,得到固体粉末COPs,并用棕色瓶收集且在4 ℃冰箱中避光冷藏保存.
1.4 单线态氧的检测
以二氯荧光素-二乙酸酯(DCFH-DA)定量分析ROS的产生效率[11].将0.5 mL的1 mmol·L-1DCFH-DA的乙醇溶液添加到2 mL的0.01 N NaOH中并室温下搅拌30 min,将DCFH-DA水解转化成二氯荧光素(DCFH).将DCFH用10 mL pH 7.4的PBS稀释,并保存在冰箱备用.配置COPs (1 mg·mL-1)与DCFH的混合溶液,在635 nm的光照条件下(0.2 W·cm-2),设定不同的时间间隔,在488 nm光激发下,测量溶液中的荧光变化,并收集490~700 nm的发射光谱.
通过1,3-二苯基异苯并呋喃(DPBF)作为捕获剂,对COPs材料产生单线态氧进行研究[12-13].取50 μL的DPBF(1 mmol·mL-1)加入3 mL的COPs (100 μg·mL-1)溶液中,在635 nm激光照射下(0.2 W·cm-2),每间隔20 s测定溶液的紫外可见吸收光谱.
1.5 共价有机聚合物负载DOX
称取25 mg COPs和10 mg DOX·HCl溶解于2 mL DMSO溶液中,加入15 μL的三乙胺,避光搅拌1 h.将混合溶液缓慢滴加到10 mL二次水中,继续避光搅拌24 h,混合溶液放入透析袋(截留分子量3 500),在pH=7.4的PBS(浓度为0.01 mol·L-1)中透析24 h,每隔4 h换1次透析液.最后,透析后的溶液在转速为5 000 r·min-1下离心分离10 min除去未包覆的DOX,得到载药聚合物溶液[14].DOX的载药率和载药效率参照以下公式进行计算.


1.6 DOX的体外释放
1.6.1 不同pH条件下的药物释放
取10 mL上述载药COPs溶液置于透析袋中(截留分子量3 500),分别浸入50 mL释放介质(PBS,pH 5.0,pH 7.4)的烧杯中,然后放置在37 ℃的水浴摇床中.按照设定的时间间隔,取出烧杯内2 mL的PBS缓冲溶液用于测定DOX并向烧杯中补加2 mL新鲜PBS缓冲液.通过紫外-可见分光光度计测量DOX在480 nm处的吸光度,根据测算的DOX的标准曲线计算样品的DOX浓度,从而反推出DOX药物的累计释放率.
1.6.2 光照与黑暗环境下的药物释放
取10 mL载药COPs溶液置于透析袋中(截留分子量3 500),再将透析袋置于2个50 mL的pH 7.4的缓冲溶液烧杯中,并放置在37 ℃的水浴摇床中.其中一个烧杯使用锡箔纸完全避光,另一个样品放置在635 nm的光照条件下(0.2 W·cm-2),按照设定的时间间隔,分别取出烧杯内2 mL的PBS缓冲溶液待测,并向烧杯中补加2 mL新鲜PBS缓冲液..通过紫外-可见分光光度计测量DOX在480 nm处的吸光度,依据DOX的标准曲线,再计算出DOX的释放比例[15-16].
2 结果与讨论
2.1 COPs的表征
对COPs的结构与形貌等进行分析,结果如图3所示.

图3 2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇 (a) 与COPs (b) 的1H-NMR 、FT-IR (c)、UV-Vis (d)、荧光发射光谱 (e)
由图3(a)所知,合成产物与设想产物结构相同,证明笔者成功合成了2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇.随后,基于TCPP与光敏剂卟啉与2,2′-(乙烯-1,2-二基双(磺胺二基))二乙醇间的酯化反应,一步法制备了光激发活性氧敏感型的COPs,并在其表面引入聚乙二醇以改善其水溶性(图1).通过核磁氢谱表征了COPs的结构,由图3(b)所示,经酯化反应后,可以看到PEG的化学位移(δ=3.3~3.8),在δ=7.8~9.8之间能观察到TCPP的特征化学位移.可能是COPs与PEG反应后形成的核壳结构,只能探测到表面的PEG,而内核结构的活动性下降并抑制了TCPP的化学结构信息[17].红外光谱结果表明,在1 720 cm-1处出现了羰基的伸缩振动峰(图3(c)),进一步表明了酯键的形成.紫外-可见光谱图显示,COPs具有TCPP的典型吸收峰 (图3(d)),且呈现出荧光淬灭(图3(e)).
接下来,笔者采用动态光散射(dynamic light scattering,简称DLS)仪、SEM 和AFM 对COPs的尺寸分布与形貌分析,结果如图4所示.

图4 COPs的DLS (a)、SEM (b) 和AFM (c) 表征
图4中,DLS结果显示COPs的平均流体动力学尺寸约为89 nm;SEM和AFM的结果表明COPs的微观形貌是球形颗粒,尺寸大小与DLS结果基本一致.
2.2 单线态氧的检测
以DCFH-CA为探针,活性氧能够氧化无荧光的DCFH生成具有绿色荧光的DCF,从而间接反映活性氧的产生效率;此外,笔者还采用了DPBF为探针,光照不同时间后,检测DPBF在415 nm处吸收峰的变化情况.结果如图5所示.
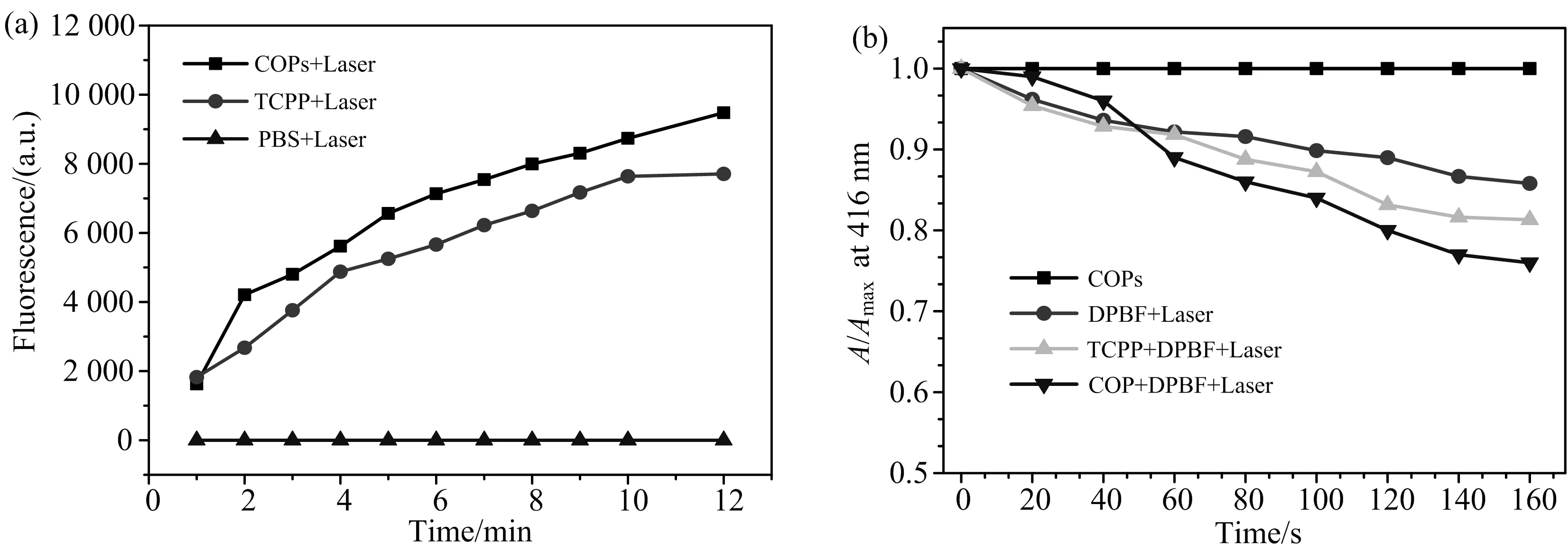
图5 DCF在530 nm处的荧光强度与时间变化曲线(a); DPBF吸光度与时间变化曲线(b)
由图5(a)可知,以缓冲溶液PBS为对照,在光照射情况下,卟啉的荧光强度会随着照射时间的增长而明显增大,且形成的COPs在TCPP当量浓度一致的情况下,COPs生成活性氧的效率更高.图5(b)显示了DPBF在415 nm处的吸收值随着照射时间的延长而逐渐减低,且COPs的吸光度降低程度更大,反映了COPs的活性氧生成效率更高,与DCFH的测试结果一致.以上结果表明:在COPs内部,由于疏水的卟啉分子彼此之间分离,降低了卟啉分子因聚集引起的活性氧自淬灭,且纳米多孔结构有利于提高ROS生成能力和扩散距离[18-19].
2.4 COPs的载药及体外释放研究
以DOX为模拟药物,通过透析法对DOX进行负载,并研究不同投料比对载药率和载药效率的影响,结果列于表1.
表1 投药比对载药效率与载药量的影响

投药比例(m(DOX)∶m(COPs))1∶81∶51∶2载药效率48.0642.65539.73载药率5.347.10213.24
由表1可以看出,以COPs为药物载体,对DOX具有高效的负载性能,随着投药比的增加,DOX的载药量逐渐增加,载药效率逐渐下降.当投药比为1∶2时,载药量和载药效率分别为13.24%和39.73%.一方面由于COPs的多孔网络结构利于DOX通过扩散作用进入其内部,另一方面COPs在制备过程中部分羧基未参与酯化反应,携带负电荷的COPs与DOX间通过静电作用结合(载药前后的表面电位由-33.6 mV转至-4.88 mV),从而达到对DOX的高效负载.后续实验中,选择投药比为1∶2时在不同pH、不同光照环境下DOX的释放性能,结果如图6所示.
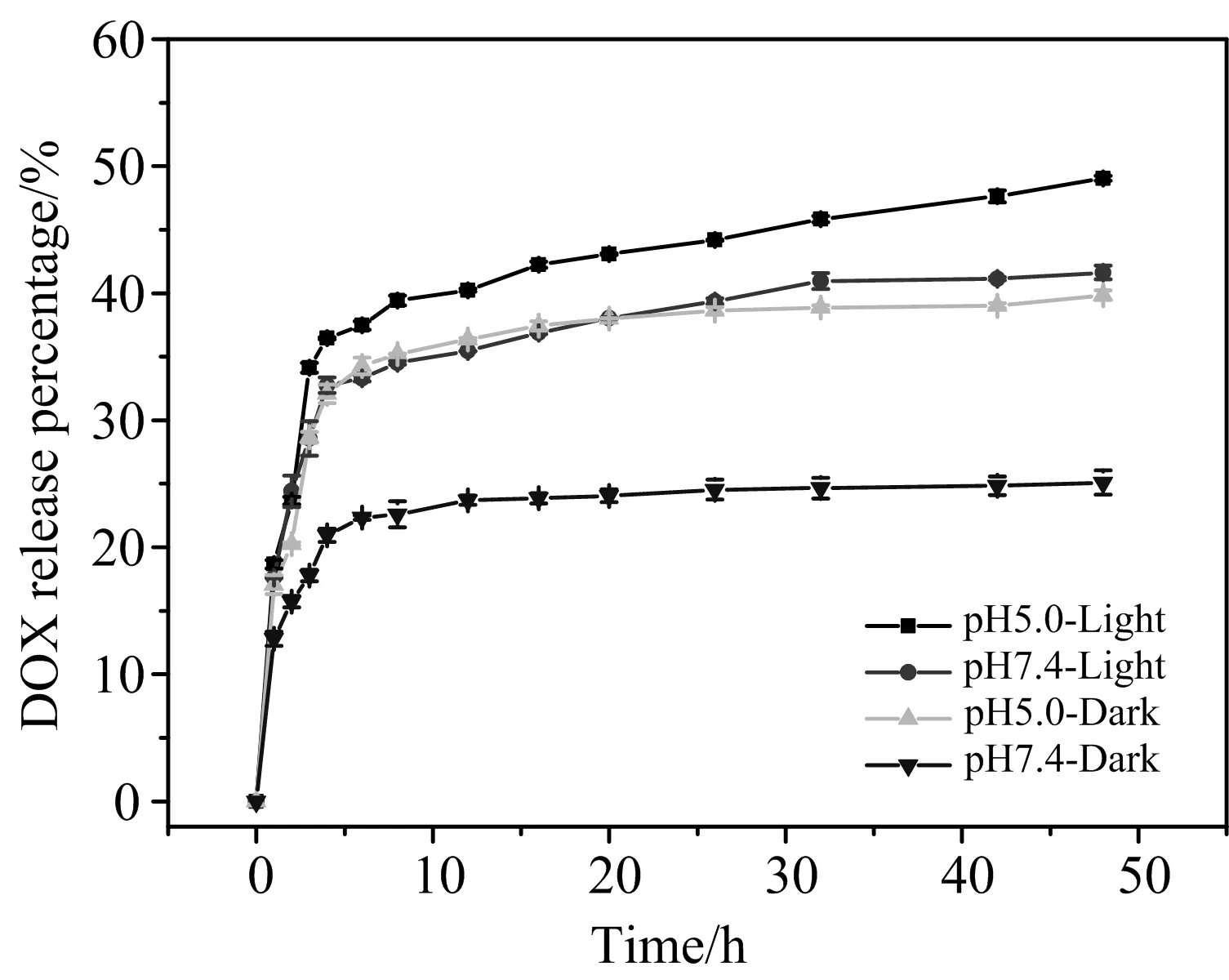
图6 负载DOX的COPs 在不同pH和光照下的药物释放曲线
由图6可以看出,与在pH 7.4环境下相比,弱酸环境下(pH 5.0)DOX的释放速率明显加快,48 h的累积药物释放比例接近50%,呈现出良好的pH 响应性.在酸性质子化的环境下,一方面DOX分子结构中的胺基质子化,提高了DOX的亲水性,另一方面COPs内部的羧基与DOX间的静电作用减弱,这些因素均会加速DOX在酸性环境下的释放速率.
在光照条件下(635 nm,0.2 W·cm-2),DOX与无光照条件下相比释放速度明显加快 (图6),48 h内的释放总量是无光照条件下的2倍.DOX在光照条件下的快速释放原因可能是光激发光敏剂TCPP产生活性氧,导致COPs内部的乙烯基二硫键的裂解,使得共聚物结构破坏.为了验证这样的设想,笔者通过透射电镜考察了COPs在光照前后的形貌变化,结果如图7所示.

图7 COPs的形貌在光照前(a)和光照后(b)的TEM图
由图7可以看出,光照前COPs的结构完整,而在光照2 min后,发现COPs的结构破坏,说明在光照刺激下COPs会产生结构解离,进而加速负载药物的释放.
3 结束语
(1) 笔者采用一步酯化反应法合成了COPs,通过探针法检测了COPs的活性氧产生效率,结果表明其内部的多孔结构降低了卟啉分子因聚集引起的活性氧自淬灭,提高了ROS的产生效率.
(2) 以DOX为模拟药物,采用透析法研究了COPs的载药及体外释放.结果显示COPs的多孔结构对DOX具有高效的负载效率,在投药比为1∶2的条件下载药量为13.24%.体外释放结果表明在弱酸环境(pH 5.0)和光照条件下,能显著增强COPs对DOX的释放效率.
