构建思维新模型 助力提升一轮复习备考效率——元素及其化合物知识复习新思路
2020-11-16江西张瑛美
江西 张瑛美
一、问题的提出
元素化合物模块知识是历年高考的必考知识点,在化学与传统文化、化学与STSE、高频考点阿伏加德罗常数、物质结构与元素周期律(表)、化学实验、化学工艺流程等具体题型中均有较多涉及,是高考考查基本理论、基本概念、实验设计和化学计量等主干考点的载体。该部分知识掌握的程度对进一步深化理解和掌握前面学习的概念性知识有着非常重要的作用,也是后续化学反应原理等相关知识学习的必备知识基础,该模块知识点多而复杂,学生学习完某一元素及其化合物的知识之后很难做到将所学的知识进行有条理性地梳理,很大一部分学生复习备考后条理不清,思维混乱,只能零星复述出其中的部分内容,这就使提取知识变得困难,从而影响解题速度。为此笔者经过大量研究和实践对该部分知识的教学模式进行大胆创新,构建出一套基于物质分类思维下的教学思路新模型。
二、物质分类思维下教学思路新模型的构建
根据《普通高中化学课程标准(2017版)》和《2019年普通高等学校招生全国统一考试大纲》对知识掌握的要求,笔者对元素及其化合物知识进行分析、总结后设计出如图1所示的教学思路总模型:

图1
讲解单质的存在形式时教师可基于物质分类,如游离态、化合态等思维角度分析物质的存在形式,如图2是单质硫基于物质分类思维角度构建的存在形式教学新思路。

图2
对于化合物知识在复习备考时很少涉及其在自然界中的存在形式,在复习备考时可复习其来源,例如在复习二氧化硫的性质时,可将“存在形式”修正为“主要来源”,经修正后二氧化硫的主要来源为化石燃料的燃烧及含硫矿石的冶炼,因此对于化合物模块知识的复习,这8个方面中的存在形式这一条可进行修正或略过,直接从物理性质开始复习,物理性质主要从状态、颜色、水溶性等思维角度分析。
化学性质是元素及其化合物知识复习备考中的重难点,学生很难系统且熟练地掌握物质的化学性质,基于此,笔者通过对所有元素及其化合物的化学性质进行分析和归纳后,从物质分类,如单质、氧化物、过氧化物、酸、碱、盐等思维角度,构建了如图3所示的物质化学性质教学思路模型,也是物质分类法思维在该模型下的核心应用,从单质出发,逐步寻找反应物,能很好地解决学生因思维混乱而对元素及其化合物化学性质难于重现的问题,笔者通过对元素及其化合物中的所有物质的化学性质进行全面的梳理后总结出了每种单质或化合物需要考虑的主要反应物,在图3中已一一列出;第7个方面(物质特有的化学性质)主要是为了解决部分物质具有特殊化学性质而设计,例如HClO具有氧化性漂白,SO2具有非氧化性漂白等,在实际教学过程中可根据具体物质的特性需要进行修正。
图3
图1所示的教学思路总模型共计8个方面,这8个方面层层递进,例如保存和用途是建立在物理和化学性质基础上的,因此在讲授物理性质和化学性质时,可得出物质的用途和保存方法,如氨气有极易液化的特点,因此可作制冷剂;过氧化钠与二氧化碳反应可生成氧气,因此可作供氧剂;物质的检验需要在掌握其化学性质的基础上才能进行,因此放在化学性质之后;物质制备主要包括反应原理、净化和收集等,涉及物质的物理性质和化学性质,制备过程中还涉及物质检验,因此放在检验之后;第7条为了解决如二氧化硫等物质,还涉及该化合物的污染与防治,具体在教学时可根据复习备考的物质需要进行修正;第8条习题巩固是为了在课后进一步巩固该课时所复习的内容而设计,习题的选择和布置根据复习内容和学生情况而定。
三、例析新模型思维下元素及其化合物教学新思路
【例1】金属钠教学新思路
金属钠是元素及其化合物知识的开篇内容,对该部分知识的教学设计模式进行大胆创新,构建出一套新的教学设计新模式,可对后续元素及其化合物的学习将起到参考与借鉴作用。金属钠与金属单质不反应,可形成合金,则化学性质的第1条应修正为与非金属单质反应;与金属氧化物不反应、与过氧化物的反应不要求掌握,无特殊化学性质,则化学性质修正简化为5个方面,综上金属钠的教学新思路模型设计如图4所示:
图4
完善图4模型得金属钠的教学新思路如下:
课题:金属钠的教学新思路
2.物理性质
(1)软—质软,硬度小
(2)亮—银白色,有金属光泽
(3)轻—密度比水小,比煤油大
(4)低—熔点低
(5)导—可导电、导热
3.化学性质
(1)与非金属单质反应
①与O2反应:
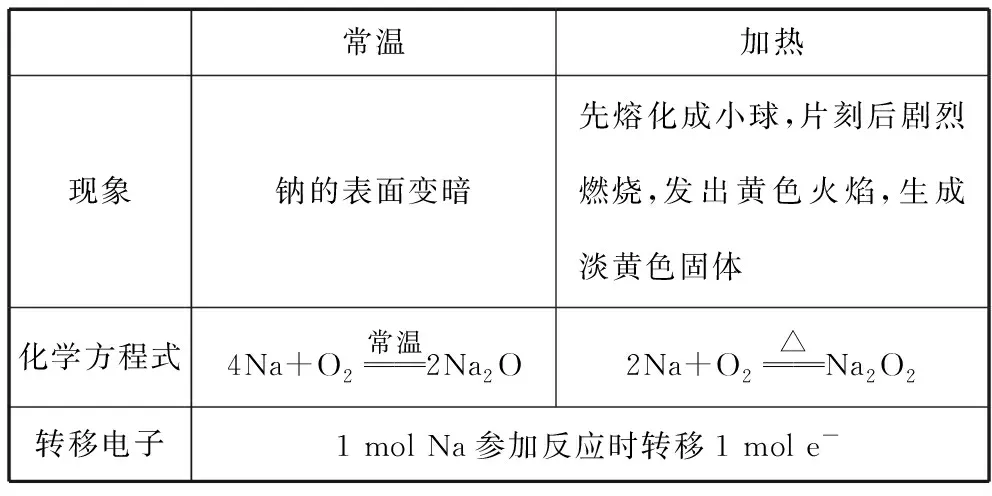
常温加热现象钠的表面变暗先熔化成小球,片刻后剧烈燃烧,发出黄色火焰,生成淡黄色固体化学方程式4Na+O2常温2Na2O2Na+O2△Na2O2转移电子1 mol Na参加反应时转移1 mol e-
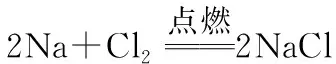
(2)与氧化物反应,以钠与水反应为例

②与滴加酚酞的水反应的现象与解释:

(3)与酸溶液反应
①与酸溶液反应时,先与酸反应,酸反应完全后与酸中的水反应。

(4)与碱溶液反应,以钠与碱溶液中水反应为例
(5)与盐溶液反应
①与盐溶液反应时,与盐溶液中的水先反应,生成的NaOH再与盐反应。
②与CuSO4溶液的反应:



4.保存与用途
(1)保存:密封保存,通常保存在煤油或石蜡油中。
(2)钠的用途
①制取Na2O2等化合物。
②钠钾合金呈液态可用于原子反应堆的导热剂。
④用作电光源,制作高压钠灯。
5.检验,以焰色反应为例
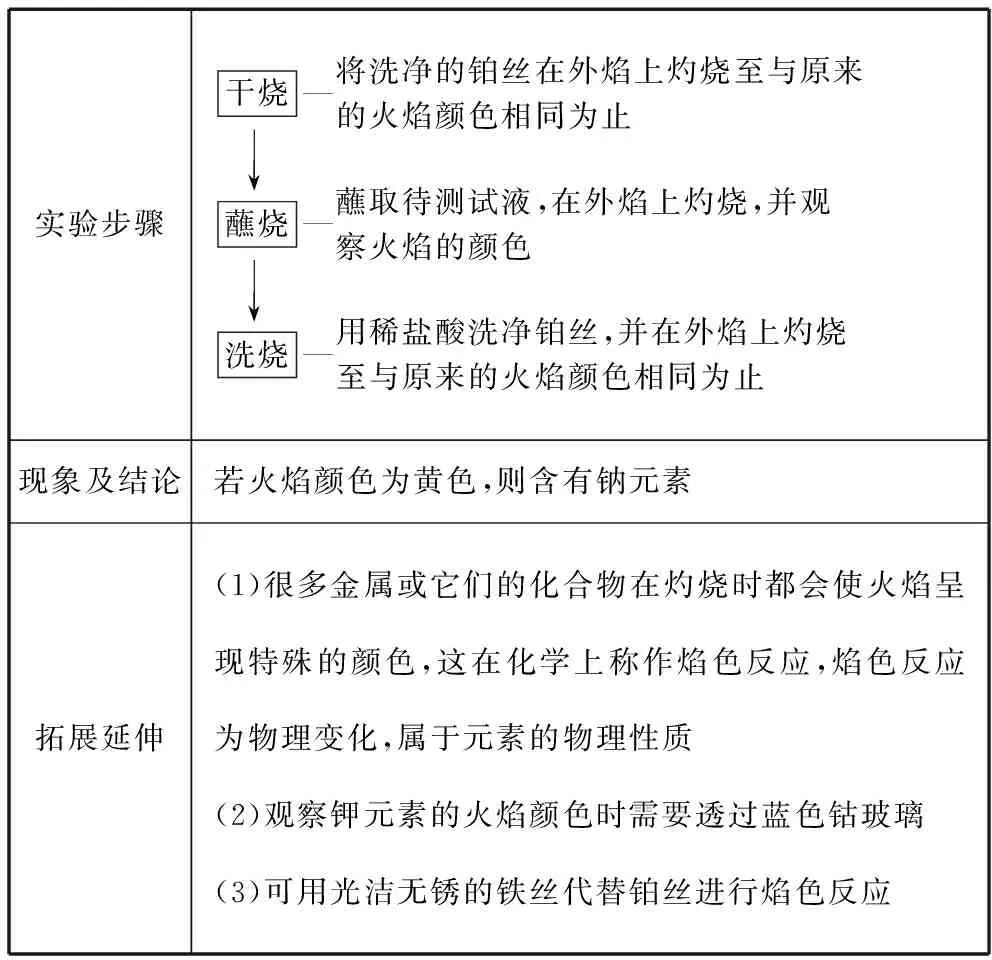
实验步骤干烧—将洗净的铂丝在外焰上灼烧至与原来的火焰颜色相同为止 ↓蘸烧—蘸取待测试液,在外焰上灼烧,并观察火焰的颜色 ↓洗烧—用稀盐酸洗净铂丝,并在外焰上灼烧至与原来的火焰颜色相同为止现象及结论若火焰颜色为黄色,则含有钠元素拓展延伸(1)很多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这在化学上称作焰色反应,焰色反应为物理变化,属于元素的物理性质(2)观察钾元素的火焰颜色时需要透过蓝色钴玻璃(3)可用光洁无锈的铁丝代替铂丝进行焰色反应
6.制备,钠单质的制备方法为电解熔融氯化钠
7.习题巩固
布置的课后习题形式多样,题型、题量视复习内容和学生情况而定,考查内容上应涵盖所复习内容中的重难点、学生的易错点进行,复习模块知识在高考中有具体的考题,也可将历年具体高考题作为课后习题的一部分,使用一轮复习资料书进行教学的可直接布置一轮复习资料书中相应的配套的习题即可。
为使新教学思路更为简洁明了,以上内容也可用新思路模型表示如图5所示:
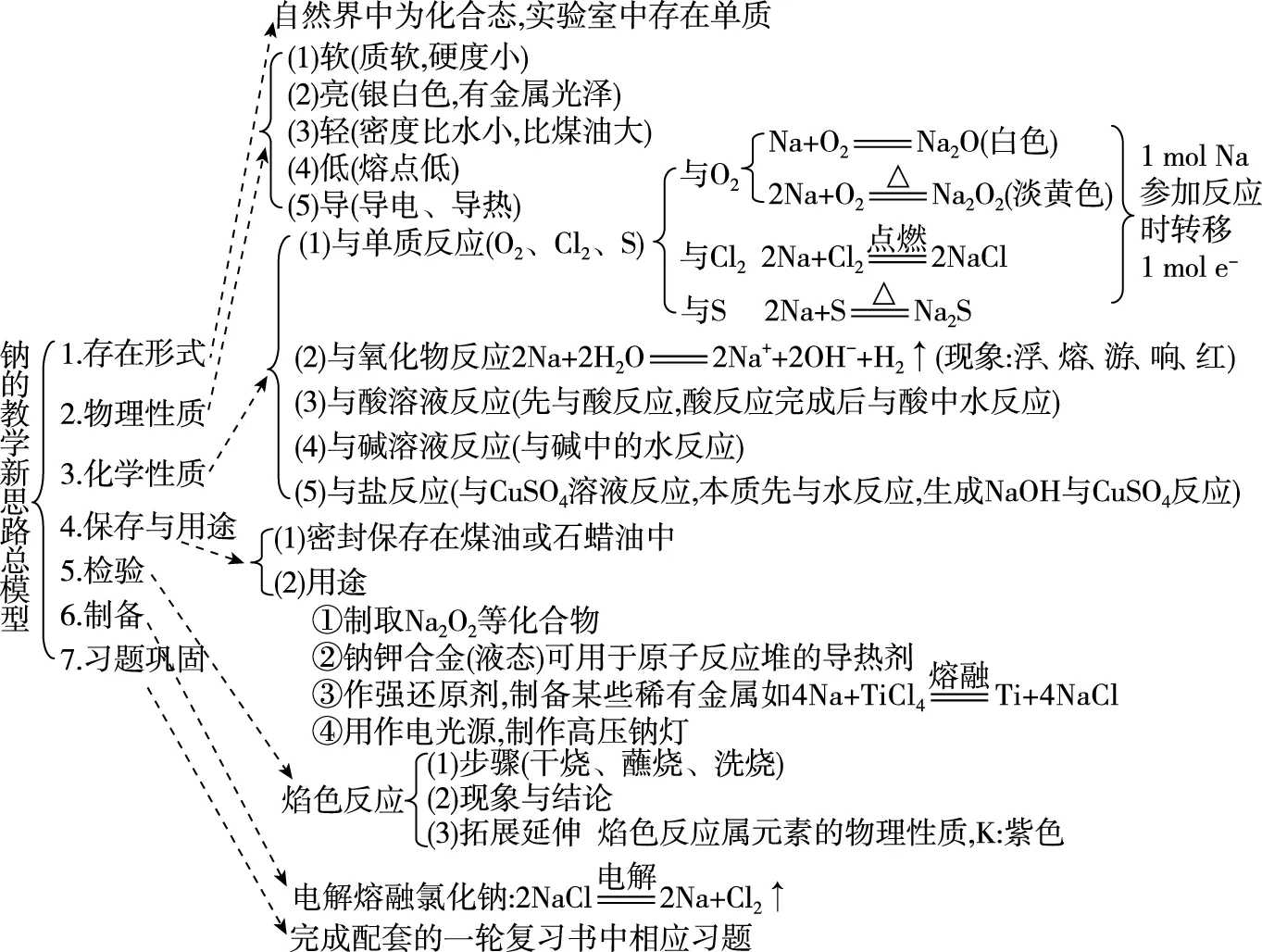
图5
【例2】二氧化硫的教学新思路
二氧化硫是元素及其化合物部分知识中性质相对复杂的化合物,其内容不仅承接了硫单质的性质,又进一步揭示了非金属及其化合物的重要性质及其在生活生产中的运用,是后续硫及其化合物间的相互转化、氮及其化合物等相关知识学习的基础,对于二氧化硫,教学思路总模型中的第1条“存在形式”修正为“主要来源”,二氧化硫不存在保存问题,因此可将图6模型中的第4条“保存与用途”修正为“用途”,SO2还有一个需要复习的内容为SO2的污染与防治,因此模型中的第7条“其他”修正为“污染与防治”,则SO2教学新思路总模型修正过程示意图及修正后的SO2教学思路总模型如图6所示:
图6 SO2教学思路总模型修正过程示意图
化学性质教学思路模型方面,SO2与氯气的反应在模型中应将“Cl2”修正为“X2”,X代表卤族元素;此外SO2有其独特的漂白性,因此将化学性质模型中的第7条“物质特有的化学性质”修正为“漂白性”。基于以上分析,根据构建的教学新模型,SO2化学性质教学新思路模型修正过程示意图及修正后的新思路模型如图7所示:
图7 SO2化学性质教学思路模型修正过程示意图
完善修正后的新思路模型即可得SO2的性质及应用教学新思路,为使新思路更为简洁明了,以上内容也可用新思路模型图表示为如图8所示:

图8
四、结束语
元素及其化合物知识是复习备考的重难点,主要的问题在于该模块涉及的知识点多,缺乏系统性和条理性,笔者根据《普通高中化学课程标准(2017版)》和《普通高等学校招生全国统一考试大纲》对知识掌握的要求,基于物质分类思维角度构建的教学思路新模型,很好地解决了复习时出现的无从下手、无方向和无目标问题,在复习备考时只需根据需要复习的具体物质对教学思路总模型进行适当修正即可高效梳理复习内容。化学性质的突破是该模块知识的最大难点,学生往往很难全面准确地重现出某个具体单质或化合物的化学性质,化学性质教学思路模型能很好地解决学生思维混乱问题,从单质出发,逐步寻找相关反应物,能较好地使学生准确完整的重现出化学性质的全部内容。

