PRX5与T2DM伴OSAS患者严重程度及颈动脉粥样硬化的关系
2020-11-12岳扬吴昊马亮杨光赵琦
岳 扬 吴 昊 马 亮 杨 光 赵 琦
2型糖尿病(type 2 diabetes mellitus,T2DM)是一种慢性疾病,易并发心、脑血管疾病、肾脏疾病等,严重危害着人们健康[1]。T2DM患者多伴有阻塞性睡眠呼吸暂停综合征(obstructive sleep apnea syndrome,OSAS),此外,OSAS患者中也多伴有T2DM[2]。T2DM和OSAS发病均与氧化应激损伤关系密切。OSAS患者长期反复的缺氧、复氧,引起氧化应激损伤并导致机体蓄积大量活性氧物质,诱发炎性反应,此外还损伤血管内皮细胞,增加心、脑血管疾病风险[3]。氧化应激损伤不仅损伤胰岛β细胞,降低胰岛素的表达和分泌水平,促进胰岛素抵抗的发生,还增加T2DM患者并发症发生风险[4]。氧化应激损伤及其引发的炎性反应与动脉粥样硬化密切相关[5]。过氧化物酶5(peroxiredoxin 5,PRX5)是一种内源性抗氧化剂。有报道显示急性脑卒中患者血浆PRX5水平与C反应蛋白、肿瘤坏死因子α和白介素-6等炎性细胞因子呈负相关[6]。此外,PRX5还可降低游离脂肪酸诱导的HepG2细胞中活性氧物质的水平,减轻氧化应激损伤[7]。但关于PRX5在T2DM伴OSAS患者中的表达及其与并发颈动脉粥样硬化的关系尚不明确。因此,本研究旨在探明PRX5与T2DM伴OSAS患者并发颈动脉粥样硬化的关系,以期为T2DM伴OSAS患者预防和治疗颈动脉粥样硬化提供帮助。
对象与方法
1.研究对象:前瞻性选取2017年12月~2019年12月在笔者医院就诊的147例T2DM伴OSAS患者作为研究对象。根据《中国2型糖尿病防治指南(2017年版)》[8]中有关T2DM诊断的相关内容进行诊断。根据《阻塞性睡眠呼吸暂停与糖尿病专家共识》[9]中有关OSAS诊断标准诊断OSAS。纳入标准:①年龄≤70岁;②T2DM病程3~10年;③糖化血红蛋白(glycated hemoglobin A1c,HbA1c)8%~11%;④能配合研究并签署知情同意书。排除标准:①服用他汀类或其他种类降脂药物;②合并下肢动脉硬化闭塞症;③合并慢性阻塞性肺疾病;④合并严重心功能不全;⑤既往有脑卒中史;⑥既往有精神病史;⑦合并呼吸道感染;⑧甲状腺功能异常。根据是否合并颈动脉粥样硬化将患者分为两组,即并发组(n=86)和对照组(n=61)。并发组男性58例,女性28例,患者年龄35~70(52.49±6.91)岁;其中轻度狭窄55例,中度狭窄23例,重度狭窄8例。对照组男性41例,女性20例,年龄36~66(52.10±7.62)岁。两组其他基线资料见表1。本研究经笔者医院医学伦理学委员会批准。
2.临床信息收集:收集所有患者年龄、性别、体重指数(body mass index,BMI)、糖尿病病程、空腹血糖(fasting plasma glucose,FPG)、HbA1c、胰岛素抵抗指数(homeostasis model assessment of insulin resistance,HOMA-IR)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)及睡眠呼吸监测结果。用便携式睡眠监测仪监测所有患者每小时睡眠发生呼吸暂停和低通气次数(AHI)。AHI 5~15为轻度,16~30为中度,>30为重度[10]。用超声诊断仪检测颈总动脉近心端、中部、远端、分叉处、颈内动脉及颈外动脉等,观察血管有无狭、两侧是否对称等情况。管腔狭窄率(%)=(颈总动脉管径-最小残存管径)/颈总动脉管径×100%。0~49%为轻度狭窄,50%~69%为中度狭窄,70%~99%为重度狭窄,100%为完全闭塞。
3.观察指标:抽取患者晨起空腹肘部静脉血5ml,3500r/min离心15min,提取上层血浆,在-20 ℃冰箱中保存,待检。采用酶联免疫吸附法检测患者血浆PRX5水平,试剂盒购自武汉USCN Life Science公司。
结 果
1.血浆PRX5水平与T2DM伴OSAS患者严重程度的关系:147例T2DM伴OSAS患者中,轻度75例(51.0%),中度41例(27.9%),重度31例(21.1%)。轻度、中度和重度患者血浆PRX5水平分别为39.98±4.57μg/L、31.32±2.41μg/L和26.34±3.04μg/L,差异有统计学意义(F=165.586,P=0.000)。轻度患者血浆PRX5水平高于中度和重度患者(q值分别为16.703、23.906,P<0.05),中度患者血浆PRX5水平高于重度患者(q=7.816,P<0.05)。T2DM伴OSAS患者血浆PRX5水平与AHI呈负相关(r=-0.378,P<0.01)。
2.两组基线资料比较:两组患者在年龄、性别、BMI、病程、MAP和TC水平方面比较,差异均无统计学意义(P>0.05)。并发组FPG、HbA1c、HOMA-IR、TG、LDL-C和AHI水平均高于对照组,差异均有统计学意义(P<0.05,表1)。
3.两组血浆PRX5水平比较:并发组血浆PRX5水平为31.28±5.13μg/L,低于对照组39.49±5.97μg/L,差异有统计学意义(t=8.925,P=0.000)。
4.影响T2DM伴OSAS患者颈动脉粥样硬化的因素分析:将是否并发颈动脉粥样硬化作为因变量,将FPG、HbA1c、HOMA-IR、TG、LDL-C、AHI和PRX5作为自变量(纳入标准α≤0.1)纳入Logistic多因素回归分析,结果显示,FPG、HbA1c、HOMA-IR、LDL-C、AHI和PRX5均和T2DM伴OSAS患者颈动脉粥样硬化密切相关(P<0.05,表2)。
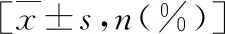
表1 两组基线资料比较

表2 影响T2DM伴OSAS患者颈动脉粥样硬化的相关因素分析
5.T2DM伴OSAS患者颈动脉粥样硬化的模型建立:将由FPG、HbA1c、HOMA-IR、LDL-C和AHI联合检测诊断T2DM伴OSAS患者颈动脉粥样硬化的模型命名为模型A,F=-29.141+0.452×FPG+1.692×HbA1c+0.505×HOMA-IR+1.129×LDL-C+0.098×AHI。将由FPG、HbA1c、HOMA-IR、TG、LDL-C、AHI和PRX5联合检测诊断T2DM伴OSAS患者颈动脉粥样硬化的模型命名为模型B,F=-1.533+0.579×FPG+1.770×HbA1c+0.550×HOMA-IR+1.395×LDL-C+0.259×AHI-0.717×PRX5。PRX5、模型A和模型B诊断T2DM伴OSAS患者颈动脉粥样硬化的AUC分别为0.844(95% CI:0.755~0.899)、0.940(95% CI:0.889~0.973)和0.974(95% CI:0.933~0.993)。模型B诊断T2DM伴OSAS患者颈动脉粥样硬化的效能高于PRX5和模型A(Z分别为4.302、2.312,P<0.05,表3、图1)。

表3 各模型诊断T2DM伴OSAS患者颈动脉粥样硬化的效能比较

图1 各模型诊断T2DM伴OSAS患者颈动脉粥样硬化的ROC曲线
讨 论
氧化应激及其引发的炎性反应可导致机体自由基增多、一氧化氮水平紊乱、血小板聚集、白细胞黏附及血管平滑肌细胞增殖等,以上异常反应均可损伤血管内皮系统,诱发动脉粥样硬化[11~13]。OSAS长期的间歇性缺氧和再氧和会诱发氧化应激,导致机体过多的氧自由基蓄积,不仅损伤胰岛β细胞,加重胰岛素抵抗,诱发T2DM病情加重及相关并发症的发生,还可促进脂质过氧化,损伤DNA和蛋白质,抑制细胞增殖或促进细胞凋亡[14,15]。此外,长时间的氧化应激损伤会抑制细胞的自噬过程,减弱自噬对细胞的保护作用,上述过程均可促进动脉粥样硬化形成及进展[16]。
PRX是一种半胱氨酸依赖性过氧化物酶,具有清除哺乳动物细胞中过氧化亚硝酸盐和其他过氧化物的功能[17]。PRX共有6个亚型,PRX5作为其中一员,较其他亚型更具有线粒体靶向性,可有效清除细胞质和线粒体内活性氧物质,降低氧化应激损伤[18~21]。Radyuk等[22]研究结果表明,过表达PRX5可抑制程序性细胞死亡,而抑制PRX5表达会加重氧化应激反应,从而诱发细胞凋亡。笔者推测PRX5可能通过调控氧化应激反应参与颈动脉粥样硬化的发生及发展过程。
本研究为避免混杂因素对实验结果造成影响,对糖尿病病程和糖化血红蛋白做了一定限制,未将病情较重和病程较长的患者纳入研究。经便携式睡眠监测仪监测所有患者睡眠呼吸状况,发现轻度患者占51.0%,中度患者占27.9%,重度患者占21.1%,与刘然等[10]研究结果接近,本研究通过比较不同严重程度T2DM伴OSAS患者血浆PRX5水平发现,随OSAS病情加重,T2DM伴OSAS患者血浆PRX5水平降低。进一步分析T2DM伴OSAS患者血浆PRX5水平与AHI的关系,发现二者呈负相关。上述结果提示,PRX5可能参与了T2DM伴OSAS的发病及病情进展。T2DM和OSAS发病均与氧化应激损伤有关,二者发病独立相关,且OSAS严重程度与T2DM发病风险一致[23,24]。T2DM和OSAS相互作用,若不及时加以干预易并发多种并发症发生,如冠心病、缺血性脑卒中等。颈动脉粥样硬化作为T2DM伴OSAS患者常见并发症之一,易诱发多种心脑血管疾病及外周血管疾病等。
本研究通过比较并发组和对照组血浆PRX5水平,发现并发组血浆PRX5水平低于对照组,该结果提示PRX5可能参与了T2DM伴OSAS患者颈动脉粥样硬化的发病。为进一步分析PRX5与T2DM伴OSAS患者颈动脉粥样硬化的关系,笔者采用单因素和Logistic多因素回归分析影响T2DM伴OSAS患者颈动脉粥样硬化的相关因素,结果显示,FPG、HbA1c、HOMA-IR、LDL-C、AHI和PRX5均和T2DM伴OSAS患者颈动脉粥样硬化密切相关,与已报道的研究结果一致[10,25]。
笔者构建了诊断T2DM伴OSAS患者颈动脉粥样硬化的模型A和模型B,通过比较PRX5、模型A和模型B诊断T2DM伴OSAS患者颈动脉粥样硬化的效能,发现模型B诊断T2DM伴OSAS患者颈动脉粥样硬化的效能高于PRX5和模型A,该结果提示纳入PRX5因素的模型B可弥补PRX5和模型A诊断的不足,提高诊断效能。
综上所述,T2DM伴OSAS患者血浆PRX5水平越低提示其OSAS病情越严重,此外,血浆PRX5水平低还与并发颈动脉粥样硬化的风险增加有关。定期检测T2DM伴OSAS患者血浆PRX5水平有助于了解颈动脉粥样硬化情况。本研究仍存在一定的不足,下一步将开展多中心研究,同时开展基础研究阐明PRX5与T2DM伴OSAS并发颈动脉粥样硬化的病理、生理机制。
