7⁃羟基三呋咱并[3,4⁃b:3′,4′⁃f:3″,4″⁃d]氮杂环庚三烯的合成与性能
2020-11-12翟连杰吴敏杰张家荣毕福强王伯周
翟连杰,霍 欢,吴敏杰,张家荣,毕福强,王伯周
(1. 西安近代化学研究所,陕西 西安 710065;2. 氟氮化工资源高效开发与利用国家重点实验室,陕西 西安 710065)
1 引言
高能和钝感是含能材料发展的两个重要方向,设计并合成兼具高能量密度和低感度的化合物一直是含能材料合成研究工作者的目标。近年来,五元或六元氮杂芳环构成的多环和稠环含能化合物展现出优异的理化性能和爆轰性能,已成为开发高能钝感含能材料的重要策略[1-5]。一方面,氮杂芳环形成的平面结构化合物分子间存在较强π⁃π 作用,能够有效拉近分子之间的距离,形成层状排列,分子之间堆积更加紧密,表现出更高的密度,已成为提升含能化合物密度的有效手段[6-9]。另一方面,氮杂芳环本身属于共轭体系,由此形成的稠环和多环平面分子共轭体系进一步扩大,能够有效提升分子的稳定性,表现出热稳定性好和感度低的特点。因此,氮杂芳环构成的含能化合物受到各国学者的广泛关注。
呋咱(1,2,5⁃噁二唑)是构建含能化合物的理想结构单元,其不仅具有热稳定性好、生成焓高等其他氮杂环普遍存在的优点,同时还有其他氮杂环所不具备的独特优势[10-14]。与吡唑、咪唑、三唑、四唑、三嗪等由碳氢氮元素组成的氮杂环相比,呋咱环分子内含有两个N—O 键,不仅能进一步提高相应化合物的密度,更重要的是其相当于硝基作用,为分子提供活性“氧”,在爆轰反应中将C、H 等氧化而释放大量能量,可以有效改善氮杂环化合物氧平衡差的问题。与异呋咱1,2,4⁃噁二唑(99.8 kJ·mol-1)和1,3,4⁃噁 二 唑(77.2 kJ·mol-1)相比,呋咱环具有更高的生成焓(216.3 kJ·mol-1)、更高爆轰性能以及更好的热稳定性[15]。
三个呋咱环通过氧或氮桥连接的七元环化合物是近年本课题组报道的一类结构新颖的含能化合物,具有密度高、热稳定性好和钝感的特性。2012 年,王锡杰等[16]以3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱为原料,在弱碱Na2CO3等催化作用下,合成了氧桥连的七元环化合物三呋咱并氧杂环庚三烯,其理论密度为1.93 g·cm-3,熔点为76.5~77.0 ℃,预估爆速为8646 m·s-1,撞击感度24%(10 kg 落锤,25 cm),特性落高为72.4 cm,表现出熔点低、感度低、能量密度高的特性。2015 年,贾思媛等[17]利用3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱与氨水、水合肼发生亲核取代反应,合成了氮桥连的七元环化合物7H⁃三呋咱并[3,4⁃b:3',4'⁃f:3″,4″⁃d]氮杂环庚三烯(HATF)和7⁃氨基三呋咱并[3,4⁃b:3',4'⁃f:3″,4″⁃d]氮杂环庚三烯,其中HATF 的晶体密度为1.871 g·cm-3、分解点为345.1 ℃、爆速为8416.5 m·s-1,综合性能优异。向氮杂环中引入N—OH 是目前提高氮杂环含能化合物性能的有效手段,故在HATF 七元环分子中氮上引入羟基,有望进一步提高其性能。然而,目前还没有含N—OH 结构的七元环呋咱化合物的相关文献报道。
鉴于上述分析,本课题组以3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱和羟胺溶液为原料,合成了具有N⁃OH结构的七元环化合物7‑羟基三呋咱并[3,4⁃b:3',4'⁃f:3″,4″⁃d]氮杂环庚三烯(HYTF),利用反应温度变化实现了HYTF 和HATF 的可控合成,提出了HYTF 与羟胺作用生成HATF 的反应机理;采用差示扫描量热仪(DSC)分析了HYTF 热稳定性,利用Explo5(V6.04)软件预估了其爆轰性能。
2 实验部分
2.1 实验仪器与试剂
NEXUS870 型傅里叶变换红外光谱仪,美国热电尼高力公司;AV500 型(500 MHz)超导核磁共振仪,瑞士BRUKER 公司;Vario EL⁃Ⅲ型元素分析仪,德国EXEMENTAR 公司;LC⁃2010A 液相色谱仪,日本岛津公司;Q⁃200 型差示扫描量热仪,美国TA 公司。
乙醚、乙腈,均为分析纯,成都市科龙化工试剂厂;碳酸钠、分析纯,天津化学试剂有限公司;浓硫酸、30%双氧水、50%羟胺溶液,均为分析纯,西安福晨化学仪器有限公司。
2.2 实验原理
HYTF 的合成路线见Scheme 1。
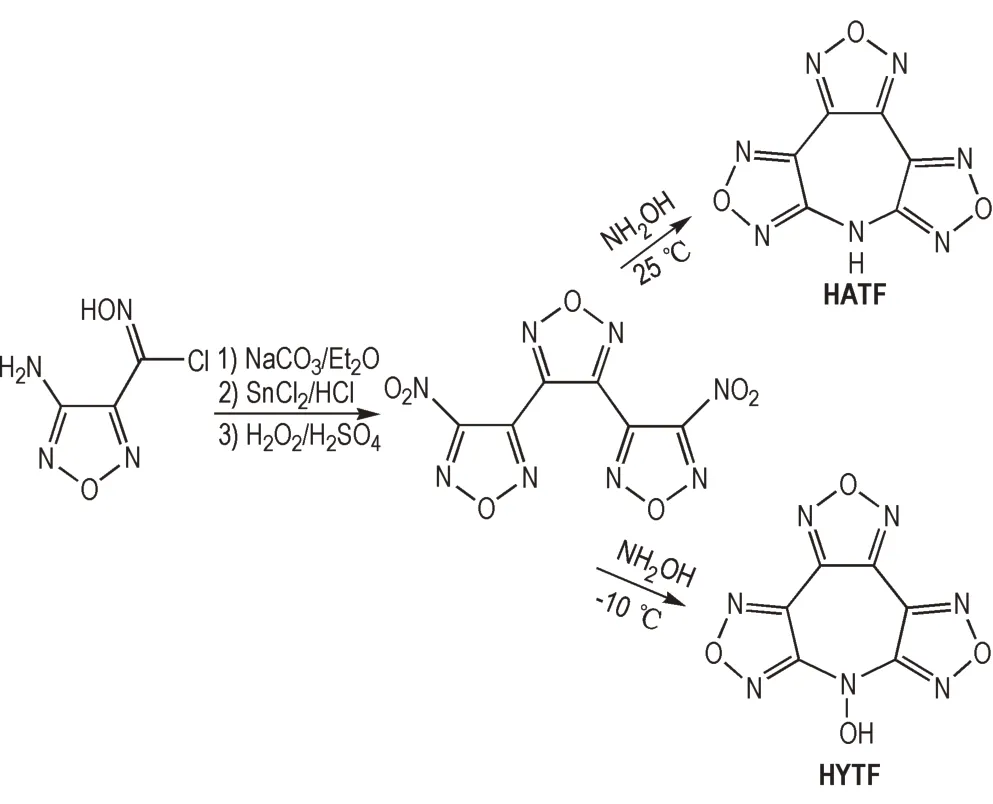
Scheme 1 Synthetic routes for HYTF
2.3 实验步骤
2.3.1 HATF 的合成
3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱依据文献[17]合成。室温下,将4.4 g(15 mmol)3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱加入到50 mL 乙腈中,搅拌溶解后缓慢滴加3.0 g(45 mmol)质量分数为50%羟胺水溶液,保温反应2 h。反应结束后减压蒸馏除去乙腈,剩余物经乙醇和水(V∶V=4∶6)重结晶得1.7 g 无色固体,收率51.8%,纯度98.4%。熔点:193.0 ℃;1H NMR(DMSO⁃d6,500 MHz),δ:12.46(s,H,NH);13C NMR(DMSO⁃d6,125 MHz),δ:152.88,144.90,137.73;R(KBr,ν/cm-1):3200,1510,1480,1001,985,1639,1604;Anal.calcd for C6HN7O3:C 32.89,H 0.46,N 44.75;found C 32.77,H 0.49,N 44.91。
2.3.2 HYTF 的合成
在-10 ℃下,将4.4 g(15 mmol)3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱加入到15 mL 乙腈中,搅拌溶解后缓慢滴加缓慢滴加3.0 g(45 mmol)(质量分数为50%)羟胺水溶液,保温反应1 h,直到原料消失完全。低温下快速过滤得1.1 g 固体,收率31.1%,纯度97.2%。dec.:161.8 ℃;1H NMR(DMSO⁃d6,500 MHz),δ:7.97(s,H,OH);13C NMR(DMSO⁃d6,125 MHz),δ:155.38,144.42,135.64;15N NMR(DMSO⁃d6),δ:33.08,30.70,-3.51,-252.34;IR(KBr,ν/cm-1):3215,2924,2740,1591,1504,1423,1378,1214,1086,1059,1014,998,987,942,894,864,837,627,600,583;Anal. calcd for C6HN7O4:C 30.65,H 0.43,N 41.70;found C 30.71,H 0.47,N 40.97。
3 结果与讨论
3.1 反应过程与环化机理
3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱与羟胺发生亲核取代反应是合成HYTF 最直接途径。然而,在室温下,将羟胺溶液滴加到3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱的乙腈溶液中,分离得到的产物最终被证实是HATF。利用薄层色板对反应实时监测发现,当加入羟胺时,首先发现反应体系中迅速生成一个中间体(极性大于HATF),随后又监测到HATF 生成。当羟胺加入完毕后,中间体迅速消失,而反应体系中HATF 浓度越来越大。我们推测,反应过程出现的中间体很可能是目标化合物HYTF,但其随着反应的进行又转化成HATF。基于此推测,作者尝试降低反应温度,降低整个反应体系的反应活性,以期HYTF 能够在低温体系中稳定存在。当反应温度降低到-5~-10 ℃时,使用薄层色板监控反应体系,发现生成的中间体在体系中能够稳定存在,且没有HATF 生成。通过直接过滤分离出该中间体,表征后最终证实该中间体确实是目标化合物HYTF。为了进一步验证推测的反应历程,在室温下,作者将羟胺溶液滴加到纯HYTF 的乙腈溶液中,发现体系中迅速生成了HATF,证实了推测反应历程的正确。
推测的反应机理如Scheme 2所示,3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱中呋咱环和硝基都具有吸电子特性,致使与硝基相连的呋咱环碳原子电子云密度降低,显示出部分正电性,NH2OH 中孤对电子进攻C—NO2中显正电性的碳原子,失去二分子HNO2,生成目标化合物HYTF。由于呋咱强吸电子性和七元环大共轭体系影响,导致HYTF分子中N—OH 电子密度更多流向氮原子,羟基氧在某种程度上显示缺电子特性。因此,NH2OH 氮上电子对继而进攻HYTF 中羟基氧原子,生成七元环阴离子和二羟基铵盐。七元环阴离子与质子结合生成HATF,二羟基铵盐经脱质子和二次脱水后,最终分解成N2O。

Scheme 2 Proposed formation mechanism for HYTF and HATF
3.2 13C 和15N 核 磁 谱
采 用 氘 代 试 剂DMSO⁃d6,完 成 了HYTF 的13C和15N NMR 实验,结果如图1 所示。HYTF 为对称性分子,其13C NMR 中出现3 个信号峰(Fig.1a),HYTF分子中N—OH 对与其相连的呋咱碳原子化学位移具有显著影响,致使化学位移大幅移向低场,故很容易将化学位移为δ=155.38 信号峰归属为C(1)。由于HYTF 中C(2)和C(3)所处的化学环境较为相似,仅仅根据文献或电子效应推导很难对其准确指认。规范不变 原 子 轨 道(Gauge Independent Atomic Orbital,GIAO)[18]方法是目前预测核磁共振化学位移较为准确的方法,王民昌等[19]已成功用于呋咱含能分子的NMR 预测。在结构优化基础上(B3LYP 方法6⁃311+G(2d,p)基组水平),采用规范不变原子轨道方法[18],对HYTF 分子中C、N 原子的化学位移进行理论计算。碳谱理论计算结果为C(1)δ=162.14、C(2)δ=148.78、C(3)δ=139.63,与 实 验 值C(1)δ=155.38、C(2)δ=144.42、C(3)δ=135.64 吻合度较好,验证了方法的准确性。同理,完成了HYTF 氮谱归属(Fig.1b)。
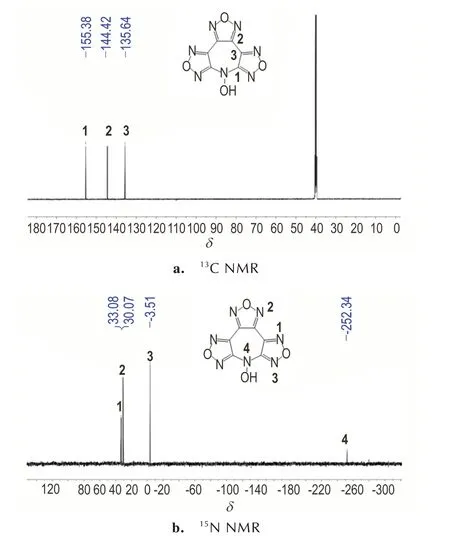
图1 HYTF 在氘代二甲基亚砜溶液中13C 和15N NMR 谱Fig. 1 13C and 15N NMR spectra of compound HYTF in DMSO⁃d6
3.3 热性能研究
采用差示扫描量热仪(DSC),在10 ℃·min-1的升温速率条件下,获得了HYTF在50~450 ℃条件下的DSC曲线。如图2所示,HYTF在150~180 ℃范围内,有两个峰型尖锐的分解放热峰,峰值分别为161.8 ℃和166.1 ℃。相比于化合物HATF(分解峰温为345.1 ℃)[17],N—OH的引入大幅降低了HYTF 热稳定性,表明HYTF 分子中的N—OH 为热不稳定点,这与合成实验中HYTF 在反应体系中不稳定更易转化成HATF 的结果相佐证。
3.4 爆轰性能

图2 HYTF 的DSC 曲 线Fig.2 DSC curve of HYTF
采用密度泛函理论(DFT)的B3LYP 方法[20],在6⁃31+G(d,p)基组水平上对HYTF 的结构进行了全优化,经振动频率分析发现无虚频,表明优化结构为势能面上的极小点,为稳定构型。使用原子化方案[21],利用完全基组方法(CBS⁃4M)[22-23]计算了298 K 时HYTF的焓值H°(Molecule,298 K),进而得出其气相生成焓(ΔfH(g))为655.8 kJ·mol-1。利用Trouton 等[24]提出的公式计算了HYTF 的升华焓(ΔHsub=82.0 kJ·mol-1),气相生成焓减去升华焓即可得到HYTF 的固相生成焓ΔfH(s,M 298 K),为573.8 kJ·mol-1。
采用排惰性气体法,测试HYTF密度为1.86 g·cm-3。基于HYTF 实测密度和固相生成焓,采用Explo 5(V6.04)程序[25]预估HYTF 的爆速为8181 m·s-1,爆压为28.0 GPa。为了更好展示HYTF 性能特点,将HYTF与RDX 的文献性能[1]比较列于表1。由表1 可知,HYTF的密度和生成焓均高于RDX,爆速和爆压均低于RDX,这是由于HYTF分子中无硝基,氧平衡相对较差所致。

表1 HYTF 的爆轰性能Table 1 The detonation performances of HYTF
4 结论
(1)以3,4⁃双(4'⁃硝基呋咱⁃3'⁃基)呋咱和羟胺溶液为原料,合成了一种新型七元环化合物7‑羟基三呋咱并[3,4⁃b:3',4'⁃f:3″,4″⁃d]氮杂环庚三烯(HYTF),发现该反应受温度控制,在低温-5~-10 ℃时生成HYTF,室温下生成7H⁃三呋咱并[3,4⁃b:3',4'⁃f:3″,4″⁃d]氮杂环庚三烯(HATF),推测了HYTF 与羟胺进一步作用生成HATF 的机理。
(2)基于实验结果和理论模拟,探讨了HYTF13C和15N NMR,完成了HYTF 的碳谱和氮谱归属。
(3)HYTF 的计算生成焓为573.8 kJ·mol-1,实测密度为1.86 g·cm-3,分解峰温为161.8 ℃,预估的爆速为8181 m·s-1,爆压28.0 GPa,表明HYTF 是一种密度大、爆轰性能较好的含能化合物。
