注射用益气复脉(冻干)中糖类成分研究
2020-11-11李耀磊岳洪水刘丽娜金红宇马双成
王 莹,李耀磊,岳洪水,刘丽娜,金红宇 ,马双成
(1.中国食品药品检定研究院,北京100025;2.天津天士力之骄药业有限公司,天津300402)
注射用益气复脉(冻干,YQFM)处方来源于古方生脉散,由红参、麦冬、五味子组方,以甘露醇和葡甲胺为辅料,具有益气复脉、养阴生津功效[1],临床主要用于治疗冠状动脉粥样硬化性心脏病心绞痛和冠状动脉粥样硬化性心脏病慢性心力衰竭等[2]。YQFM于2007年批准上市,现行法定质量标准为国家药品标准YBZ07062006-2009Z-2015,主要对其皂苷类、木脂素类及糖类成分进行控制。YQFM主要化学成分包括三萜皂苷、甾体皂苷、木脂素、糖等[3-6],其中对皂苷类成分的研究较深入,对单糖及双糖成分的研究则较少。糖类成分作为主要质控指标,现行标准采用苯酚硫酸-紫外分光光度法对总糖进行测定,但缺乏专属性,无法获取糖的种类信息,且操作步骤复杂,重复性不佳。故本研究中拟对YQFM中糖类成分的测定方法进行研究。目前,糖组成测定方法包括薄层色谱(TLC)法、气相色谱(GC)法、高效液相色谱(HPLC)法等。TLC法具有简单、方便、经济的特点,常作为糖类鉴别方法[7-9]。由于糖极性大、难气化,故使用GC分析前需对糖进行硅烷化或酯化等处理;由于糖无紫外吸收,若采用HPLC-UV检测器分析,需先对其进行衍生化,操作较烦琐;蒸发光散射检测器(ELSD)是一种质量型检测器,在对无紫外吸收化合物进行分析时具有基线稳定、结果准确、样品处理简单等优点,常用于糖类物质尤其是单糖和双糖的检测[10-11]。电喷雾检测器(CAD)是一种通用型检测器,其检测信号不依赖于被检测物质的化学结构,能检测大部分非挥发性或半挥发性物质,作为通用型检测器目前已有报道将其应用于单糖和寡糖的检测[12-13]。本研究中分别采用TLC法和HPLC-CAD法对YQFM中糖的种类和含量进行测定,以期为YQFM的质量控制提供科学依据。现报道如下。
1 仪器与试药
1.1 仪器
Thermo Ultimate 3000型液相色谱仪,配置CAD检测器(美国赛默飞世尔科技公司);TLC点样系统,TLC薄层显像系统,均购自瑞士卡玛公司。
1.2 试药
果糖对照品(批号为100231-201807,质量分数为99.6%),D-无水葡萄糖对照品(批号为110833-201707,含量为99.9%),蔗糖对照品(批号为111507-201303,含量为99.8%),麦芽糖对照品(批号为100287-201303,含量为94.3%),均购自中国食品药品检定研究院;TLC硅胶G薄层板(Merck公司);注射用益气复脉(冻干,天津天士力之骄药业有限公司,编号分别为S1~S5,规格为每瓶0.65 g)。
2 方法与结果
2.1 TLC法鉴别糖组成
溶液制备:分别取葡萄糖、果糖、麦芽糖、蔗糖,制成质量浓度为1 mg/mL的单标溶液。分别吸取1 mL,置10 mL容量瓶中,加水定容,摇匀,即得混标溶液。精密称取样品100 mg,置10 mL容量瓶中,加水制成质量浓度为10 mg/mL的溶液,摇匀,即得供试品溶液。
薄层展开条件:取对照品溶液及供试品溶液,在薄层板上各点样2μL,展开剂为正丁醇-异丙醇-水-醋酸(7∶5∶2∶1,V/V/V/V),展开,取出,吹干,苯胺-二苯胺显色剂显色,置加热板(105℃,加热10 min),在日光下观察。
样品测定:采用上述方法对5批样品进行TLC检测,供试品溶液在与对照品溶液相对应的位置上,应显相同颜色的斑点。由图1可见,5批样品均包括葡萄糖、果糖、麦芽糖、蔗糖,其中果糖、葡萄糖、蔗糖主斑点显色明显,蔗糖斑点显色略弱于其他3种单糖,显示可能蔗糖含量较低。
2.2 HPLC-CAD法分析糖组成
2.2.1 色谱条件
色谱柱:Shodex Asahipak NH2P-50柱(250 mm×4.6 mm,5μm);流动相:水(A)-乙腈(B),梯度洗脱(0~35 min,10%A→40%A);流速:0.8 mL/min;柱温:30℃;CAD雾化温度:45℃;进样量:10μL;PF值:1.3。在此色谱条件下的色谱图见图2。
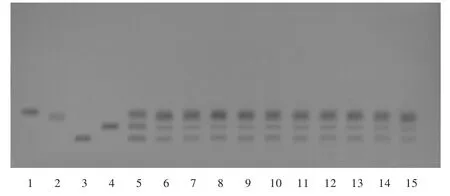
图1 薄层色谱图
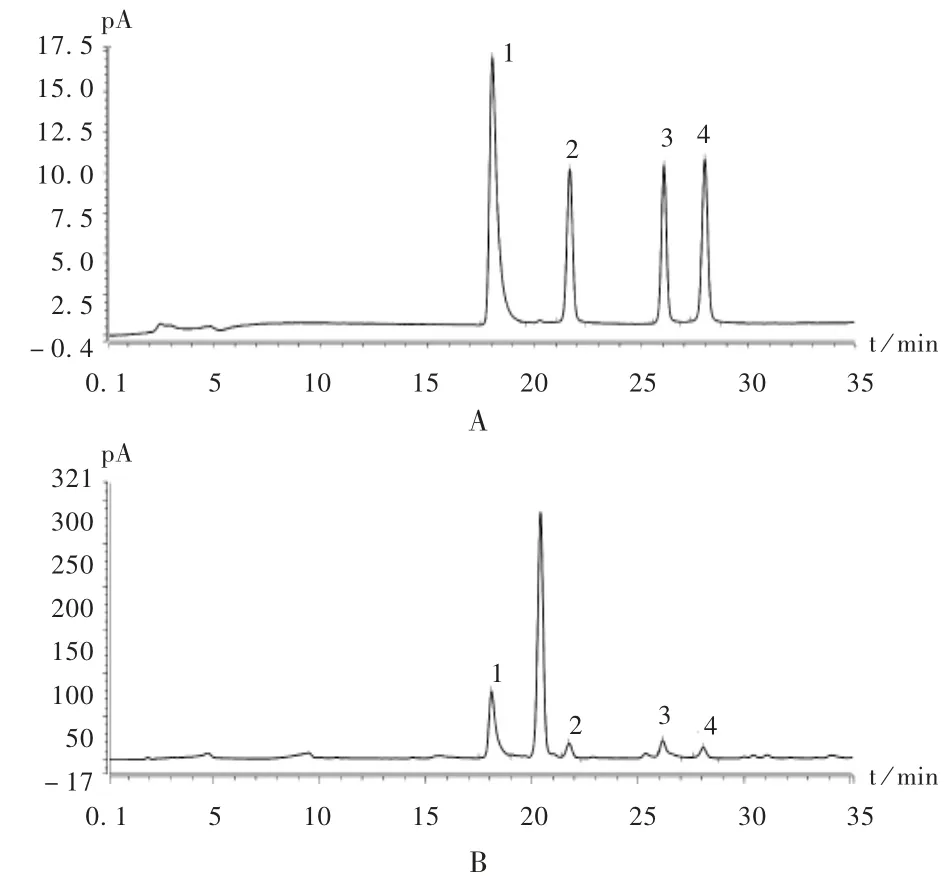
图2 高效液相色谱-电喷雾检测器色谱图
2.2.2 溶液制备
分别精密称取果糖、葡萄糖、蔗糖和麦芽糖对照品适量,制成质量浓度为0.60,0.20,0.20,0.20 mg/mL的混合对照品溶液。精密称取120 mg的样品,置10 mL容量瓶中,加水稀释至刻度,摇匀,0.45μm微孔滤膜滤过,取续滤液,即得供试品溶液。
2.2.3 方法学考察
线性关系考察:分别精密吸取2.2.2项下混合对照品溶液2,5,10,15,20μL,注入高效液相色谱仪,测定各成分的峰面积,以进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归。结果见表1。

表1 线性关系考察结果(n=5)
精密度试验:精密吸取供试品溶液10μL,注入高效液相色谱仪,测定各成分的峰面积。结果果糖、葡萄糖、蔗糖、麦芽糖峰面积的RSD分别为3.26%,1.60%,1.41%,1.14%(n=6),表明仪器精密度良好。
加样回收试验:取已知含量的样品(编号为S1)60 mg,精密称定,共6份,分别按样品-对照品1∶1的比例加入对照品,依法制备供试品溶液,摇匀,按拟订色谱条件测定各成分的峰面积,并计算回收率。结果见表2。
重复性试验:取样品适量,依法平行制备供试品溶液6份,并测定其果糖、葡萄糖、蔗糖、麦芽糖的含量,计算RSD值。结果果糖、葡萄糖、蔗糖、麦芽糖含量的RSD分别为1.67%,2.50%,3.22%,1.35%(n=6),表明方法重复性良好。
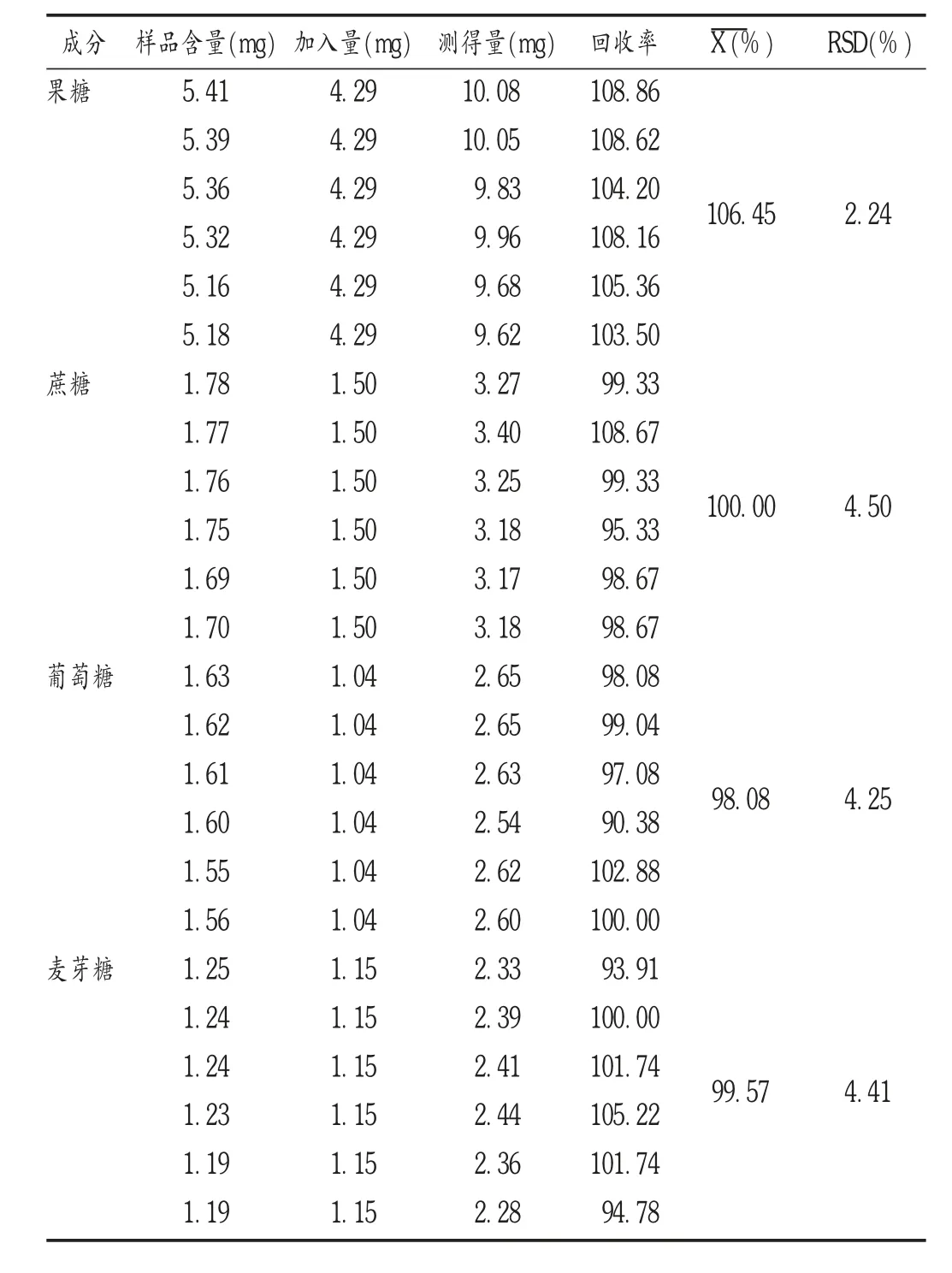
表2 加样回收试验结果(n=6)
稳定性试验:取样品(编号为S1)适量,依法制备供试品溶液,分别于0,5,10,15,20,24 h时进样,测定各成分的峰面积。结果果糖、葡萄糖、蔗糖、麦芽糖峰面积的RSD分别为4.84%,3.97%,3.96%,2.37%(n=6),表明供试品溶液在24 h内稳定。
2.2.4 样品含量测定
取5批样品(批号分别为S1~S5),各2份,依法制备供试品溶液,按拟订色谱条件进样10μL,记录峰面积,以标准曲线法计算4种糖的含量。结果见表3。5批样品中4种糖的平均质量比为3.4∶1.0∶1.1∶0.7,糖总量为16.05%~17.68%,均符合现行法定标准要求。
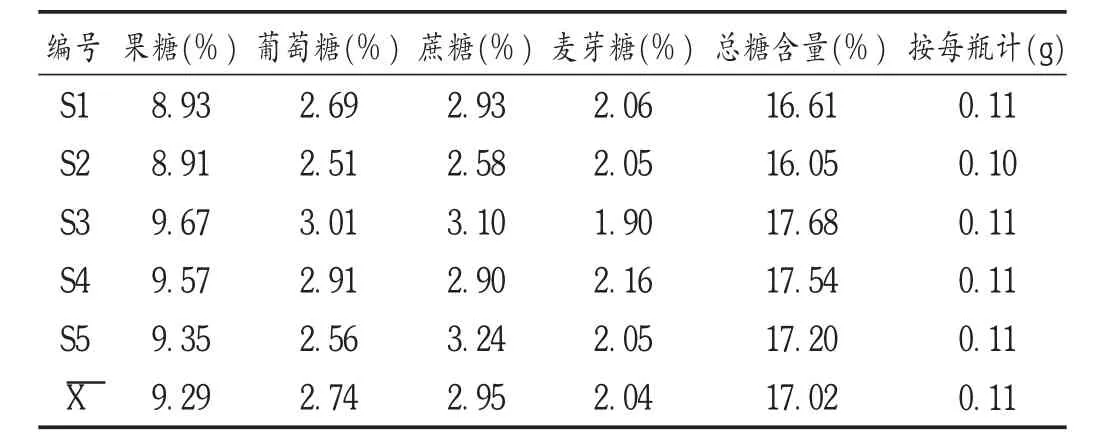
表3 5批样品中4种糖含量测定结果(n=2)
3 讨论
3.1 TLC条件优化
对TLC展开系统及显色剂进行考察,分别采用正丁醇-异丙醇-水-醋酸为展开溶剂,苯胺-二苯胺为显色剂;正丁醇-0.1 mol/L磷酸氢二钠-丙酮为展开剂,α-萘酚试液为显色剂;正丁醇-醋酸乙酯-异丙醇-乙酸-吡啶-水为展开剂,苯胺-邻苯二甲酸溶液为显色剂。结果表明,正丁醇-异丙醇-水-醋酸的分离效果最佳,故以此为展开条件。
前期研究中采用确定的TLC条件,对9种单糖(葡萄糖、果糖、麦芽糖、蔗糖、半乳糖、乳糖、甘露糖、木糖、阿拉伯糖)、双糖及样品进行测定及鉴别,发现YQFM中主要由4种糖类成分组成,即果糖、葡萄糖、蔗糖和麦芽糖。文献[14]显示,YQFM中红参的主要糖成分为蔗糖和麦芽糖,麦冬中主要糖成分为果糖和葡萄糖,故上述4个单糖可作为YQFM中反映药味质量的有效指标。
3.2 HPLC-CAD条件优化
曾考察流动相梯度洗脱和等度洗脱,结果梯度洗脱时分离效果好,最终确定流动相为乙腈-水、梯度洗脱。
3.3 CAD法与紫外可见分光光度法测定结果比较
采用HPLC-CAD法及现行标准中的苯酚硫酸法对3批样品中糖含量进行测定,发现2种方法存在一定差异,紫外分光光度法测定结果均显著高于CAD法的测定结果,这可能与苯酚硫酸法显色原理有关。不同单糖显色程度有差异,以葡萄糖作为对照品计算可能导致结果存在误差[15]。由总糖含量测定结果可知,2种方法的测定结果均符合现行法定标准(总糖含量限度为每瓶不得少于0.10 g)。
3.4 方法评价
采用TLC结合HPLC-CAD法对益气复脉中糖类成分组成及其含量进行分析,该方法相较于原标准中的苯酚硫酸-紫外分光光度法,专属性强,简便快速,成本低,可用于生产过程及成品制剂的质量控制。
