人淋巴细胞国家参考品的研制
2020-11-10胡泽斌高飞曲守方孙彬裕杨振孙晶黄杰
胡泽斌,高飞,曲守方,孙彬裕,杨振,孙晶,黄杰
淋巴细胞是正常机体免疫功能最重要的一大细胞群,按其发生迁移、表面分子和功能的不同可分为 T 细胞、B 细胞和自然杀伤(NK)细胞。T 细胞亚群与细胞免疫功能有关,B 细胞与体液免疫功能有关,NK 细胞与非特异免疫功能有关。外周血 T、B 和 NK 淋巴细胞亚群检测已成为临床医学中最常用的检查项目之一。对于评价机体的免疫功能,诊断与监测肺部疾病、艾滋病、恶性肿瘤、器官移植等具有重要意义[1-3]。目前临床检测中常用流式细胞法(flow cytometry,FCM)对淋巴细胞亚群的表型和数量进行分析[1,4]。
流式细胞法分析是一种在大分子水平上对单细胞或其他生物粒子进行定量分析的检测手段,可以在短时内高速分析大量细胞或生物粒子的物理和化学特征参数。流式细胞分析主要靠流式细胞仪和各种特定发光物质标记的单克隆抗体试剂组合检测来实现[4]。
目前 T/B/NK 淋巴细胞亚群检测试剂主要有两类:单一的单克隆抗体试剂和组合类的单克隆抗体试剂盒。近年来,涉及流式细胞分析对淋巴细胞亚群进行检测的企业越来越多,不同厂家的产品在抗体原材料克隆号和荧光素的选择、试剂组合方式,是否有匹配的溶血素、适用机型及配套自动分析软件或手动分析软件、产品绝对计数的方式(体积法/微球法)和成品质量控制等方面有所差异,导致检测结果的准确性也受到影响[5-8]。如何公正客 观地衡量同一项目不同厂家试剂的质量优劣?目前国内外尚无此类标准物质,临床操作或实验室质控通常使用进口的不同厂商的商品化质控血,不仅价格昂贵、购买费时费力、有效期较短,而且还缺乏标准化的赋值结果[9-12]。为解决这些问题,就需要研制基质效应小、均一性和稳定性良好的人淋巴细胞国家标准物质,不仅可填补国内市场的空白,降低使用成本,还可以提高检验结果的准确性和互认度,以及保障此类体外诊断试剂检验检测、审评和监管的需要。因此根据实际调研情况和探索实验结果,本科室开展了人淋巴细胞国家参考品的研制工作。
1 材料与方法
1.1 材料
1.1.1 仪器 冷冻离心机购自德国 Eppendorf 公司;倒置显微镜购自上海光学仪器六厂;生物安全柜购自江苏苏净集团有限公司;分装机购自保定兰格恒流泵有限公司;冻干机购自宁波新芝生物科技有限公司;电子天平购自福州华志科学仪器有限公司;移液器购自美国 Thermo 公司;涡旋仪购自上海医大仪器厂;FACS Calibur 和 Canto II 流式细胞仪由美国 BD 公司提供;ACEA Novocyte 流式细胞仪由艾森生物提供;Navios 流式细胞仪由北京旷博生物技术股份有限公司提供。
1.1.2 试剂 人淋巴细胞分离液为深圳市达科为 生物工程有限公司产品;PBS 溶液为美国 BD 公司产品;细胞固定液和冻干保护剂为巴德生物科 技有限公司产品;淋巴细胞亚群检测试剂盒和绝 对计数管为美国 BD Biosciences 公司产品;6 色 CD3-FITC/CD16+56-PE/CD45-PerCP-Cy5.5/CD4- PC7/CD19-APC/CD8-APC-Cy7 荧光单克隆抗体试剂盒(流式细胞仪法)和绝对计数微球为北京同生时代公司产品;ACEA CD3/CD16+56/CD45/CD4/ CD19/CD8 淋巴细胞亚群检测试剂盒为艾森生物公司产品。
1.2 方法
1.2.1 人淋巴细胞国家参考品候选品的制备 收集健康志愿者的新鲜外周血白细胞,用 PBS 稀释后缓慢加入人淋巴细胞分离液上方,300 × g 离心 30 min。小心吸取离心后的中间白细胞层,即得到外周血单个核细胞(PBMCs)。将 PBMCs 均匀重悬于细胞固定液,于 2 ~ 8 ℃ 静置过夜。之后离心去除细胞固定液,加入适量冻干保护液重悬细胞。每支西林瓶按 1 ml 进行分装,分装后的细胞进行冻干,制备成人淋巴细胞国家参考品候选品。
1.2.2 人淋巴细胞国家参考品候选品液体瓶间分装均匀性检验 按照国家标准 GBT15000.3-2008《标准样品工作导则⑶标准样品定值的一般原则和统计方法》、CNAS-GL03《能力验证样品均匀性和稳定性评价指南》及《一级标准物质技术规范》进行。在候选品制备过程中溶液分装的初始、中 间、终结阶段进行随机取样,各随机抽样 10 支,共 30 支。采用精密度良好的电子天平对抽取样本进行称重测定。
1.2.3 人淋巴细胞国家参考品候选品冻干瓶间均匀性检验 随机抽取冻干后的候选品 24 支,采用流式细胞法,使用 BD 淋巴亚群检测试剂盒以免 洗方案进行细胞染色后,在 BD FACS Calibur 流式细胞仪上进行 T/B/NK 淋巴细胞表面抗原百分比检测和数据收集。所获取的 FCS 文件,使用 FlowJo 软件分析:CD3+、CD3+CD4+、CD3+CD8+、CD3-CD16+CD56+、CD3-CD19+细胞亚群的百 分数。
1.2.4 人淋巴细胞国家参考品候选品的基质效应评估 参考卫生行业标准 WS/T356-2011《基质效应与互通性评估指南》进行基质效应评估。收集至少 20 份健康人的新鲜抗凝全血临床样本,标记 BD 公司的 4 色 T/B/NK 检测抗体,使用 BD 公司的绝对计数管,采用流式细胞法在两种检测平台 (BD FACS Calibur 和 BD Canto II)上同时对选定的新鲜临床样本和标准物质候选品进行 T/B/NK 淋巴细胞亚群的百分比和绝对计数的检测和分析,利用两种平台测定临床样品的结果建立数学关系(回归)。以临床样本测定结果做散点图,y 轴为以 BD FACS Calibur 测定的结果,x 轴为 BD Canto II 测定的结果,进行线性相关性分析。
1.2.5 人淋巴细胞国家参考品候选品稳定性实 验 候选标准物质采用不同时间点放入,最终时间点取出,统一检测,每个温度和时间点放入 2 ~ 3 支候选品;采用同一批号的试剂盒、同一台测 试仪器、同一批实验人员在同一天内完成测试, 每个样本测定 2 次。候选品在加热 37 ℃、室温 (20 ~ 25 ℃)两种温度条件下,分别放置 3、7、14、21、30 d,以 -20 ℃ 保存的候选品为对照,使用 CD3-FITC/CD16+56-PE/CD45-PerCP-Cy5.5/ CD4-PC7/CD19-APC/CD8-APC-Cy7 荧光单克隆抗体试剂盒(流式细胞仪法)和绝对计数微球试剂盒(流式细胞法)在 Naviuos 流式细胞仪上对以上稳定性样本进行 T/B/NK 淋巴细胞亚群的百分比和绝对计数的分析测定。
1.2.6 人淋巴细胞国家参考品候选品复溶稳定性实验 将 5 支候选标准物质复溶后放置2 ~ 8 ℃ 冷藏,在 0、2、6 h 3 个时间点分别取出 50 μl,标记 6 色 T/B/NK 淋巴细胞亚群抗体试剂在流式细胞仪上进行百分比和绝对计数的分析测定。使用 GraphPad Prism 软件,利用秩和检验对所得数据进行统计分析。
2 结果
2.1 候选品分装均匀性检验结果
液体分装过程的前中后段随机抽取 30 瓶,每瓶称重 1 次,结果如表 1 所示,30 瓶间液重总体变异系数的 CV 值仅为 0.08%,说明分装瓶间均匀性良好。
2.2 T/B/NK 细胞表面抗原冻干均匀性检验结果
随机抽取冻干后的候选品 24 支,每支检测 T/B/NK 淋巴细胞百分比 3 次,然后求平均值,实验操作和数据分析亚群需参照 WS/T 360-2011《流式细胞术检测外周血淋巴细胞亚群指南》。结果如表 2 所示,24 支瓶间 CD3+、CD4+、CD8+、CD19+、CD16+56+淋巴细胞百分比的总体变异系数 CV 值分别仅为 0.37%、1.13%、0.99%、2.24%、2.24%,说明冻干瓶间均匀性良好。

表1 候选品分装称重数据Table 1 Weighing data of sub-packed candidates
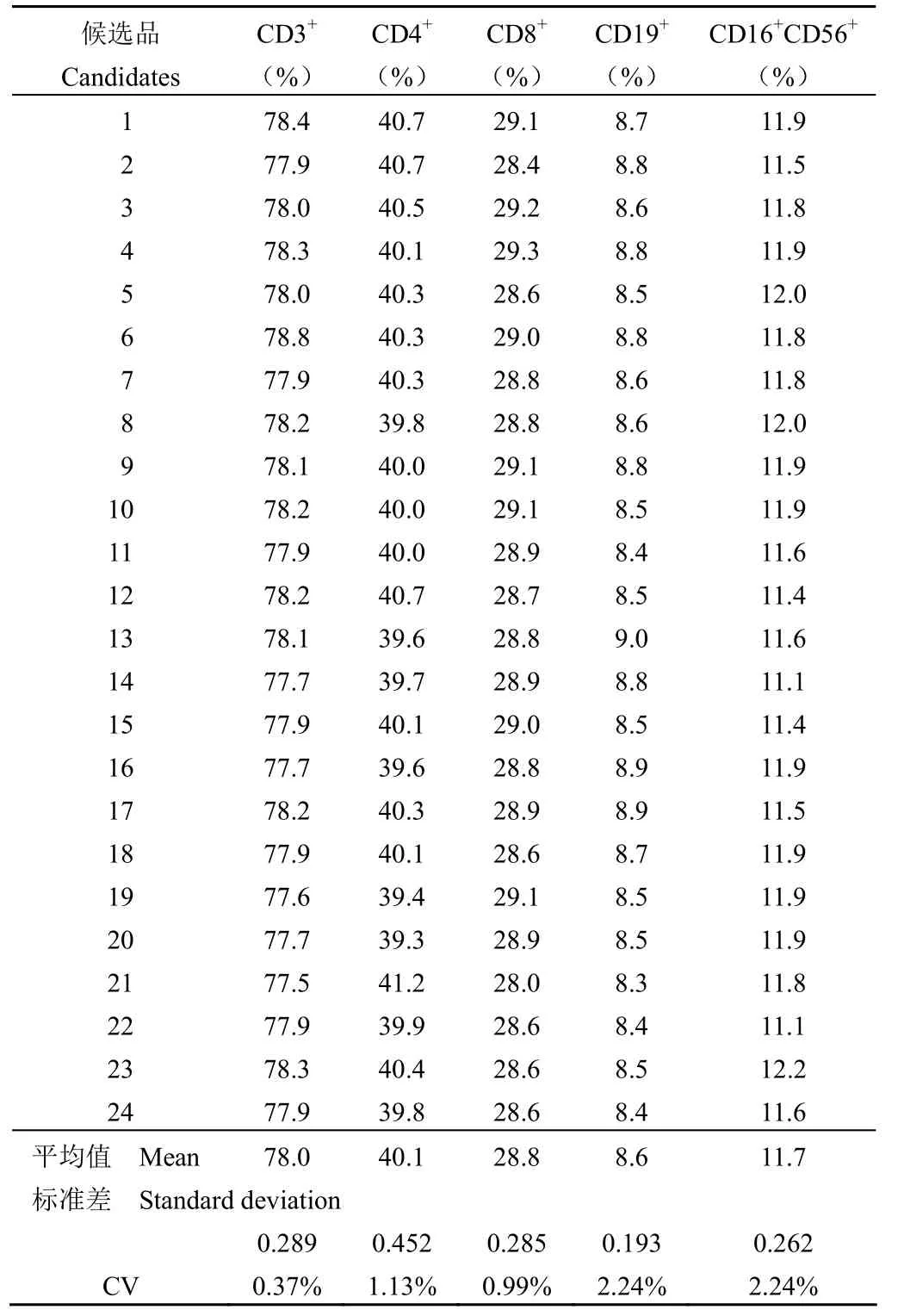
表2 候选品冻干后 T/B/NK 细胞表面抗原检测数据Table 2 Detection data of T/B/NK cell surface antigen after lyophilization

表3 稳定性研究实验结果Table 3 The results of stability study
2.3 人淋巴细胞国家参考品候选品稳定性实验结果
冻干候选品在室温和 37 ℃ 条件下,放置不同时间之后,与 -20 ℃ 保存的标准品候选品(作为 0 天对照)进行 T/B/NK 淋巴细胞亚群的百分比和绝对计数的分析比较,效价均在 0.89 ~ 1.01 之间。结果表明,候选品在室温条件和 37 ℃ 条件下保存 30 d 内非常稳定,见表 3 和表 4。
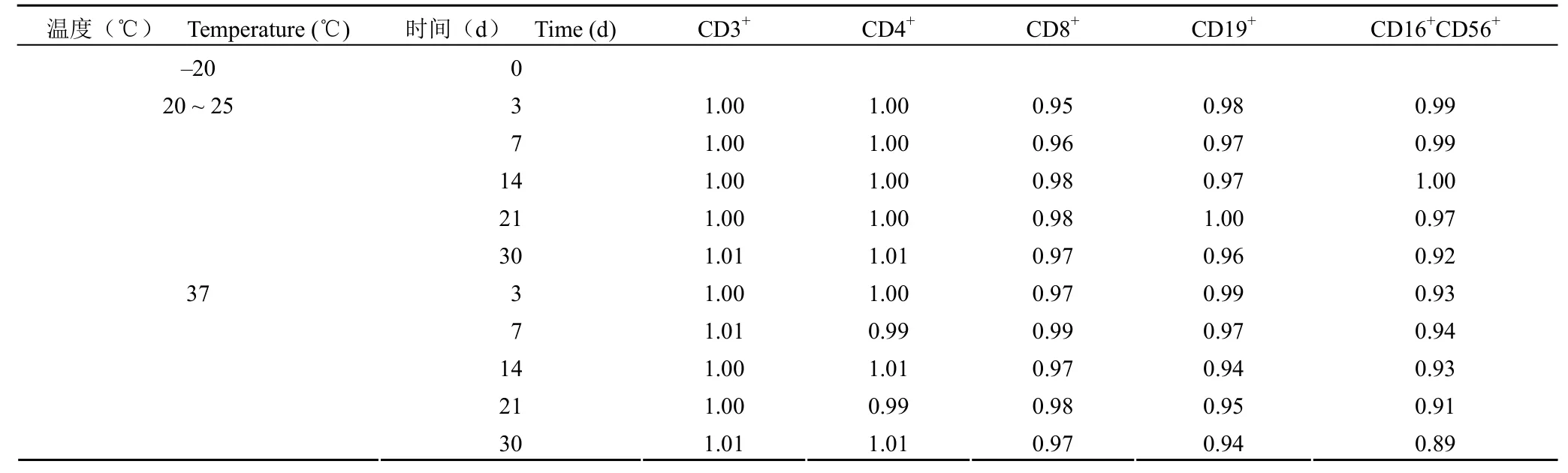
表4 不同实验条件与 -20 ℃ 的效价比较Table 4 Comparison the titer of different experimental conditions with -20 ℃

图1 复溶稳定性研究实验结果Figure 1 The stability results of dissolved candidates
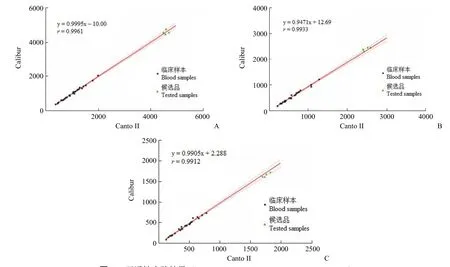
图2 互通性实验结果(A:CD3Abs;B:CD4Abs;C:CD8Abs)Figure 2 The results of commutability evaluation (A: CD3Abs; B: CD4Abs; C: CD8Abs)
2.4 复溶稳定性结果
秩和检验对复溶稳定性实验结果进行数据统计分析,结果如图 1 所示,复溶 2 h 和 0 h 相比,T/B/NK 的百分比结果并无显著性差异,P 值均大于 0.05,复溶 6 h 和 0 h 相比,除 NK 细胞(CD16+CD56+)的 P 值为 0.02 外,其他 T/B 细胞的 P 值均大于 0.05,说明候选品复溶后在 2 ~ 8 ℃ 条件下可保存至少 2 h。
2.5 互通性评估
以 25 份临床样本 CD3+、CD4+、CD8+各亚群淋巴细胞绝对数量的测定结果做散点图,y 轴 为以 BD FACS Calibur 测定的结果,x 轴为 BD Canto II 测定的结果,进行线性回归分析。样本回归曲线及其 ±95% 上下限区间以及相关系数 r 值,如图 2 所示。图中以虚线标示 ±95% 上下限区间,绿色散点代表 4 支国家参考品候选品在此 2 个流式平台测得的数值。结果表明,CD3+、CD4+、CD8+细胞绝对数量在此 Calibur 和 Canto II 平台的互通性良好。
3 讨论
适用于流式细胞法的 T/B/NK 淋巴细胞亚群检测试剂在临床上主要用于评价机体的免疫功能、诊断与监测恶性肿瘤、器官移植、免疫性疾病如 艾滋病、原发性免疫缺陷病、自身免疫病等,尤其是 CD4 阳性的淋巴细胞的绝对数量和 CD4/CD8 比值监测还是艾滋病患者用药指导的一个重要指 标[13-14]。制定统一的国家标准品有助于使各实验室间的检测结果具有可比性,实现检测标准化。将健康人外周血淋巴细胞进行冻干之后作为标准物质具有易于操作标准化、方便客户使用、利于运输保存的优势,相比传统液氮深低温保存的细胞更适合作为标准物质[15-17]。
本文通过对标准物质瓶间均匀性、稳定性分析和互通性评估的实验研究,此批冻干型人淋巴细胞国家参考品候选品满足作为国家标准物质的要求,可用于人 T/B/NK 淋巴细胞亚群检测试剂的准确性评价。
