基于网络药理学及分子对接技术的痰热清胶囊治疗新冠肺炎的物质基础及机制研究*
2020-11-09韦祖猛黄卫清赵宁波廖金花彭双凤徐丽丽
韦祖猛 黄卫清 赵宁波 廖金花 彭双凤 凌 利 徐丽丽△ 李 林△
(1.江西中医药大学,江西 南昌 330004;2.江西中医药大学附属医院,江西 南昌 330006;3.上海凯宝药业股份有限公司,上海 201401)
新型冠状病毒肺炎(新冠肺炎)由β属冠状病毒的2019-nCoV感染引起[1],可通过呼吸道飞沫、密切接触以及气溶胶传播。目前新冠肺炎大流行正以指数级速度增长,被世界卫生组织(WHO)列为国际关注的突发公共卫生事件。目前还未有对COVID-19的特效抗病毒药物,而中药成分多样,具有多靶点、整体调节的独特优势,临床反馈提示中医药治疗新冠肺炎疗效显著[2]。痰热清胶囊是由上海凯宝药业股份有限公司研制的中成药制剂,由5味中药组成,其中黄芩为君药,性苦寒,清肺热,燥湿解毒;熊胆粉和山羊角为臣药,具有清热解毒、息风止痉、祛痰平喘等作用;金银花和连翘为佐使药以助清热解毒、宣透散邪[3]。在抗击新冠肺炎疫情中,痰热清注射液在国家卫生健康委、国家中医药管理局发布的第六版、第七版诊疗方案中被纳入重症、危重症推荐用药,而痰热清胶囊则在部分省市的诊疗方案中被列为轻症推荐用药[4-5]。目前由上海市公共卫生临床中心负责的《痰热清胶囊治疗新型冠状病毒肺炎(COVID-19)临床试验》(注册号ChiCTR2000029813)正在进行,以评价痰热清胶囊治疗新冠肺炎有效性及安全性。本研究拟借助于网络药理学及分子对接的研究方法对痰热清胶囊治疗新冠肺炎的潜在活性成分及作用机制进行预测,以期为该药治疗新冠肺炎提供理论参考。
1 资料与方法
1.1 痰热清胶囊主要活性成分筛选 在CNKI、万方、维普及中国生物医学数据库中以“痰热清胶囊”以及主要组成药物为主题,“活性成分”为全文搜索关键词,检索痰热清胶囊已见于文献报道的化学成分。通过Pubchem数据库检索药物成分的2D分子结构,以SDF格式保存,构建痰热清胶囊小分子结构数据库。将分子结构的SDF文件导入SwissADME平台(http://www.swissadme.ch/)进行类药性及口服生物利用度分析。同时,结合文献报道中经实验证实具有药理活性的药物组分,经分析后获取痰热清胶囊的主要活性成分。
1.2 主要成分及疾病靶点预测 将成分分子结构的SDF文件导入SwissTargetPrediction平台(http://www.swisstargetprediction.ch/)进行成分靶点预测,获取药物成分靶点。在 GeneCards(https://www.genecards.org/)数据库中以“Novel coronavirus pneumonia”为关键词检索疾病相关的基因。
1.3 药物-成分-靶点通路及核心靶点PPI网络构建运用R语言将主要活性成分的相关靶标蛋白基因名称进行统一。经Excel2019规范处理后导入Cytoscape3.7.0构建药物、成分、靶点互助网络。将药物与疾病的交集靶点导入String11.0数据库(https://stringdb.org/)获取靶标蛋白互作网络数据,并借助Cytoscape3.7.0软件进行可视化。
1.4 核心靶点通路分析 为进一步了解核心靶点基因的功能和痰热清胶囊治疗病毒性肺炎的主要作用通路,借助R语言对药物成分靶点与疾病相关基因取交集。然后将交集基因输入Metascape平台(https://metascape.org/gp/index.html)的“Multiple Gene list”的功能界面,物种选定为“H.sapiens(human)”,进行 GO功能注释及KEGG通路富集分析,结果借助R语言可视化。
1.5 分子对接 冠状病毒的3CL水解酶为冠状病毒的主要蛋白酶之一,与病毒复制和转录密切相关,可作为药物设计的关键靶标[6]。目前上海科技大学饶子和、杨海涛课题组公布了COVID-19 3CL水解酶的X射线晶体结构(PDB 6LU7)。本研究从PDB数据库(https://www.rcsb.org/)下载该晶体结构的3D结构,利用PyMol软件对蛋白进行去水,分离原配体的处理后,在AutoDockTools完成蛋白和原配体的加氢,计算电荷,保存为相应的PDBQT结构文件。从Pubchem下载痰热清胶囊主要成分及瑞德西韦及氯喹的二维结构的sdf文件,通过ChemBioDraw3D软件将其全部转化为三维结构的MOL2格式文件。借助AutoDockTools软件对MOL2格式的小分子进行加氢,计算电荷,加Root处理后,保存为对接必备的PDBQT结构文件,完成配体的准备工作。对于3CL水解酶蛋白活性口袋的位置,借助POCASA 1.1平台(http://altair.sci.hokudai.ac.jp/g6/service/pocasa/)基于滚动探针球的蛋白口袋识别算法进行预测,获得可能性最高的5种预测结果,从中选取与蛋白原配体坐标重合度最高的口袋位置。最后运行AutoDock进行对接,取能量最低的构象为最优构象,并以3CL水解酶与原配体返回对接结果为阳性对照。
2 结果
2.1 活性化合物的筛选及靶点预测 见表1。文献检索共纳入87个药物成分[7],经SwissADME平台筛选后,共获得痰热清胶囊的主要活性成分26个,其中黄芩苷、绿原酸及其异构体口服利用度虽较低,但仍以主要化合物而得以保留。将候选成分的2D分子结构导入SwissTargetPrediction平台进行靶蛋白预测,共获得相关靶标蛋白293个。
2.2 药物-化合物-靶点网络 见图1。药物-化合物-靶点网络共有324个节点和757条边。网络拓扑学分析显示的平均度值为4.67、平均最短路径3.5,平均相邻节点数4.6,网络集中度0.3。度值表示预测出该成分与作用靶点的关联个数,度值越大说明该成分越重要。经统计发现大于平均度值的网络节点的有68个,其中药物成分26个,靶点42个;度值排名前10的化合物包括:黄芩素、异绿原酸C、鹅去氧胆酸、熊去氧胆酸、异绿原酸B、咖啡酸、亮氨酸、苯丙氨酸、胆酸、木樨草苷。此外,度值大于15的化合物还包括既往文献报道的主要化合物如黄芩苷、连翘苷。排名前10的靶点包括:AKR1B1、AKR1B10、CA2、CA12、MMP2、ADORA1、CA7、PTGS2、ADRA2A、NOX4。
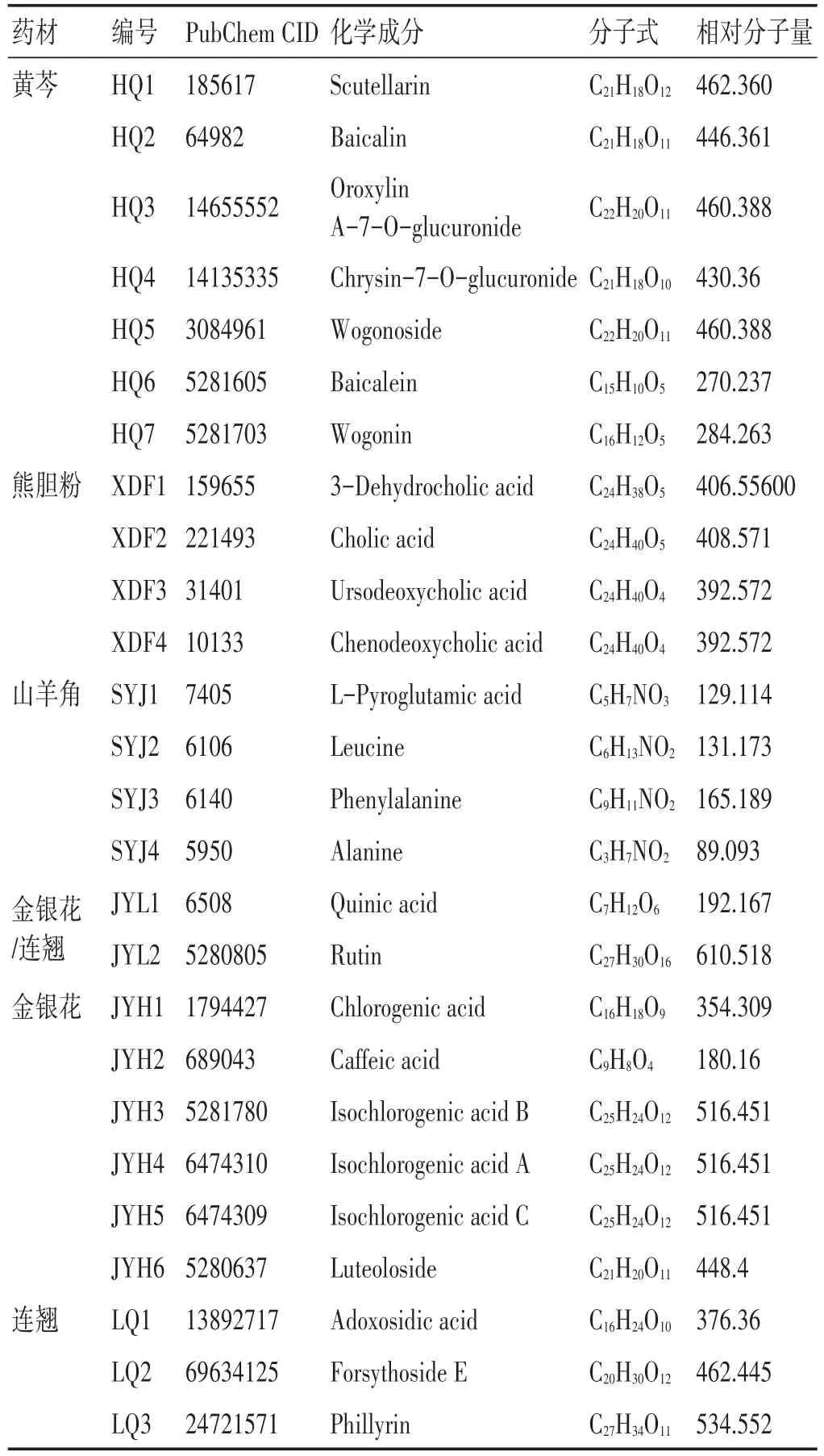
表1 痰热清胶囊主要成分

图1 药物-化合物-靶点网络
2.3 痰热清胶囊治疗新冠肺炎PPI互作网络 见图2~图3,表2。根据GeneCards数据库检索疾病靶点,得到259个靶点。运用R语言将主要活性成分的调控靶点与疾病靶点取交集,得到26个痰热清胶囊治疗新冠肺炎的靶点。将26个靶点基因导入String平台进行PPI网络分析,核心网络图包含26个节点,174条边,其中节点表示蛋白,每条边则表示蛋白与蛋白之间的相互作用关系,线条越多表示关联度越大。靶蛋白平均节点度值为10,超过平均度值的靶蛋白有15个,说明这15个靶蛋白是PPI网络中的关键靶点。痰热清胶囊的药理作用很可能是通过作用于这些靶点得以发挥,将度值由高到低排序。
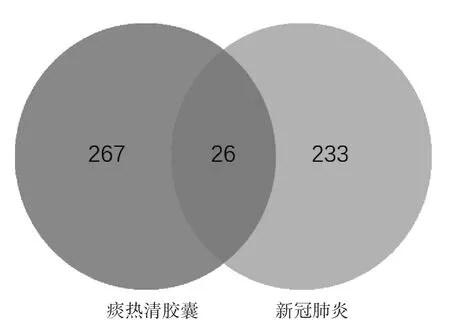
图2 痰热清胶囊与新冠肺炎靶点(Vene图)
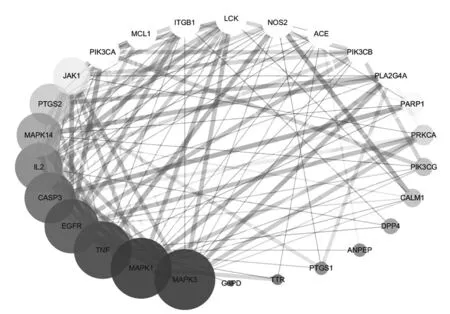
图3 痰热清胶囊与新冠肺炎核心靶蛋白(PPI网络图)
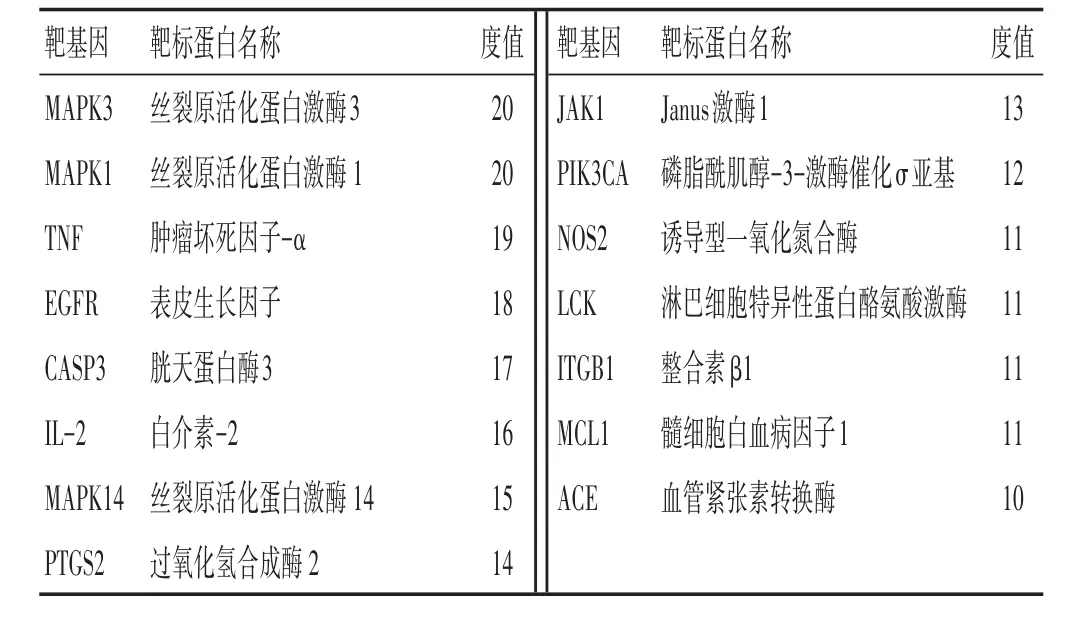
表2 PPI网络关键靶标蛋白
2.4 核心靶点通路分析 见图4。将上述得到的26个交集靶点导入Metascape平台进行GO及KEGG功能富集分析,所得结果经R语言可视化处理(见图4A),KEGG通路富集筛选获得前19条相关通路,涉及PI3K-Akt信号通路、人乳头瘤病毒感染、MAPK信号通路、甲型流感、自然杀伤细胞介导的细胞毒性、TNFα信号途径、T细胞受体信号通路、Toll样受体信号通路、IL-17信号通路、NF-κB信号通路等。GO功能富集分析后获得相关条目50条(见图4B、C、D)。GO-BP涉及炎症反应的调节、病毒生命周期、病毒入侵宿主细胞、免疫反应激活、T细胞活化、中性粒细胞介导免疫、免疫反应中细胞因子分泌的调节、MAPK级联调节等。GO-CC涉及膜筏、细胞质核周区、溶酶体、质膜外侧、细胞-基质粘附连接等。GO-MF涉及病毒受体活性、受体配体活性、细胞因子受体结合、MAP激酶活性、磷脂酰肌醇3激酶活性等。

图4 KEGG富集分析(A)、GO生物学过程分析(B)、GO细胞组分分析(C)、GO分子功能分析(D)
2.5 分子对接结果 见表3。一般认为配体与受体结合的构象稳定时能量最低,发生的作用可能性最大。分子对接结果显示,原配体的最优结合能为-6.77 kcal/mol,瑞德西韦及氯喹的结合能分别为-7.46、-7.04 kcal/mol。将网络拓扑分析中度值大于15的药物成分进行对接,其中结合能低于-8 kcal/mol药物成分共有6个。
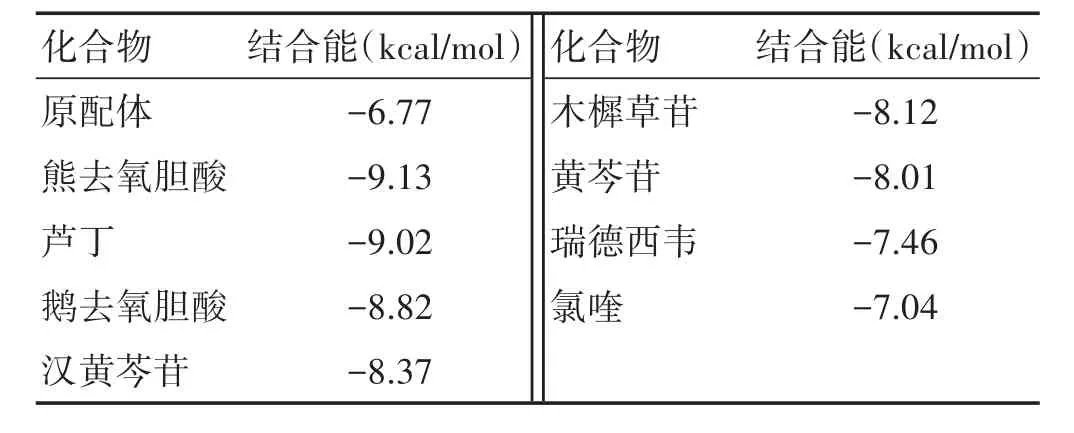
表3 代表性成分及临床推荐化学药物与2019-nCoV 3CL水解酶的结合能
3 讨论
新冠肺炎传染性强,传播迅速,人群广泛易感,属于中医学“疫病”范畴。目前学者普遍认为湿毒是本病的关键,同时极易变燥、化热、伤阴,由于区位气候的差异,又有湿温、寒湿、湿毒夹燥等证候特点[8-10]。痰热清胶囊具有燥湿解毒、清热化痰、宣散透邪之效,可用于风温肺热、湿毒为甚患者的辨证用药。
本研究运用分子对接技术发现熊去氧胆酸、芦丁、鹅去氧胆酸、汉黄芩苷、木樨草苷、黄芩苷的结合能普遍低于原配体及临床上推荐的抗病毒药物瑞德西韦、氯喹,表明上述6个成分与COVID-19 3CL水解酶的结合能力较强,可抑制病毒的复制,发挥抗病毒作用。而GO生物学过程分析亦提示痰热清胶囊的药理作用涉及病毒生命周期、病毒入侵宿主细胞,细胞组分主要在细胞膜及细胞质核周区,分子功能与病毒受体活性相关,表明痰热清胶囊的抗病毒作用可能贯穿于病毒入侵、转录复制、播散等过程。有研究显示黄芩素可通过抑制流感病毒的中后期mRNA的转录和复制或抑制流感病毒的神经氨酸苷酶的活性,降低病毒的毒力而发挥抗病毒作用[11]。黄芩苷作为黄芩的主要成分以及黄芩素在人体内的代谢产物,有抑菌、抗氧化、抗病毒的作用,有实验发现黄芩苷可作用于甲型流感病毒的核蛋白转录过程,负性调控基因的转录而发挥抗病毒作用[12]。鹅去氧胆酸、熊去氧胆酸熊胆粉水解提取物的主要成分,现代药理表明其具有抑菌、抗病毒、消炎的作用[13]。木樨草苷作为金银花的黄酮类有效成分,研究显示对呼吸道合胞体病毒有很强的抗病毒活性[14]。
机体免疫系统过度激活及促炎因子大量释放引发的“炎症风暴”被认为是新冠肺炎重症化的重要诱因[15]。PPI互助网络显示TNF-α及IL-2是痰热清胶囊活性成分的重要靶点,KEGG通路富集分析涉及TNF-α、IL-17及NF-κB信号通路。其中TNF-α是重要的促炎症因子[16],IL-2被称为T细胞生长因子(TCGF),对于调控体内淋巴细胞功能和稳态起重要作用[17]。芦丁、绿原酸及其异构体作为痰热清胶囊中良好的抗氧化剂,可对抗炎症过程中大量ROS释放对肺组织的氧化损伤,同时抑制ROS对NF-κB的活化,减少促炎因子的释放,起到抗炎作用[18-20]。此外GO生物过程分析还涉及T细胞活化、中性粒细胞介导免疫、免疫反应中细胞因子分泌的调节、炎症反应调节,亦可作为痰热清胶囊调节免疫及炎症反应的佐证。
EGFR是受体酪氨酸激酶EerbB家族成员,目前认为在炎症因子如TNF-α、IL17等的刺激下可导致EGFR磷酸化而激活下游的ERK、p38MAPK信号通路,上调黏蛋白5AC(MUC5AC)的表达,导致黏蛋白过度分泌,痰液黏稠度升高[21-22]。目前新冠肺炎患者遗体解剖报告指出死亡患者肺内渗出性反应明显,肺腔内见大量胶冻状黏液痰[23]。有研究表明,黄芩的提取物且同为痰热清胶囊有效成分的野黄芩苷(Scutellarin)可通过抑制由人中性粒细胞弹性蛋白酶(HNE)诱导的PKC-ERK信号传导途径激活,下调MUC5AC的表达,减少气道黏膜黏液的分泌[23]。因此,推测痰热清胶囊可能通过减少炎症因子的释放以及抑制EGFR、ERK、p38MAPK的活化而下调黏蛋白的表达从而减少渗出、降低痰液黏稠度,促进痰液排出。
综上,本研究通过网络药理学及分子对接方法证实痰热清胶囊通过多成分、多靶点、多通路治疗新冠肺炎,其涉及的机制包括抗病毒、下调炎症反应、免疫调节、抗氧化、调节气道黏液分泌等,可为痰热清胶囊治疗新冠肺炎及下一步的实验提供参考。鉴于网络药理学及虚拟对接的局限性,后期还需通过体内、体外实验来验证本次研究结果,以期为痰热清胶囊治疗新冠肺炎提供实验依据。
