十二烷基酰胺丙基磷酸酯甜菜碱的复配性能研究
2020-11-08沈俊肖小峰刘佳佳林良良
沈俊,肖小峰,刘佳佳,林良良
(1.联合利华(中国)有限公司上海分公司,上海 200335;2.涟水新源生物科技有限公司,江苏 淮安 223400;3.江南大学 化学与材料工程学院,江苏 无锡 214122)
工业上使用的表面活性剂大多是不同类型的混合物,表面活性剂复配使用能显著改变表面活性[1-7],不仅能节约成本还能获得优良的性能。十二烷基酰胺丙基磷酸酯甜菜碱(C12-APA)既有两性表面活性剂的多功能特性[8-10],又因结构类似于细胞中的磷酸甘油酯而具有特殊的滑腻感,被广泛用于化妆品、洗涤剂、纺织工业等日用化学品领域[11-12]。目前对这种表面活性剂的研究主要基于其表面性能以及应用性能,对其二元体系还未有报道[13-14]。本文侧重于C12-APA与常用的阴离子表面活性剂十二烷基硫酸钠(SDS)和非离子表面活性剂脂肪醇聚氧乙烯醚9(AEO9)的复配性能研究。
1 实验部分
1.1 试剂与仪器
十二烷基酰胺丙基磷酸酯甜菜碱(≥ 95%),自制;十二烷基硫酸钠、十二烷基聚氧乙烯(9)醚、NaCl、二苯甲酮、芘均为分析纯;超纯水,电阻率18.2 MΩ·cm(25 ℃),自制。
JF1004型电子分析天平;DF-101S型集热式恒温磁力搅拌器;DC-0506型低温恒温槽;OCA-40型光学接触角测量仪;CARY Eclipse型荧光分光光度计。
1.2 实验方法
1.2.1 表面张力测定 按照一定的摩尔比,用0.1 mol/L NaCl溶液配制不同浓度的复配表面活性剂溶液,采用悬滴法测溶液的表面张力,温度为(25±0.5) ℃,然后作γ-lgc曲线。
1.2.2 微极性的测定 采用荧光探针法[15]测定胶束的微极性,使用芘作为荧光探针物质。用饱和芘的NaCl(0.1 mol/L)水溶液作为溶剂,按照一定的摩尔比,制备一系列不同浓度的二元表面活性剂复配体系。在(25±0.5) ℃下测量不同溶液中芘的荧光光谱。激发波长为335 nm,读取波长为373 nm和384 nm处的荧光强度I1和I3,作I1/I3-lgc曲线。
1.2.3 胶束聚集数的测定 通过稳态荧光探针法[16]测定表面活性剂水溶液的胶束聚集数。使用饱和芘的NaCl(0.1 mol/L)水溶液作为溶剂,按照一定的摩尔比,制备一系列不同浓度的二元表面活性剂复配体系。其中,溶液中添加的猝灭剂为二苯甲酮,再配制一组浓度相同但不含猝灭剂的溶液作对比。然后将配制的溶液置于恒温水浴中24 h,从低浓度到高浓度依次测量各溶液中芘的荧光发射光谱,测定温度为(25±0.5) ℃。
假设荧光探针和猝灭剂遵循胶束之间的Poisson分布,胶束为单分散,则探针的荧光强度与胶束聚集数存在以下关系:
(1)
其中,I0是不含猝灭剂时的荧光强度;Nm为胶束聚集数;CQ是猝灭剂浓度,为0.04 mmol/L;ST是表面活性剂总浓度;cmc为临界胶束浓度;I1是含猝灭剂时的荧光强度。
2 结果与讨论
2.1 复配体系的表面化学性质
在(25±0.5) ℃下,分别测定SDS/C12-APA和AEO9/C12-APA复配体系在0.1 mol/L NaCl水溶液中的表面张力,作γ-lgc曲线(见图1和图2),由此可以得出cmc和γcmc的值。表1和表2分别列出了复配体系SDS/C12-APA和AEO9/C12-APA的表面活性参数(Γmax,Amin,pC20,Γmax,Amin和cmc/C20)。
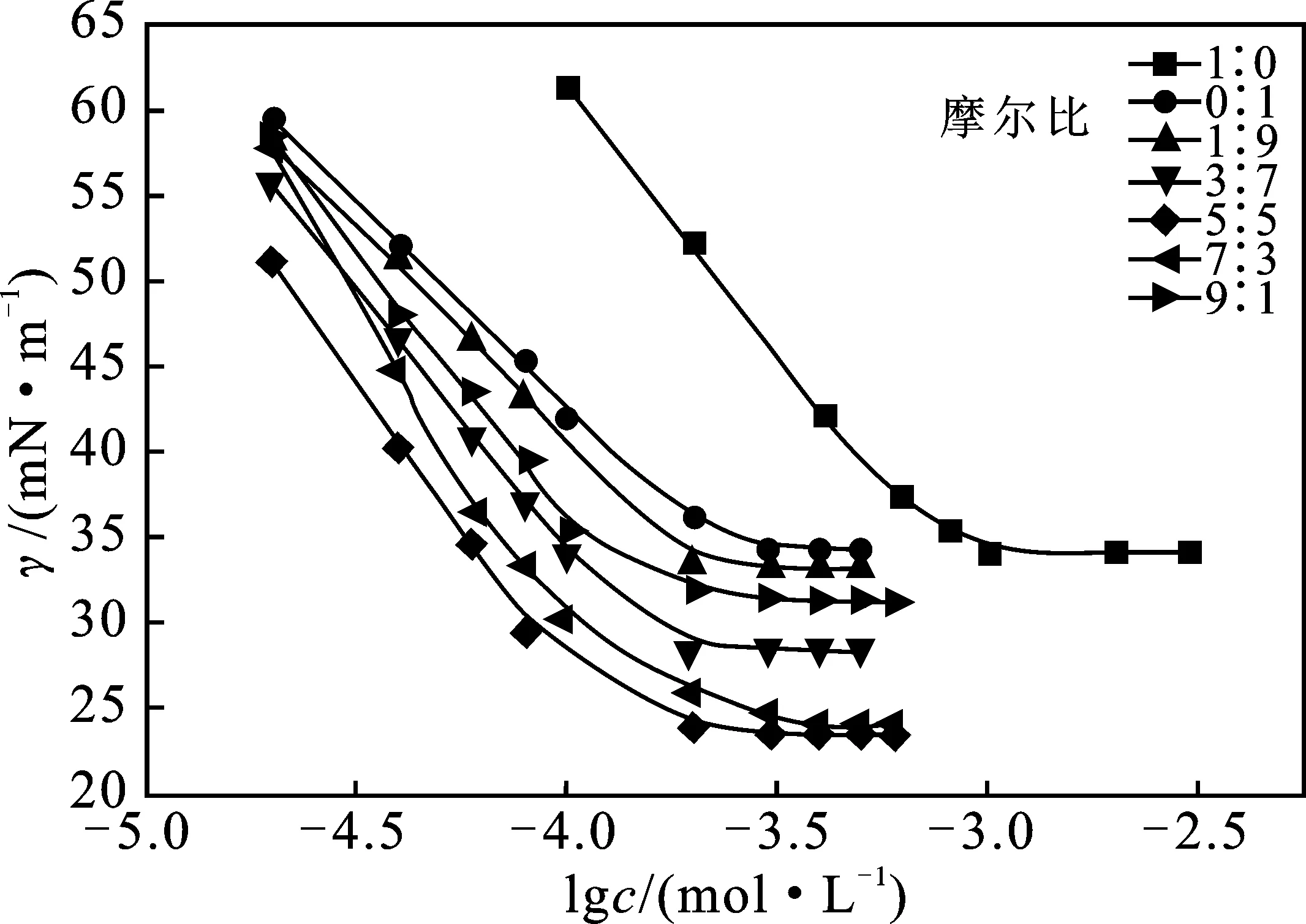
图1 SDS/C12-APA复配体系的γ-lgc曲线Fig.1 Surface tension vs molar concentration plots for SDS/C12-APA mixture
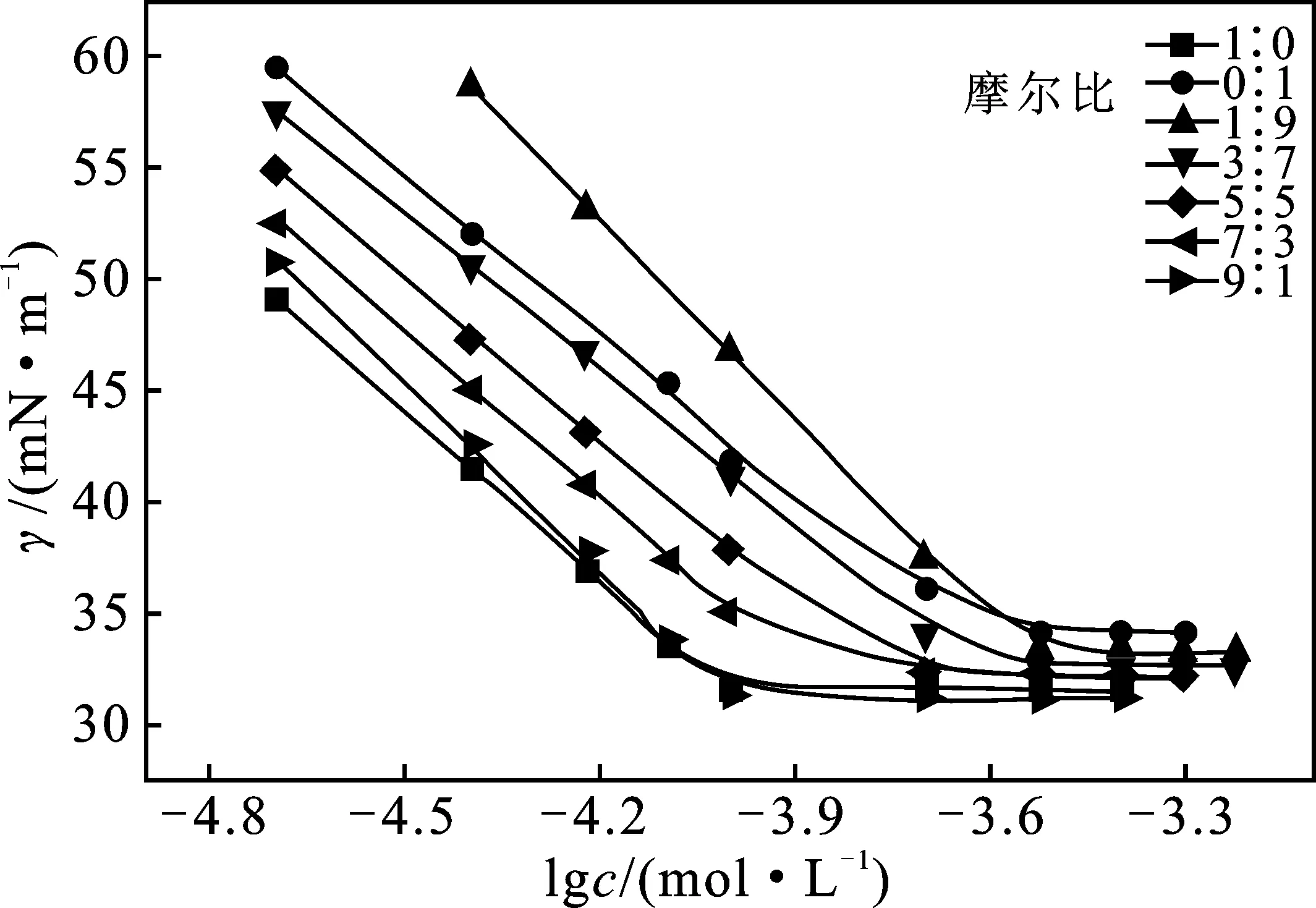
图2 AEO9/C12-APA复配体系的γ-lgc曲线Fig.2 Surface tension vs molar concentration plots for AEO9/C12-APA mixture
对于复配体系,理想吸附状况下分子的平均截面积Amin(ide)可以由式(2)计算得到:
(2)
式中,Amin,1和Amin,2是表示表面活性剂1、2在溶液表面的平均分子占有面积。
由表1可知,复配体系的cmc和γcmc比单一表面活性剂的都低,当α1= 0.5时,cmc和γcmc均达到最低,此时的cmc/c20值也达到最大,说明在这个比例下,比起胶束化,表面活性剂更容易吸附在界面上。 复配体系的Amin介于两种单一表面活性剂的Amin之间,随着C12-APA在混合体系中摩尔占比的增加而增大,说明C12-APA与SDS之间发生了很强的相互作用,当SDS加入到C12-APA中后,二者形成了很强的静电吸引(类似于图3),同时减弱C12-APA离子头基之间的静电排斥力,碳氢链之间的疏水作用使得表面活性剂分子在气/液界面排列得更紧密,吸附量增大,所以复配体系的表面活性增大。从熵增原理来看,C12-APA与SDS分子形成混合胶束以后,分子间结合得更加紧密,离子头基之间的空隙减小,头基周围水分子的自由度增加,导致体系混乱度增加,这有利于胶束的形成。
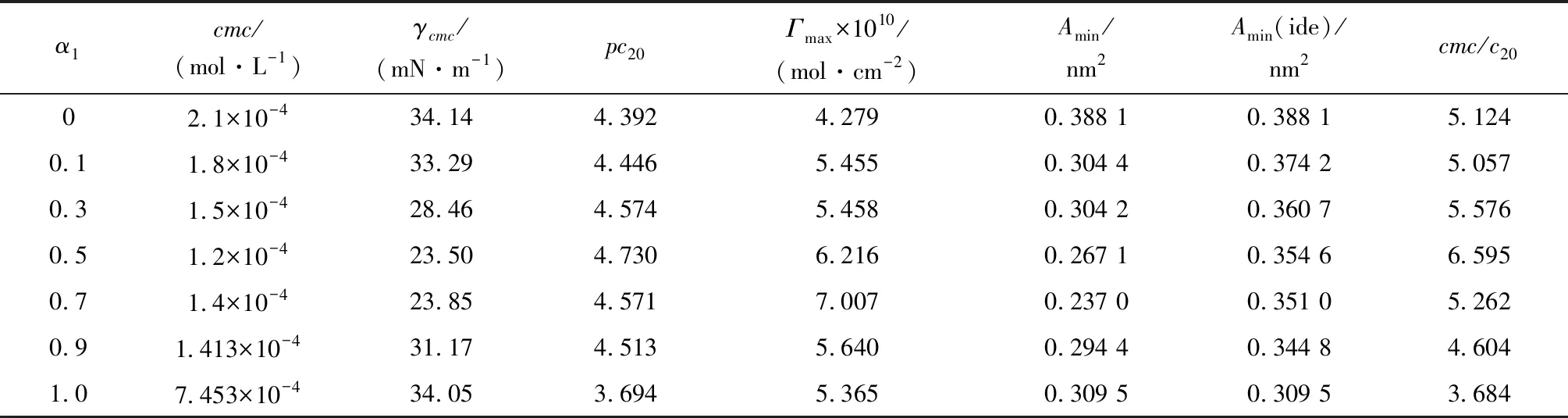
表1 SDS/C12-APA复配体系的表面活性参数((25±0.5) ℃,[NaCl]=0.1 mol/L)Table 1 Surface active parameter of SDS/C12-APA mixtures in 0.1 mol/L NaCl at(25 ± 0.5) ℃
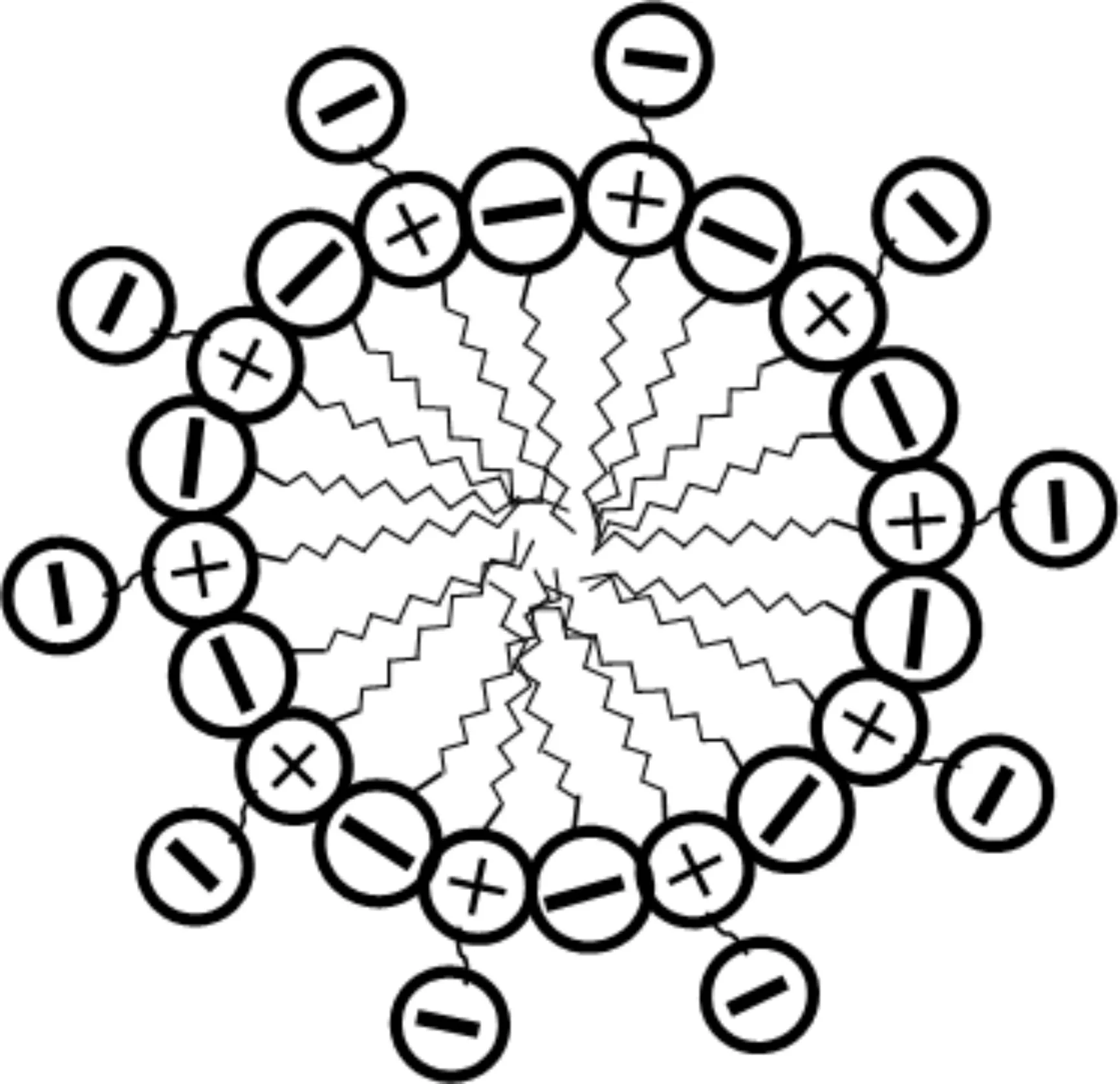
图3 SDS/C12-APA混合体系分子间的相互作用示意Fig.3 The orientations of the monomers of SDS/C12-APA binary mixed system on the micelle layer
由表2可知,AEO9/C12-APA复配体系的表面活性参数基本介于单一表面活性剂AEO9和C12-APA之间,未表现出明显的协同增效作用。这是因为C12-APA分子的亲水头基同时具有季铵盐基团和磷酸酯基团,较强的空间位阻使得AEO9分子很难与C12-APA分子有效结合,AEO9分子未能有效屏蔽C12-APA离子头基之间的静电排斥作用,导致复配体系无法在气/液界面形成更加稳定、紧密的单分子膜,因而AEO9分子和C12-APA分子之间的相互作用较弱。因此,两性表面活性剂不一定总能与其他类型表面活性剂表现出明显的协同增效作用。

表2 AEO9/C12-APA复配体系的表面活性参数((25±0.5) ℃,[NaCl]=0.1 mol/L)Table 2 Surface active parameter of AEO9/C12-APA mixtures in 0.1 mol/L NaCl at(25 ± 0.5) ℃
2.2 复配体系的协同作用
大量研究表明,复配使用不同种类的表面活性剂时,能显著增强表面活性剂的表面活性,获得比单一表面活性剂更好的性能,即产生协同效应。这主要是因为混合体系分子间存在相互作用(包括在界面形成混合吸附单层和在溶液中形成混合胶束)。由正规溶液理论[17]可知,两种不同表面活性剂之间相互作用的性质和强度通常用参数β来表示,如βσ和βm可判定表面活性剂分子间是否存在以下几个方面的协同效应。
2.2.1 降低表面张力的效率方面 对于复配体系,给定表面张力下降所需的混合表面活性剂浓度低于任意单一表面活性剂所需的浓度时,即具有降低表面张力的效率方面的协同效应。βσ为表面活性剂分子在气/液界面形成的混合吸附单层的相互作用参数,用来判定体系是否存在协同效应:
(3)
(4)
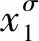
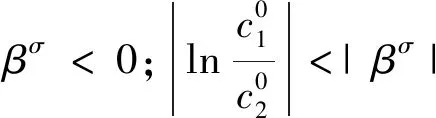
(5)
2.2.2 混合胶束的形成方面 对于复配体系,当混合表面活性剂的cmc低于任意单一表面活性剂cmc时,即具有混合胶束形成方面的协同效应。βm为表面活性剂分子在气/液界面形成的混合胶束之间的相互作用参数,用来判定体系是否存在协同效应。
(6)
(7)
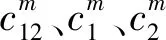
(8)
2.2.3 降低表面张力的效能方面 对于复配体系,当混合表面活性剂浓度达到cmc时的γcmc低于任意单一表面活性剂达到的γcmc,即具有降低表面张力的效能方面的协同效应。βσ为表面活性剂分子在气/液界面形成的混合吸附单层的相互作用参数,用来判定体系是否存在协同效应。
βσ<0;βσ-βm<0;
(9)
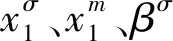

表3 SDS/C12-APA复配体系的分子相互作用和协同效应参数Table 3 Molecular interaction and synergistic effect parameters of SDS/C12-APA mixtures
根据|β|值的大小,可以将二元混合体系分子间的相互作用分为三类[18]:①当|βσ|或|βm|>10,则认为复配体系分子间存在强相互作用,例如二元混合体系阴/阳离子在常温下βm的平均值为-19;②当3 ≤|βσ|或|βm|≤ 10,则认为复配体系分子间存在中等相互作用,通常指阴/两性离子和阴/非离子复配体系,例如二元混合体系阴/非离子在常温下βm的平均值为-3.4;③当|βσ|或|βm|<3,则认为复配体系之间是弱相互作用,例如二元混合体系阴/阳离子在常温下βm的平均值为-2.7。
由βσ或βm值可知,对于SDS/C12-APA复配体系而言,分子间的作用属于中等相互作用,这是因为两性离子表面活性剂兼具阳离子头基和阴离子头基,使得SDS/C12-APA之间的静电吸引要弱于阴/阳离子表面活性剂之间的静电引力。
对于AEO9/C12-APA复配体系,由于不存在协同效应,此处不作讨论。
2.3 聚集体状态研究
2.3.1 微极性 在(25± 0.5) ℃下,分别测定SDS/C12-APA和AEO9/C12-APA复配体系在0.1 mol/L NaCl的饱和芘水溶液中的微极性,作出I1/I3-lgc曲线(见图4和图5)。
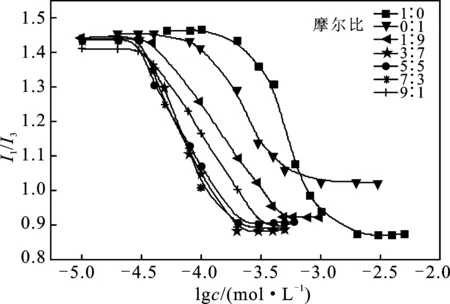
图4 SDS/C12-APA复配体系的微极性Fig.4 Micropolarity of SDS/C12-APA binary system

图5 AEO9/C12-APA复配体系的微极性Fig.5 Micropolarity of AEO9/C12-APA binary system
由图4和图5可知,SDS/C12-APA和AEO9/C12-APA复配体系的I1/I3值随着表面活性剂浓度的增加,下降到某一平台后基本保持不变,这是因为胶束的形成使得探针芘增溶到栅栏层。由I1/I3-lgc曲线得到的复配体系的cmc与悬滴法测得的数值基本一致。
由图4可知,随着浓度的增加,C12-APA的I1/I3值从1.46降低到0.87,SDS的I1/I3值从1.45降低到1.02。对于复配体系,I1/I3值则更快地降低至某一更低的水平。这主要是因为复配体系形成的混合胶束比单一表面活性剂的更为紧密,所以微极性更低。从微极性等温线可以初步判断复配比例在3∶7,5∶5,7∶3时,体系协同效应最为明显。
由图5可知,在所有的复配比例下,体系的微极性等温线均在AEO9和C12-APA的微极性等温线之间,得到的cmc也在两种单一表面活性剂的之间。初步判定AEO9和C12-APA形成的混合体系没有协同效应。
2.3.2 胶束聚集数 在(25± 0.5) ℃时,分别测定SDS/C12-APA和AEO9/C12-APA复配体系在0.1 mol/L NaCl水溶液中的胶束聚集数(Nm),复配体系的总浓度均为7cmc,结果见表4和表5。

表4 SDS/C12-APA复配体系的胶束聚集数Table 4 Nm of SDS/C12-APA compounding system

表5 AEO9/C12-APA复配体系的胶束聚集数Table 5 Nm of AEO9/C12-APA compounding system
由表4和表5可知,SDS/C12-APA和AEO9/C12-APA复配体系所形成的胶束聚集数均小于单一表面活性剂的胶束聚集数,而且在不同的复配比例下,体系的胶束聚集数相差不大。这说明复配体系形成的胶束结构更加紧密,混合体系形成了比原来更小更稳定的胶束结构。
3 结论
(1)在(25± 0.5) ℃,0.1 mol/L NaCl的条件下,研究了SDS/C12-APA和AEO9/C12-APA复配体系的表面性能及相互作用。结果表明,当在C12-APA溶液中加入一定量的SDS时,体系的表面活性大大提高。利用正规溶液理论研究两个复配体系之间的协同作用,发现仅适用于SDS/C12-APA复配体系;SDS/C12-APA复配体系在降低cmc、表面张力的效率和效能方面均具有协同作用,由β值可以判定SDS/C12-APA复配体系分子间存在中等相互作用,而对AEO9/C12-APA复配体系的研究表明,无协同作用。
(2)在(25± 0.5) ℃下,0.1 mol/L NaCl的条件下,采用荧光探针法研究了SDS/C12-APA和AEO9/C12-APA复配体系的微极性。结果表明,由I1/I3-lgc曲线得到的复配体系的cmc与悬滴法测得的数值基本一致。对于SDS/C12-APA复配体系,从微极性等温线可以初步判断复配比例在3∶7,5∶5,7∶3时,体系协同效应最为明显。对于AEO9/C12-APA复配体系,初步判定AEO9和C12-APA形成的混合体系没有协同效应。
(3)在(25± 0.5) ℃下,采用稳态荧光探针法研究了SDS/C12-APA和AEO9/C12-APA复配体系在0.1 mol/L NaCl水溶液中的胶束聚集数。结果表明,SDS/C12-APA和AEO9/C12-APA复配体系所形成的胶束聚集数,均小于单一表面活性剂的胶束聚集数,而且在不同的复配比例下,体系的胶束聚集数相差不大。
