雷珠单抗联合Ahmed青光眼引流阀植入治疗NVG的Meta分析
2020-11-02陈帅征穆雅林
陈帅征,穆雅林
0 引言
新生血管性青光眼(neovascular glaucoma,NVG)作为继发性青光眼的一种,是严重的、难以预防且易复发的致盲性眼病。Weiss等[1]在1963年首次应用“新生血管性青光眼”这个概念,用来描述由于新的血管及结缔组织生成而导致眼压升高的一类青光眼。现在NVG是指由新生血管的形成导致血管膜长入,进而阻塞房角,使房水流出受阻形成的继发性医学状态。其病因复杂多样,95%以上由伴随眼部缺血症状的全身或眼部疾病所导致[2]。NVG最常见的三种诱发病因是糖尿病视网膜病变(DR)(33%)、视网膜中央静脉阻塞(CRVO)(33%)和眼部缺血性综合征(OIS)(13%)。其他可导致眼部明显缺血症状的疾病如视网膜中央动脉阻塞(CRAO)、视网膜分支静脉阻塞(BRVO)、视网膜静脉周围炎和镰状细胞贫血性视网膜病变也可导致NVG[3]。
2006年,雷珠单抗获批用于临床眼科疾病治疗[4],随着大量的临床应用,玻璃体腔内注射雷珠单抗被证实可改善眼底组织缺血缺氧状态,减少虹膜新生血管,降低NVG患者的眼内压[5]。虽然雷珠单抗的可靠性和安全性已得到证实,但其潜在的眼内炎、晶状体损伤、眼压升高、玻璃体积血、血管栓塞等并发症不可忽视,而重复注射雷珠单抗也给患者带来巨大的经济负担[6]。Ahmed青光眼引流阀(Ahmed glaucoma valve,AGV)植入术适用于各种原发病引起的青光眼。Tan等[7]研究认为,AGV植入术和小梁切除术在手术成功率、降眼压药物使用改善率和术中并发症发生率相近,但前者可明显减少术后并发症。随着AGV植入术及雷珠单抗在临床治疗NVG中的应用越来越多,已经有较多探讨相关治疗措施的临床效果及预后的研究,但其结论纷繁不一。本研究通过检索筛选高质量的临床研究,以评估玻璃体腔内注射雷珠单抗联合AGV植入术相对于单纯应用AGV植入术治疗NVG的有效性和安全性。
1 资料和方法
1.1 资料
1.1.1 文献检索检索策略:应用计算机检索PubMed、EMbase、Cochrane Library、美国科学引文索引数据库(SCI)、中国知网(CNKI)、中文科技期刊数据库(VIP)、万方数据库、中国生物医学文献服务系统(CBM)等多个数据库。中文检索采用主题词模糊检索,检索词包括:“雷珠单抗”、“新生血管性青光眼”、“青光眼引流阀”或“Ahmed引流阀”。英文检索采用主题词和自由词进行检索,检索词包括:Glaucoma,Neovascular、Glaucomas,Neovascular、Neovascular Glaucoma、Neovascular Glaucomas;Ranibizumab、RhuFab V2、V2,RhuFab、Lucentis;Ahmed Valve、Ahmed Glaucoma Valve、Glaucoma Valve,检索条目根据各网站不同特性做相应调整。检索时限均为自建库至2020-03-20。
1.1.2 纳入标准(1)研究类型:前瞻性和回顾性临床对照研究,无论是否采用盲法、有无失访。(2)研究对象:明确诊断的NVG患者,性别、年龄、种族、国家及地区等不限。(3)干预措施:玻璃体腔注射雷珠单抗+Ahmed引流阀植入术vsAhmed引流阀植入术。(4)结局指标:眼压、最佳矫正视力、术后前房出血发生率、抗青光眼药物使用数量。
1.1.3 排除标准(1)文摘、综述和述评类文献。(2)非临床研究,如动物模型研究等。(3)缺乏对照组的研究。(4)检测结果数据缺乏,模糊不可收集,如计数资料未提供原始数据而仅有计算后的率,计量资料无具体均数和标准差。(5)除玻璃体腔注射雷珠单抗和AGV植入术外同时应用其他干预措施的研究。(6)纳入总样本量小于20及文献评估质量较差的研究。(7)基于相同数据重复发表的文章。
1.2 方法由2位研究员根据纳入和排除标准独立查询上述数据库,应用文献管理工具排除重复文献,并通过阅读文献题目、摘要、全文,最后得出拟纳入文献。核对拟纳入文献和筛选过程,分歧点进行讨论后得出最终纳入文献。对前瞻性对照试验采用Cochrane系统评价手册5.1版进行文献质量评价,对回顾性队列研究采用Newcastle-Ottawa Scale(NOS)文献质量评价量表进行文献质量评价。由2位研究人员对纳入文献资料进行独立提取并交叉核对,内容包括作者、发表年份、研究设计方案、随访时间、研究对象特征、干预治疗方案及对照方案、结局测量指标、失访人数及不良事件等。
统计学分析:运用RevMan 5.3和STATA 12.0软件行Meta分析。异质性检验采用Cochran Q检验,并用I2定量评估异质性的大小,当I2<40%且Q检验P>0.1时认为纳入的研究同质性好,选用固定效应模型,当I2≥40%或Q检验P≤0.1时表明纳入的研究有异质性,采用随机效应模型。采用敏感性分析检查结果的同质性和稳定性。由于纳入的文献为前瞻性对照试验和回顾性队列研究,计数资料采用相对危险度(relative risk,RR)及其95% 置信区间(confidence interval,CI)为疗效分析统计量;各纳入研究中对视力和眼压等计量资料的测量方法和测量单位一致,故计量资料采用均数差(mean difference,MD)及其95%CI为疗效分析统计量,Meta分析结果以森林图显示。采用Begger和Egger检验评估各研究间发表偏倚。P<0.05为差异具有统计学意义。
2 结果
2.1 文献检索结果初检得到115篇文献,依据纳入和排除标准筛选后,最终纳入7篇临床研究,其中5篇前瞻性对照试验[8-12],2篇回顾性队列研究[13-14],共计纳入患者346例349眼。文献筛选流程见图1。试验组和对照组患者年龄、性别、术前最佳矫正视力和眼压等基线数据合并后比较显示均无统计学差异,纳入文献的一般情况见表1。
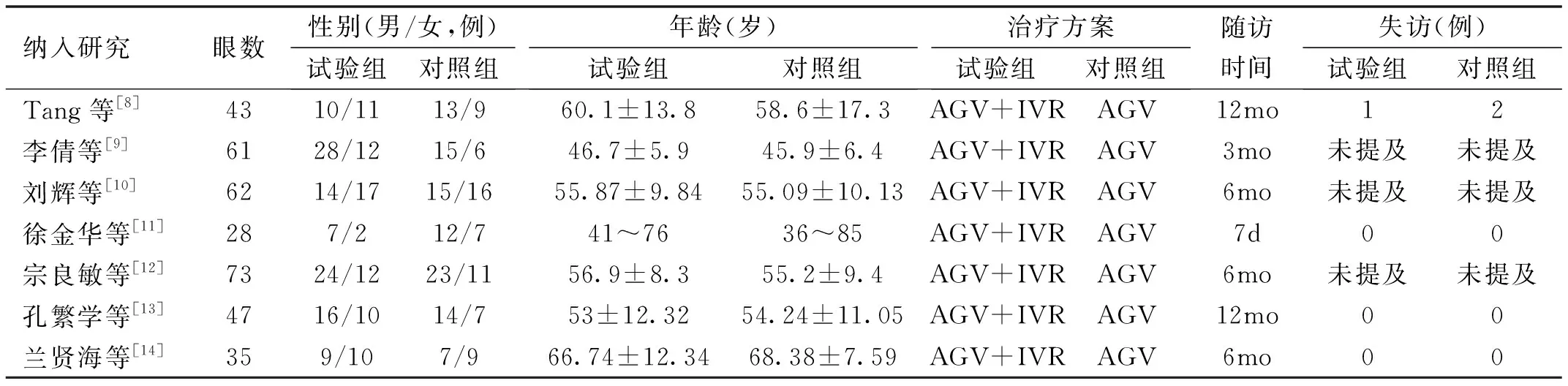
表1 纳入研究的基本资料特征

表2 纳入的前瞻性研究的Cochrane质量评价
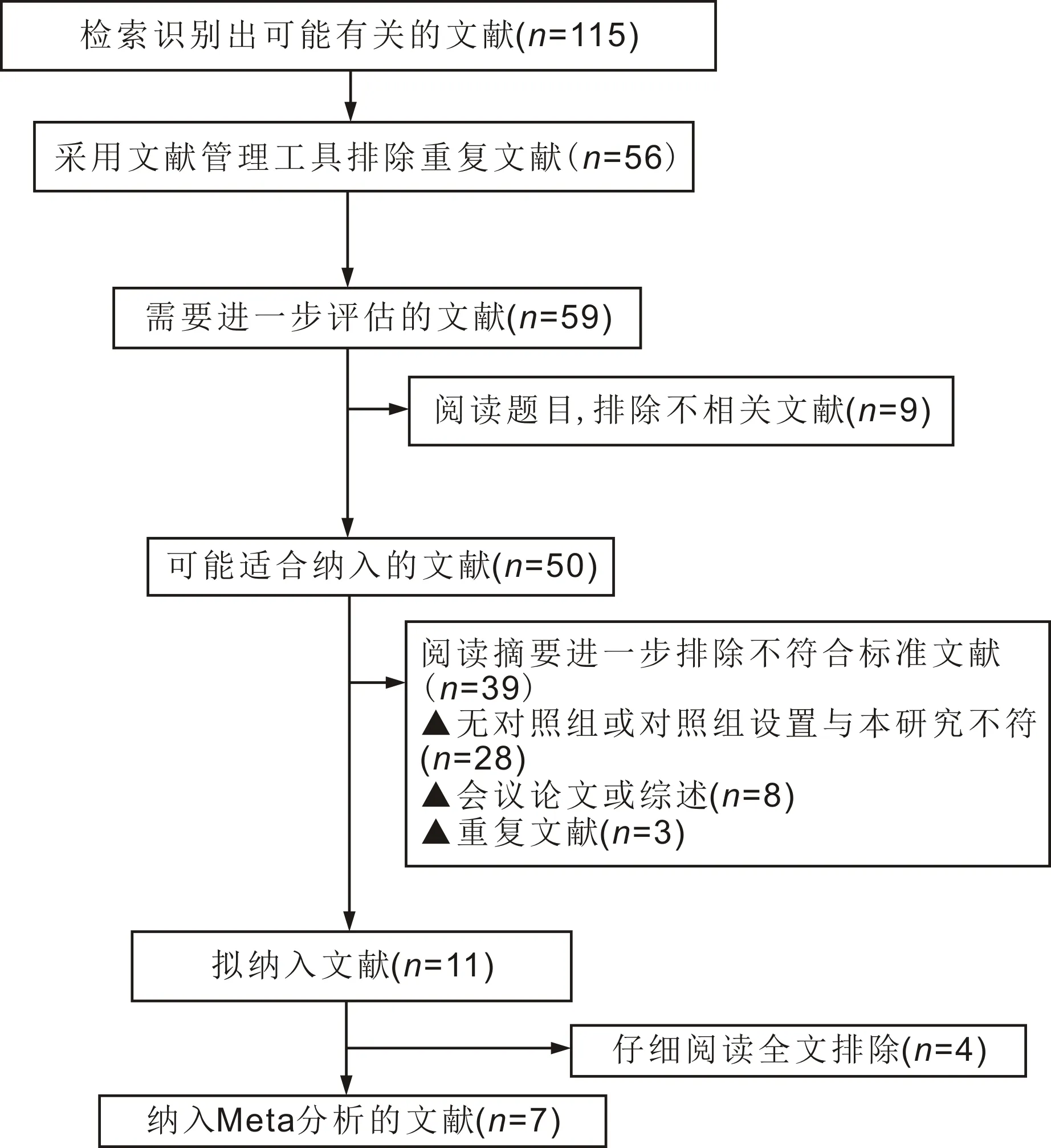
图1 文献筛选流程及结果。
2.2 纳入研究的偏倚风险评价纳入5篇前瞻性对照试验的文献质量评价见表2。根据NOS量表,纳入的2篇回顾性队列研究在暴露队列的代表性、非暴露队列的选择、暴露的确定、结果测定方法、随访时间、随访完整性6个方面均评估为低风险,在暴露与非暴露的可比性方面评估为未知风险,在研究开始时间相对结局出现时间方面评估为高风险,提示纳入的2篇回顾性队列研究的总体文献质量评估均为中高质量。
2.3 Meta分析结果
2.3.1 术后眼压术后眼压比较的森林图见图2。3篇文献记录了术后1wk的眼压,各研究间存在异质性(P=0.15,I2=47%),采用随机效应模型合并统计量。Meta分析结果显示,两组术后1wk眼压差异有统计学意义(MD=-3.35,95%CI-5.62~-1.09,P=0.004),提示术后1wk,雷珠单抗联合AGV植入患者眼压较单纯AGV植入患者低。5篇文献记录了术后1mo的眼压,纳入研究之间存在异质性(P<0.001,I2=96%),采用逐一剔除法行敏感性分析,发现剔除李倩等[9]研究后异质性下降(P=0.006,I2=76%),Meta分析结果显示,两组术后1mo眼压差异有统计学意义(MD=-2.87,95%CI-5.55~-0.19,P=0.04),提示术后1mo,雷珠单抗联合AGV植入患者眼压较单纯AGV植入患者低。4篇文献记录了术后6mo的眼压,纳入研究之间存在异质性(P=0.03,I2=66%),采用随机效应模型合并统计量。Meta分析结果显示,两组术后6mo眼压差异无统计学意义(MD=-1.75,95%CI-4.15~0.66,P=0.15),提示术后6mo,雷珠单抗联合AGV植入患者眼压与单纯AGV植入患者相比无明显统计学差异。
2.3.2 术后最佳矫正视力术后最佳矫正视力比较的森林图见图3。2篇文献记录了术后1、3、6mo最佳矫正视力(均采用LogMAR视力记录法),各研究之间均不存在异质性(P=0.65,I2=0%;P=1.00,I2=0%;P=0.60,I2=0%),采用固定效应模型合并统计量。Meta分析结果显示,两组术后1、3mo最佳矫正视力差异均有统计学意义(MD=-0.23,95%CI-0.37~0.08,P=0.003;MD=-0.20,95%CI-0.35~0.05,P=0.007),提示术后1、3mo,雷珠单抗联合AGV植入患者最佳矫正视力较单纯AGV植入患者好;两组术后6mo最佳矫正视力差异无统计学意义(MD=-0.07,95%CI-0.21~0.08,P=0.35),提示术后6mo雷珠单抗联合AGV植入患者最佳矫正视力与单纯AGV植入患者无明显差异。
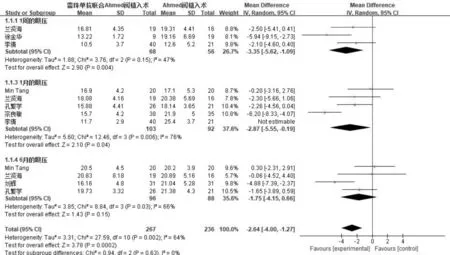
图2 两组患者术后眼压比较的Meta分析森林图。
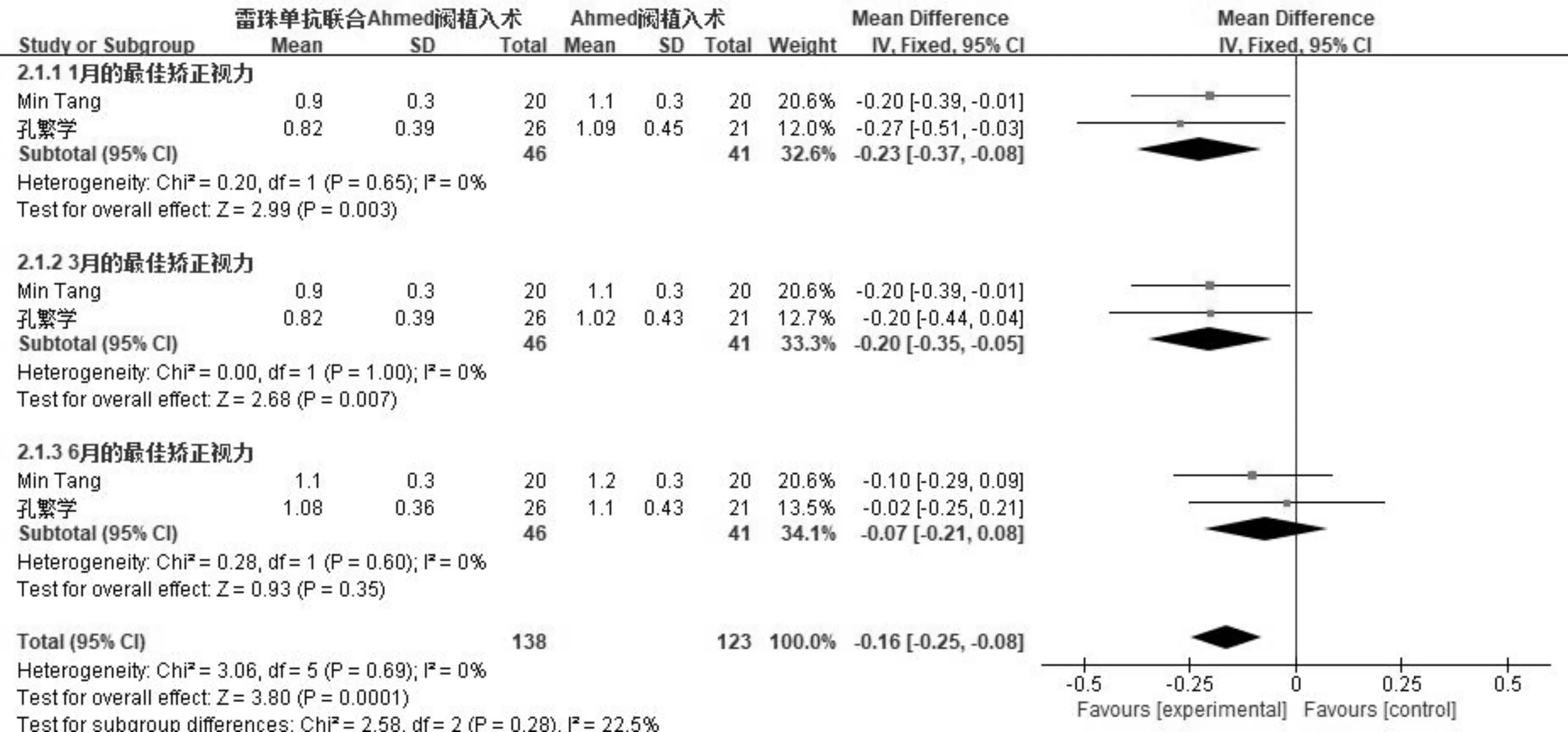
图3 两组患者术后最佳矫正视力比较的Meta分析森林图。
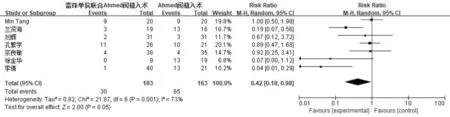
图4 两组患者术后前房出血率比较的Meta分析森林图。
2.3.3术后前房出血率术后前房出血率比较的森林图见图4。纳入的7篇文献均记录了术后前房出血率,各研究之间存在异质性(P=0.001,I2=73%),采用随机效应模型合并统计量。Meta分析结果显示,两组术后前房出血率差异无统计学意义(RR=0.42,95%CI0.18~0.98,P=0.05),提示两组患者术后前房出血率无明显差异。
2.3.4 术后抗青光眼药物使用数量术后抗青光眼药物使用数量比较的森林图见图5。2篇文献记录了术后抗青光眼药物使用数量,各研究之间不存在异质性(P=1.00,I2=0%),采用固定效应模型合并统计量。Meta分析结果显示,两组术后抗青光眼药物使用数量差异无统计学意义(MD=-0.10,95%CI-0.34~0.14,P=0.42),提示雷珠单抗联合AGV植入患者术后抗青光眼药物使用数量与单纯AGV植入患者无明显差异。
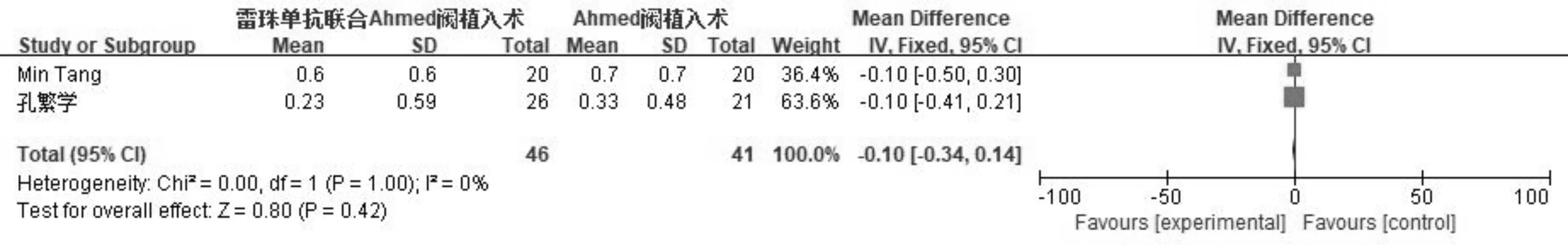
图5 两组患者术后抗青光眼药物使用数量比较的Meta分析森林图。
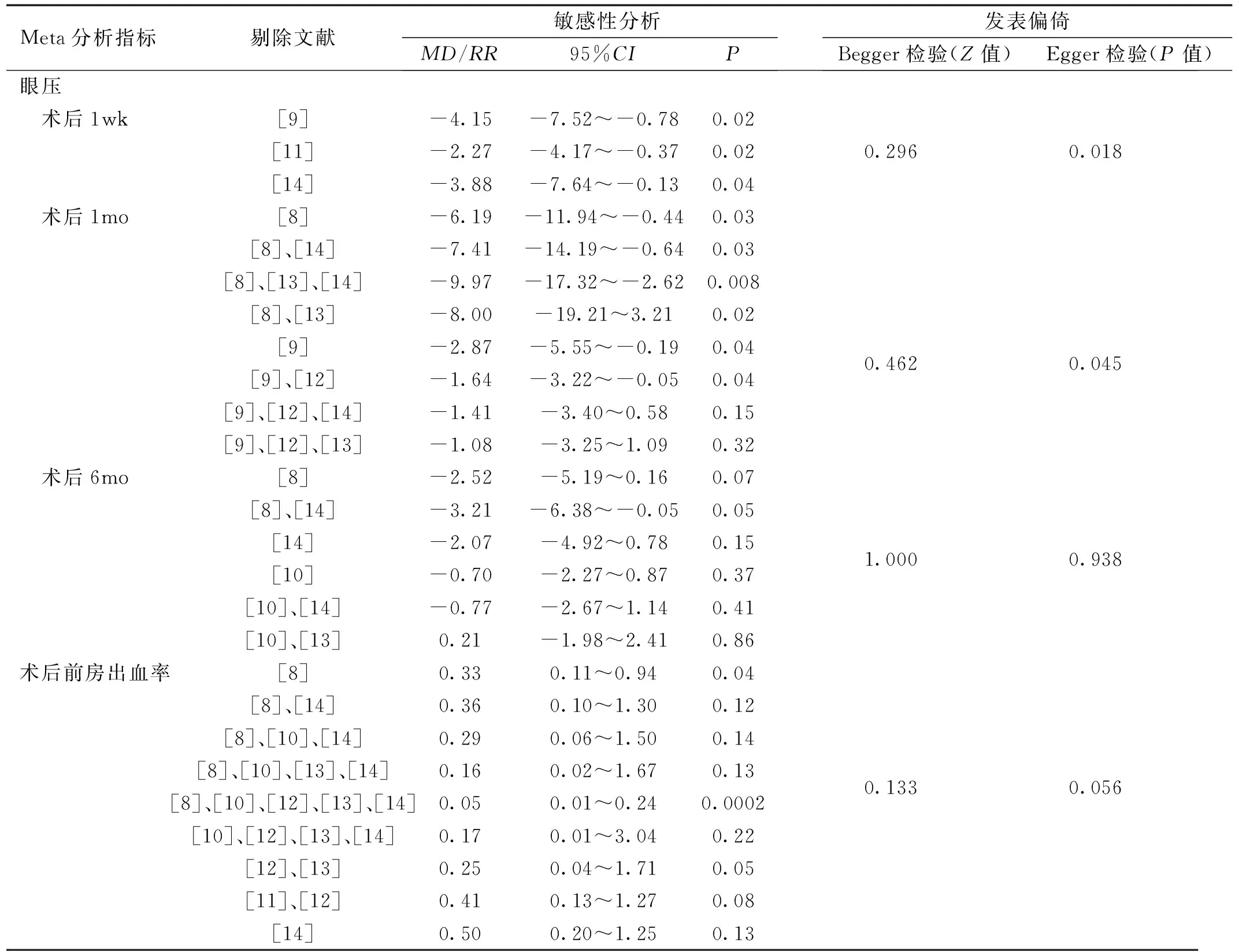
表4 基于不同Meta分析指标的敏感性分析和发表偏倚检验
2.3.5敏感性分析和发表偏倚对纳入研究>2的结局指标采用逐一剔除法行敏感性分析,其中术后眼压采用MD及其95%CI作为疗效分析统计量,术后前房出血率采用RR及其95%CI作为疗效分析统计量。结果显示,术后1wk,6mo眼压和术后前房出血率合并效应结果在剔除研究前后统计学意义基本一致,故受剔除研究的影响较小,提示以上合并效应的结果稳定性较好。但术后1mo眼压的合并结果中,合并效应受剔除研究的影响较大(剔除文献[9]前后对合并结果的影响大),见表4。采用Begger和Egger检验评估各研究间的发表偏倚,结果显示,术后1wk,1mo眼压的合并效应存在一定程度的发表偏倚,分析是由于纳入的研究较少,故该合并效应有待后期进一步证实。
3 讨论
NVG为难治性青光眼,属于难以挽救视力的疾病之一。临床中NVG患者面临多种痛苦,如眼压持续或间歇升高导致眼部炎症及疼痛,原发病及新生血管出血导致视力下降,眼压升高对视神经压迫进而导致视神经萎缩,视网膜神经节细胞损害,神经纤维丢失导致视野缺损,角膜水肿乃至继发性角膜大泡形成,角膜失代偿导致视力进一步下降及眼磨等。NVG的高眼压状态又可导致视网膜缺血加剧,从而形成恶性循环。因此NVG对视功能的损伤极其严重,其致盲率高达92.4%[15]。
传统的小梁切除术在NVG治疗中由于术后前房出血、房角新生血管长入、滤过泡瘢痕化等原因,有着较高的失败率。Ahmed引流阀的出现为NVG的手术治疗提供了新的方案。Tan等[7]对507例行AGV植入术和小梁切除术的患者进行Meta分析,发现两组手术成功率、降压药物使用改善率和术中并发症发生率相近,但AGV植入术后并发症发生率明显下降。AGV的引流盘置于赤道部附近,也可用于因眼前节手术而导致瘢痕增生的患者[16]。
抗血管内皮生长因子(VEGF)药物的应用为眼底病患者带来了福音,雷珠单抗作为其中分子量较小的一种抗VEGF药物,有着作用迅速、穿透能力强等优点[17]。随着临床的大量应用,雷珠单抗在NVG治疗中的有效性和安全性也得到证实[18]。Kitnarong等[19]认为雷珠单抗联合小梁切除术治疗NVG相对于单纯小梁切除术可降低手术并发症,提高术后短期疗效。雷珠单抗与AGV植入术的联合应用在临床中也越来越多,基于近年出现的此类研究,本研究从中筛选高质量文献,合并分析结果以找寻更可靠的结论,希望为临床实践提供一定的参考。
本研究最终纳入7篇文献,Meta分析结果显示玻璃体腔注射雷珠单抗联合AGV植入术与单纯AGV植入术治疗NVG相比,术后早期眼压降低,中晚期眼压无明显差异。高丽花[20]纳入5篇抗VEGF药物联合AGV植入术的研究并行Meta分析,虽然该研究纳入的研究中有2项研究使用的抗VEGF药物为贝伐单抗,1项研究联合使用了视网膜激光光凝(PRP),但该研究认为抗VEGF药物联合AGV植入患者术后早期眼压较单纯AGV植入患者低,中晚期降眼压效果无明显差异,与本研究结论相似。分析原因可能为单纯应用玻璃体腔注射雷珠单抗在术后早期也可产生降眼压的效果[21],这一效果与AGV植入术产生协同作用,故联合治疗的患者术后早期眼压较低,而随着玻璃体腔雷珠单抗分子量的衰减,其作用逐渐消失,眼压无明显差异。
此外,本研究结果表明,玻璃体腔注射雷珠单抗联合AGV植入患者相较于单纯AGV植入患者在术后早中期能提高最佳矫正视力,术后晚期效果不明显。本研究分析记录术后最佳矫正视力的2项研究发现,纳入的NVG患者原发病主要构成为DR、CRVO和BRVO,而玻璃体腔注射雷珠单抗本身可以用于治疗DR和视网膜静脉阻塞(RVO)导致的黄斑水肿,促进玻璃体腔和前房的积血吸收,从而提高视力,这可能是导致术后早期最佳矫正视力产生统计学差异的原因。本研究还发现,与单纯AGV植入术相比,雷珠单抗联合AGV植入术不能降低术后前房出血率,也不能减少抗青光眼药物使用数量。
然而,本研究也存在一定的局限性:(1)纳入研究数量较少,有些合并效应量存在一定发表偏倚、检验效能不足等,可能对结果产生影响;(2)纳入研究对患者既往视网膜激光治疗史记录不统一,其中5篇文献未提及患者既往视网膜激光光凝史,可能对结果产生影响;(3)虽然各纳入研究的原发病种主要组成均为DR、RVO和OIS,但其具体比例并不统一,是潜在的混杂因素。基于上述因素,本研究得出的结论还需要谨慎对待,未来还需扩大研究对象,纳入更多的前瞻性、多中心的随机临床对照研究来进一步支持相关结论。
