酶法测定糖化白蛋白试剂盒质量控制指标分析
2020-11-02郭世富毕春雷
郭世富 毕春雷
(1.国家药品监督管理局医疗器械标准管理中心、中国食品药品检定研究院,北京 102629;2.北京市医疗器械检测所,北京 101111)
糖化白蛋白(glycated albumin,GA)是葡萄糖通过非酶促糖基化反应与血浆中白蛋白结合形成的酮胺类化合物,是临床上血糖监测的重要指标之一,能反映近期血糖(2~3 周)情况,适用于血糖波动较大的新发糖尿病(diabetes mellitus,DM)患者治疗效果评价、餐后高血糖症,且GA 与糖尿病血管并发症相关,可预测心血管事件的发生,具有较高临床价值。而糖化血红蛋白(glycated hemoglobin,HbA)可反映检测前2~3 个月内的平均血糖水平,作为临床监测长期血糖控制的金标准。与HbA相比,糖化白蛋白反映血糖短期波动,避免因血红蛋白变异而影响检测结果,作为血糖检测与控制的重要指标,在临床上越来越受到重视[1-5]。
目前,临床实验室使用的糖化白蛋白测定试剂盒大部分是采用酶法在自动生化分析仪上进行GA 定量,利用对白蛋白特异性更高的溴甲酚紫(bromocresol purple,BCP)替代原来的溴甲酚绿(bromocresol green,BCG),对白蛋白的含量进行测定,以减少球蛋白对测定结果的影响。通过糖化白蛋白与白蛋白比值的百分数报告,作为临床诊断的依据。已批准上市的酶法测定糖化白蛋白试剂盒五十余种,由于没有统一的质量控制指标,造成上市产品质量参差不齐,同时造成不同检验机构的检验结果缺乏可比性,不利于上市后产品质量控制和监督及糖化白蛋白指标的进一步临床应用研究。该研究主要对糖化白蛋白质量控制指标进行评估分析[6-8]。
1 仪器与试剂
HITACHI7020 自动生化分析仪,上市中三个厂家GA 酶法检测试剂盒。在自动生化分析仪上设置检测程序,由仪器自动完成检测。每次测定同时用质控品予以监控[9]。
2 测定原理
首先利用前处理液修饰血清白蛋白的-SH 基,与BCP 作用生成青紫色结合体,测定其吸光度(A)值得出白蛋白浓度。再利用特异性蛋白酶将GA水解为糖化氨基酸,后者被特异性的酮胺氧化酶(KAOD)生成过氧化氢,利用过氧化物酶指示系统生成色素,测定此色素的A 值,得GA 含量。
3 方法与结果
门诊收集正常和异常人群的血清样本40 例,冷冻,复融。HITACHI7020 自动生化分析仪,按厂家说明书,先校准,质控品符合要求。参照国家标准《临床化学体外诊断试剂(盒)》质量控制指标项目,建立糖化白蛋白质量控制指标,对相关项目进行测试[10]。
3.1 空白吸光度
空白样本应不含被测物,但其基质应与待测常规样本相同。如果空白样本难获得,可选用相应基质的样本,但应注意将基质效应减至最少。用三家试剂盒测试空白样本,测得规定读数点主波长下的吸光度值(A),见表1。
3.2 分析灵敏度
在糖化白蛋白样本浓度为15g/L 时,测其吸光度变化的范围。三家A、B、C 测得GA 的吸光度变化分别为0.094253,0.070898,0.069464。
3.3 线性
线性是指给出的测量结果与样品中被测量的值直接成比例的能力。将高浓度GA 样本、低浓度GA 样本和生理盐水以几种比例进行溶解而得到测试样本,对各种浓度梯度的样本的GA 浓度和ALB浓度进行测定,各测定3 次,计算均值。测定三家试剂盒GA 线性参考物质的测定值与标称值的回归值之间的偏离程度。GA 检测值与理论值进行线性回归分析见图1、图2、图3。

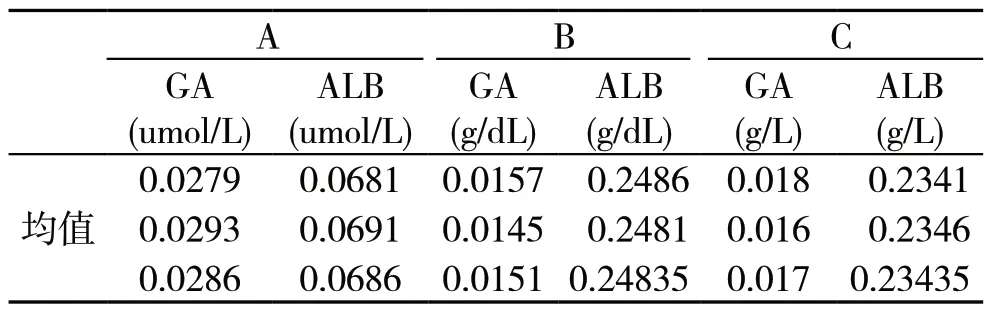
表1 三个厂家试剂盒空白吸光度分析结果
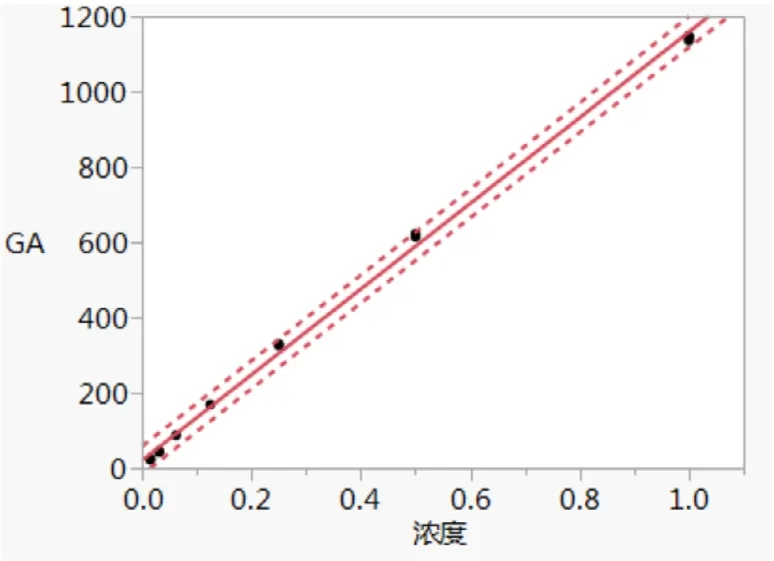
图1 厂家一试剂盒GA 线性拟合曲线
GA1 y=20.5997+1137.5325x,R2=0.998。
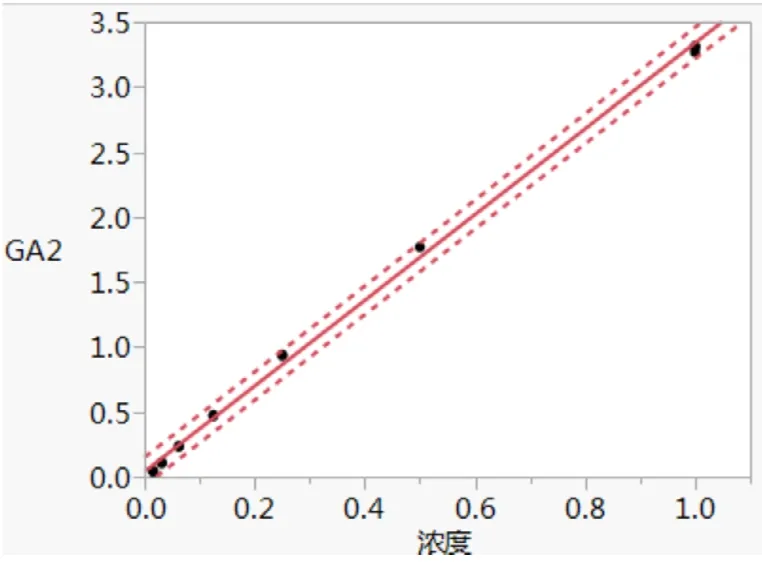
图2 厂家二试剂盒GA 线性拟合曲线
GA2 y=0.0407+3.2978x,R2=0.998。
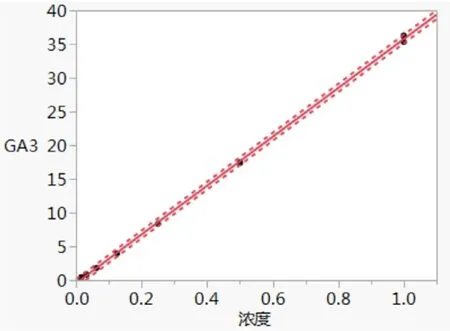
图3 厂家三试剂盒GA 线性拟合曲线
GA3 y=-0.4546+36.2066x,R2=0.9996。
3.4 重复性
重复性反映在一组测量条件下的测量精密度。用试剂盒测试已知浓度的样品,反复测定10 次,计算均值和标准差S,及变异系数CV。计算的结果均在2.0%之内,具体结果见表2。
3.5 准确性
准确性反映测得量值与被测量的真值的一致程度。由于目前缺乏糖化白蛋白国家标准品,采用不同厂家的产品进行比对(B 与C),对糖化白蛋白进行方法学比对分析,分析测定结果差异。准确性分析结果如图4 所示。

图4 厂家2 与厂家3 试剂盒的比对结果
线性回归方程为:y=0.0273+0.9789x,r=0.9998。
由分析结果可以看出,C 和B 的糖化白蛋白结果更加相近,二者的相关系数大于0.975,回归直线斜率在[0.9,1.1]内,最大偏差不大于0.8g/L,说明二者的参照系统有相关性。
4 讨论
糖化白蛋白能反映短期血糖变化的情况,因此可在早期发现糖尿病,评价降糖药物疗效,预测糖尿病血管并发症的风险以及监测造血系统疾病患者的血糖控制方面具有重要的临床诊断价值。针对酶法糖化白蛋白测定试剂盒建立统一的行业控制指标,保证产品的统一和质量可控,使试验结果具有可比性,促进临床应用研究。
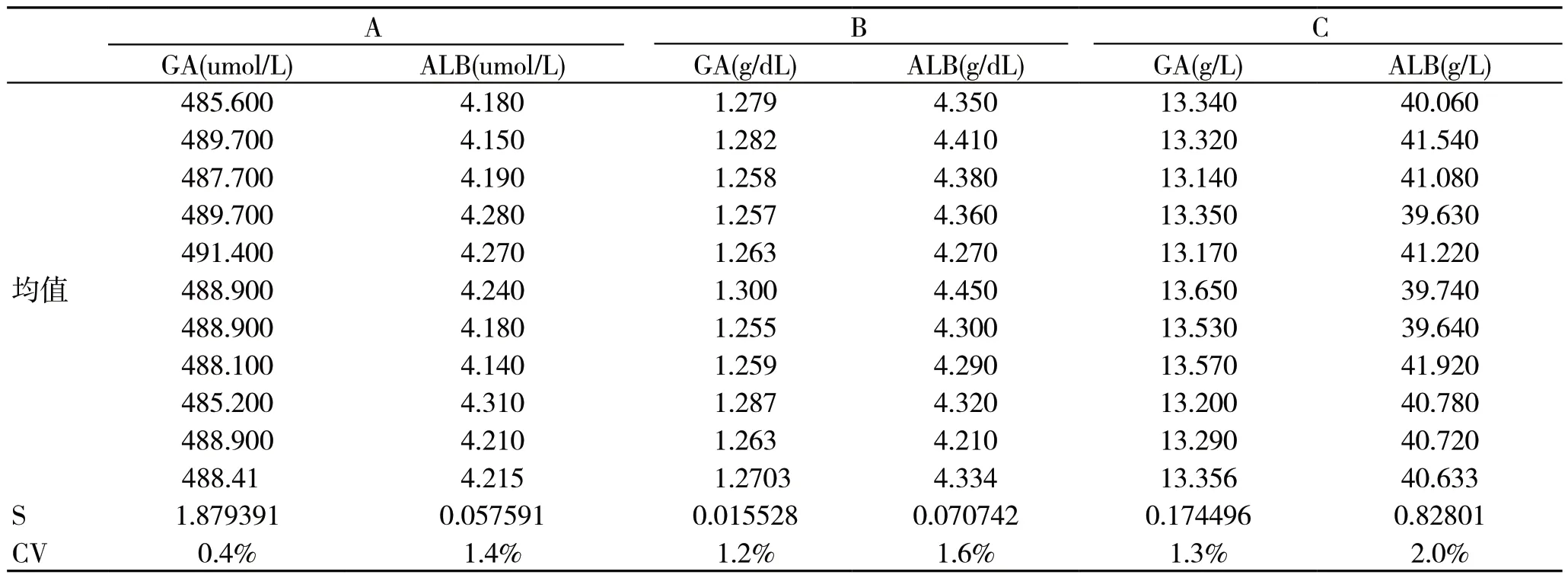
表2 三个厂家试剂盒的重复性分析结果
针对糖化白蛋白诊断试剂盒建立了空白吸光度、分析灵敏度、线性、重复性、准确性的质量控制指标,此质量控制指标的建立为此类试剂产品质量控制标准的统一奠定了良好的基础。针对上市的三家试剂盒产品进行试验分析结果表明,酶法糖化白蛋白试剂均具有较好的空白吸光度、分析灵敏度、线性及重复性。同时,由于不同厂家采用各自的标定系统,采用不同的生产工艺和原材料,缺乏统一国家标准物质和溯源体系,因此比对结果存在一定的差异。但由于准确性是行业标准非常重要的性能指标,建议规范偏差极限范围,以鼓励企业通过技术完善,提高产品控制质量。同时建议加强糖化白蛋白国家标准品的研发,建立起国内糖化白蛋白产品的溯源体系,保证各生产企业之间的统一性,促进行业的规范和发展,同时为临床使用者带来方便。
