中空铋材料的制备及药物体外释放的研究
2020-10-30徐英之吴风收
徐英之,吴风收 ,王 凯*,2
1. 武汉工程大学化工与制药学院,湖北 武汉 430205;2. 湖北大学化学化工学院,湖北 武汉 430061
过去的几年中,中空纳米结构[1]的材料因其特殊的孔道结构,而获得了广泛的关注。其中其较窄的禁带宽度2.75 eV,较大特征吸收波长,较高的可见光转化效率,可控调节的形貌[2-4],而在光催化[5-7]、选 择 性 氧 化[8-9]、降 解 污 染 物[10-11]、CO2转换[12]、肿瘤治疗[13]等方面都有良好的应用。
与相同尺寸的纳米材料相比,中空纳米铋材料具有较大的比表面积、可修饰的表面、可控的孔径以及高的生物相容性被广泛的应用于医药领域。如Shi 课题组[14]就在中空介孔的二氧化硅结构上表面功能化,将其孔道作为药物封存运输的通道,达到了同时对亲水/疏水药物的双重负载,并实现了对布洛芬等疏水药物和阿霉素等亲水药物的高效双负载与控制性释放。又如Li 等[15]通过溶剂热法合成制备具有中空结构的Bi2Se3海绵状材料,经过体内外的研究,发现其具有多种生物治疗和成像功能,其既可以在单独的光热治疗中显示较高的抗肿瘤疗效,材料所具有的中空结构和高表面积也使其对阿霉素药物装载能力高达600%,并且显示出对pH 和光照刺激的双敏感性响应行为,充分发挥光热治疗与高负载化药的肿瘤抑制协同效应,并在三模态高对比度成像(包括X 射线计算机断层成像、多光谱光声学断层成像和红外热成像)方面表现出优异的性能。
为了进一步研究关于钨酸铋中空纳米材料作为载药体系在不同pH 环境下控制药物释放的功能应用,我们在前人的研究基础上,改进了钨酸铋中空材料的制备条件,并将其体外应用于盐酸阿霉素(doxorubicin hydrochloride,DOX)的药物负载与释放方面,为其体内的胃肠道缓控释应用奠定一定的理论研究基础。
1 实验部分
1.1 主要药品和仪器
药品:DOX(上海阿拉丁生化有限公司);五水合硝酸铋(bismuth nitrate pentahydrate,BNP)、钨酸钠、聚乙烯吡咯烷酮(polyvinyl pyrrdidone,PVP)(国药集团化学试剂有限公司)。
仪器:EVO-MA15LS 扫描电子显微镜(scanning electron microscope,SEM,德国卡尔蔡司);HT-7700透射电镜(transmission electron microscope,TEM,日本日立公司);D2-PHASER X 射线粉末衍射仪(X-ray diffractometer,XRD,德国布鲁克公司);TU-1901 双光束紫外可见分光光度计(Ultraviolet,UV,北京普析公司)。
1.2 中空钨酸铋纳米材料的制备与功能化
在钨酸铋材料的制备方法基础上[16],对于原料及溶剂等方面做了相应的改进。精确量取铋原料BNP(0.048 5 g)溶于10 mL 醇-水-乙酸溶液(体积比为1∶4∶1),再加入0.5 g PVP 粉末,超声搅拌直至完全溶解成为溶液A。随即将溶液A 分散至100 mL 无水乙醇中,搅拌20 min 后,加入10 mL 的0.015 mol 的钨酸钠水溶液B,继续搅拌30 min 后,把混合溶液转移到有聚四氟乙烯内胆的不锈钢反应釜中,将反应釜装入程序控温烘箱中,并控制两阶段温升程序,第一阶段80 ℃维持4 h,第二阶段100 ℃维持6 h。待升温程序结束后,等反应釜自然冷却至室温。并静置沉淀一段时间,待溶液中大部分白色胶状颗粒物都下沉至底部。滤出大部分白色固体,并离心分离,取下层白色固体,真空干燥箱60 ℃过夜烘干,得到最后的中空纳米铋材料(hollow nanobismuth material,HNBS)。
1.3 药物释放实验
将等量的负载DOX 的HNBS 颗粒置于透析袋中,并且加入10 mL 的不同pH 的磷酸缓冲盐溶液(phosphate buffer solution,PBS)中。在量取50 mL缓冲溶液于烧杯中,将上述透析袋放置其中,在室温下磁力轻微搅拌,每间隔2 h 离心收集上层清液,并且不断补充新的PBS 缓冲溶液,上清液离心通过紫外可见光谱标定的标准质量浓度曲线计算释放的DOX 的含量。实验过程分别是在pH=5.0,7.5 的PBS 缓冲溶液中进行的。
通过以下公式可以计算材料对药物的负载量:
Drug releasing capacity=mDOXinsuspenatant/minit;minit是指开始时加入的DOX 的质量,mDOXinsuspenatant是指上清液中DOX 的质量。
2 结果与讨论
2.1 催化剂表征
2.1.1 样品电镜分析 图1 的钨酸铋材料的透射电镜则进一步显示,在材料深色边界处与浅色中心处有明显区别,这证明了制备的材料具有明显的中空结构,中间大致呈现20~30 nm 的孔状结构,壁厚大致6~10 nm 左右。图2 为制备的钨酸铋中空材料的扫描电镜图片。由图1,2 可知:制备的材料主要呈现单分散的中空球状颗粒,粒径大约为40~50 nm,大小均一,形态规整。并且,没有检测到其他形貌,结果表明通过这种方法可以制备大量中空孔状铋颗粒材料。
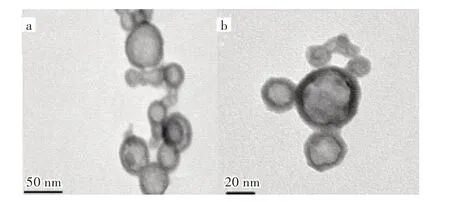
图1 HNBS 的TEM 图:(a)低倍率,(b)高倍率Fig.1 TEM micrographs of HNBS:(a)low magnification,(b)high magnification

图2 HNBS 的扫描电镜图:(a)高倍率,(b)低倍率Fig.2 SEM micrographs of HNBS:(a)high magnification,(b)low magnification
2.1.2 制备材料结构及性质分析 为了进一步对材料的结构进行分析,采用XRD 对样品结构进行分析。由图3 可知,样品在27.84°、49.95°均出现了Bi2WO6的2 个特征衍射峰,和文献提供[16]的中空纳米球Bi2WO6衍射图完全一致,并无其他晶相衍射峰存在。说明形成了Bi2WO6中空材料,且材料在49.95°处显示较宽的峰形,由Scherrer 公式可知,这是材料具有较小粒径的一个特征。
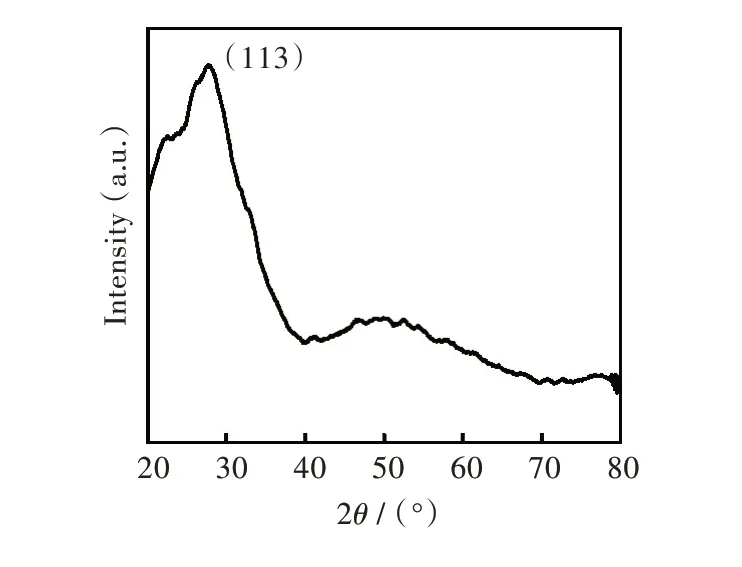
图3 HNBS 的XRD 粉末衍射图Fig.3 XRD pattern of HNBS
2.1.3 制备材料的负载性能分析 使用钨酸铋材料选用DOX 作为载药模型,评价药物传递系统的性能好坏。通过中空材料HNBS 和HNBS-DOX 的热重曲线研究(图4),两者在100~180 ℃区间内有重量损失但相差并不明显,可能是材料中结合水造成的;而在200~400 ℃的区间内有明显的质量损失相差明显,这主要是因为中空材料中DOX 分子(熔程201~205 ℃)在高温下发生了相态的变化。说明了HNBS 材料确实可以负载相应的DOX 分子。在500 ℃的高温下,整个体系也只有9%的质量损失,说明载药体系具有一定的热稳定性。本次实验制备的材料的热重结果说明,这个材料在高效药物负载方面具有一定应用前景。
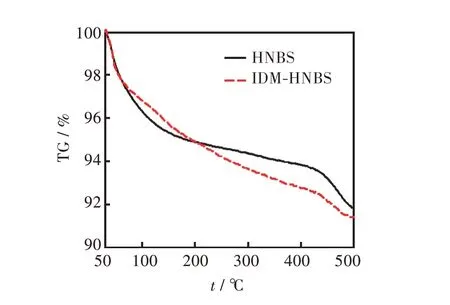
图4 负载和未负载DOX 药物的中空材料体系热重曲线Fig.4 TG curves of HNBS-DOX system before and after loading DOX
2.1.4 钨酸铋材料的药物负载与释放测定 实验选用DOX 作为载药模型来评价药物传递系统的性能的好坏。HNBS 具有典型中空特征,也许这一特征决定了药物在负载与选择性释放方面发挥了巨大的作用。
由图5 中结果显示,DOX 作为模型药物时,在HNBS 中负载量以质量分数来计可以达到55.72%。在药物负载过程结束后,DOX 的特征吸收峰有明显的降低,暗示着部分DOX 分子已经载入到HNBS 中。同样图4 中的热重的对比结果也佐证了这一观点。
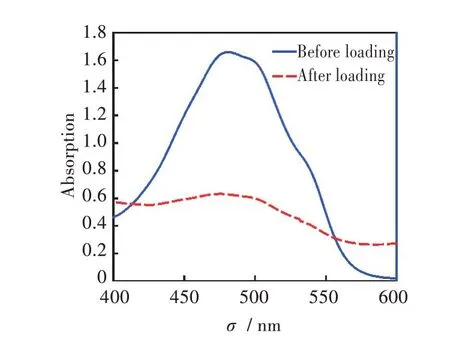
图5 DOX 负载前后的吸光度变化Fig.5 Absorption variations of material before and after DOX loading
图6 显示了在不同pH 值的PBS 缓冲溶液中HNBS-DOX 体系48 h 内的释放行为,药物大多在前12 h 内释放相对较快,然后以更平缓的方式释放,直到实验结束。为了模拟人体正常组织的弱碱性环境和肿瘤弱酸性环境,选择了pH=7.5 和pH=5.0 作为进一步探讨在不同的pH 环境下,DOX的响应性释放行为。正如图5 显示的那样,DOX在弱碱性环境下释放行为变得平缓,先前负载的药物中在48 h 内只有大约14%释放了出来。而在酸性条件下,先前负载的药物中在最初的12 h 内有大约31%释放出来。而48 h后,释放出43%。类似于这样的pH 响应性释放行为初步估计可以用来减小药物在血管中渗漏,避免在输送过程中的释放而最终达到在肿瘤细胞中有效富集并大量释放的作用。这种缓释性行为对于那些需要先高剂量而后稳定剂量达到抑制DOX 不良反应的临床病例是有用的。因此,可以合理推断这种材料可以用作药物的载体,作为一种新剂型使用。
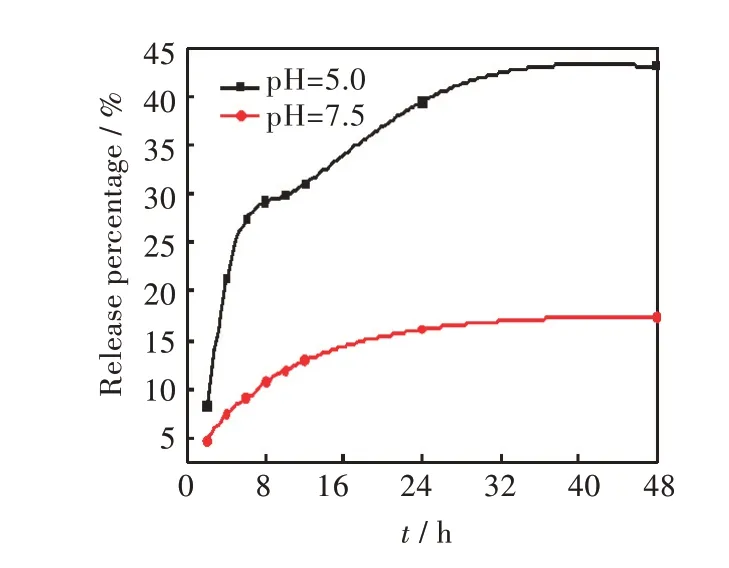
图6 DOX 在不同pH 溶液中释放曲线Fig.6 DOX release curves in solutions with different pH values
3 结 论
本文在前人基础上改进并制备了具有中空形貌的纳米Bi2WO6材料并将其首次应用到DOX 的负载与释放。中空的孔状结构的限制作用为模型药物客体分子从空心孔道扩散进出提供了位点,从而影响了其在不同pH 溶液中的缓释行为。
由UV 光谱分析可知,DOX 在中空纳米铋材料中的负载能力以质量分数来计可以达到55.72%,体外的释放试验表明,HNBS-DOX 体系具有一定的缓释特性,pH=7.5 时,只有14%的药物释放出来,而pH=5 时,药物释放量增加到43%,实验结果再次表明HNBS-DOX 体系在酸性条件下缓释效果优于弱碱性环境条件,说明中空结孔道结构的限制作用确实会影响DOX 在不同pH 溶液中的缓释行为。与正常的组织和血液相比,肿瘤部位环境的pH 相对较低,约为pH=5.5~6.0,而瘤细胞内环境的pH 值,约为pH=4.5~5.0。这样的响应行为可以尽量避免载体在体内输送过程中的药物释放,从而保证药物的靶向性,提高药物在瘤细胞内的快速、大量的积聚与释放。
本文利用水热法,在较低浓度的原料浓度下,通过控制溶剂配比,制备了具有中空结构的纳米铋材料,作为DOX 的载体,可以具有较高的DOX药物的负载量,负载后药物的释放是pH 可控的,内部中空的结构能保证其准确的运输以及在肿瘤细胞内的酸性环境中大量的积聚释放。因此,这种中空纳米材料在治疗癌症方面的靶向给药系统具有一定的潜在应用。
