酪蛋白对乳清浓缩蛋白自组装形成纳米纤维的影响
2020-10-29徐红华鞠婷婷马彩虹
徐红华 王 欣 鞠婷婷 马彩虹 关 琛
(东北农业大学食品学院, 哈尔滨 150030)
0 引言
在非常规条件下,蛋白质分子通过疏水相互作用而形成的线状聚合物被称作纳米纤维[1-3],这种聚合结构对蛋白质单体及其常规聚合形态赋予了高级功能性质,不但具有更好的粘度、持水性、乳化性和起泡性等常规功能性质[4],还具有酸可逆性、导电性[5],可作为超分子材料用于生物传感器。研究发现,乳清蛋白在pH值2.0和低离子强度下高温加热,可形成纳米纤维[6],且形成的纤维具有共同的结构特征,即有支链或无支链的丝状结构,直径为5~15 nm,长度为几微米[7-8]。文献[9]研究发现,被胰蛋白酶修饰过的乳清浓缩蛋白(WPC)在加热过程中聚合得更多,且纤维形成速率高于未修饰的WPC。酪蛋白(CN)是牛乳中的主要蛋白质(约占蛋白质总量80%),常以酪蛋白胶束形式存在[10]。不同于其他蛋白质,CN带有相对较高的电荷,具有较高的疏水性和松散的卷曲结构,且所有的CN均无游离巯基,但CN中的成分αs2-CN和κ-CN分子均有半胱氨酸残基,分子间可以形成分子间二硫键而发生交联[11-12]。目前,关于乳蛋白纤维的研究主要集中在乳清蛋白聚合条件及形成机理方面,缺乏复杂蛋白组分干扰的研究。CN作为主要乳蛋白基料成分,对乳清蛋白纤维结构的形成至关重要。本文以WPC、CN为原料,在非常规条件下和WPC纤维形成的不同时期混入酪蛋白,观察酪蛋白介入对纤维形成的影响,探究形成的WPC-CN纤维与非纤维聚合物的主要作用力和聚合动力学过程,以期为拓展乳蛋白纳米纤维聚合物在食品工业中的应用以及不同乳蛋白基料的应用提供理论依据。
1 材料与方法
1.1 材料与试剂
脱脂乳粉(蛋白质质量分数34.67%、CN质量分数27.92%、乳清蛋白质量分数6.75%)来自新西兰恒天然公司;乳清浓缩蛋白粉WPC-80(蛋白质质量分数76.93%)购自美国HILMAR公司;大豆色拉油(九三集团哈尔滨惠康食品有限公司);丙烯酰胺(美国Amersco公司);TEMED(美国Sigma公司);8-苯氨基-1-奈酚-碘酸(ANS)(美国Sigma公司);硫黄素T(ThT)(美国Sigma公司);考马斯亮蓝R250(美国Amresco公司);甲叉双丙烯酰胺(北京Solarbio公司);十二烷基硫酸钠(SDS)(美国Sigma公司),所用其他试剂均为国产分析纯。
1.2 主要仪器设备
GL-21M型离心机(上海精密仪器研究所),KDN-102C型半自动定氮仪(上海纤检仪器有限公司),F-4500型荧光分光光度计(日本日立公司),JEM-1200EX型透射电子显微镜(日本日立公司),DELTA320型pH计(梅特勒-托利多仪器有限公司)。
1.3 试验方法
1.3.1CN的制备
参照文献[13]的方法并加以改进。用去离子水溶解脱脂乳粉,搅拌1.5 h,使其充分水合,7 000g离心15 min,取上清液,调其pH值至4.6(6 mol/L HCl和0.1 mol/L HCl),1 000g离心15 min(室温),弃上清液,用去离子水洗沉淀,1 000g离心10 min,弃上清液,再用去离子水溶解沉淀,并调pH值至2.0(6 mol/L HCl和0.1 mol/L HCl)或6.5(2 mol/L NaOH和0.1 mol/L NaOH),搅拌1.5 h,使其充分溶解,7 000g离心15 min,取上清液并测定蛋白质含量,溶液4℃保存。
1.3.2纤维与常规WPC聚合物的制备
纤维聚合物的制备参照文献[14]的方法并加以改进。用去离子水溶解WPC-80粉,2 mol/L和0.1 mol/L盐酸将溶液pH值调至2.0,在19 000g、4℃条件下离心30 min,吸其中层清液,测定清液蛋白质含量,并用去离子水将溶液的蛋白质质量分数稀释为3.0%,再用盐酸将溶液pH值调至2.0,90℃水浴10 h,每间隔1 h取样并立即冷却,于4℃保存。
常规WPC聚合物的制备是在上述过程中去除调节pH值的步骤,其他部分同上。
1.3.3WPC-CN聚合物的制备
在WPC溶液不同的热处理时间混入CN,混合均匀,即在纤维(或常规WPC)聚合物形成的过程中混入CN,继续90℃水浴至10 h,每间隔1 h取样并立即冷却,于4℃保存。
1.3.4CN混杂对WPC纤维形成的影响因素
(1)CN混入时间点
在固定WPC、CN溶液浓度的条件下,研究CN的混入时间点对WPC纳米纤维形成的影响。试验条件确定为:pH值2.0、90℃条件下热处理蛋白质量分数3.0%的WPC溶液,在不同热处理时间点(0、0.5、1.5、2、3、4、5、7、9 h)时与蛋白质量分数3.5%的CN溶液以体积比2∶1的比例混合,并继续加热至10 h,每间隔1 h取样后立即冷却,于4℃保存。
(2)CN质量分数
选择4种质量分数的CN:1.5%、2.0%、3.5%、6.0%。试验条件确定为:将pH值2.0、蛋白质量分数3.0%的WPC溶液,在90℃条件下热处理至不同时间点(0、0.5、1.5、2、3、4、5、7、9 h)时与pH值2.0、不同蛋白质量分数CN以体积比2∶1的比例混合(以质量分数3.0%的WPC与pH值2.0的去离子水以2∶1的比例混合,即质量分数2%的WPC为对照),并继续加热至10 h,每间隔1 h取样后立即冷却,于4℃保存。
1.3.5硫黄素T荧光强度
根据文献[15]的方法并加以改进,取400 μL待测样品加入10 mL质量浓度16 mg/L的ThT工作液中,混匀,用荧光分光光度计(激发波长为460 nm,发射波长为490 nm,狭缝宽度分别设为5 nm和10 nm)进行测量。
1.3.6透射电子显微镜
根据文献[16]的方法并加以改进,用透射电子显微镜(Transmission electron microscopy, TEM)(采用80 kV电压处理)观察样品微观结构。
1.3.7表面疏水性
参照文献[17]的方法并加以改进,利用ANS荧光探针法测定蛋白质的表面疏水性。用0.01 mol/L磷酸缓冲液(pH值7.0)将样品溶液稀释至蛋白质量分数分别为0.01%、0.005%、0.002 5%和0.001 25%,然后向6 mL稀释液中加入16 μL浓度8 mmol/L的ANS溶液,混匀,避光15 min,后用荧光分光光度计(激发波长和发射波长分别设为390 nm和470 nm,狭缝5 nm)测量,利用荧光强度对稀释液的蛋白质质量浓度作图,将斜率作为蛋白质表面疏水性指数。
1.3.8游离巯基
参照文献[17]的方法并稍加改进。将10.4 g Tris(氨基丁三醇)、6.9 g甘氨酸、1.2 g EDTA(乙二胺四乙酸)、480 g脲素用水溶解,并定容至1 000 mL,调节pH值至8.0,得到Tris-Gly(氨基丁三醇-甘氨酸)缓冲溶液。将待测样品稀释到蛋白质量分数为2.5%,取0.25 mL稀释液加入到5 mL的Tris-Gly缓冲溶液中,向其加入20 μL的DTNB(二硫代二硝基苯甲酸)试剂,混匀,静止15 min,并在412 nm波长下测定其吸光度,以不加样品的溶液用于空白。巯基质量摩尔浓度计算公式为
X=(73.53A412D)/C
(1)
式中A412——在412 nm的吸光度
C——固形物质量浓度,mg/mL
D——稀释系数
X——巯基质量摩尔浓度,μmol/g
1.3.9未聚合乳清蛋白含量
将质量分数3.0%的WPC与3.5%的CN混合进行热处理,将15 mL不同热处理时间(0~10 h)下的样品溶液pH值调至4.6(使用2 mol/L HCl和0.1 mol/L HCl),然后1 000g离心15 min,取上清液,并定容至25 mL,利用凯氏定氮方法测定:不同热处理时间下未聚合WPC的含量;单位时间内与CN聚合的WPC占总聚合WPC的百分比;时间t时混入CN热处理1 h内形成的不同聚合物的聚合速率常数k。计算公式分别为
Y1=Ct/C0
(2)
Y2=1-Ct/C0
(3)
M=(Ct-1-C1)/(1-C10)×100%
(4)
k=(Ct-Ct+1)/(1-Ct)
(5)
式中Y1——WPC未聚合率
Y2——WPC聚合率
M——单位时间聚合WPC百分比,%
k——聚合速率常数
C0、C1、C10——0、1、10 h时WPC质量浓度,mg/mL
Ct-1、Ct、Ct+1——t-1 h、t、t+1 h时未聚合WPC质量浓度,mg/mL
1.4 统计方法
使用Excel软件对试验数据进行统计分析,其中每组试验有3个重复(n=3),数据用平均数±标准差表示。
2 结果与分析
2.1 CN对WPC纤维形成的干扰
2.1.1形貌分析
pH值2.0、90℃加热10 h的条件下,CN单独存在不能形成纤维,如图1a所示,其形成的是较大的不规则聚合物。而此条件下WPC单独存在形成的纤维如图1b所示,其形成杆状细长的纤维。

图1 CN和WPC热聚合后的TEM结果Fig.1 TEM results after thermal polymerization of CN and WPC
WPC纤维化过程主要有3个阶段,成核期、生长期、稳定期对应的时间段可分别划为0~2 h、2~5 h、5~10 h[18]。CN混入WPC后形成纤维的微观结构如图2所示,在5、9 h混入CN对WPC纤维的形成影响不大,在0、0.5 h混入CN破坏了WPC纤维的结构,对WPC纤维的形成影响较大。CN混入的时间越晚,纤维结构越清晰,大量的CN附着在纤维表面上,因此,在WPC纤维形成的不同时期混入CN对其结构的影响有很大不同,成核期混入CN,严重破坏了WPC纤维的结构;生长期混入CN,纤维形态已经初步形成,CN对其有一定影响,但是纤维结构的总体结构框架没有被破坏;稳定期混入CN,纤维形态良好,大量CN附着在纤维表面上。
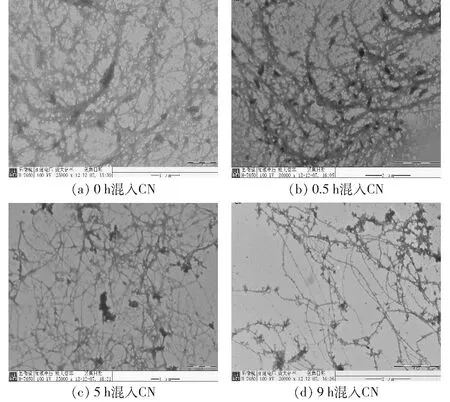
图2 WPC纤维形成不同时期CN混杂共聚的TEM结果Fig.2 TEM images of aggregate solution by adding casein to WPC at different periods of heat-induced formation of WPC fibrils

图3 CN混入时间对纤维形成的干扰Fig.3 Interference of mixing time of CN on fibril formation
2.1.2酪蛋白混入时间对纤维形成的干扰
纤维形成过程中,β-折叠数量不断增加,ThT是一种能与β-折叠特异性结合的染料,结合后其荧光强度会随折叠数量的增加而上升[19],因此通常用此方法间接反映纤维形成的情况。以单一质量分数2.0%的WPC为对照,可将ThT结果分为3类,如图3a所示,A类为ThT曲线明显低于质量分数2.0%的WPC,即其对纤维结构形成有明显的抑制作用,B类为ThT的曲线与质量分数2.0%的WPC相近;C类为ThT结果明显高于质量分数2.0%的WPC,即不抑制WPC纤维形成。故将A、B、C类混入CN的时间点归纳如下:A类:0、0.5、1.5 h混入CN;B类:2 h混入CN;C类:3、4、5、7、9 h混入CN。
如图3b所示,三者的差异在加热至5 h后愈发明显,在A类时间点混入CN加热至10 h时,荧光强度增加缓慢,B类的荧光强度增加量是A类的1.22倍,C类的荧光强度增加量分别是A类、B类的1.47、1.20倍。结果表明,CN在WPC纤维形成的不同时间点混入时,其荧光强度变化规律与TEM的纤维形貌结果一致,CN加入的时间越早,对应纤维形成的抑制作用越明显,在C类时间点(3~9 h)混入CN时,不影响WPC纤维形成,故认为质量分数3.0%的WPC与质量分数3.5%的CN混合时,3 h为不影响纤维形成的CN混入时间点,此时形成的是WPC-CN纤维聚合物。
2.1.3酪蛋白混入质量分数对纤维形成的干扰
由于pH值2.0下的CN粘度很大,可以得到最大的质量分数为6.0%,故选取4个CN质量分数分别为1.5%、2.0%、3.5%、6.0%,形成的不同聚合物的荧光强度均随着加热时间的延长呈增长趋势至稳定,荧光强度的变化情况如图4所示。

图4 混入CN质量分数对纤维形成的干扰Fig.4 Interference of CN concentration on fibril formation
在CN质量分数为1.5%~3.5%时,WPC热处理2 h之前混入CN,皆可破坏WPC纤维的形成,3 h之后混入CN不会破坏WPC纤维的形成,此时形成的是WPC-CN纤维聚合物。而当CN质量分数进一步增加到6.0%时,WPC热处理4 h之前混入CN,皆破坏WPC纤维的形成,5 h之后混入CN不会破坏WPC纤维的形成,故ThT结果可划分为:A类:0、0.5、1.5、3 h混入CN;B类:4 h混入CN;C类:5、7、9 h混入CN。故5 h是不影响纤维形成的CN混入时间点,此时形成的是WPC-CN纤维聚合物。在WPC热处理2 h混入质量分数6.0%的CN时,高于其他时间点混入CN的ThT结果。综上,A、B类破坏纤维形成,C类不影响纤维形成,且随着CN质量分数增大,形成WPC-CN纤维聚合物的CN混入时间点延后。
2.2 WPC-CN聚合物形成的主要作用力

图5 不同pH值下WPC与CN混合共聚的表面疏水性变化曲线Fig.5 Changes in surface hydrophobicity of aggregate solution by adding casein to WPC at different periods of heat-induced WPC
在热处理过程中,乳清蛋白与酪蛋白会发生变性,乳清蛋白自身或者与酪蛋白之间都会发生聚合,继而导致聚合过程中作用力的变化,而聚合过程的主要作用力是表面疏水作用和游离巯基浓度变化导致的[20],故试验继续探究了不同条件下WPC-CN聚合物的表面疏水性、游离巯基之间的差异。试验选择中间浓度CN(质量分数3.5%)参与反应,根据3.5%CN的3类CN混入时间点分别为:A类(0、0.5 h)、B类(2 h)、C类(3、5、9 h)。
2.2.1表面疏水性
如图5所示,pH值2.0的表面疏水性高于pH值6.5。这可能是由于在pH值2.0条件下,蛋白质所带电荷量较大,分子间斥力较大,疏水氨基酸暴露程度较大所致[21]。而在pH值2.0的环境下,混入CN形成聚合物的表面疏水性明显低于质量分数2.0%的WPC的表面疏水性,表明CN的介入整体上降低了聚合物的表面疏水性。表面疏水性从大到小依次为:质量分数2.0%的WPC、B类、C类、A类,WPC纤维表面疏水性的出峰时间是热处理5 h,该点对应的表面疏水性指数提高率为195.61%。而CN的混入改变了聚合物表面疏水性的出峰时间,使出峰时间点前移。WPC-CN纤维聚合物(即C类)出峰时间对应的表面疏水性指数提高率约为0 h混入的1.46倍,约是WPC纤维的44.77%,WPC-CN非纤维聚合物的表面疏水性指数是WPC纤维的38.64%。结果表明,CN混入得越早,其表面疏水性变化越低,即疏水相互作用越小,可能越抑制纤维的形成。
2.2.2游离巯基
如图6所示,在WPC热处理过程中,混入CN所形成的聚合物,随着热处理时间的延长,游离巯基含量呈下降趋势,这可能是由于蛋白质在热处理过程中,蛋白质结构打开,游离巯基暴露并向二硫键转变所致[22-23]。不同pH值间游离巯基的差异如下:pH值6.5条件下,游离巯基在1~2 h迅速降低,之后变化平缓,加热至10 h其游离巯基质量摩尔浓度约降低了76.33%,而pH值2.0条件下的相应值约降低了13.0%,前者降低幅度远高于后者,是后者的5.87倍;说明pH值6.5乳蛋白热聚合的主要作用力为二硫键。相反,在pH值2.0条件下,二硫键在乳蛋白热聚合中起到的作用较弱,对质量分数2.0%的WPC纤维而言,游离巯基质量摩尔浓度仅降低了8.40%,而不同时间点混入CN,游离巯基质量摩尔浓度变化量差异不大,约降低了13.76%,结果表明CN的加入提高了游离巯基质量摩尔浓度的变化量,其是WPC纤维的1.64倍。由图可知,不同时间点混入CN的游离巯基质量摩尔浓度变化速率不同,从大到小依次为:A类(0、0.5 h)、B类(2 h)、C类(3、5、9 h),A类和B类在热处理0~5 h时,游离巯基含量下降明显。

图6 质量分数3.0%的WPC与3.5%的CN混合共聚的游离巯基含量变化曲线Fig.6 Change of free sulfhydryl group by mixed copolymerization of 3.0%WPC and 3.5%CN
综上所述,pH值2.0下,WPC与CN聚合的主要作用力为表面疏水性(见表1),CN早期的混入,可以促进二硫键的形成,降低表面疏水性的提高。两种作用力的共同作用促进了CN与WPC的聚合,弱化了WPC自身间的作用,继而抑制WPC的纤维自组装,这种抑制作用在纤维形成初期混入CN尤为明显,而在纤维形成的中后期混入CN,这种抑制减弱,可能是聚合发生在CN与初具纤维形态的WPC聚集体之间的缘故。

表1 不同pH值下聚合物主要作用力的差异Tab.1 Differences among major force of aggregate solution with two pH values
2.3 聚合动力学
为了定量比较WPC纤维形成不同时期混入CN的聚合量,试验研究了聚合动力学过程。
2.3.1聚合量
如图7所示,质量分数2.0%的WPC未聚合率高于WPC与CN混合的。在pH值6.5时,热处理1 h内,WPC与CN聚合基本完成,并且不同时间点混入CN,WPC与CN聚合量差异不大;pH值2.0下,在WPC纤维形成过程中,WPC在热处理1~5 h聚合逐渐增加,5 h以后聚合量很少;而在WPC纤维形成过程中混入CN时,WPC与CN在1~5 h内缓慢发生聚合。

图7 WPC未聚合率曲线Fig.7 WPC unpolymerization rate curves
2.3.2WPC纤维形成不同时期CN混杂聚合的动力学差异
计算不同时间点混入CN后,单位时间内参与聚合的WPC占总聚合WPC的百分比见表2,WPC与CN的聚合主要发生在混入CN后的1~2 h里,并且CN加入得越早,与CN聚合的WPC越多。这种聚合量的变化不同于单一WPC形成纤维的聚合,在纤维形成过程中,WPC的聚合主要发生在前1~5 h,随后的聚合量非常低。
混入CN热处理1 h后,形成了不同聚合物的聚合速率常数k,WPC与CN在pH值6.5热处理的聚合速率常数是pH值2.0的3.83倍,而pH值2.0时不同时间混入CN间的聚合速率常数从大到小依次为:2 h、0 h、5 h、WPC+WPC、2.0%WPC、9 h,即WPC-CN纤维聚合物的聚合速率低于非纤维聚合物。0 h混入CN聚合速率常数是5、9 h混入的2.33、25.13倍,而2 h混入CN聚合速率常数是0 h混入的1.76倍,表明在与WPC热聚合物过程中,CN混入越晚,WPC与CN聚合的速率越慢,这里2 h较为特殊,这可能与其表面疏水性有关[24-25]。

表2 单位时间内参与聚合的WPC占总聚合WPC的百分比Tab.2 Percentage of aggregated WPC per hour of aggregate WPC %
综上,CN在WPC纤维的成核期混入时,由透射电镜可知愈加破坏纤维的微观形态;由荧光强度可知愈加降低β-折叠结构的形成;由作用力可知愈加促进二硫键形成,愈加降低表面疏水性;而由聚合量可知,WPC与CN聚合速率快,CN竞争性地与WPC结合,弱化了WPC的纤维化进程,致使破坏混杂纤维的形成。CN在纤维的生长期和稳定期混入时,WPC已经初具纤维形态,此时发生的是CN与WPC纤维的聚合,CN大多聚合在纤维的表面,不影响混杂纤维的形成。
3 结论
(1)在纤维形成不同阶段混入CN,决定了形成聚合物的结构形态。在WPC纤维形成的成核期混入CN,严重破坏了WPC的纤维结构;在生长期混入CN,对纤维结构有一定影响,但纤维结构的总体结构框架没有破坏;在稳定期混入CN,纤维形态良好,没有破坏WPC的纤维结构。
(2)WPC-CN聚合物的作用力主要为疏水相互作用,二者间二硫键的过多形成会破坏混杂共聚纤维结构的形成。
(3)混入酪蛋白越晚(5 h以后混入),聚合速率常数k越小,多数乳清蛋白已在前期初步形成纤维,酪蛋白只与少量的乳清蛋白发生聚合,而这种聚合也主要发生在纤维结构表面;反之,混入酪蛋白越早,聚合速率常数k越大,乳清蛋白与酪蛋白的聚合量越多,破坏了纤维的构架,减弱了WPC间的聚合,形成更多的WPC-CN纤维聚合物。
