电纺丝法制备功能化聚丙烯腈纳米纤维及其对U(Ⅵ)的吸附
2020-10-28姜芸捷王兴磊郭治军张红霞
姜芸捷,王 繁,王兴磊,郭治军,张红霞
兰州大学 核科学与技术学院,甘肃 兰州 730000
按照中国核电中长期发展的规划推测,截至2020年核电发电量将达我国发电总量的5%左右[1]。铀是核能生产中最关键的燃料,其具有很强的化学毒性和放射性效应,在整个核燃料循环过程中产生的含铀废水如果得不到有效的治理,将会对人类健康构成极其严重的危害[2]。因此,研究处理含铀废水的有效方法显得尤为重要。目前从废水中去除铀的方法有化学沉淀法、溶剂萃取法、离子交换法、生物法以及吸附法等,它们各有自己的优缺点[3-5],而吸附法因其经济高效、工艺简单等优点,在众多方法中脱颖而出。研究吸附法的关键就在于研究出具有高容量与高选择性的吸附剂[6]。
许多无机及有机材料都可以作为铀的吸附剂,而偕胺肟基类材料因其肟基O原子和氨基N原子的孤对电子对铀具有很强的螯合作用,是处理含铀废水的最佳有机吸附剂之一[7]。同时,在偕胺肟基类材料的基础上引入羧基等官能团,可大大提高材料的亲水性能及其对铀的络合能力[8]。高压静电纺丝法作为一种新的纳米材料制备技术,被广泛地应用于包括电池催化[9]、生物医学[10]等在内的各个领域,由其制备的纳米材料孔隙率高且比表面积大,比普通材料在吸附领域的表现更为出色。Teng等[11]曾利用电纺丝技术制备出一种PVA/SiO2复合纳米纤维膜,发现其可用作废水中染料的高效吸附剂;而Hallaji等[12]用电纺丝法合成了一种PVA/ZnO复合纳米纤维材料,其可以很好地从水溶液中去除U(Ⅵ)、Cu(Ⅱ)以及Ni(Ⅱ)等金属离子。
近年来曾有学者用静电纺丝法合成过聚丙烯腈纳米纤维[13-14],也有学者研究过功能化聚丙烯腈材料的制备及其应用[15-16],但鲜少有关于电纺丝法制备功能化聚丙烯腈纳米纤维并将其用于U(Ⅵ)的吸附的报道。本工作拟以聚丙烯腈(PAN)作为原料,利用静电纺丝技术制备偕胺肟基聚丙烯腈纳米纤维材料(AO-PAN),并将其碱法水解得到羧基/偕胺肟基聚丙烯腈纳米纤维材料(AC-PAN)。用批式法对比研究U(Ⅵ)在AO-PAN和AC-PAN上的吸附行为,包括pH、离子强度、接触时间、U(Ⅵ)初始浓度、温度以及共存离子对吸附的影响,同时研究AO-PAN和AC-PAN的解吸与重复利用价值,为功能化聚丙烯腈纳米纤维的制备及其用于U(Ⅵ)的吸附提供实验和理论支撑。
1 实验部分
1.1 仪器与试剂
SHA-C水浴恒温振荡器,常州国华电器有限公司;7200型紫外可见分光光度计,尤尼柯仪器有限公司;TG16-Ⅱ高速离心机,长沙平凡仪器仪表有限公司;DZF-6020真空干燥箱,上海一恒科学仪器有限公司;FA1104电子天平,精度0.000 1 g,上海良平仪器仪表有限公司;DW-P303-1ACF0高压直流数显电源,东文高压电源股份有限公司;TYD01-01-CE注射泵,保定雷弗流体科技有限公司;Apreo S扫描电子显微镜,美国Thermo公司;NEXUS 670傅立叶变换红外光谱仪,美国Nicoler公司;Vario EL元素分析仪,德国Elementar公司;Zetasizer Nano系列Zeta电位,英国Malvern公司;PB-10酸度计,精度为0.01,赛多利斯科学仪器有限公司;AXIS Ultra DLD X射线光电子能谱仪,英国Kratos公司。
聚丙烯腈粉末,国药集团化学试剂有限公司;硝酸铀酰,中核四零四有限公司;N,N-二甲基甲酰胺,天津化学试剂有限公司;硝酸,天津耀华化学试剂有限责任公司;偶氮胂Ⅲ,上海展云化工有限公司;无水碳酸钠,天津市大茂化学试剂厂;氢氧化钠,天津市光复科技发展有限公司;盐酸羟胺,天津市凯通化学试剂有限公司。所用试剂除硝酸为优级纯外,其余均为分析纯,溶液均由去离子水配制而成。
1.2 功能化聚丙烯腈纳米纤维的制备
1.2.1AO-PAN纳米纤维的制备 在250 mL的圆底烧瓶中加入100 mLN,N-二甲基甲酰胺以及16.00 g盐酸羟胺固体,常温搅拌至其完全溶解。称取8.50 g氢氧化钠粉末加入到烧瓶中,在常温下剧烈搅拌30 min。向烧瓶中加入10.00 g PAN粉末,将反应装置密封好后在80 ℃下磁力搅拌反应8 h。冷却至室温后将溶液转移到离心管中,在10 000 r/min离心30 min取上清液,即可得到AO-PAN纺丝液。通过如图1所示的静电纺丝装置制得AO-PAN纳米纤维,并在50 ℃下真空干燥24 h。
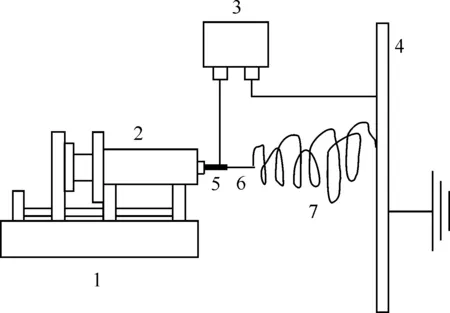
1——微量注射泵,2——溶液注射器,3——高压数显直流电源,4——金属收集装置,5——金属毛细针管,6——射流区,7——不稳定区
1.2.2AC-PAN纳米纤维的制备 AO-PAN和AC-PAN的合成过程示于图2。称取5.00 g AO-PAN纳米纤维,并将其加入到盛有200 mL0.20 mol/L的氢氧化钠溶液中。加热磁力搅拌1 h后,用去离子水反复洗涤至样品呈中性。在50 ℃下真空干燥24 h,得到AC-PAN纳米纤维材料。
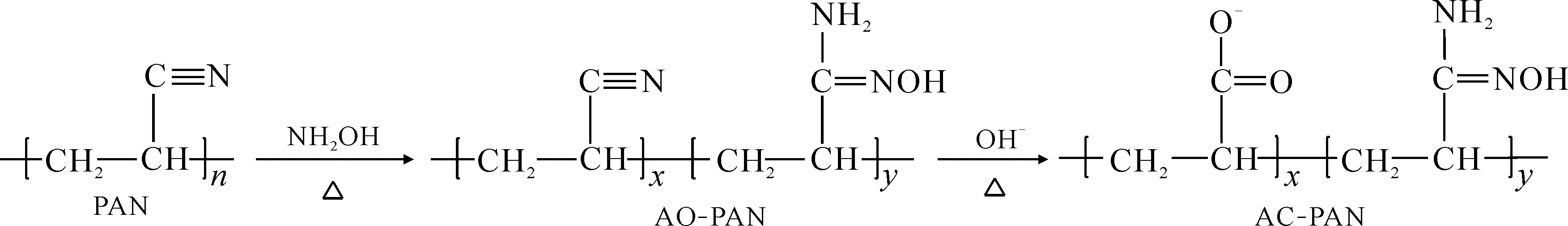
图2 AO-PAN和AC-PAN的合成示意图
1.3 吸附实验
分别于10 mL聚乙烯离心试管中称取适量的AO-PAN和AC-PAN纳米纤维,并向其加入U(Ⅵ)标准溶液、NaNO3溶液以及去离子水,使离心管中溶液总体积为5.00 mL。用NaOH和HNO3溶液调节体系pH后,置于水浴恒温振荡器中。吸附过程中,用0.1 mol/L NaOH 或 HNO3溶液微调体系pH至所需值。吸附结束后,离心30 min(10 000 r/min)并取出上清液,以偶氮胂Ⅲ溶液为显色剂,通过紫外-可见分光光度法在652 nm处测定溶液中的U(Ⅵ)浓度。U(Ⅵ)的吸附率和吸附量可由公式(1)和(2)求出:
(1)
(2)
式中:R,U(Ⅵ)的吸附率,%;c0和ce分别表示U(Ⅵ)的初始浓度和平衡浓度,mol/L;q,U(Ⅵ)的吸附量,mol/g;V,体系中液相的体积,L;m,体系中吸附剂的质量,g。
1.4 解吸与重复利用
吸附实验后,将富集了U(Ⅵ)的AO-PAN以及AC-PAN纳米纤维在50 ℃下真空干燥至完全。重新向聚乙烯离心管中加入5.00 mL不同浓度的HNO3溶液和Na2CO3溶液作为解吸剂,密封包好并放入水浴恒温振荡器中反应48 h。解吸结束后取出试管,离心并测量上清液中的U(Ⅵ)浓度。U(Ⅵ)解吸率可由公式(3)求出:
(3)
式中:D,U(Ⅵ)的解吸率,%;cd和cad分别表示解吸后上清液中和解吸前吸附剂上的U(Ⅵ)浓度,mol/L。选择出AO-PAN和AC-PAN的最佳解吸剂,对其进行三次吸附-解吸-吸附循环实验,以评估AO-PAN和AC-PAN纳米纤维的循环利用价值。
2 结果与讨论
2.1 AO-PAN和AC-PAN的表征结果
2.1.1扫描电镜表征 工业PAN纤维与电纺丝法制备的AO-PAN纳米纤维在扫描电镜下的图像示于图3。由图3可知:工业PAN纤维直径大约为10 μm;静电纺丝法制备的AO-PAN纳米纤维材料粗细均匀,其平均直径在200~300 nm,并且表面光滑没有珠串的连结,缩小为工业PAN纤维直径的1/40。

图3 工业PAN纤维(a)和AO-PAN纳米纤维(b)的扫描电镜图

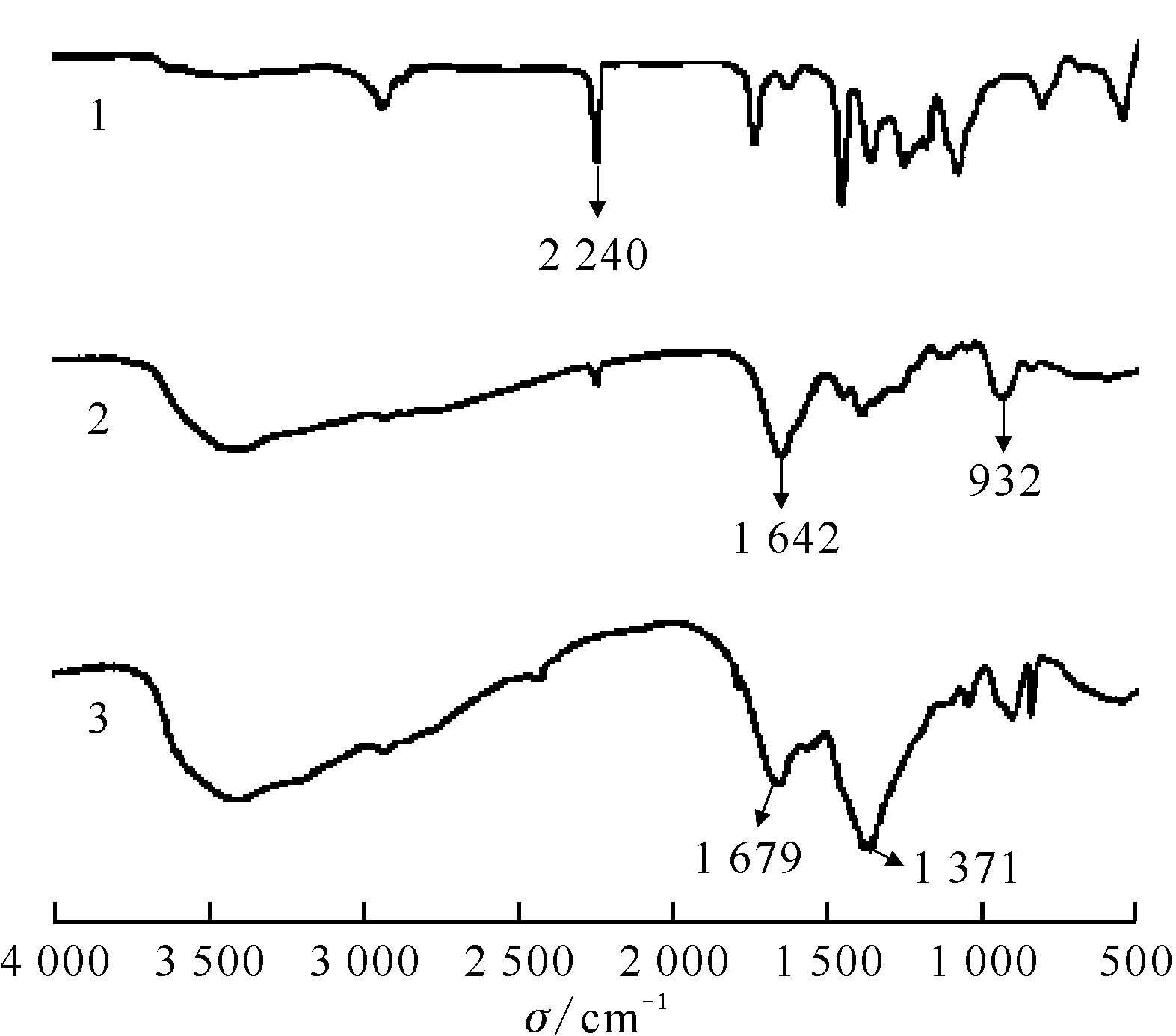
1——PAN,2——AO-PAN,3——AC-PAN
2.1.3元素分析 元素分析所得数据结果列入表1,根据其C、H和N含量的变化可以推断合成材料上所存在官能团的变化。由表1可知:AO-PAN中的w(C)/w(N)值比PAN中的w(C)/w(N)值有所降低,可以证明PAN纳米纤维上的氰基成功地被盐酸羟胺还原为偕胺肟基;而AC-PAN中的w(C)/w(N)值比AO-PAN又有所升高,且其w(C)/w(O)值比AO-PAN明显降低,说明AO-PAN经碱法水解后有羧基生成。

表1 PAN、AO-PAN和AC-PAN的元素分析结果
2.1.4Zeta电位 AO-PAN和AC-PAN随pH变化的Zeta电位图示于图5。由图5可知:随着体系pH增大,AO-PAN和AC-PAN的Zeta电位呈下降趋势,其中,AO-PAN零电荷点对应的pH≈4.4,而AC-PAN零电荷点对应的pH≈5.0。

c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,T=298 K
2.2 AO-PAN和AC-PAN对U(Ⅵ)的吸附
2.2.1吸附动力学研究 图6是接触时间对U(Ⅵ)在AO-PAN和AC-PAN上吸附的影响。随着接触时间的增加,AO-PAN对U(Ⅵ)的吸附率先逐渐增大,随后趋于平衡,达到平衡所需时间大约为36 h;AC-PAN对U(Ⅵ)达到吸附平衡很快,只需30 min,且AC-PAN对U(Ⅵ)达到吸附平衡时的吸附率远高于AO-PAN。这是由于AC-PAN中同时含有羧基和偕胺肟基,羧基的引入有效改善了材料的亲水性能,提高了材料对U(Ⅵ)的络合动力学效率,并且羧基本身也对U(Ⅵ)具有络合作用[8]。此外根据Zeta电位结果表明,在pH=4.0时AC-PAN对带正电荷的U(Ⅵ)的静电斥力小于AO-PAN[14]。用准一级动力学模型和准二级动力学模型进一步研究AO-PAN和AC-PAN对U(Ⅵ)的吸附机理,结果示于图7,动力学拟合参数列入表2。准一级和准二级动力学模型可由公式(4)和(5)分别描述。
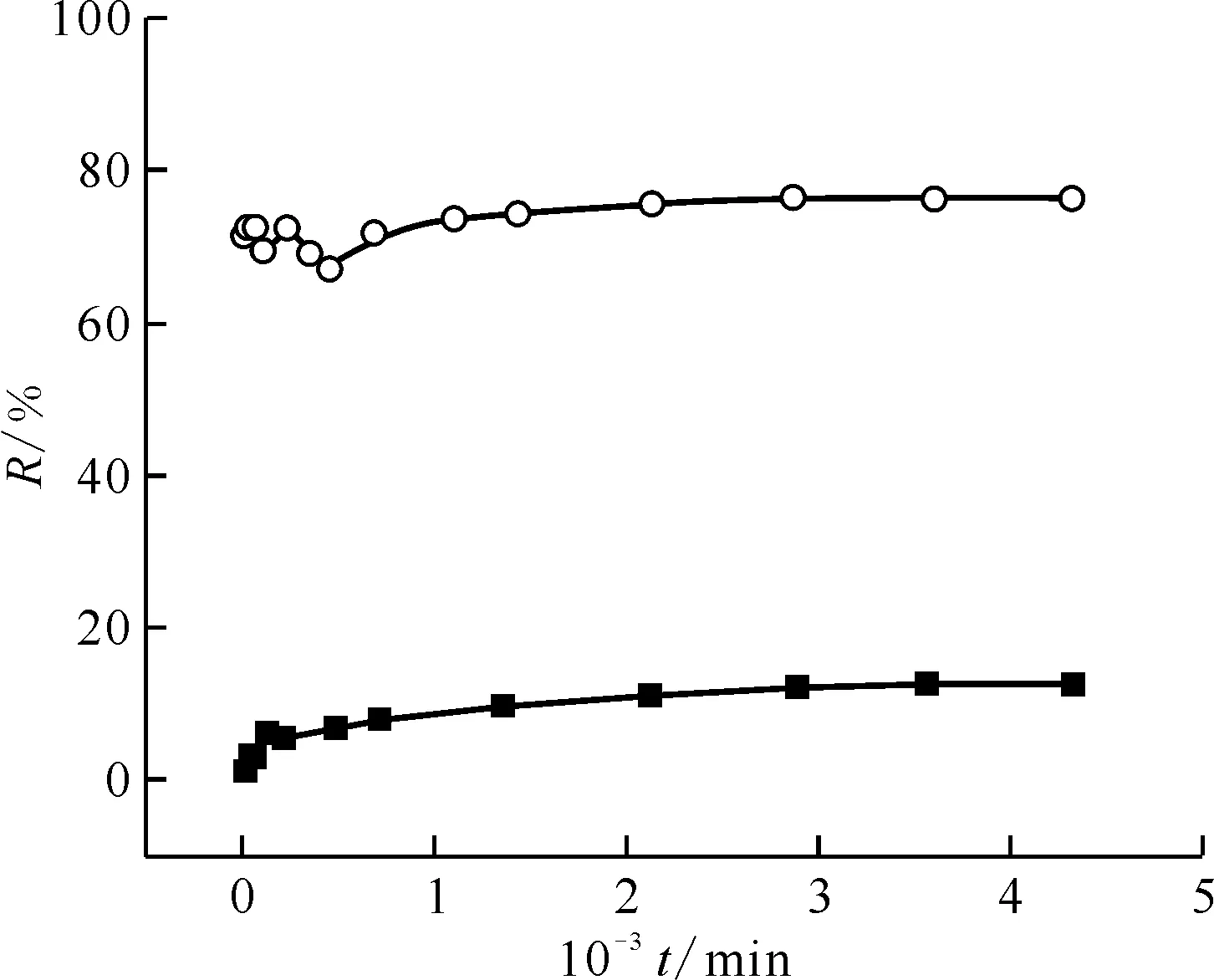
c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,T=298 K,pH=4.0±0.1
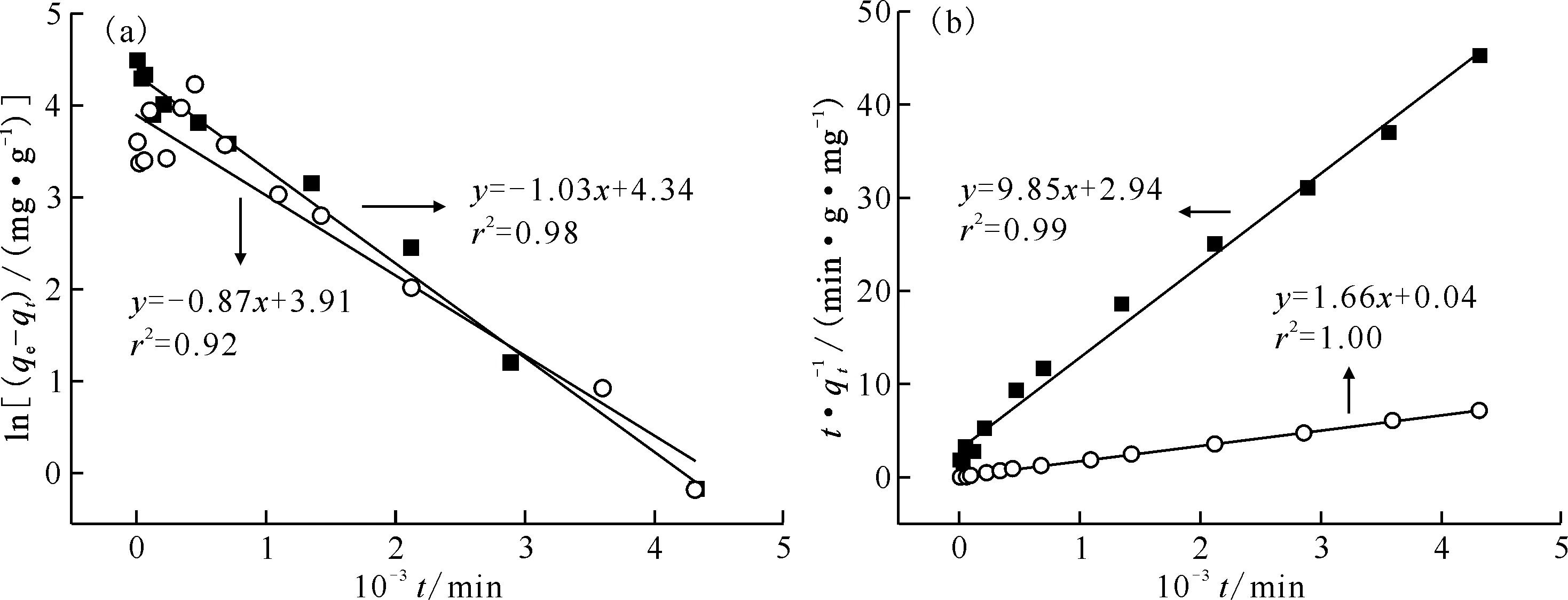
c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,T=298 K,pH=4.0±0.1
ln(qe-qt)=lnqe-k1t
(4)
(5)
式中:t,接触时间,min;qe和qt分别表示平衡时和t时刻U(Ⅵ)的吸附量,mg/g;k1,准一级动力学速率常数,min-1;k2,准二级动力学速率常数,g/(mg·min)。表2结果表明,AO-PAN和AC-PAN对U(Ⅵ)吸附的准二级动力学模型相关系数r2比准一级动力学模型更接近1,且其准二级动力学模型下拟合计算的理论吸附容量与实验值更相符。说明AO-PAN和AC-PAN对U(Ⅵ)的吸附更符合准二级动力学模型,在吸附过程中化学吸附占主导[15]。

表2 动力学拟合参数

c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,T=298 K,t=48 h
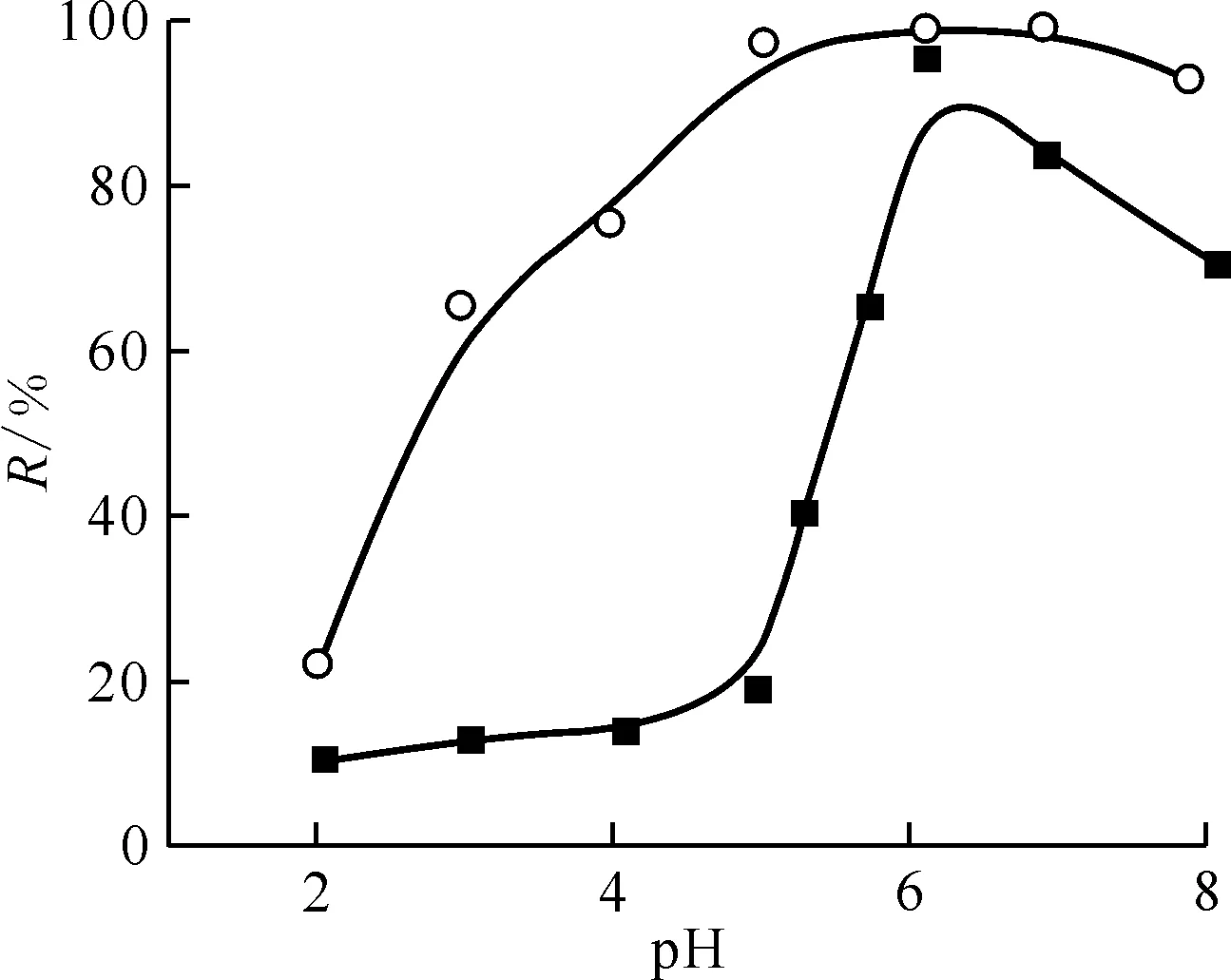
2.2.3离子强度对吸附的影响 离子强度对U(Ⅵ)在AO-PAN和AC-PAN上吸附的影响示于图9。由图9可知,离子强度对U(Ⅵ)在AO-PAN上的吸附有微弱促进作用,而对其在AC-PAN上的吸附影响较小。离子强度对吸附行为的影响可以用来区分吸附剂与吸附质之间的络合类型,如果离子强度的增大对吸附有促进作用或者影响较小,则说明此时吸附剂与吸附质之间形成的是内层表面络合物;而如果离子强度的增大对吸附有抑制作用,则说明此时吸附剂与吸附质之间形成的是外层表面络合物[18-19]。因此推测,AO-PAN和AC-PAN对U(Ⅵ)吸附的主导机制是形成内层表面络合物,它们之间存在化学键。其中,NaNO3溶液浓度在0~0.25 mol/L时,U(Ⅵ)在AC-PAN上的吸附率有一段微弱下降的趋势,推测在低盐度下AC-PAN对U(Ⅵ)吸附的主要机理是离子交换/外层表面络合物[20]。

c0(U(Ⅵ))=4.00×10-4 mol/L,m/V=0.14 g/L,T=298 K,t=48 h,pH=4.0±0.1
2.2.4吸附等温线及热力学研究 不同U(Ⅵ)初始浓度和温度下AO-PAN和AC-PAN对U(Ⅵ)的吸附结果示于图10。由图10可知:随着U(Ⅵ)初始浓度的增大,AO-PAN和AC-PAN对U(Ⅵ)的吸附量逐渐增大,且U(Ⅵ)在AC-PAN上的吸附量始终高于其在AO-PAN上的;较高的温度有利于U(Ⅵ)的吸附,说明吸附是吸热反应。用Langmuir、Freundlich以及Dubinin-Radushkevich吸附等温线模型对298 K下的吸附数据进行拟合,结果示于图11(a)—(c)和表3。Langmuir、Freundlich以及D-R等温线模型可由公式(6)—(8)描述:
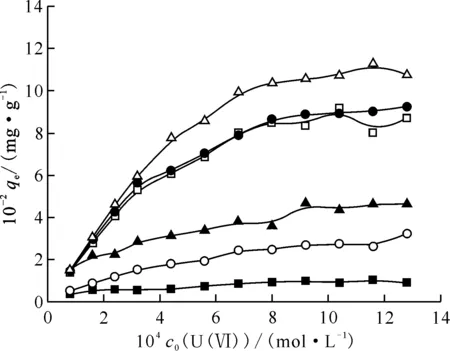
c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,pH=4.0±0.1,t=48 h
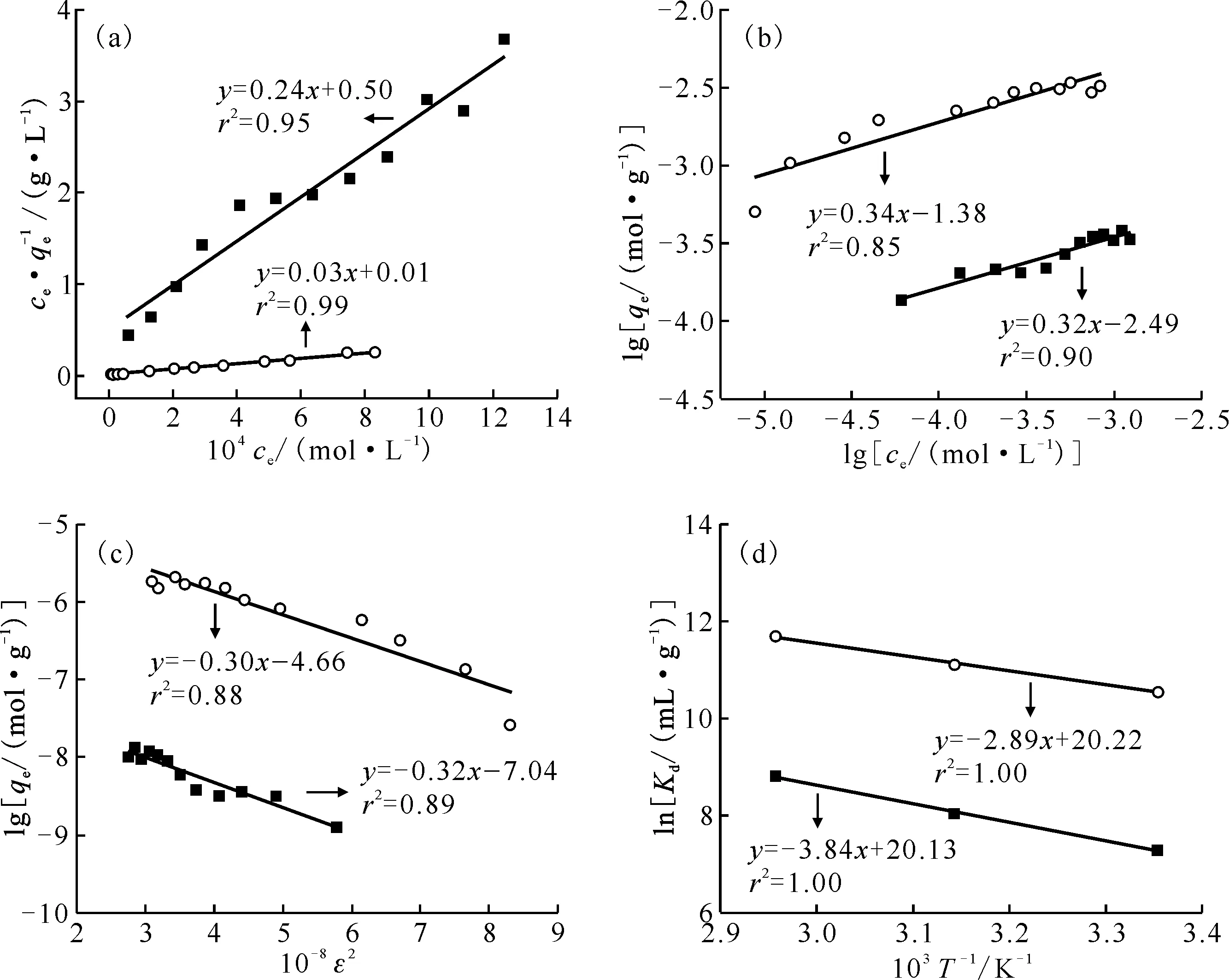
c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,pH=4.0±0.1,t=48 h

表3 等温线模型相关参数
(6)
(7)
lnqe=lnqmax-βε2
(8)
式中:ce,平衡时液相中U(Ⅵ)的浓度,mol/L;qe,平衡时固相中U(Ⅵ)的浓度,mol/g;qmax,U(Ⅵ)的最大吸附容量,mol/g;KL,Langmuir模型平衡常数,L/mol;n,Freundlich方程经验常数;KF,Freundlich模型平衡常数,mol1-nLn/g;β,平均自由能活度系数,mol2/J2。而Polanyi电位ε和平均吸附自由能E(J/mol)可根据公式(9)和(10)计算:
(9)
(10)
式中:R,气体常数,8.314 J/(mol·K);T,绝对温度,K。表3结果表明,相比于Freundlich模型,AO-PAN和AC-PAN对U(Ⅵ)的吸附都更符合Langmuir模型,说明AO-PAN和AC-PAN对U(Ⅵ)的吸附过程更符合单分子层吸附[21],其表面具有均匀的吸附能,并且每个U(Ⅵ)只占据一个吸附位点[22]。在T=298 K时,AC-PAN对U(Ⅵ)的最大吸附容量为3.33 mmol/g,是AO-PAN的8倍左右。而根据D-R模型,AO-PAN和AC-PAN对U(Ⅵ)的平均吸附自由能均高于8 kJ/mol,说明其对铀的吸附是以化学吸附为主[23]。吸附分配系数Kd(mL/g)可由公式(11)计算,热力学参数焓ΔH(kJ/mol)、熵ΔS(J/(mol·K))和吉布斯自由能ΔG(kJ/mol)可通过公式(12)和(13)计算:
(11)
(12)
ΔG=ΔH-TΔS
(13)
图11(d)是U(Ⅵ)在AO-PAN和AC-PAN上吸附的lnKd对T-1的线性拟合图,由其斜率和截距计算所得的热力学参数列于表4。ΔH>0,说明AO-PAN和AC-PAN对U(Ⅵ)的吸附是一个吸热的过程;ΔS>0,表明随着吸附的进行,体系混乱度增大;ΔG<0,说明AO-PAN和AC-PAN对U(Ⅵ)的吸附行为是一个自发的过程,并且ΔG的值会随着温度的升高而减小,表明较高的温度有利于U(Ⅵ)的吸附[24],这与实验结果一致。
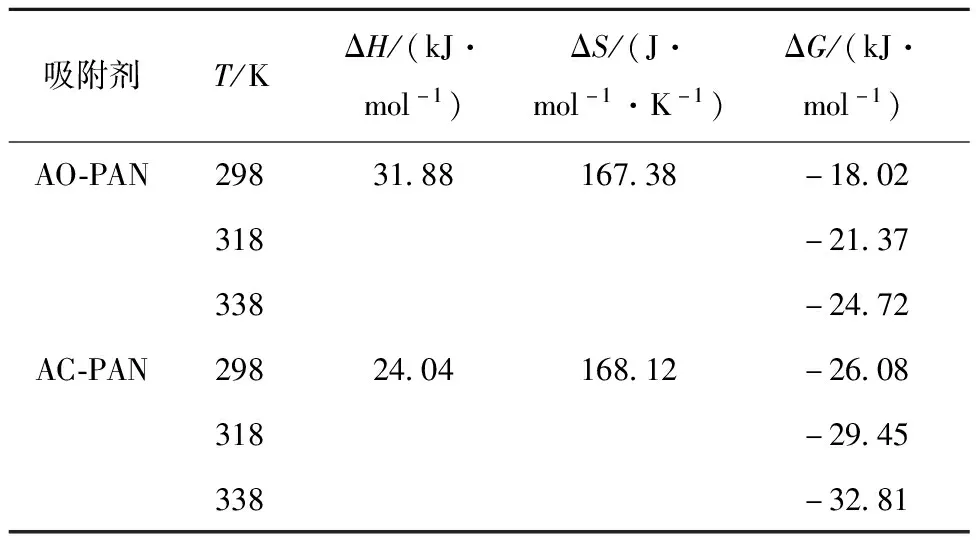
表4 不同温度下热力学参数
2.2.5共存离子对吸附的影响 几种与U(Ⅵ)相同浓度的常见阳离子存在时,U(Ⅵ)的吸附情况示于图12。由图12可知,在其他竞争离子存在时,AO-PAN和AC-PAN对U(Ⅵ)的吸附率并没有明显下降,说明其对U(Ⅵ)具有良好的吸附选择性。其中,Cd(Ⅱ)对U(Ⅵ)吸附的影响最小,而Cr(Ⅱ)对U(Ⅵ)吸附的影响最大。
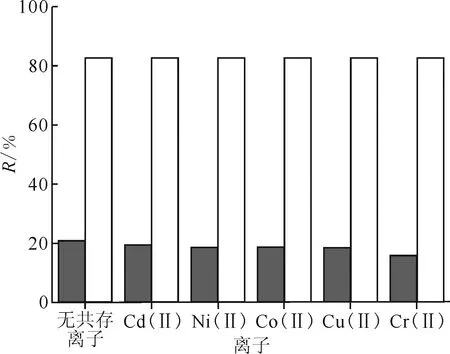
c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V=0.14 g/L,T=298 K,t=48 h,pH=4.0±0.1
2.3 解吸与重复利用
材料是否可解吸与重复利用,是判断其经济实用性的重要依据。不同浓度HNO3溶液和Na2CO3溶液对富集U(Ⅵ)后的AO-PAN和AC-PAN的解吸情况示于图13。由图13可知:随着解吸剂浓度增大,U(Ⅵ)的解吸率逐渐增大,HNO3溶液对U(Ⅵ)的解吸率高于Na2CO3溶液,且U(Ⅵ)在AO-PAN上的解吸率均高于其在AC-PAN上的。其中,Na2CO3溶液浓度在0~0.20 mol/L时,U(Ⅵ)在AC-PAN上的解吸率有一段先急剧增大后下降的趋势,这与低盐度下U(Ⅵ)在AC-PAN上吸附机理涉及到的离子交换有关。
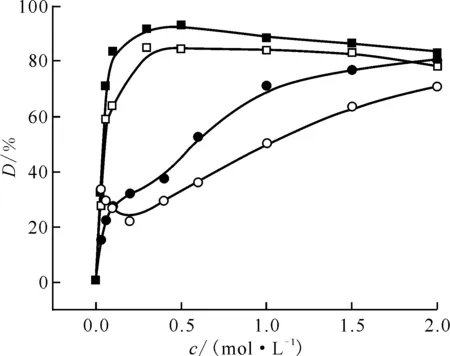
c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V(AO-PAN)=2.00 g/L,m/V(AC-PAN)=0.50 g/L,T=298 K,t=48 h,pH=4.0±0.1
虽然HNO3溶液对U(Ⅵ)的解吸效果略优于Na2CO3溶液,但较低浓度的HNO3溶液对U(Ⅵ)的解吸率不高,而当HNO3溶液浓度达到0.10 mol/L时会破坏材料的结构,影响其重复利用性能。因此选择2.00 mol/L的Na2CO3溶液处理富集U(Ⅵ)后的AO-PAN和AC-PAN,并进行三次吸附-解吸-吸附实验,结果示于图14。由图14可知:经过三次的吸附-解吸-吸附过程,AO-PAN和AC-PAN对U(Ⅵ)的吸附率仍能维持在99%以上,说明AO-PAN和AC-PAN具有优异的重复利用性能,是经济实用的U(Ⅵ)吸附剂。
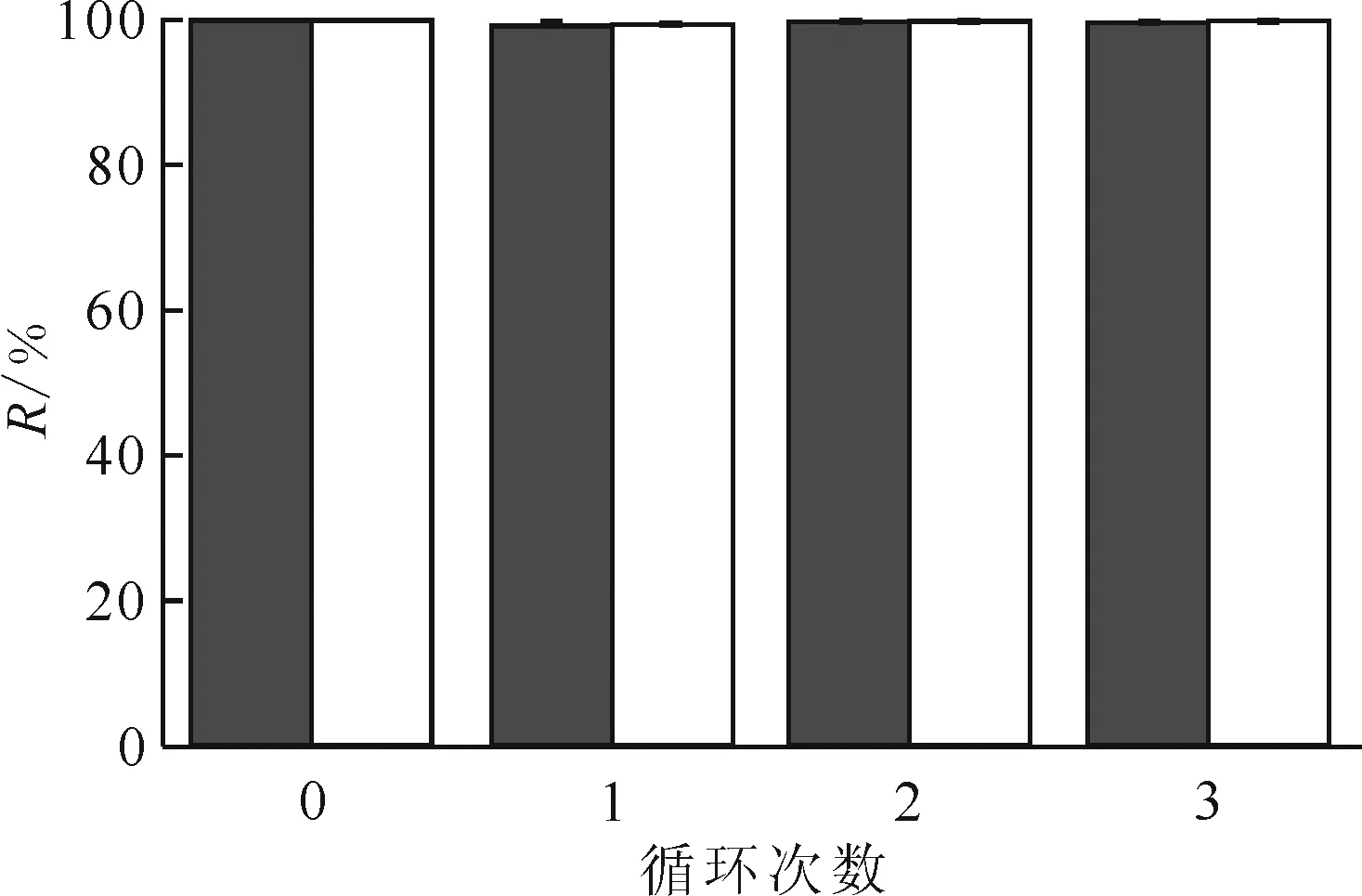
c0(U(Ⅵ))=4.00×10-4 mol/L,c(NaNO3)=0.08 mol/L,m/V(AO-PAN)=2.00 g/L,m/V(AC-PAN)=0.50 g/L,T=298 K,t=48 h,pH=4.0±0.1,c(Na2CO3)=2.00 mol/L
2.4 吸附机理研究
AO-PAN和AC-PAN吸附U(Ⅵ)前后的XPS谱图示于图15。与图15(a)相比,图15(b)和(c)上出现了U(Ⅵ)的特征峰,说明U(Ⅵ)确实被吸附到了AO-PAN和AC-PAN上。对于AO-PAN,未吸附U(Ⅵ)时其N 1s光谱可拟合为两个峰,分别对应—NH2(E=397.3 eV)和—NOH(E=397.9 eV)(图15(d)),而吸附U(Ⅵ)后,在E=404.6 eV处出现了一个新的N 1s峰(图15(h)),同时对应于—NH2的N 1s峰偏移了0.1 eV,可认为是氨基N与U络合的结果;未吸附U(Ⅵ)时其O 1s光谱可拟合为两个峰,分别对应—OH(E=531.2 eV)和N—O(E=530.3 eV)(图15(e)),而吸附U(Ⅵ)后,在E=531.9 eV处出现了一个新的O 1s峰(图15(i)),可认为是肟基O与U络合的结果。对于AC-PAN,未吸附U(Ⅵ)时其N 1s光谱可拟合为两个峰,分别对应—NH2(E=397.3 eV)和—NOH(E=397.9)(图15(f)),而吸附U(Ⅵ)后,在E=405.2 eV处出现了一个新的N 1s峰,同时对应于—NH2的N 1s峰偏移了0.2 eV(图15(j)),可认为是氨基N与U络合的结果;未吸附U(Ⅵ)时其O 1s光谱可拟合为三个峰,分别对应—OH(E=531.2 eV)、N—O(E=530.3 eV)和C—O(E=529.5 eV)(图15(g)),而吸附U(Ⅵ)后,在E=531.9 eV处出现了一个新的O 1s峰,同时对应于N—O的O 1s峰偏移了0.3 eV,对应于C—O的O 1s峰偏移了0.5 eV(图15(k)),可认为肟基O与羧基O共同参与了对U(Ⅵ)的络合。综上所述,AO-PAN对U(Ⅵ)的主要作用机理可能是其偕胺肟基上的氨基N和肟基O与U(Ⅵ)络合;而AC-PAN对U(Ⅵ)作用的主要机理可能是其偕胺肟基上的氨基N和肟基O以及其羧基上的O共同与U(Ⅵ)络合[6]。
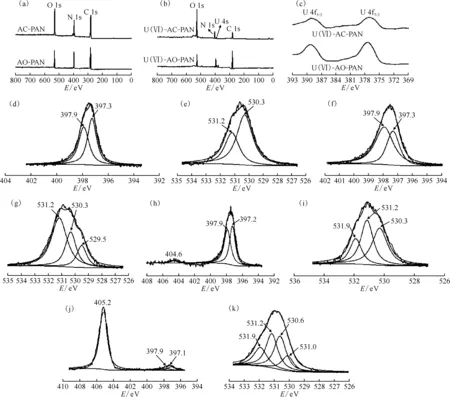
(a)——AO-PAN和AC-PAN吸附U(Ⅵ)前的XPS全谱图,(b)——AO-PAN和AC-PAN吸附U(Ⅵ)后的XPS全谱图,(c)——U 4f的高分辨谱图,(d)——AO-PAN吸附U(Ⅵ)前的N 1s高分辨谱图,(e)——AO-PAN吸附U(Ⅵ)前的O 1s高分辨谱图,(f)——AC-PAN吸附U(Ⅵ)前的N 1s高分辨谱图,(g)——AC-PAN吸附U(Ⅵ)前的O 1s高分辨谱图,(h)——AO-PAN吸附U(Ⅵ)后的N 1s高分辨谱图,(i)——AO-PAN吸附U(Ⅵ)后的O 1s高分辨谱图,(j)——AC-PAN吸附U(Ⅵ)后的N 1s高分辨谱图,(k)——AC-PAN吸附U(Ⅵ)后的O 1s高分辨谱图
3 结 论
(1)通过电纺丝法成功制备了偕胺肟基聚丙烯腈纳米纤维材料AO-PAN以及羧基/偕胺肟基聚丙烯腈纳米纤维材料AC-PAN。AO-PAN纳米纤维的直径约为200~300 nm,缩小为工业PAN纤维直径的1/40。
(2)AO-PAN和AC-PAN对U(Ⅵ)吸附的最佳pH均在6左右;离子强度对U(Ⅵ)在AO-PAN上的吸附有微弱促进作用,而对其在AC-PAN上的吸附影响不大,说明AO-PAN和AC-PAN对U(Ⅵ)吸附的主要机理是形成内层表面络合物。
(3)AO-PAN和AC-PAN对U(Ⅵ)的吸附符合准二级动力学模型和Langmuir等温线模型。AC-PAN对U(Ⅵ)吸附达到平衡只需30 min,其最大吸附容量为3.33 mmol/g,约为AO-PAN的8倍;热力学研究表明AO-PAN和AC-PAN对U(Ⅵ)的吸附是自发行为,且吸附过程是吸热反应。
(4)AO-PAN和AC-PAN对U(Ⅵ)具有良好的吸附选择性,有利于其在干扰离子存在的情况下处理含铀废水;AO-PAN和AC-PAN经2.00 mol/L的Na2CO3溶液处理后可重复利用3次以上,在含铀废水处理方面具有很好的商业前景。
(5)XPS谱图分析表明,AO-PAN对U(Ⅵ)的吸附机理可能是其偕胺肟基上的氨基N和肟基O与U络合;而AC-PAN则是其偕胺肟基上的氨基N和肟基O以及其羧基上的O共同与U络合。
