EGFR、ALK、KIT及KRAS基因Panel体细胞突变高通量测序检测法室内质量控制的建立*
2020-10-28吴小延李丹杨鑫华刘小云龙亚康王芳邓玲
吴小延,李丹,杨鑫华,刘小云,龙亚康,王芳,邓玲
510060 广州,中山大学肿瘤防治中心,华南肿瘤学国家重点实验室(吴小延、杨鑫华、刘小云、龙亚康、王芳、邓玲);510095广州,广州医科大学附属肿瘤医院 核医学科(李丹)
近年来,随着国家大力推进精准医疗计划,高通量测序技术在临床检测应用上取得极大的发展,其应用已扩展至肿瘤个体化治疗、遗传疾病风险预测、传染性疾病基因及心血管疾病等其他复杂疾病的临床诊断和治疗中,检测范围涵盖各个领域[1-8]。然而,高通量测序技术作为一种快速崛起的新技术,目前尚缺乏系统性的法规或指南来规范高通量测序技术检测项目的开展,只能参考国内外有关学会已出台的零散的相关共识与指南[9-14]。高通量测序技术是由许多细小过程联结或嵌套组成的一个极为复杂的检测过程,由于该技术实验操作步骤较多,检测流程复杂,数据信息量大等因素,故需要进行合理的质量控制才能使检测质量达到既定要求[15-17]。国内高通量测序技术平台多,设计Panel的大小及检测基因类型均有差别,因此,对高通量测序技术进行质量控制已经成为临床实验室迫切的需求和面临的巨大挑战[10,18-19]。为了保证检测结果的准确性、稳定性和可靠性,应建立具体的规范化的检测流程与增加必要的内部质量控制方案,来及时发现及把控检测过程中存在的质量风险。因此将质控样本和临床样本同时进行检测可保证检测过程的有效性。本研究利用Illumina NextSeq500平台,人多基因突变检测通用试剂盒(燃石医学检验所有限公司,295 Panel),结合我们实验室的建库流程,对携带表皮生长因子受体(epidermal growth factor receptor,EGFR)、间变淋巴瘤激酶(anaplastic lymphoma kinase,ALK)、酪氨酸激酶受体(tyrosine kinase receptor,KIT)和大鼠内瘤病毒癌基因(kirsten rat sarcoma viral oncogene,KRAS)4种已知基因及7种突变类型样本,按比例混合稀释成基因突变频率均为5.00%和2.50%的两个质控品,通过对质控品特异性、均一性及稳定性的高通量检测结果差异对比分析,以期使高通量测序技术流程更稳定,结果更可靠。
1 材料与方法
1.1 标本来源
收集中山大学肿瘤防治中心分子诊断科标本库经过燃石医学检验所有限公司,295 Panel高通量检测已知EGFR、ALK、KIT和KRAS基因突变类型及野生型的福尔马林固定石蜡包埋(formalin-fixed paraffin-embedded,FFPE)组织样本,并通过苏州吉因加生物医学工程有限公司的人1 021基因突变检测试剂盒的高通量测序法校验其突变,且分别将EGFR、ALK、KIT和KRAS4种基因共7个突变位点按5.00%、2.50%的突变频率混入全阴野生型样本,作为外部质控品。
1.2 高通量测序
常规石蜡包埋组织切片,根据HE染色结果,富集肿瘤细胞区域(大于20%)并按试剂盒说明书进行组织DNA提取(FFPE DNA Kit试剂盒,QIAGENA公司)。利用Illumina公司NextSeq500测序仪进行测序,其检测流程及工作原理(图1)为:将基因组DNA经超声波打断成200 bp左右的片段;进行末端修复加碱基A;加上接头制备成文库。将样本文库加入到测序芯片上,进行桥式PCR扩增,形成DNA簇,通过有荧光标记的脱氧核糖核苷三磷酸,进行边合成边测序。
1.3 数据分析
使用燃石医学有限公司提供的标准化自动样本管理与数据分析系统对原始数据进行过滤并进行生物信息学分析。
1.4 均一性评价
为保证质控样本的均一性,将制备好的质控品随机抽取10支进行均一性评价,用相同的仪器、试剂及同一人进行检测。
1.5 稳定性评价
1.5.1短期稳定性实验 随机抽取在冷冻条件下(-20℃)保存的5.00%、2.50%的突变质控品,做好标记,分别放于指定温度(2℃~8℃、25℃),每种条件放置10支。从第0周开始,每周抽取2支,用高通量检测试剂盒检测,连续监测1个月。
1.5.2长期稳定性实验 随机抽取置于-20℃冷冻保存的5.00%、2.50%的突变质控品2支,用高通量检测试剂盒检测,每月分别检测1次,连续检测12个月。
1.5.3测序深度评价 将稀释好的5.00%、2.50%阳性质控品分别降采样到3 000×、2 000×、900×、700×、500×、400×、350×、200×,每个深度分别取3次,然后利用Illumina公司NextSeq500测序仪进行检测,以观察测序深度与灵敏度的关系,进一步验证质控品的稳定性。


图1 基于捕获高通量测序技术检测流程
1.6 特异性实验
采用人多基因突变检测通用试剂盒(燃石医学检验所有限公司,295 Panel)分别对5.00%、2.50%的突变质控品进行检测,检测中使用相同的剂量,仪器消耗品及同一位操作人员。对比结果。
1.7 统计学分析
2 结 果
2.1 人1 021基因突变检测结果
本研究对选取已知EGFR、ALK、KIT和KRAS4种基因突变类型的FFPE肿瘤样本的人1 021基因突变检测试剂盒检测情况分析结果显示,选取的样本均携带基因突变,共有7种突变类型(包括小片段缺失、插入、点突变和融合),说明选取的临床样本含有目的片段,将临床样本测序后证明符合预期实验结果。具体结果见图2、表1。
2.2 质控品5.00%、2.50%的高通量检测结果
通过对质控品5.00%的高通量测序结果分析显示,共检出5种基因突变类型(因5.00%突变频率高,稀释量超出总体积量,故只选取了5个突变类型的样本),突变频率在3.70%~5.60%(表2)。通过对质控品2.50%的高通量测序结果分析显示,共检出7种基因突变类型,突变频率在1.90%~3.10%(表2)。
2.3 均一性实验
对随机抽取的10个5.00%、2.50%质控品进行室内质控品日内重复性测定,突变率差异在正常变化范围内,5.00%质控品和2.50%质控品CV均<10%,从图3、4所示数据可以看出符合质控品的日内重复性要求,证明重复性良好结果。
2.4 稳定性实验


图2 突变型标本和野生型标本的高通量测序结果
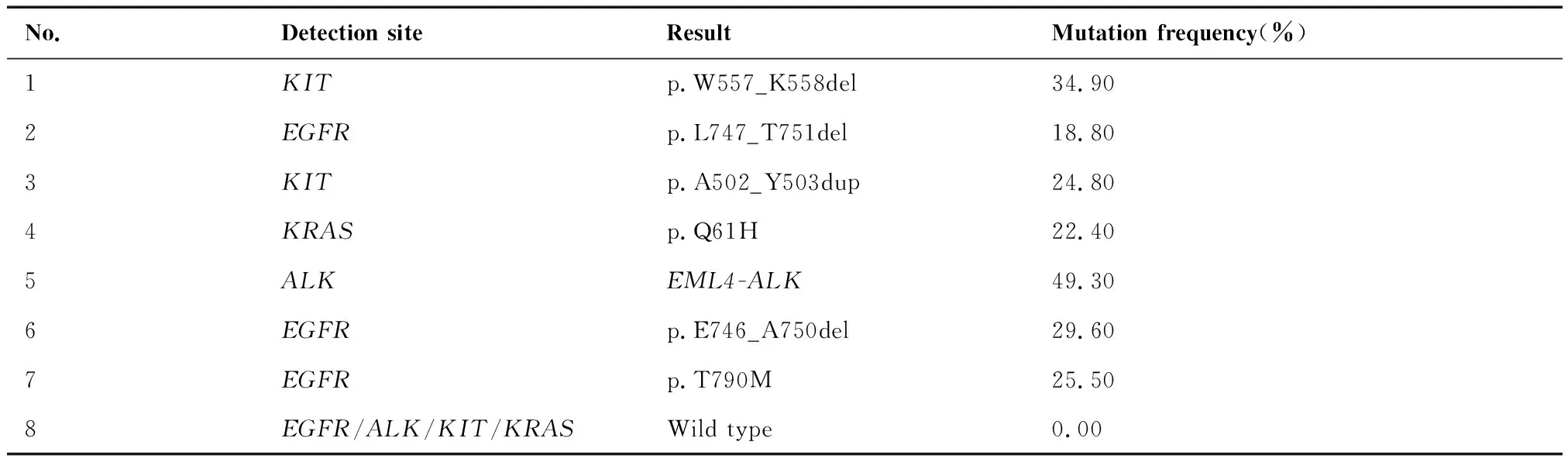
表1 高通量测序检测阳性标本结果

表2 质控品5.00%、2.50%高通量测序结果

图3 5.00%质控品的室内质控日内重复性分析(N=10)

图4 2.50%质控品的室内质控日内重复性分析(N=10)
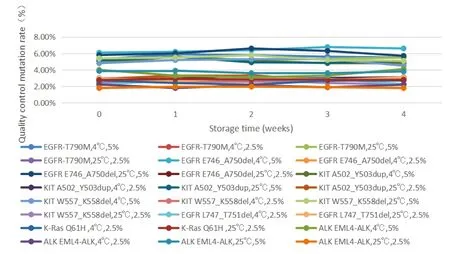
图5 5.00%、2.50%质控品不同温度下短期稳定性结果
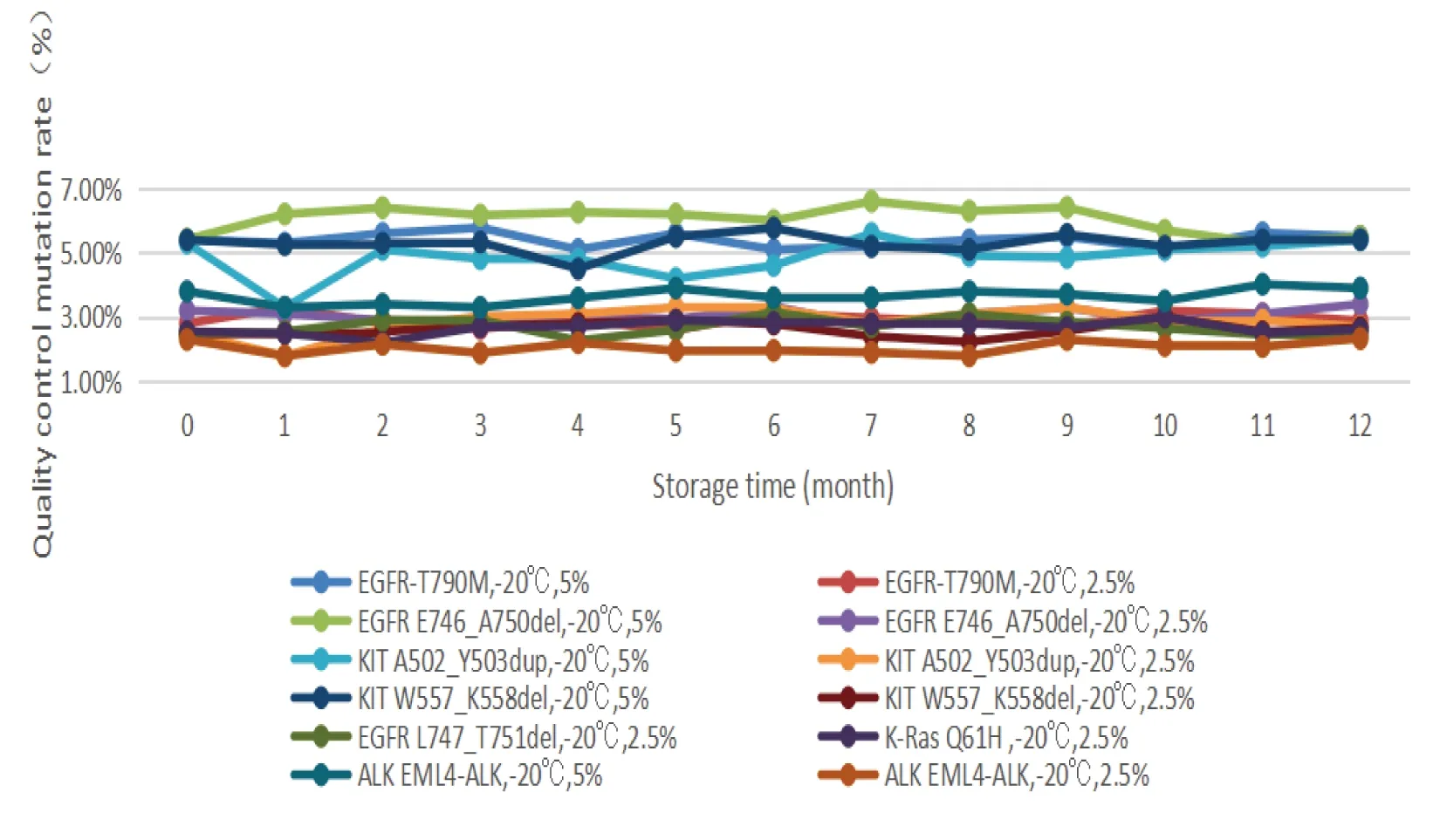
图6 5.00%、2.50%质控品-20℃长期稳定性结果

图7 5.00%质控品不同测序深度与灵敏度的关系

图8 2.50%质控品不同测序深度与灵敏度的关系

图9 5.00%质控品Levey-Jennings质控图

图10 2.50%质控品Levey-Jennings质控图
2.5 特异性试验
同时采用人多基因突变检测通用试剂盒(燃石医学检验所有限公司,295 Panel)分别对5.00%、2.50%的突变质控品进行检测,只有7个突变位点,并无其他交叉阳性,特异性符合要求。
3 讨 论
目前我国和世界上各实验室所使用的高通量检测均为实验室自建试验。这意味着高通量检测在临床应用中具有非常大的灵活性,也意味着高通量检测临床应用具有较大的风险性,这给高通量检测实验室的管理、人员培训和质量控制等(包括检测实验和生物学信息分析)带来巨大的压力[21-23]。二代测序检测项目与传统检测项目相比具有质控点多、自配试剂多、指南标准少及检验过程的性能验证和确认还不完备[24-25]等特点。因此,高通量实验室室内质量控制(internal quality control,IQC) 是保证实验结果准确的重要环节,已成为各级实验室日常工作中一项不可或缺的内容。本研究严格按照高通量测序技术的质量控制要求及方法,并且自制外部质控品进行IQC,以保证检测结果的准确性与稳定性。分析前对样本的运输和保存进行质量控制,分析中需要病理医师对可评估的样本进一步明确病理诊断,并评价标本有无出血、坏死和不利于核酸检测的前处理(例如含盐酸脱钙液处理),病变细胞(如肿瘤细胞)的总量和比例,避免假阴性:组织标本中肿瘤细胞含量建议达到20%以上,低于此标准可富集后检测[26-29];再如,在进入高通量检测流程环节,核酸质量是高通量检测成功的关键因素[30],在制备文库前应采用多种方法对核酸质量进行评估,包括纯度、浓度和完整性分析[31-33];在文库制备过程中,需要对文库的浓度,片段大小等进行质量分析,每个检测项目应设定其文库质量的要求,明确接受或拒绝的标准;分析后需要对下机数据进行初步质量控制,看数据质量是否满足生信分析需求等等。
基因组DNA能够涵盖包括野生型、纯合突变型和杂合突变型在内的所有突变类型。因此本研究利用日常检验阳性及阴性样本自制质控品,将检测样本作为质控品可以模拟基因组复杂性,与检测标本具有相同性质,既符合临床检测的需要又节省了成本,同时该质控物稳定性和特异性较强。此核酸质控品从日常检测的样本中获取,一般选择核酸溶液超过100 μL且浓度高于100 ng /μL 的样本核酸,根据200 ng的投入量需求,每次实验仅需要1~2 μL质控核酸,此质控品可以保证一个实验室6个月以上的IQC需要。本实验选择的自制质控品从来源上难以大量获得,且未经过严格的标准物筛选检测,但样本混合后检测的实际突变频率与预期突变频率基本一致,但是也有个别差异稍大,原因可能有如下几点:样本间的差异性、探针捕获效率的不同、在稀释混合样本中带来的误差等,这些都可能导致后面检测结果突变频率的偏差。虽然质粒没有来源限制,且突变频率比较容易控制,但是质粒不能检测核酸提取过程,不能全面地监控试剂盒的检测能力。
综上,本实验室自制质控品达到了本研究所建立的高通量测序技术检测流程及内部质控标准体系的全部参考数值,突变频率在2.50%~5.00%也能被稳定检测出,未出现假阴性,说明质控品的建立可以使检测结果可靠、准确度高,显示该标准体系的参数具有广泛的参考意义,对测序结果正确性、稳定性起到举足轻重的作用,也为同行或即将开展该门技术的相关医技和科研人员提供参考或借鉴意义,同时促进高通量测序技术更好地进入临床应用和科研工作中,以助精准医疗一臂之力。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。
