锂原电池正极MnO2-Ag的制备及放电性能研究
2020-10-27王鑫,蒋妍
王 鑫,蒋 妍
(1湖北工业大学电气与电子工程学院,湖北 武汉 430068; 2 湖北工业大学理学院,湖北 武汉 430068)
金属离子电池的起源可以追溯到20世纪50年代开始的锂离子电池研究。1958年,Johnston提出用锂、钠等碱金属做为电池负极材料后[1],锂电池研究就引起了人们极大的兴趣。当时的锂电池正极材料大部分含有氟元素和硫元素[2],对环境会造成氟污染和硫污染,再加上成本高昂、高倍率放电性能差、安全性差等因素[3]而不被认可。随着21世纪的到来,人们的环境保护意识和安全意识越来越强[4],成本低、对环境友好、安全性能和放电性能优异的锂锰原电池受到科学家的广泛关注[5-6]。锂锰原电池中最关键的一部分是正极材料,为了得到性能优异的正极材料[7],常用的解决办法是对正极材料进行改性,主要改性方法有掺杂[8-10]、复合[11-12]和包覆[13-15]。其中,包覆改性可以减少电解液和电极材料的副反应,并且根据不同的包覆物会有不同的特殊效果[16]。本文通过固相热分解法将银沉积在电解二氧化锰表面,提高正极材料的导电性,从而提高锂锰原电池的放电性能。
1 实验部分
1.1 材料与仪器
实验材料:硝酸银、无水乙醇、N-甲基吡咯烷酮(NMP)和乙炔黑,分析纯,国药集团有限公司;聚偏氟乙烯(PVDF),分析纯,美国苏威;六氟磷酸锂电解液,电池级,东莞市杉杉电池有限公司;电解二氧化锰,电池级,山西力之源电池材料有限公司;去离子水为实验室自制超纯水。
实验仪器:Land CT2001A测试仪(武汉蓝电);CHI660E电化学工作站(上海辰华);KSL-1200X-J马弗炉(合肥科晶);SHZ-D(III)循环水式真空泵、CJB-S-5D多点磁力搅拌器(巩义予华);D8 ADVANCE型号X射线衍射分析仪(Bruker,德国);JSM-6700F型号场发射扫描电子显微镜(JEOL,日本);Super系列手套箱(MIKROUNA,上海)。
1.2 制备方法
1.2.1MnO2-Ag正极材料的制备实验通过固相热分解法制备MnO2-Ag正极材料。首先,称取不同质量的AgNO3粉末分别置于5个小烧杯中,各加入0.1 mol去离子水,搅拌均匀;称取0.04 mol电解二氧化锰粉末分别加入5份AgNO3水溶液中。搅拌器搅拌2 h后,将小烧杯置于鼓风干燥箱中干燥8 h。将干燥好的5份样品分别放入研钵中进行研磨,研磨后平铺至小瓷舟中,用铅笔在瓷舟上标记a1-a5,将未包覆Ag的电解二氧化锰研磨后也平铺在小瓷舟中,标记a0;将6个小瓷舟置于马弗炉400 ℃烧制10 h后,得到MnO2和MnO2-Ag正极材料。Ag的包覆量见表1。
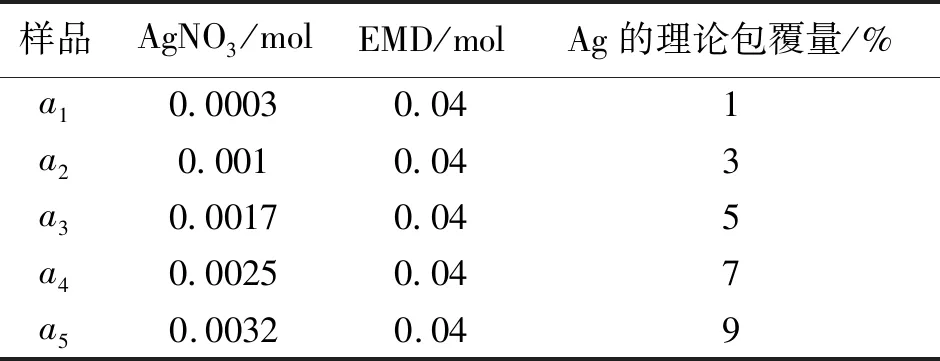
表1 研究Ag最佳包覆量(马弗炉煅烧温度400 ℃)
1.2.2 电极片的制备将活性物质(MnO2-Ag正极材料)、导电剂(乙炔黑)、粘结剂(PVDF)按质量比8∶1∶1称量后移至研钵中,研磨混合1 h,滴加少量助磨剂NMP进行研磨,研磨成粘稠匀浆后,擦净集流体表面,将浆料用刮膜器涂在铝箔集流体上,膜面尽量保持平整,随后将涂布好的极片置于80 ℃鼓风干燥箱干燥12 h,确保NMP挥发干净,取出极片将其夹在辊压机模具中间,用10 MPa的压力保压1 min,压实后,用切片机将其切成10 mm的圆片,得到电极片,选取边缘整齐,无掉粉的极片用于下一步。
1.2.3 锂锰电池的制备采用型号CR2032纽扣电池,在充有高纯氩气(Ar)的手套箱里进行半电池的组装,手套箱的使用条件:水含量≤ 0.1×10-6,氧含量≤ 0.1×10-6。半电池安装示意见图1,组装过程按正极壳、电极片、隔膜、锂片、垫片、弹片、负极壳的顺序在手套箱中自下向上组装。以金属锂为对电极,隔膜选用聚丙烯膜(Celgard 2400),电解液选用LiPF6。
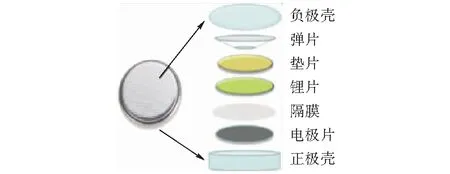
图1 锂电池扣式电池示意图
1.3 材料表征与锂锰电池性能测试
通过XRD分析样品的物相结构;通过SEM对样品的形貌进行表征;通过EDS测试制备材料中Ag的含量;通过蓝电CT2001A电池测试系统(0.01~2.5 V)和上海辰华CHI660E电化学工作站(0.01~2.0 V)对制备材料进行电化学性能测试分析。
2 结果与讨论
2.1 材料的物相及形貌分析
图2中a1-a5曲线分别代表Ag的理论包覆量为1%、3%、5%、7%和9%,可以看出,所有样品的XRD图谱中均在2θ为27.86°、37.44°、42.82°和56.4°出现衍射峰,对应标准粉末衍射卡片PDF号04-0779的(110)、(101)、(111)和(211)晶面,说明制备样品主晶相均为-MnO2[17]。XRD图谱表明,虽然Ag的包覆量有变化,但在a1-a5号样品的XRD图谱中均没有出现Ag单质和AgOx的衍射峰,说明Ag的包覆改性并未使MnO2的晶型发生改变,且均匀地分散在二氧化锰表面。
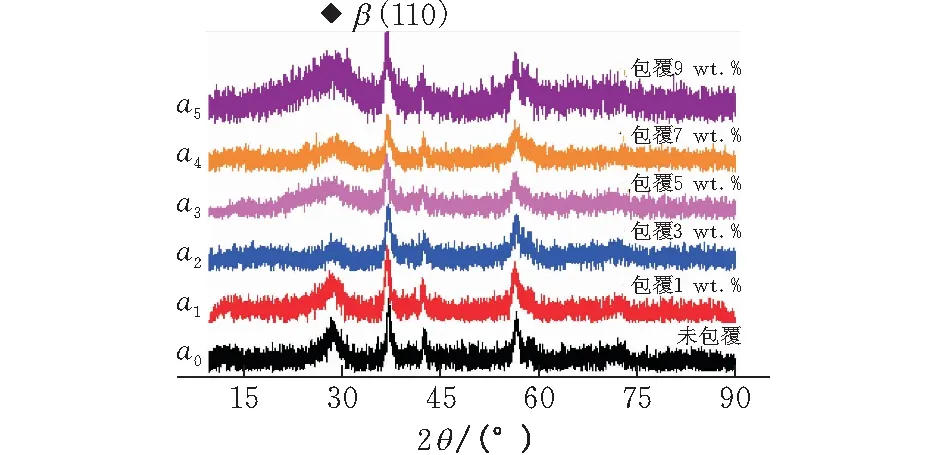
图2 电解二氧化锰和不同包覆量的MnO2-Ag的X射线衍射(XRD)图谱
图3为未经热处理的电解MnO2和理论包覆量1%~9%的MnO2-Ag正极材料放大5万倍后的微观形貌图。从SEM图上可看出,未处理过的MnO2团聚现象明显,颗粒尺寸大,而经过Ag表面处理之后的MnO2颗粒尺寸明显小于前者。这说明Ag的表面修饰可以有效阻止MnO2的团聚。从SEM图上看不出Ag单质的存在,下一步通过X射线能谱仪结合表面形貌表征来说明。

图3 不同包覆量的MnO2-Ag材料的SEM图
(a)AgNO3-1%
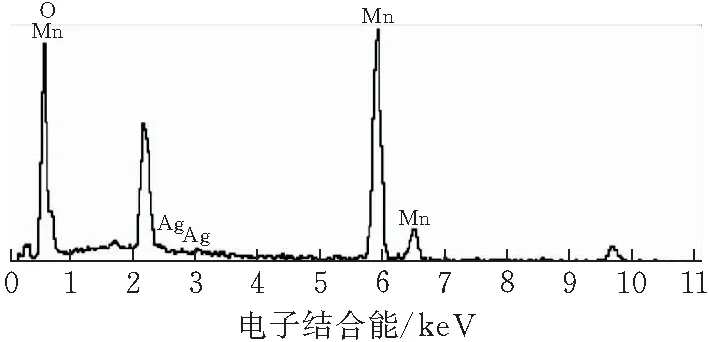
为了验证Ag是否成功包覆在MnO2的表面,进一步对MnO2-Ag复合正极材料做了EDS测试分析。由图4可知,有Mn和O元素的存在,也有Ag元素的存在,表明Ag成功与MnO2进行了复合。图4中右上角表格为Mn、O和Ag的质量比和原子数百分比。从表中可得,Ag的实际质量分数分别是1.18%、3.28%、4.56%、7.16%和8.67%,基本与理论包覆量吻合,证明Ag确实存在于复合材料中,同时也说明使用固相热分解法得到了与期望值非常接近的Ag的改性结果。
2.2 电化学性能分析
图5为MnO2和Ag包覆量为1%~9%的MnO2-Ag正极在锂锰原电池中的放电曲线。从图中可以看出,当Ag的包覆量为5%时的放电性能最优。电解MnO2在0.1、0.2、0.5和1 C电流密度下的放电比容量分别为144.4、128.1、106.8和91.3 mAh/g,而Ag包覆量5%的MnO2-Ag复合正极材料在相同倍率下的放电比容量分别为194.5、169、139.2和98.1 mAh/g,放电比容量分别提高了34.7%、32%、30%和7%。这说明有Ag包覆后,MnO2的电化学性能得到很大的提升。
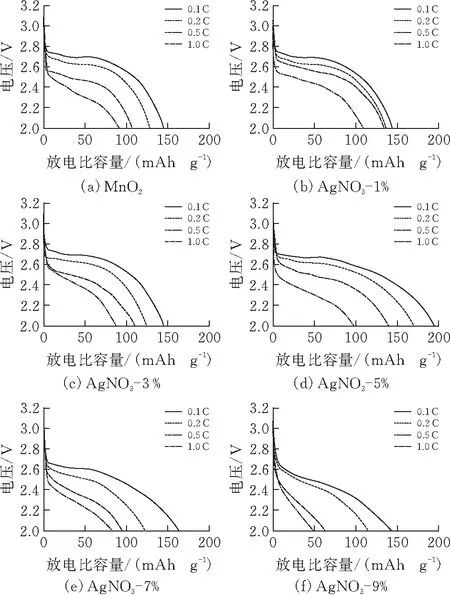
图5 不同材料的放电性能
2.3 交流阻抗分析
图6是电解MnO2和包覆量5%的MnO2-Ag电极的EIS图谱。图中可以看出,两条曲线都是由高频区的压缩半圆和低频区的直线构成。其中,半圆对应为电荷迁移电阻,半圆的直径与电荷迁移电阻的大小相关[18-20];直线则对应体系的Warburg阻抗,与材料中Li+的扩散有关,反映了其在活性物质材料体相中扩散的难易程度。两者的电荷迁移电阻大小关系为MnO2>MnO2-Ag,电解MnO2和5%包覆量的MnO2-Ag电极的电荷传递电阻分别为459和180 Ω,说明以AgNO3为银源的固相热分解法制备的MnO2-Ag比未包覆Ag的MnO2材料具有更低的电荷迁移电阻,有利于电子传递,从而改善电池的放电性能。
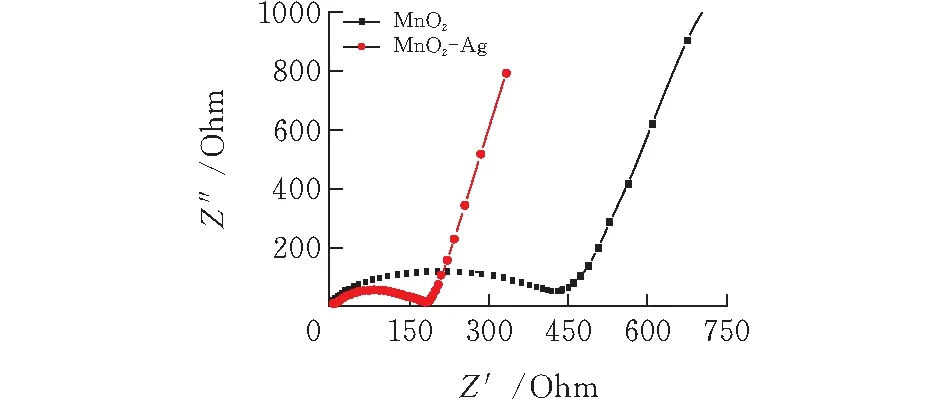
图6 电解MnO2和包覆量5%的MnO2-Ag电极的交流阻抗(EIS)图谱
3 结论
本文采用了一种制备工艺简单、成本低的固相热分解法制备了5组不同Ag包覆量的MnO2-Ag正极材料,并封装成锂锰原电池。研究表明,Ag的包覆并未改变MnO2的晶型结构,将Ag包覆到MnO2表面并400 ℃热处理后,Ag包覆量5%的样品在锂锰原电池中表现出最佳的性能。在不同电流密度(0.1、0.2、0.5和1 C)下放电比容量分别为194.5、169、139.2和98.1 mAh/g,放电比容量比未包覆的MnO2材料分别提高了34.7%、32%、30%和7%。这可能是由于银的加入提高了材料的导电性,从而大大提高了锂锰电池的电化学性能。
