BI-1在心肌缺血再灌注损伤中的作用及机制研究
2020-10-26钟小兰班努库肯景江新
钟小兰 班努·库肯 景江新
RoleandMechanismofbi-1inMyocardialIschemia-reperfusionInjury.ZhongXiaolan,Bannu·Kuken,JingJiangxin.DepartmentofCardiology,TheSecondAffiliatedHospitalofXinjiangMedicalUniversity,Xinjiang830063,China
AbstractObjectiveTo investigate the role and mechanism of BI-1 in myocardial ischemia-reperfusion injury.MethodsRat models of myocardial ischemia-reperfusion injury and oxidative stress injury of H9c2 cardiomyocytes were constructed. The expression of BI-1 was evaluated by RT-qPCR and Western blot, and subcellular localization of BI-1 was observed by laser confocal microscopy. BI-1 overexpression plasmids and BI-1 shRNA were transfected into H9c2 myocardial cells. BI-1 expression, cell survival rate, activity of LDH, caspase-3 and caspase-9, and apoptotic rate of cardiomyocytes were detected.ResultsCompared with the sham group, the myocardial infarction area appeared in the I/R group, and the LDH level was significantly increased (P=0.000). Both mRNA and protein level of BI-1 were increased in heart tissues of rats with ischemia-reperfusion injury in a time-dependent manner (P<0.01). In cardiomyocyte oxidative stress injury model, the expression level of BI-1 was increased with H2O2stimulation (P<0.01). Overexpression of BI-1 decreased the activity of LDH (P<0.05) and the number of apoptotic cells (P<0.01), but inhibited the activity of caspase-3, caspase-9 and increased the cell survival rate (P<0.01). Knockdown of BI-1 increased the activity of LDH (P<0.01), decreased the cell survival rate (P<0.05), and increased the number of apoptosis of cardiomyocytes (P<0.01). In addition, BI-1 was located on mitochondria by laser confocal observation.ConclusionIschemia reperfusion injury and oxidative stress promoted the expression of BI-1 in cardiomyocytes, which could inhibit the apoptosis of cardiomyocytes caused by oxidative stress, exerting a protective role in the myocardium.
KeywordsCardiac ischemia-reperfusion injury; Bax inhibitor-1; Apoptosis; Oxidative stress injury
冠状动脉急性和持续性缺血缺氧所导致的心肌坏死称为急性心肌梗死[1],如今社会老龄化严重,饮食习惯改变,生活节奏加快,急性心肌梗死的发生率在我国不断升高,居高不下的高病死率给人们的身体健康和社会的稳定发展带来很大的危害[2,3]。支架置入术、直接冠状动脉介入治疗及溶栓治疗等技术的不断进步,明显降低了急性心肌梗死的病死率[4]。但是,心肌梗死患者因缺少改善冠状动脉血管再灌注损伤的有效方案,预后受到极大的影响。研究表明心肌缺血再灌注损伤中有大量心肌细胞凋亡现象[5,6]。心肌凋亡是造成损伤进一步恶化的重要事件,而凋亡作为程序性细胞死亡,是可以经过调控被阻断的,因此靶向凋亡有助于缓解损伤。近年来发现的存在于细胞中的凋亡抑制因子BI-1(Bax inhibitor-1),能够通过抑制线粒体相关凋亡途径来阻止细胞凋亡相关过程[7]。研究表明,BI-1是一种抗凋亡蛋白,可保护细胞免受许多不同的固有死亡刺激包括内质网应激引起的细胞凋亡等,BI-1可以抑制Bax介导TNF相关的凋亡诱导配体(TNF related apoptosis inducing ligand,TRAIL)诱导的细胞凋亡[8~10]。控制心肌缺血再灌注损伤的关键途径之一是抑制心肌细胞凋亡。BI-1作为细胞凋亡调控蛋白,其对缺血再灌注心肌是否具有保护作用以及如何发挥作用,仍然不清楚。因此,本实验旨在研究BI-1在心肌缺血再灌注损伤和氧化应激损伤下抗心肌细胞凋亡的作用,进一步探讨其发挥心肌保护的作用机制。
材料与方法
1.材料: 体质量约250g,7~8周龄的清洁级雄性Sprague Dawley大鼠,来自新疆医科大学实验动物中心。大鼠H9c2心肌细胞购自中国科学院上海细胞生物研究所。DMEM(Dulbecco′s-modified Eagle′s medium)培养基购自美国Gibco公司;Prime Script TM RT reagent Kit with gDNA Eraser(Perfect Real Time)购自大连TaKaRa公司;线粒体荧光探针(Mito Tracker)购自上海翊圣生物科技有限公司;BI-1单克隆抗体购自圣克鲁斯生物技术(上海)有限公司;鼠抗GAPDH多克隆抗体购自天津三箭生物技术有限公司;辣根过氧化物酶标记的山羊抗兔二抗(Goat Anti-Rabbit IgG Secondary Antibody)、辣根过氧化物酶标记的山羊抗鼠二抗(Goat Anti-Mouse IgG Secondary Antibody)购自北京义翘神州科技有限公司;ECL化学发光试剂盒购自上海碧云天生物技术有限公司;乳酸脱氢酶活性检测试剂盒购自南京建成生物公司;pcDNA3.1(-)-BI-1质粒购自上海吉玛公司;shRNA NC和BI-1 shRNA质粒购自上海吉玛制药技术公司;Turbofect转染试剂购自赛默飞世尔科技(中国)公司。37℃恒温细胞培养箱购自自黑龙江东拓仪器制造有限公司;组织切片仪购自徕卡显微系统(上海)贸易有限公司;荧光定量PCR仪购自赛默飞世尔科技(中国)公司;激光扫描共聚焦显微镜购自德国Carl Zeiss公司产品;凝胶成像仪和蛋白电泳仪购自美国伯乐公司。
2.大鼠心肌缺血再灌注损伤(Ischemia-reperfusion injury,I/R)模型的建立:按照文献方法制备模型[11]:用10%水合氯醛麻醉Sprague-Dawley大鼠,仰卧位固定大鼠,通过左胸廓切开术打开胸腔暴露心脏。将5/0丝线缝合在左冠状动脉前降支(Left anterior descending,LAD)周围,使用活结打结。关闭开胸手术,左冠状动脉前降支结扎15、30或45min后,允许心脏再灌注不同的时间(1、2、4、8h),再灌注期结束后,收集血液,并迅速取出左心室游离壁缺血区心脏。假手术组冠状动脉不结扎,模型制备方法和上述相同。
3.乳酸脱氢酶(lactate dehydrogenase, LDH)活性测定:根据LDH测定说明书测定LDH活性:收取假手术组和缺血再灌注组血清,将相同体积的蒸馏水、待测样本和标准液分别加到标准管、空白管、对照管和测定管中。再向各管添加250μl基质缓冲液,将50μl辅酶Ⅰ加到待测管里,充分混匀后在37℃水浴锅中孵育15min,将2,4-二硝基苯肼加入到各管中,37℃孵育15min,添加2.5ml氢氧化钠(0.4mmol/L)溶液于各管中,静置5min,测定各管吸光度,利用公式LDH活性(U/L)=(ODu-ODc)/(ODS-ODB)×Cs×N×1000进行计算。
4.大鼠心肌细胞氯化三苯基四氮唑(triphenyl tetrazolium chloride,TTC)染色:建立大鼠缺血再灌注损伤模型后,将各组细胞心脏取出,用PBS冲洗几次,吸干水分后置于-20℃冷冻30min,用组织切片仪切取冷冻的心脏,将切取的冷冻切片置于2%TTC溶液中,于室温浸泡20min,注意避光,用4%多聚甲醛固定染好的心脏切片,观察灰白色区域(梗死区)和砖红色区域(非梗死区)并拍取照片。
5.心肌细胞培养及处理:在含10%胎牛血清的DMEM培养基的培养瓶中培养H9c2细胞,放于37℃、5%CO2培养箱中培养。每天按时观察细胞状态,用1mmol/L 过氧化氢(hydrogen peroxide,H2O2)刺激心肌细2、4、8、16h后收集细胞RNA样和蛋白样用于检测,不同浓度(0.25、0.50、0.75、1.00mmol/L)H2O2刺激细胞16h收集细胞RNA样和蛋白样用于后续实验。
6.细胞转染:将H9c2细胞以1×105个/孔接种于12孔板,待细胞密度生长至约70%时,将pcDNA3.1(-)-BI-1、pcDNA3.1(-)、BI-1shN和shNC质粒(序列为: BI-1-shRNA:5′-GCATCCTTATCACTGCATTTG-3′,shNC:5′-GTTCTCCGAACGTGTCACGT-3′)按照Tubfect转染试剂的说明书转染到H9c2细胞中,放于37℃、5% CO2培养箱中小心培养一定时间后,收集细胞RNA样和蛋白样用于后续实验。
7.Cell Counting Kit-8(CCK-8)法检测细胞存活率:将转染pcDNA3.1(-)-BI-1、pcDNA3.1(-)、BI-1-shRNA和shNC质粒的H9c2细胞株按照1×105个/毫升铺于96孔板中,放在37℃、5%CO2培养箱中培养,用1mmol/L的H2O2刺激细胞16h,同时设置未用H2O2刺激的细胞作为对照组,然后去除上清液,每个孔加入100μl混合培养液(CCK8工作液和培养液比例为1∶10),继续自培养箱中培养2h后,用酶标仪读取各孔细胞在450nm处的吸光值。
8.实时荧光定量PCR(RT-qPCR):按照实验要求收取细胞RNA样,利用Trizol试剂提取细胞的RNA,测定浓度后,参照TaKaRa公司两步法反转录试剂盒说明书反转成cDNA,使用Applied Biosystems 7300实时PCR系统完成RT-qPCR,用2-△△Ct法分析定量结果。实验所用的引物见表1。
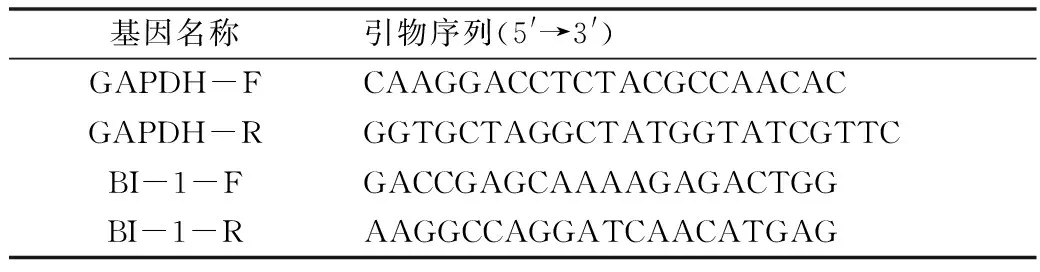
表1 引物序列
9.Western blot法检测:收取蛋白样,提取出蛋白质后,通过BCA法测定上清液中蛋白质的浓度,配置SDS-PAGE胶,浓缩胶80V、30min,分离胶120V、1.5h的程序进去电泳,结束后根据蛋白大小湿转或半干转至PVDF膜上,室温下用50g/L脱脂奶粉封闭2h,用Tris-HCl缓冲盐溶液(TBST)按比例稀释特异性一抗,将封闭后的PVDF膜转移至一抗稀释液中4℃孵育过夜,TBST洗5洗,每次5min,再将PVDF膜转移至TBST稀释好的二抗中,37℃孵育2h,TBST洗5洗,每次5min,将PVDF膜置于ECL发光成像仪中显影照相,分析结果。
10.激光共聚焦显微镜检测了BI-1的亚细胞定位:培养H9c2细胞于激光共聚焦皿中,待细胞密度合适时,将重组质粒GFP-BI-1转染于细胞里,培养24h后,加入Mitotracker探针,37℃、5%CO2培养箱中培养45min,PBS清洗3次,每次5min,加入40g/L多聚甲醛固定20min,PBS清洗3次,每次5min,加入Hoechst 33258染核10min,PBS清洗3次,每次5min,在激光共聚焦显微镜下观察细胞。
11.caspase-3、caspase-9活性检测:在指定的时间段内,用1mmol/L的H2O2处理细胞。用50μl细胞裂解液裂解细胞10min,在4℃条件下以12000r/min离心1min,通过Bradford法(DingGuo Biotechnology)测定上清液中的蛋白质浓度。含有等量蛋白质的上清液用于caspase-3比色测定或caspase-9活性测定,在37℃下孵育1~2h后,用微量滴定板读数器测量405nm处的吸光度。
12.流式细胞仪(flow cytometry,FCM)检测心肌细胞凋亡:用1mmol/L H2O2处理H9c2心肌细胞,胰酶消化后,用含10%胎牛血清的DMEM进行中和,1000r/min离心10min弃上清,PBS洗3次,沉淀置于70%的乙醇中于4℃固定过夜,用流式细胞仪检测各组细胞的细胞凋亡水平,收集数据进行显著性分析。

结 果
1.缺血再灌注损伤模型中BI-1的表达量:建立缺血再灌注损伤模型,通过RT-qPCR检测不同缺血时间和不同再灌注时间细胞中BI-1的基因水平,Western blot法检测BI-1的蛋白水平,测定乳酸脱氢酶活性和TTC染色观察心肌梗死范围。与假手术组比较,缺血再灌注组乳酸脱氢酶活性明显升高(P=0.000,图1A),出现了心肌梗死区,心肌梗死组织大面积呈现灰白色(图1B);不同缺血时间(15、30、45min)后再灌注8h,细胞中BI-1的基因水平和蛋白水平均明显升高,且随缺血时间依赖性升高(P=0.000,图1C,图1D);缺血45min后,再灌注不同时间(1、2、4、8h), BI-1的基因和蛋白表达量也明显升高,且随再灌注时间依赖性升高(P<0.01,图1E,图1F)。
2.H9c2心肌细胞氧化应激损伤模型中BI-1的表达量:建立H9c2心肌细胞氧化应激损伤模型,通过RT-qPCR、Western blot法检测同一浓度H2O2刺激不同时间BI-1的基因和蛋白表达量和不同浓度H2O2刺激相同时间BI-1的基因和蛋白表达量。与对照组比较,用1mmol/L H2O2刺激心肌细2、4、8、16h后BI-1的基因水平和蛋白水平均明显提高,且随刺激时间依赖性升高(P<0.01,图2A,图2B)。不

图1 BI-1在大鼠心肌缺血再灌注损伤细胞中的表达A.假手术组和缺血再灌注组乳酸脱氢酶活性测定;B.心肌细胞TTC染色(×200);C. RT-qPCR检测不同缺血时间BI-1的表达量;D. Western blot法检测不同缺血时间BI-1的表达量; E. RT-qPCR检测不同再灌注时间BI-1的表达量;F. Western blot法检测不同再灌注时间BI-1的表达量。与假手术组比较, *P<0.01,**P=0.000
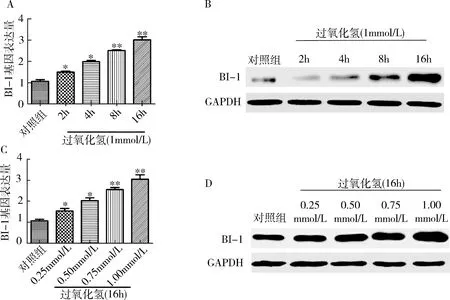
图2 BI-1在氧化应激损伤心肌细胞中的表达A.RT-qPCR检测1mM H2O2刺激心肌细不同时间后BI-1的表达量;B. Western blot法检测1mmol/L H2O2刺激心肌细不同时间后BI-1的表达量;C. RT-qPCR检测不同浓度H2O2刺激细胞16h后BI-1的表达量;D. Western blot法检测不同浓度H2O2刺激细胞16h后BI-1的表达量。与对照组比较, *P<0.01,**P=0.000
同浓度H2O2(0.25、0.50、0.75、1.00mmol/L)刺激细胞16h后,BI-1的基因水平和蛋白水平均显著提升,且随刺激浓度依赖性升高(P<0.01,图2C,图2D)。
3.过表达BI-1对H2O2所致H9c2细胞损伤的影响:构建了pcDNA3.1(-)-BI-1重组质粒,转染H9c2细胞并用1mmol/L H2O2刺激细胞,检测过表达BI-1对H2O2所致H9c2细胞损伤的影响。RT-qPCR和Western blot法检测BI-1的基因和蛋白表达量都高于对照组,pcDNA3.1(-)-BI-1重组质粒在H9c2细胞中成功表达(图3A,图3B)。过表达BI-1使乳酸脱氢酶的活性降低(P<0.05),还能减少细胞毒性,使细胞存活率升高(P<0.01,图3C,图3D);过表达BI-1抑制了氧化应激所引起的caspase-3、caspase-9活性上升(P<0.05,图3G,图3H);过表达BI-1明显抑制了氧化应激损伤所致细胞的凋亡(P<0.01,图3E,图3F)。

图3 过表达BI-1对H2O2所致H9c2细胞损伤的影响A.RT-qPCR检测pcDNA3.1(-)-BI-1的过表达效果;B. Western blot法检测pcDNA3.1(-)-BI-1的过表达效果;C.乳酸脱氢酶活性测定;D.心肌细胞存活率测定;E.流式细胞仪检测心肌细胞凋亡率;F.心肌细胞凋亡率统计;G. caspase-3活性检测;H. caspase-9活性检测。*P<0.05,**P<0.01,***P=0.000
4.干扰BI-1表达对H2O2所致H9c2细胞损伤的影响:构建了BI-1-shRNA重组质粒,转染H9c2细胞并用1mmol/L H2O2刺激细胞,检测干扰BI-1表达对H2O2所致H9c2细胞损伤的影响。RT-qPCR和Western blot法检测BI-1的基因和蛋白表达量都低于对照组,BI-1-shRNA重组质粒在H9c2细胞中成功表达(图4A,图4B)。干扰BI-1表达使乳酸脱氢酶的活性升高(P<0.01),细胞存活率下降(P<0.05,图4C,图4D)。干扰BI-1表达使H9c2细胞的凋亡数增加(P<0.01,图4E,图4F)。

图4 干扰BI-1表达对H2O2所致H9c2细胞损伤的影响A. RT-qPCR检测干扰BI-1表达后BI-1的表达量;B. Western blot法检测干扰BI-1表达后BI-1的表达量;C. 乳酸脱氢酶活性测定;D. 心肌细胞存活率测定;E. 流式细胞仪检测心肌细胞凋亡率;F. 心肌细胞凋亡率统计。*P<0.05, **P<0.01,***P=0.000
5.激光共聚焦观察BI-1的亚细胞定位:构建GFP-BI-1重组质粒,通过激光共聚焦观察BI-1的亚细胞定位,BI-1定位于线粒体上,和线粒体标志物存在共定位(图5)。

图5 激光共聚焦观察BI-1的亚细胞定位A.激光共聚焦观察BI-1-GFP的定位;B.激光共聚焦观察线粒体的定位;C.激光共聚焦观察细胞核的定位;D.激光共聚焦观察BI-1与线粒体的共定位
讨 论
随着人们生活方式的不断改变,急性心肌梗死患者病死率不断上升,作为心血管危重症,其危害性很大。笔者在心肌梗死早期利用溶栓治疗或放置支架进行干预[12,13]。然而心肌梗死后使用冠状动脉搭桥术常出现心肌缺血再灌注损伤,引起心肌细胞凋亡和死亡,进而引发冠状动脉疾病[14]。心肌缺血再灌注损伤是复杂的病理学过程,研究表明该损伤与氧自由基的产生、白细胞激活和腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)合成障碍等有关,对急性心肌梗死患者的预后产生很大的影响,但其生理机制尚未完全清楚。研究发现BI-1作为一种凋亡抑制因子,已参与了机体各种病理和生理过程。因此,本实验利用过表达和干扰等技术探讨BI-1在心肌缺血再灌注损伤和氧化应激损伤中的作用及其机制。
研究表明BI-1在脑、心脏、肾脏、肝脏等大部分组织中均有表达,在很多疾病中都发挥关键作用。有文献报道BI-1基因对于哺乳动物肝脏和肾脏心肌缺血再灌注损伤具有内在抵抗力。另外发现在脑损伤和急性脑梗死模型中, BI-1能够通过抑制海马区内ERS调控其诱导的细胞凋亡[15]。本实验中笔者首先检测了BI-1在大鼠心肌缺血再灌注损伤中的表达量,结果发现BI-1基因和蛋白表达量均升高;在氧化应激模型中,BI-1的表达量也明显上升,笔者认为表达量上调是由缺血再灌注和氧化应激损伤所诱导产生的。猜想BI-1表达量上升可能会起到心肌保护作用,所以构建了BI-1过表达和干扰重组质粒,转染细胞后检测过表达和干扰BI-1对H2O2所致H9c2细胞损伤的影响,结果发现过表达BI-1能够明显抑制氧化应激引起的细胞损伤和凋亡,由此可见BI-1具有心肌保护作用。caspases-3、caspase-9凋亡执行蛋白酶在细胞凋亡过程中起关键作用,笔者检测了过表达BI-1对caspase-3、caspase-9活性的影响,发现过表达BI-1能够降低caspase-3、caspase-9活性,进一步说明了BI-1能够在细胞中发挥抗凋亡功能。之前研究发现,在调节细胞凋亡过程中,线粒体发挥着枢纽作用。而通过激光共聚焦发现BI-1定位于线粒体上,和线粒体标志物存在共定位,更进一步证明了BI-1的抗凋亡作用。
综上所述,凋亡抑制因子Bax inhibitor-1(BI-1)在缺血再灌注损伤和氧化应激中表达量增加,能够抑制损伤所导致的心肌细胞凋亡,从而起到心肌保护作用。然而这可能仅是一方面,有关BI-1抗心肌细胞凋亡的作用机制还需要进一步探讨,为BI-1在急性心肌梗死靶向治疗中的应用提供更多的依据。
