产超广谱β-内酰胺酶大肠埃希菌和肺炎克雷伯菌血流感染的危险因素分析
2020-10-24王梓凝田硕涵杨靖娴崔一民航天中心医院药剂科北京00049北京大学第一医院药剂科北京0004航天中心医院检验科北京00049
谢 清,周 颖,孔 妍,王梓凝,田硕涵,刘 桦,杨靖娴,崔一民#(.航天中心医院药剂科,北京 00049; .北京大学第一医院药剂科,北京 0004; .航天中心医院检验科,北京 00049)
抗菌药物耐药是全球健康和发展的威胁之一,包括大肠埃希菌、肺炎克雷伯菌和不动杆菌在内的耐药革兰阴性菌的传播是最紧迫的问题。产超广谱β-内酰胺酶(extended spectrumβ-lactamase,ESBL)的肠杆菌科细菌已传播到世界各地。随着抗菌药物的广泛应用,细菌耐药情况日益严重,细菌耐药导致医疗保健费用增加,死亡风险增加。在所有的感染中,血流感染(bloodstream infection,BSI)病死率最高,危害性最强。近年来,随着抗菌药物、激素和免疫抑制剂等药物的不合理应用,放疗、化疗、器官移植以及侵入性诊疗技术的开展,BSI发病率呈升高趋势[1]。产ESBL肠杆菌科细菌感染可能导致患者住院时间延长、医疗费用增加和病死率升高,且产ESBL大肠埃希菌和肺炎克雷伯菌引起的BSI患者往往伴有不明原因发热或者中毒性休克,而微生物检验需要一定的时间,如果在获得微生物检验结果后再开始抗感染治疗,往往已错过最佳治疗时机[2-3]。因此,临床需要准确评估产ESBL大肠埃希菌和肺炎克雷伯菌BSI的危险因素,尽早制订适宜的抗感染治疗方案。
1 资料与方法
1.1 研究对象
1.1.1 纳入标准:同时满足以下所有条件者可入选。(1)2015—2018年某三级医院(以下简称“该院”)出院的患者;(2)年龄≥18周岁;(3)临床诊断为BSI;(4)血培养结果为大肠埃希菌或肺炎克雷伯菌。
1.1.2 排除标准:符合下列任意1条者将被排除。(1)病历信息(病例资料调查涉及的内容)不全;(2)住院时间<48 h;(3)血培养出现2种及以上细菌;(4)没有进行ESBL检测。
1.2 菌株来源、药物敏感试验与仪器
菌株来源于2015—2018年该院接收的血液标本,同一患者相同标本仅取第1株。对临床送检标本的细菌分离和培养参照《全国临床检验操作规程》进行。采用VITEK 2 Compact全自动微生物鉴定及药敏分析仪(法国生物梅里埃公司)对菌株进行细菌鉴定和药物敏感试验。药物敏感试验判断参照美国临床和实验室标准协会(clinical and laboratory standards institute,CLSI)M100-S27文件标准。质控菌:大肠埃希菌ATCC25922和肺炎克雷伯菌ATCC700603。
1.3 病例资料调查
由2名临床药师按照设计好的信息收集表,采用Excel软件独立进行数据的收集,并进行交叉核对,不一致的信息通过讨论或咨询老年医学科临床医师解决。收集的具体信息包括:(1)人口统计学资料,如姓名、性别及年龄;(2)基本住院信息,如病历号、入院日期、出院日期及出院诊断;(3)实验室检查结果,如白细胞计数、中性粒细胞百分比、C反应蛋白、血浆降钙素原、血肌酐、血培养送检时间、血培养药物敏感试验结果报告时间和结果;(4)BSI抗菌药物治疗方案,如抗菌药物通用名称、用药途径、用药剂量和频次、治疗开始和结束时间;(5)合并疾病,如高血压、糖尿病、脑卒中、冠状动脉疾病、外伤、恶性肿瘤、肝炎、慢性肾功能不全、肠梗阻、结核、慢性阻塞性肺疾病和慢性支气管炎;(6)危险因素,如是否入住ICU、近3个月是否有住院史、侵入性操作史(BSI前2周内是否接受外科手术、气管切开及置入中心静脉导管等穿刺操作,鼻饲管,导尿管,内镜检查和血液滤过)、抗菌药物使用史(是否使用抗菌药物及药品名称)以及其他用药史(BSI前2周内是否使用糖皮质激素、免疫抑制剂、化疗药和质子泵抑制剂)。
1.4 统计学方法
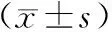
1.5 伦理审批
本研究通过该院伦理委员会审批,允许豁免患者知情同意书。
2 结果
2.1 大肠埃希菌和肺炎克雷伯菌BSI的来源和科室分布
本研究共纳入280例大肠埃希菌和肺炎克雷伯菌所致BSI病例,检出大肠埃希菌196株(检出率为70.00%),肺炎克雷伯菌84株(检出率为30.00%);其中,产ESBL大肠埃希菌、产ESBL肺炎克雷伯菌检出率分别为53.57%(105株)、32.14%(27株)。检出菌主要来自呼吸、消化和泌尿系统疾病患者;检出菌株数排序居前3位的科室分别为老年医学科、肝胆外科和血液科。
2.2 大肠埃希菌和肺炎克雷伯菌BSI患者的临床特征
280例大肠埃希菌和肺炎克雷伯菌所致BSI患者的平均年龄为(62.1±19.0)岁,51.79%(145/280)的患者是男性;51.07%(143/280)的患者为院内感染;44.29%(124/280)的患者近3个月内有住院史;19.64%(55/280)的患者有ICU入住史;50.71%(142/280)的患者近2周内使用过抗菌药物;16.79%(47/280)的患者近2周内使用过糖皮质激素;40.71%(114/280)的患者近2周内使用过质子泵抑制剂,见表1。
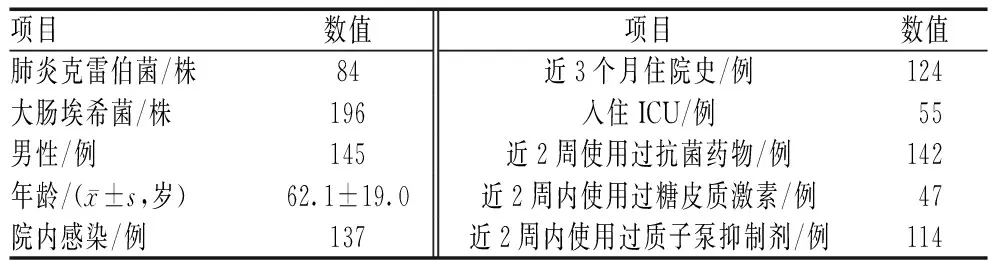
表1 大肠埃希菌和肺炎克雷伯菌BSI患者的临床特征Tab 1 Clinical feature of patients with bloodstream infection of E.coli and K.pneumoniae
2.3 产ESBL大肠埃希菌和肺炎克雷伯菌BSI的危险因素分析
产ESBL大肠埃希菌和肺炎克雷伯菌BSI危险因素的单因素分析见表2。进一步将上述危险因素纳入多因素分析,结果显示,大肠埃希菌感染、近3个月内住院史、近2周内使用头孢菌素类抗菌药物和近2周内使用头孢菌素类抗菌药物/β-内酰胺酶抑制剂复方制剂为产ESBL大肠埃希菌和肺炎克雷伯菌BSI的独立危险因素,见表3。

表2 产ESBL大肠埃希菌和肺炎克雷伯菌BSI危险因素的单因素分析Tab 2 Univariate analysis of risk factors of patients with bloodstream infection of ESBL-producing E.coli and K.pneumoniae
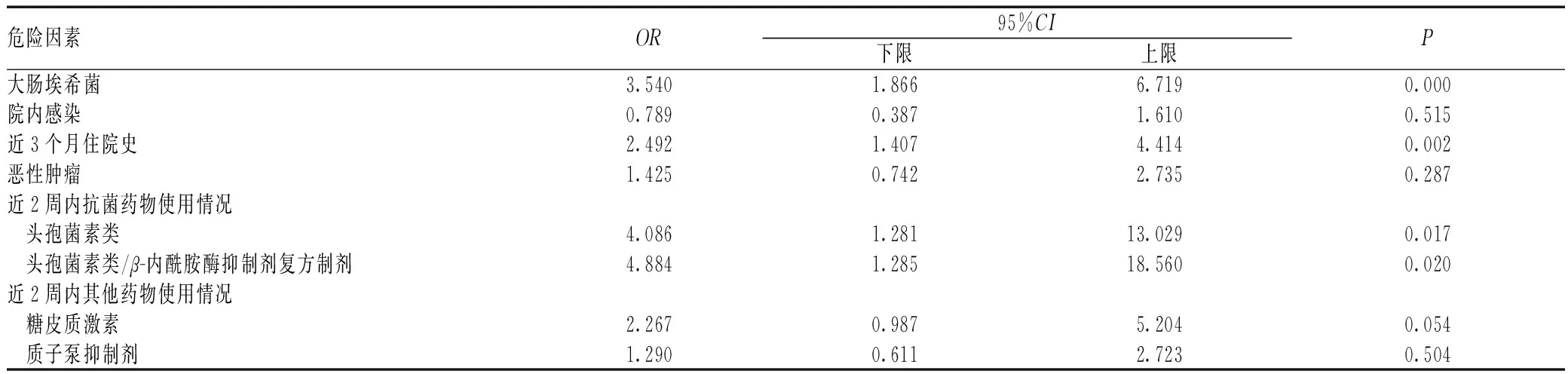
表3 产ESBL大肠埃希菌和肺炎克雷伯菌BSI危险因素的多因素分析Tab 3 Multivariate analysis of risk factors of patients with bloodstream infection of ESBL-producing E.coli and K.pneumonia
3 讨论
本研究结果显示,大肠埃希菌和肺炎克雷伯菌BSI中产ESBL菌株的检出率分别为53.57%和32.14%,与国外报道一致[4];肺炎克雷伯菌BSI中产ESBL菌株的检出率稍高于国内报道的社区肺炎克雷伯菌BSI中产ESBL菌株的检出率[5]。BSI中大肠埃希菌和肺炎克雷伯菌菌株数和产ESBL菌株检出率均靠前的科室包括老年医学科、血液科和肝胆外科等,提示上述科室大肠埃希菌或肺炎克雷伯菌BSI时需警惕产ESBL菌株感染的可能。老年医学科、血液科的住院患者肠杆菌科细菌BSI可能与患者反复入院、免疫功能低下以及有创操作多等因素有关;外科系统肠杆菌科细菌BSI可能与手术操作、留置尿管或引流管等有创操作有关。
本研究结果显示,近3个月内住院史为产ESBL大肠埃希菌和肺炎克雷伯菌BSI的独立危险因素(OR=2.492,95%CI=1.407~4.414,P=0.002)。多项研究结果表明,住院史为产ESBL肠杆菌科细菌BSI的独立危险因素,有报道近3个月内住院史是产ESBL大肠埃希菌和肺炎克雷伯菌BSI的独立危险因素[6]。郭亮等[7]报道,近3个月住院史为大肠埃希菌BSI的独立危险因素。因此,对于近3个月有住院史的BSI患者,需考虑其产ESBL菌株感染的可能。
多因素分析结果显示,近2周内使用头孢菌素类抗菌药物为产ESBL大肠埃希菌和肺炎克雷伯菌BSI的独立危险因素(OR=4.086,95%CI=1.281~13.029,P=0.017)。Kaya等[8]经研究发现,近3个月内使用头孢菌素是产ESBL大肠埃希菌BSI的危险因素;韩国一项研究调查发现,30 d内使用β-内酰胺类抗菌药物是产ESBL肠杆菌科细菌BSI的危险因素[9];另一项研究发现,近3个月内使用第3代头孢菌素是产ESBL大肠埃希菌BSI的危险因素[10];我国一项前瞻性多中心研究结果显示,3个月内使用头孢菌素是产ESBL肠杆菌科细菌BSI的独立危险因素[5]。因此,对于发生BSI前2周内使用过头孢菌素类抗菌药物的大肠埃希菌和肺炎克雷伯菌BSI患者,需警惕其产ESBL菌株感染的可能,也提示临床应尽量减少不必要的头孢菌素类抗菌药物的使用。
多因素分析结果还显示,近2周内使用头孢菌素类抗菌药物/β-内酰胺酶抑制剂复方制剂为产ESBL大肠埃希菌和肺炎克雷伯菌BSI的独立危险因素(OR=4.884,95%CI=1.285~18.560,P=0.020)。有研究结果表明,哌拉西林他唑巴可通过其选择性压力增加肠杆菌科细菌产ESBL[11]。推测产ESBL大肠埃希菌和肺炎克雷伯菌的检出率升高可能与β-内酰胺酶抑制剂大量使用有关,建议临床严格把握β-内酰胺酶抑制剂的适应证,谨慎选择。
单因素分析结果显示,发生BSI前2周内使用糖皮质激素为产ESBL大肠埃希菌和肺炎克雷伯菌BSI的危险因素(OR=2.837,95%CI=1.458~5.522,P=0.002)。有文献报道,使用糖皮质激素或免疫抑制剂是住院患者粪便中检出产ESBL大肠杆菌的独立危险因素[12];韩国一项研究结果指出,产ESBL肠杆菌科细菌定植为社区产ESBL肠杆菌科细菌BSI的独立危险因素[9];日本一项研究结果显示,感染前使用免疫抑制剂或糖皮质激素和氟喹诺酮类抗菌药物是产ESBL大肠埃希菌BSI的独立危险因素[13]。糖皮质激素可能导致机体免疫功能降低,引起肠道细菌易位[14];产ESBL肠杆菌科细菌常在下消化道定植,这些定植的产ESBL肠杆菌科细菌易位可能导致产ESBL肠杆菌科细菌感染,如泌尿系感染、血流感染等[15]。本研究结果提示,近2周内使用糖皮质激素可能会增加产ESBL肠杆菌科细菌BSI的风险,一方面,对于2周内使用过糖皮质激素的患者,需警惕其产ESBL菌株感染的可能;另一方面,也提示临床应尽量减少不必要的糖皮质激素的使用。
本研究较其他研究增加了近2周内使用质子泵抑制剂的危险因素分析。单因素分析结果显示,近2周内使用质子泵抑制剂是产ESBL大肠埃希菌和肺炎克雷伯菌BSI的危险因素(OR=1.737,95%CI=1.073~2.810,P=0.025)。质子泵抑制剂可抑制胃酸分泌,使胃液pH升高,当胃液pH>3.8时,胃内细菌会过度生长[16];同时,质子泵抑制剂可破坏肠道微生物群,为外源性病原体定植肠道并引起感染提供了机会[17]。正是因为上述特点,质子泵抑制剂的使用与感染密切相关,并且有研究结果表明,使用质子泵抑制剂增加了感染相关的住院治疗(OR=1.66,95%CI=1.11~2.48,P<0.05)[18]。质子泵抑制剂与产ESBL肠杆菌科细菌直肠定植相关[19]。有研究结果显示,12个月内使用质子泵抑制剂是大肠埃希菌和肺炎克雷伯菌携带ESBL的独立危险因素(OR=1.84,95%CI=1.05~3.23,P<0.05)[20];而产ESBL细菌定植与产ESBL肠杆菌科细菌引起的BSI有关[21-22]。有文献报道,6个月内使用质子泵抑制剂是产ESBL肠杆菌科细菌引起感染的危险因素(OR=1.15,95%CI=0.68~1.95,P<0.05)[23]。质子泵抑制剂是否会增加产ESBL肠杆菌科细菌BSI的风险,目前鲜有研究。本研究中单因素分析结果提示,对于发生BSI前2周内使用质子泵抑制剂的患者,需警惕其产ESBL菌株感染的可能。
本研究主要的不足:一是本研究为观察性研究,报告回顾性分析的结果,尽管对其他混杂因素进行了多因素的逻辑分析以控制,但仍然可能存在未被调整的隐性偏倚;二是本研究的病例数有限,有些影响因素可评估的患者数有限,限制了多变量分析的能力。如果能够设计前瞻性多中心的研究,无疑会大大提高结论的准确性。
综上所述,对于大肠埃希菌感染、近3个月内有住院史、近2周内使用头孢菌素或头孢菌素类抗菌药物/β-内酰胺酶抑制剂复方制剂的BSI患者,应高度警惕产ESBL菌株感染的可能,及时制订适宜的抗感染方案;同时提示,应尽量减少不必要的质子泵抑制剂和糖皮质激素的使用。
