钽铌冶炼厂含氟废水资源化治理技术
2020-10-23杜璞欣宋卫锋周吉奎吕先谨
杜璞欣,宋卫锋,刘 勇,周吉奎,吕先谨
(1. 广东工业大学 环境科学与工程学院,广东 广州 510006;2. 广东省资源综合利用研究所,广东 广州 510650;3. 稀有金属分离与综合利用国家重点实验室,广东 广州 510650;4. 广东省矿产资源开发和综合利用重点实验室,广东 广州 510650)
钽铌行业在生产Ta2O5和Nb2O5的同时,也产生了大量的废水。其中,洗涤废水占钽铌冶炼厂废水总量的90%。该类废水主要含F-、SO42-、NH4+及少量NH3·H2O,而废水中F-和SO42-浓度低,不利于资源化利用。常规处理方法是采用石灰沉淀F-及SO42-,然后吹脱氨氮处理,但该方法产生的CaF和CaSO4混合废渣属于危险废物,不易处理;产生的低浓度氨水不利于工业应用;废水含Ca2+浓度高,易使脱氨塔结垢堵塞,且尾水难以回用。此外,该废水的总盐质量浓度为10~20 g/L,有较高的渗透压,直接蒸发浓缩成本高,也不适于常规反渗透浓缩。电渗析技术工艺简单、设备廉价、能耗小,在化工、冶金、医药、食品等行业的废水处理中得到广泛应用[1-3],也有关于地下水电渗析法脱氟的报道[4],而使用的离子交换膜多为异相膜或均相膜,有关合金膜脱氟的研究未见报道。
本研究采用合金膜电渗析法去除钽铌冶炼厂含氟废水中的F-,考察了膜面流速、膜对电压(每对膜施加的电压,V)、废水pH对F-去除率的影响,优化了运行参数,并在优化条件下探究了合金膜对F-和SO42-的分离机制,提出一条浓淡水资源化处理路线。
1 实验部分
1.1 废水水质
实验用废水取自某钽铌冶炼厂,水质见表1。
1.2 试剂和仪器
NH4F、(NH4)2SO4、氨水、Na2SO4、浓硫酸均为分析纯。

表1 废水水质
DDS-303A型电导率仪、E-201-C型复合电极、PHS-3C型台式酸度计、PXSJ-226型离子计:上海雷磁仪器有限公司;UV1800型紫外-可见光分光光度计:上海隽凯仪器设备有限公司;PANalytical EMPYREAN型X射线衍射仪、PANalytical AxiosmaxX射线荧光光谱仪:荷兰帕纳科X射线仪器公司;ICE 3300GF AA 型石墨炉原子吸收光谱仪、iCAP 7200型电感耦合等离子体发射光谱仪(ICP):赛默飞世尔科技公司。
1.3 实验装置
本实验使用KM-EDI-500L型电渗析器(广州凯膜过滤设备有限公司制造),膜堆由40对200 mm×400 mm的合金阴阳离子交换膜(杭州蓝然环境技术有限公司提供)交替排列构成,膜与膜之间用聚丙烯隔板隔开,阳离子交换膜为Ionsep-AMC磺酸基阳膜,阴离子交换膜为Ionsep-AMA季胺基阴膜,有效膜面积为2 m2。离子交换膜的性能参数见表2。
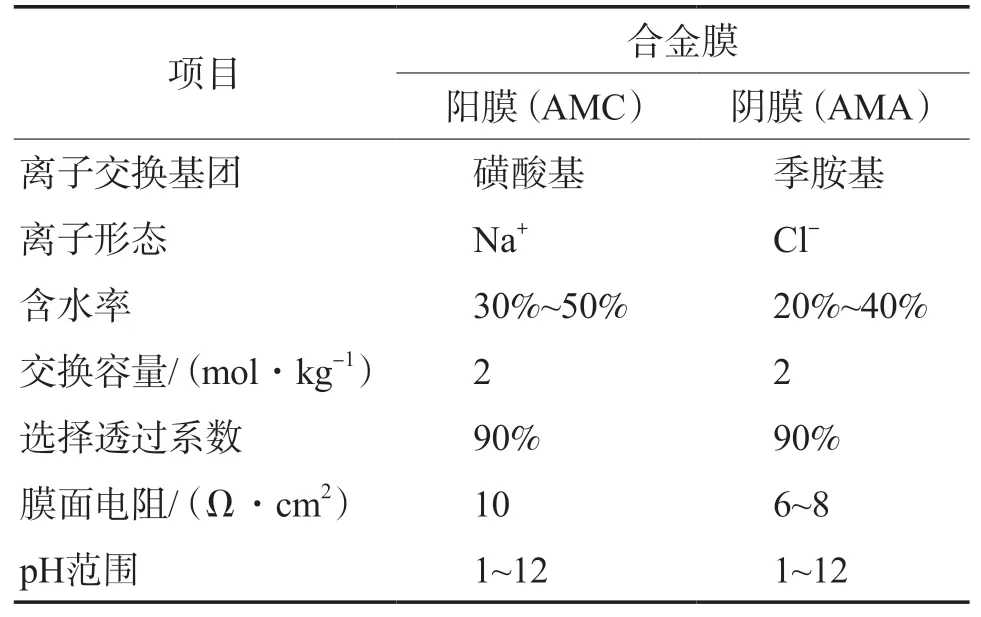
表2 离子交换膜的性能参数
1.4 电渗析器工作原理
电渗析器的工作原理见图1。废水进入浓室和淡室,极室内是Na2SO4溶液。电渗析器开始运行,在电场力的推动下,废水中的NH4+,F-,SO42-不断从淡室往浓室迁移,NH4+透过阳离子交换膜迁移,F-和SO42-则透过阴离子交换膜迁移,淡室中的NH4F和(NH4)2SO4含量会逐渐降低,电导率也相应下降,浓室中的盐浓度则不断增大,电导率增加。

图1 电渗析器工作原理
1.5 实验过程
向浓室和淡室中分别加入4 L废水,向极室加入4 L质量分数为2.4%的Na2SO4溶液。先调节浓室和淡室的循环流量,用废水在浓室和淡室中循环3~5 min至溶液电导率不再下降,更换废水,重复操作,直至循环时水箱中溶液电导率与原液电导率一致。调节极水流量,稳定运行1 min。调节膜对电压,保持电压不变,记录电压和电流值,每隔一段时间在淡室、浓室中取样测量F-,SO42-,NH4+的质量浓度。
1.6 分析方法
采用离子选择电极法测定废水的F-质量浓度[5];采用硫酸钡浊度法测定废水的SO42-质量浓度[21];采用ICP分析废水中主要离子浓度;采用蒸馏-硝酸钍容量法[21]测定LiF中F-的含量。
2 结果与讨论
2.1 膜面流速的确定
浓室、淡室内废水的循环流量决定了离子交换膜两侧的压力,两侧压力不一致导致溶液渗漏,因此实验控制浓室和淡室的废水循环流量相同。膜对电压设置为0.625 V,圆形膜直径为3.6 cm,将循环流量转换成膜面流速,膜面流速对F-去除率的影响见图2。由图2可见:膜面流速越大,F-去除率越高;但当膜面流速为4.91 cm/s时,转子流量计中有气泡进入,转子上下波动,无法稳定读数,且膜面流速过大会损坏膜堆,故选择膜面流速为4.09 cm/s。
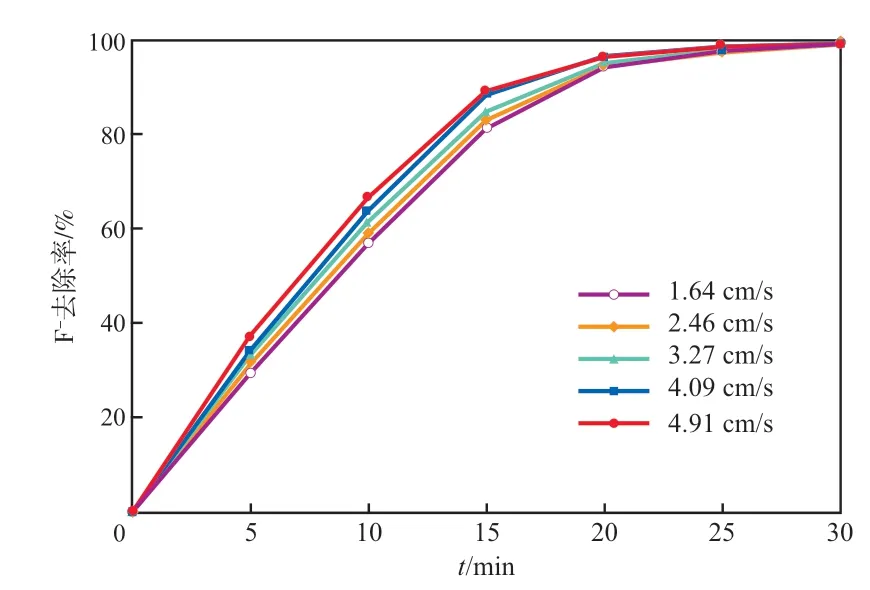
图2 膜面流速对F-去除率的影响
2.2 膜对电压的确定
2.2.1 膜对电压对F-去除率的影响
电场力是F-迁移的主要驱动力,但电压过高,离子迁移速率过快又会引起极化现象[6]。在膜面流速为4.09 cm/s的条件下,膜对电压对F-去除率的影响见图3。由图3可见:电渗析器开始运行后,淡水的F-不断往浓水中迁移,且随着反应时间的延长,F-迁移速率变缓;当膜对电压为0.250 V时,单位时间内通过膜的F-数量为定值,这是因为膜对电压较低时,溶液中F-的迁移速率较慢,并与膜面上F-的迁移速率相等;当膜对电压为0.500 V时,淡室内大量的F-透过离子交换膜快速迁移到浓室中,电渗析30 min后,淡水F-去除率达97.53%;但膜对电压越高,膜堆电阻和能耗越高。综合考虑,选择膜对电压为0.500 V。
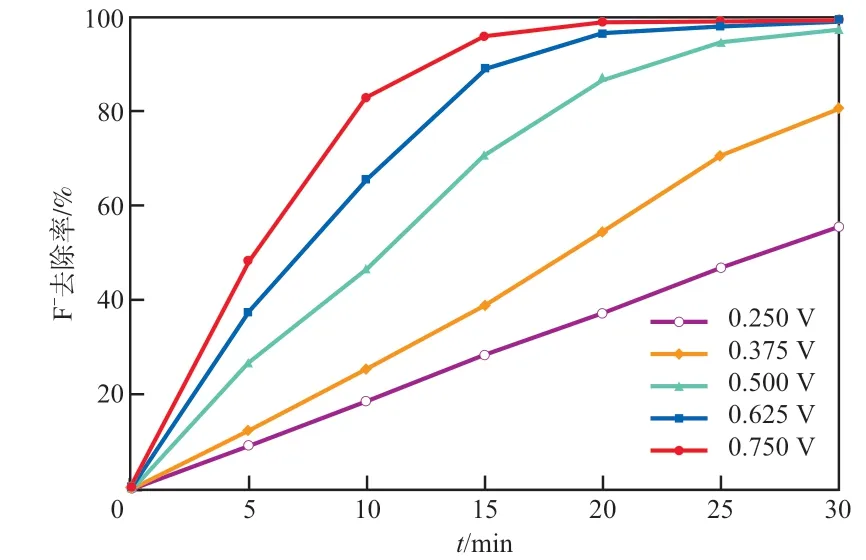
图3 膜对电压对F-去除率的影响
2.2.2 膜对电压对SO42-去除率的影响
在电渗析过程中,不同价态的离子均能与离子交换膜上的交换基团结合[7],观察不同膜对电压下SO42-的迁移状况能够间接反映出SO42-和F-在迁移过程中的相互作用。在膜面流速为4.09 cm/s的条件下,膜对电压对SO42-去除率的影响见图4。由图4可见:当膜对电压为0.500 V、电渗析30 min时,SO42-去除率接近100%,SO42-的去除率要高于F-。
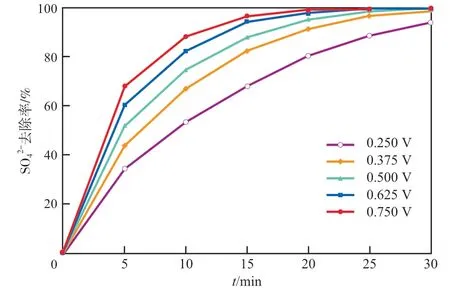
图4 膜对电压对SO42-去除率的影响
比较图3和图4可知,随着膜对电压的升高,该AMA季胺基阴膜对F-和 SO42-的去除效果有相似的变化趋势,说明离子浓度不高时,废水中的SO42-和F-的都能有效地和阴离子交换膜上的位点结合,参与离子传质过程,此时的位点数目大于离子数量,两种离子都能以一定的速率通过膜,竞争吸附作用[8]不明显。
2.3 合金膜对F-和SO42-的分离机制
离子交换膜对离子的选择透过性是膜的孔隙作用、静电作用和外力作用下的定向扩散的共同结果[9]。膜内带电荷的基团形成强烈电场,吸引反离子从水相转移至膜相,并在外加电场力的作用下定向迁移至另一侧。高价反离子因电荷数量多更容易被膜电场吸引到膜表面聚集,水合离子半径小的离子更容易进入膜内孔道中迁移。EISENMAN[10]指出:膜对离子的选择性是静电作用和去水化作用的共同结果,对于同价离子间的交换,水合离子半径大、水合自由能大的离子去水化作用弱,被水相选择;而水合离子半径小、水合自由能小的离子被膜相选择。在本实验中,F-的水合离子半径和水合自由能均小于SO42-,合金膜对F-的选择吸附量应该更高,但实验发现SO42-的去除率大于F-,为此提出如下假设:1)F-的渗析作用比SO42-显著;2)SO42-对F-的排斥作用降低了F-的迁移效率。
2.3.1 F-的渗析作用
由Donnan平衡理论可知,反离子迁移过程导致浓室积累大量的电解质,由于离子交换膜的选择透过性不是绝对的,浓室中已迁移过膜的反离子在渗析作用下会重新扩散回淡室,降低电渗析效率。在本实验中,F-水合离子半径小,在膜的孔道中迁移速率更快,较SO42-更易于迁移和扩散,故F-的反向通量更高,这部分扩散作用降低了F-去除率,使得F-去除效果不如SO42-。
为了证实假设1),在浓淡室废水均为4 L、膜对电压为0.500 V、膜面流速为4.09 cm/s的条件下处理废水30 min,然后将膜对电压调为0.125 V,继续运行30 min,整个废水处理过程中F-和SO42-质量浓度的变化情况见图5。由图5可见:运行前30 min,随运行时间延长淡室内的SO42-和F-质量浓度均明显下降;运行35 min时淡室内的SO42-和F-质量浓度略有增加,之后表现出完全相反的趋势;运行35~60 min,F-质量浓度由372.3 mg/L逐渐升高至700.5 mg/L,而SO42-质量浓度则由186.87 mg/L缓步下降至54.33 mg/L。说明35~60 min时,尽管反离子迁移过程仍在推动淡室F-往浓室迁移,但由于渗析引起的反向扩散使淡室F-质量浓度逐渐增大,此时F-的传质过程以浓差扩散为主;而SO42-则反之,这证实了F-的渗析作用强于SO42-。
尽管渗析作用“弱化”F-的正向迁移过程,但这绝对不足以说明F-的迁移量低于SO42-的原因就是由于F-渗析作用。因为在电渗析初始5 min,浓淡室还未形成较大浓度差时,渗析作用较弱,F-扩散通量低,F-和SO42-迁移以正向迁移为主,但图3和图4结果显示,反应前5 min SO42-去除率已然高于F-,渗析作用显然不能完全解释合金膜对SO42-的更高选择性。

图5 F-和SO42-质量浓度的变化情况
2.3.2 SO42-对F-的排斥作用
F-的迁移过程受到SO42-浓度影响较大,而SO42-受到F-的影响较小,故当交换容量较高的合金膜的膜内基团同时吸引二者到达膜面上时,由于界面分配和去水化作用的影响,膜面上的F-数量比SO42-数量多,多出的F-会接触到属于SO42-的膜基团,由于二者都是反离子,且SO42-携带的电荷数量高于F-,同种电荷相斥,SO42-会对这部分F-产生强烈的排斥作用,因此降低了F-的整体迁移速率。
为了验证F-的迁移速率下降是受到SO42-的影响,实验配制了与原废水F-质量浓度相同的NH4F溶液,并用氨水调节至原废水pH,在膜对电压为0.500 V、膜面流速为4.09 cm/s的条件下处理NH4F溶液30 min,NH4F溶液和废水中F-去除率的比较见图6。

图6 NH4F溶液和废水中F-去除率的比较
由图6可见,废水中F-的去除率始终低于NH4F溶液中F-的去除率,证实了SO42-对F-的排斥作用降低了F-的迁移效率。
2.4 废水pH对F-去除率的影响
废水pH影响离子在溶液中的电离程度和存在形式。F-在pH<3.45的条件下多以HF或H2F+的形式存在,不能通过阴离子交换膜[11],但可以由阳离子交换膜迁移到浓室。而在碱性条件下,pH越高,OH-对吸附位点的竞争能力越强,离子交换膜对F-的吸附能力越弱[12],导致F-去除率越低。在膜对电压为0.500 V、膜面流速为4.09 cm/s的条件下,废水pH对F-去除率的影响见图7。由图7可见,废水pH越高,F-去除率越低,但整体上影响不大,故无需调节废水pH。
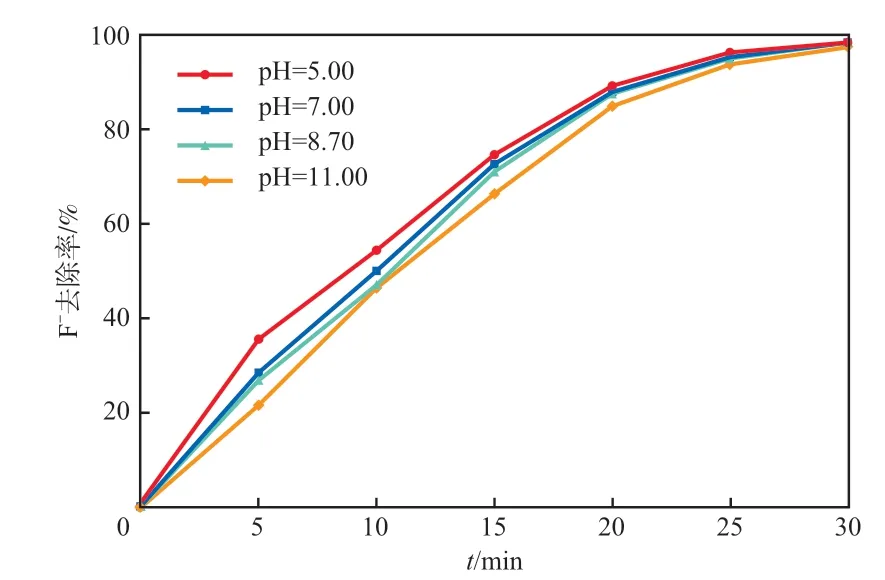
图7 废水pH对F-去除率的影响
2.5 极限电流密度
电渗析极化会导致膜面结垢,不利于电渗析脱盐。极限电流密度是电渗析发生极化现象时的电流密度值。采用电流-电压法测定电渗析处理废水的电流密度,具体方法是在浓淡室各加入4 L废水,极液为4 L Na2SO4溶液,保持膜面流速为4.09 cm/s,逐步增大膜对电压,同时记录下对应的电流值,得到I-U曲线,见图8。由图8可见:当膜对电压较小时,电流密度随着电压的增大呈线性增加;当膜对电压大于0.875 V后,电流密度恒定不变,此时发生电渗析极化,故该电渗析器在膜面流速为4.09 cm/s时处理废水的极限电流密度为0.315 mA/cm2,极限膜对电压为0.875 V。
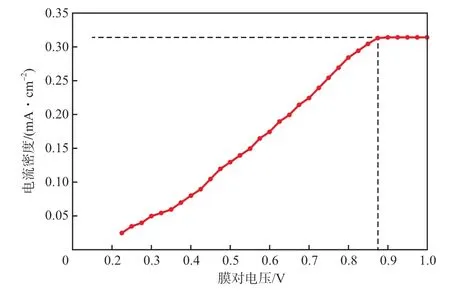
图8 电渗析处理废水的I-U曲线
2.6 电渗析循环稳定性
在膜对电压为0.500 V、膜面流速为4.09 cm/s的条件下运行电渗析器,浓室和淡室的废水体积均为4 L,以30 min为一个周期进行循环实验,每个周期结束时将浓淡室内废水更换为初始废水,记录每个周期结束时淡室和浓室的F-质量浓度及水迁移体积,计算膜通量,电渗析循环实验结果见表3。
由表3可见,随着循环次数的增多,合金膜对F-的去除率略有下降,水迁移体积略有减小,这是由于合金膜结垢量增加的缘故。膜通量略有下降,但整体影响不大,证明合金膜处理钽铌冶炼厂含氟废水有较大潜力。
3 尾水处理
二级电渗析回收废水中氟的工艺流程见图9。

图9 二级电渗析回收废水中氟的工艺流程
在优化条件下一段电渗析30 min后的淡水水质见表4。由表4可见,经过一段电渗析,淡水中大部分的F-和SO42-均被去除,仅剩1.64 g/L的氨氮,这部分氨氮主要是游离氨。这部分淡水可作为稀氨水直接回用到沉淀洗涤车间。
一段电渗析的浓水经多段电渗析(膜对电压0.500 V下电渗析80 min+膜对电压0.875 V下电渗析40 min)处理后的二级浓水的水质见表5。由表5可见,二级浓水为高含盐废水[13]。工业上对于高含盐废水,通常的处理方法是蒸发浓缩制盐,但二级浓水中高浓度的F-会影响产品(NH4)2SO4的纯度。
考虑到LiF的广泛工业应用空间及新能源行业对LiF日益增长的需求[14-16],在蒸发浓缩处理二级浓水之前加入LiOH·H2O来合成LiF[17-20]。取400 mL二级浓水,在水浴锅中加热至90 ℃,转速为130 r/min,按照n(Li+)∶n(F-)=1∶1.05 的比例缓慢加入LiOH·H2O,充分反应8 h。反应结束后,过滤,多次洗涤,烘干,称量,得到LiF产品。分别检测滤液和洗涤水中的F-浓度,经计算,F-沉淀率为94.45%,LiF收率为84.92%,F-整体回收率为79.45%。LiF产品中的主要化学成分见表6,可见LiF产品杂质较少,纯度达99.06%,符合GB/T 22666—2008标准[21]的3级品要求。
LiF产品的XRD谱图见图10。

表4 淡水水质

表5 二级浓水的水质

表6 LiF产品中的主要化学成分 w,%
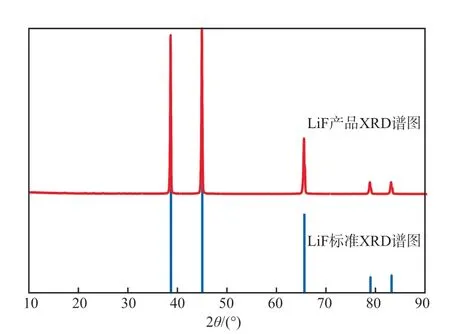
图10 LiF产品的XRD谱图
由图10可知,LiF产品的各个峰与标准LiF的峰较为吻合,杂峰很少,证明得到的产品LiF纯度高,结晶效果好。
4 结论
a)采用合金膜电渗析法脱除钽铌冶炼厂含氟废水中的F-和SO42-,最优的工艺运行条件为:膜对电压0.500 V,膜面流速4.09 cm/s。在此条件下电渗析30 min,F-去除率达97.53%,SO42-去除率接近100%。
b)经证实,F-的渗析作用比SO42-显著,SO42-对F-的排斥作用降低了F-的迁移效率,因此电渗析的SO42-的去除率高于F-。
c)合金膜电渗析的膜面流速为4.09 cm/s时,处理废水的极限电流密度为0.315 mA/cm2,极限膜对电压为0.875 V。
d)优化条件下运行电渗析器,一段淡水中大部分的F-和SO42-均被去除,可以直接回用。一段电渗析的浓水再经多段电渗析后的二级浓水,以LiOH·H2O沉淀F-得到LiF产品,该LiF产品纯度达99.06%,满足GB/T 22666—2008标准的3级品要求,LiF收率为84.92%,F-整体回收率为79.45%。
