叠氮胶粘剂3,3'-双(叠氮甲基环氧丁烷)四氢呋喃共聚醚的炔基固化反应研究*
2020-10-22于倩倩乔宗文
于倩倩,乔宗文
(陕西国防工业职业技术学院,陕西 西安 710300)
引 言
胶粘剂在推进剂配方中起到骨架和基体的作用,是维持复合固体推进剂完整性和良好力学性能的重要组分。在不影响推进剂配方的综合性能的前提下使用含能胶粘剂一直是复合推进剂重要的发展方向之一[1]。在含能胶粘剂中,叠氮胶粘剂具有放热量大、分解时不需要消耗氧和分解产物相对分子质量低等诸多优势,叠氮类含能胶粘剂在与贫氧的黑索金(RDX)、奥克托今(HMX)组合使用时可以获得良好的性能[2]。此外,叠氮胶粘剂与硝酸酯类增塑剂也具有良好的相容性,可以通过硝酸酯增塑剂赋予配方体系更高的能量。叠氮类含能胶粘剂主要有聚叠氮缩水甘油醚(GAP)、3,3'- 双叠氮甲基环氧丁烷(BAMO)的均聚物及共聚物等[3,4]。
叠氮胶粘剂BAMO-THF 共聚醚由于四氢呋喃嵌段的引入较BAMO 均聚物具有更低的玻璃化温度以及更为优异的力学性能,受到固体推进剂、气体发生器和高能炸药领域研究者的广泛关注,被认为是未来最具应用前景的含能胶粘剂[5]。由于传统的异氰酸酯固化技术存在对水分敏感、与高能氧化剂ADN 相容性差等固有的缺点,近年来叠氮胶粘剂的炔基固化技术得到了大量的研究,国内外的研究主要围绕着叠氮胶粘剂GAP 开展。例如德国ICT 研究所的Keicher、韩国国防发展局的Min、印度的Reshmi 和国内武汉理工大学的黄进课题组均采用商品化的GAP 与不同结构的双炔化合物进行反应成功制备了三唑交联弹性体[7~10]。然而关于BAMO
THF 共聚醚的炔基固化反应研究还未见文献报道。
本文采用低熔点的双炔化合物环己烷二甲酸丙炔醇酯(BPHA)与叠氮胶粘剂BAMO-THF 共聚醚进行了三唑交联弹性体的制备,重点研究了叠氮胶粘剂BAMO-THF 与BPHA 组成的固化体系的固化反应特性。
1 实验部分
1.1 试剂与仪器
环己烷二甲酸,丙炔醇,对甲苯磺酸,甲苯,阿拉丁试剂,以上试剂均为分析纯。3,3’- 双(叠氮甲基环氧丁烷)四氢呋喃共聚醚(BAMO-THF),二官能度,羟值0.398mmol·g-1,黎明化工研究院生产。
红外光谱:美国Nicolet 公司Bruker TENSOR27型傅立叶变换红外光谱仪,样品量约0.7mg,粉碎成粉末状,加入干燥研细的溴化钾粉末150mg,充分研磨后压片进行红外光谱测试;核磁共振:瑞士Bruker 公司 AV500 型(500MHz)超导核磁共振仪;元素分析:德国Exementar 公司VARI-EL-3 型元素分析仪;STA 449C 型热质(TG-MS)联用仪,德国 NETZSCH 公司。
1.2 实验过程
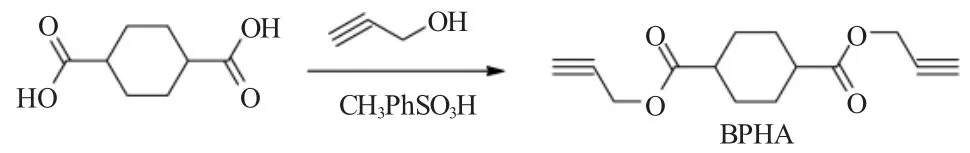
1.2.1 环己烷二甲酸丙炔醇酯(BPHA)的合成
在装有分水器的反应瓶中加入34.4g(0.2mol)环己烷二甲酸,56g(1mol)丙炔醇、1.72g(0.01mol)对甲苯磺酸和150mL 甲苯。升温至回流反应12h,反应生成的水被甲苯带入分水器中。反应结束后,反应液自然冷却到室温,用5%质量比的碳酸钠溶液洗涤两次,每次100mL,后去离子水洗至中性。经无水硫酸钠干燥后,浓缩得到淡黄色块状固体,乙醇重结晶得到32g 白色固体,收率64.5%。1H NMR(DMSO-d6, 500MHz):δ=4.69 (d, 4H, J=2.50Hz), 3.51(t,2H,J=2.50 Hz),2.56(m,2H),1.71(m,8H);13C NMR(DMSO-d6,125MHz):δ=174.0,79.0,77.9,52.1,40.0,25.8;IR(KBr,cm-1):ν=3265,2934,2126,1731,1449,1038, 996, 679; Calc. for C14H16O4: C 67.73, H 6.50;Found:C 67.69,H 6.52.熔点,36.4℃。
1.2.2 三唑交联弹性体的制备
将叠氮胶粘剂BAMO-THF 共聚物与固化剂BPHA 加入单口烧瓶,升温至40℃混合均匀。所得黏稠液体在旋转蒸发仪上除气后浇于约2mm 厚的聚四氟乙烯模具中。流平后于水浴烘箱中60℃固化7d,取出进行相应的性能测试。为了考察不同的固化剂含量对弹性体性能的影响,采用不同的固化剂含量制备了系列的聚三唑弹性体。将炔基的物质的量与羟基的物质的量之比定义为R 值用来计量体系中叠氮胶粘剂及固化剂的量。
1.2.3 固化反应动力学研究
采用实时红外光谱法研究固化反应的反应动力学。炔基和叠氮基的固化反应在红外谱图上表现为叠氮基和炔基峰强度的降低以及三唑环特征吸收峰的不断增强,然而体系中叠氮基的物质的量相对于炔基大大过量,叠氮基的消耗变得不明显,而炔基的吸收峰由于附近水峰的干扰也不适合作为研究反应动力学的定量基团。固化反应所生成的三唑环上sp2杂化的C-H 伸缩振动在红外上具有特定的吸收(3146cm-1),虽然其强度弱,但是其不受其他峰的干扰,因此固化反应行为的研究可通过研究特定温度下3146cm-1处峰的强度随时间的变化进行。将叠氮胶粘剂和固化剂BPHA 混合均匀(R=2),取少量液体涂在溴化钾晶片上,置于设定温度进行固化,采用Bruker TENSOR27 红外光谱仪监测固化反应进程,每间隔一段时间取出测试。随着固化反应的进行,3146cm-1处吸收峰的强度不断增加,而1733cm-1对应的C=O 伸缩振动保持不变。反应混合物为液体,在KBr 压片之间具有一定的流动性,不同的测试时刻测量浓度会有一定的偏差,而吸光度与反应物的浓度有关,因此采用3146cm-1对1733cm-1的相对强度变化来评价固化反应速率以确保不受样品浓度及厚度的影响。固化反应转化率可以通过公式计算得到,其中AC-H和AC=O分别为sp2杂化的C-H 伸缩振动和C=O 伸缩振动峰的峰面积。
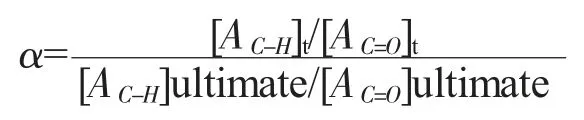
2 结果与讨论
2.1 三唑交联弹性体的结构表征
叠氮基和炔基参与的固化反应生成三唑交联的网络结构,采用红外对其结构进行了表征。图1 为叠氮胶粘剂BAMO-THF 共聚物和BPHA 固化反应前后的红外谱图对比。从图中可以发现,3303cm-1处炔基峰完全消失表明固化反应完全,而过量叠氮基的吸收峰出现在2098cm-1。此外,三唑环上sp2杂环CH 的伸缩振动峰出现在了3146cm-1, 表明三唑交联点的生成。由于三唑交联点在整个弹性体中的质量分数较低,三唑环上CH 的伸缩振动峰强度很弱。其余的吸收峰在固化反应前后并无明显变化,说明叠氮基和炔基参与的固化反应没有副产物的生成。
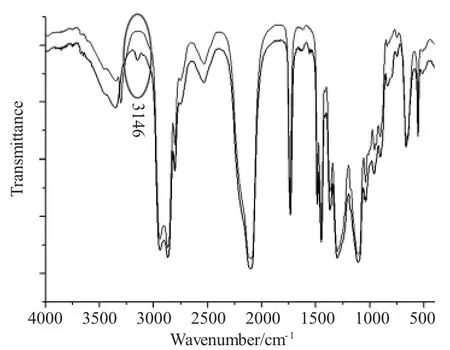
图1 BAMO-THF 共聚物固化前后的红外光谱Fig.1 The infrared spectrum of BAMO-THF copolymer before and after curing
2.2 聚三唑胶粘剂体系的固化反应特性

图2 BAMO-THF 共聚物与BPHA 在不同温度下的固化反应转化率和反应时间的关系Fig.2 The relationship between conversion rate and reaction time of curing reaction between BAMO-THF copolymer and BPHA at different temperatures
叠氮胶粘剂BAMO-THF 共聚物与BPHA 在不同温度下的固化反应转化率和反应时间的关系如图2 所示,反应刚开始时曲线斜率大,反应进行到一定时间后慢慢变小,且通过对比不同固化温度下的曲线可以看到固化反应速度对反应温度存在严重的依存关系。BAMO-THF 共聚物与BPHA 的固化反应,在50、60 和70℃下达到85%的转化率所需的固化时间分别为6h、3.5h 和1.25h。李娜等[11]采用微量热法研究了叠氮胶粘剂炔基固化的反应动力学,发现其反应级数接近于1。将-ln(1-α)对时间t作图,在转化率0%~90%的范围内呈现出非常好的线性关系,进一步证实了该反应符合一级反应动力学模型,与李娜等人的研究结果相吻合。
固化体系在不同温度下的-ln(1-α)-t 关系图如图3 所示,拟合所得直线的斜率即为给定温度下的总反应速率常数。将不同温度下的反应速率常数带入阿伦尼乌斯公式(1)中可以进一步求得固化反应的表观反应活化能Ea以及指前因子A,其中T 为热力学温度,R 为气体常数[12]。将计算得到的表观反应活化能Ea以及指前因子A 代入公式(2)中可以得到固化反应动力学方程。固化反应的动力学三因子如表1 中所示。
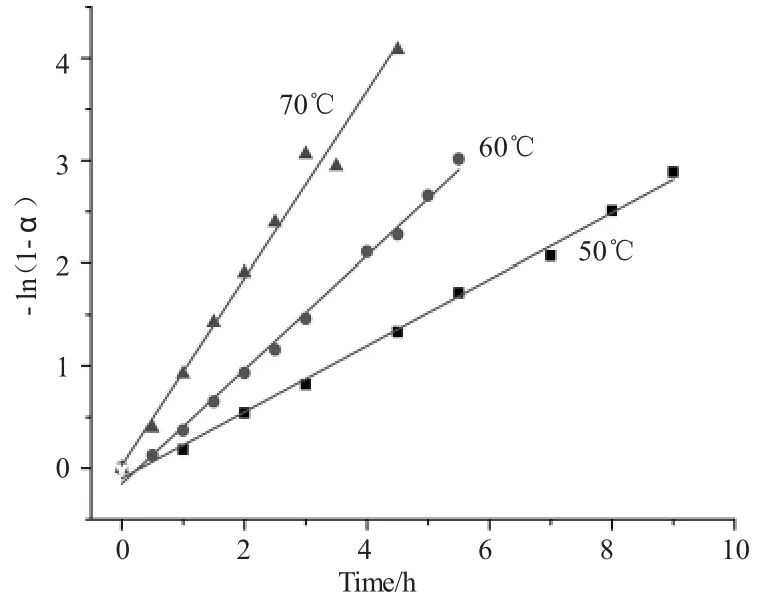
图3 固化体系在不同温度下的-ln(1-α)-t 关系图Fig.3 The diagram of - ln(1-α)- t relationship of curing system at different temperatures


表1 叠氮胶粘剂BAMO-THF 共聚物与BPHA 固化反应的动力学三因子Table 1 The three factors of kinetics of curing reaction between BAMO-THF copolymer and BPHA
3 结 论
(1)通过点击化学反应制备了基于叠氮胶粘剂BAMO-THF 共聚物的三唑交联弹性体,红外谱图中3146cm-1的吸收峰证实了三唑交联点的生成;
(2)通过实时红外法研究了叠氮胶粘剂BAMOTHF 与BPHA 反应的固化反应动力学,获得了其活化能、指前因子和动力学方程为84.5kJ·mol-1,6.1×1012s-1和 dα/dt=6.1×1012exp(10164/T)(1-α)。
