光催化材料去除水中病毒的研究进展
2020-10-20王佳豪李家成许锴林子增王郑
王佳豪,李家成,许锴,林子增,王郑
(南京林业大学土木工程学院,江苏南京210037)
2020 年席卷全球的新型冠状病毒引发的病毒性肺炎已被认定为一种大流行病,目前疫情依然在全世界范围蔓延。病毒对人类的健康安全构成严重威胁,水中病原微生物引起的传染病事件也屡见不鲜。根据世界卫生组织(WHO)统计,全球近20亿人口正在饮用受粪便污染的水源[1],面临着感染霍乱、痢疾、伤寒、脊髓灰质炎等水传播疾病的风险。病毒较细菌体积更小,感染的剂量低传染性却很强,在水环境中难以检测及去除。国内外专家针对水中致病菌的研究较多,而病毒的结构、抗性以及失活机制与细菌有很大不同,近年来对病毒的研究也越来越受到相关人员的重视。WHO 将肠道病毒、甲肝病毒、戊肝病毒、轮状病毒、诺如病毒等界定为饮用水中健康风险高的病毒,腺病毒和星状病毒的健康风险为适中。噬菌体是一类专以细菌为宿主的病毒,由于其结构、抗性与人类致病病毒类似,易于实验操作且对人类无致病性,故被广泛应用于水中病毒指示物,其中噬菌体MS2 是最受欢迎的替代物[2]。
美国环保局(USEPA)饮用水水质标准中对病毒指标进行了严格的限定,要求病毒的灭活率不低于4log(即99.99%)[3]。我国现行《生活饮用水卫生标准》(GB5749—2006)对病毒的最高允许浓度没有明确限定,而是通过浊度等指标确保饮用水水质的安全。然而,常规水处理消毒工艺(氯化、臭氧、紫外线消毒等) 完全去除病毒是非常困难的[4]。
光催化法作为绿色高效的消毒技术,克服了传统消毒方法的局限性,逐渐被应用于水中病原体的去除,越来越多研究人员致力于开发更加高效且低成本的光催化材料。如前所述,水中病毒和细菌的去除不能一概而论,故本文综述了近年来国内外学者对于光催化材料应用于去除水中病毒的研究进展,介绍了光催化技术的原理及优势,并指出未来光催化材料的发展趋势,为未来光催化消毒技术的发展提供借鉴。
1 光催化技术的原理及优势
1.1 光催化的氧化和杀毒机理
光催化技术最主要的消毒机制是通过光催化剂产生的活性氧物种(ROS)实现对病毒的灭活。其原理是通过光激发TiO2、ZnO等半导体材料产生电子(e-)-空穴(h+)对,并分离迁移至半导体表面进而引发一系列氧化还原反应:光生电子与水中溶解氧反应生成O·-2;O·-2可进一步与H+生成·OOH 和H2O2;空穴本身具有氧化性,其与H2O 或OH-生成·OH。这些具有强氧化性的ROS,如O·-2、·OOH、H2O2和·OH 等可以分解破坏病毒的蛋白质和遗传物质,从而灭活水中病毒。其中,O·-2和·OH 在光催化灭活病毒过程中起到主要作用。TiO2光催化原理如图1。
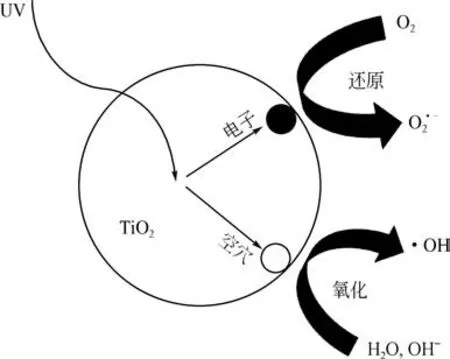
图1 TiO2光催化原理
对于细菌等微生物的灭活,可以通过·OH 等强氧化性自由基破坏细胞壁、细胞膜以及细胞质等物质,对细菌的多种生命结构破坏,导致其死亡[5]。然而,病毒与细菌结构形态不同,主要由蛋白质衣壳和遗传物质(DNA 或RNA)组成;代谢过程也相差很大,病毒没有独立的代谢活性,只能利用位于蛋白质外壳中的结合位点将自身附着于宿主,并将其遗传物质注入细胞的细胞质中,然后利用宿主细胞的机制进行繁殖进一步感染。因此对病毒的光催化灭活不能简单从蛋白质的氧化损伤确定病毒死亡,因为它们具有在适当条件下自我修复和再生的能力,必须破坏其遗传物质,从基因的角度彻底杀死病毒[6]。
1.2 光催化的优势
国内外水厂现行消毒工艺虽能一定程度上去除病毒,然而依旧存在不足。氯消毒应用广泛,游离氯在水中生成的次氯酸对病毒蛋白质外壳损伤较大,足够高的剂量还可以破坏核酸,通过增加剂量或延长接触时间,即提高CT 值便可有效提高灭活效果。臭氧作为强氧化剂也具有杀菌消毒作用,在去离子体水中,当初始投加氯浓度1mg/L或臭氧浓度0.25mg/L 时,即能有效灭活MS2 噬菌体,达到USPEA 饮用水标准的4log(99.99%),实际在组合工艺中,臭氧和氯还能起到协同作用,增强对病毒的灭活效果[7]。Xue等[8]研究发现ClO2对人体轮状病毒(HRV)的消毒效果优于氯;荷兰Berenplaat 水厂在实际的研究中发现,二氧化氯发挥着灭活人体腺病毒的主要作用[9]。然而这些消毒法的缺陷就是会产生对人类健康危害极大的消毒副产物(disinfection byproducts,DBPs)[10],紫外线消毒虽无副产物生成,但不能持续消毒,且部分病毒对紫外线有一定抗性(如腺病毒、噬菌体MS2[11]等),因此研究出多色紫外光(双波长UV-C 发光二极管)通过增强破坏病毒蛋白质来提高灭活率[12-13],但却增加了更多的运行和维护成本。
传统消毒法的局限性使得开发出高效、绿色安全且低成本的消毒技术成为当今迫切解决的问题。光催化氧化作为一种环境友好型新消毒技术逐渐引起人们重视:其一,操作简单、反应条件温和且能耗低;其二,氧化能力强、成本低廉、无毒无害;其三,半导体催化剂在光辐照下的稳定性和耐久性以及高结晶度和高表面积使得这一消毒技术越来越受到研究者的青睐。
2 光催化材料
光催化作为一种新型的消毒技术,由于其具有利用太阳光的潜力而吸引了许多研究人员的关注。对于光催化材料的研究则是这项技术的关键,迄今为止已经开发了许多类型的半导体材料,如ZnO、TiO2、WO3等应用于有机污染物的降解和消毒等领域[14]。学者们一直致力于开发出高效稳定的光催化剂,通过对半导体材料的改性,提高太阳能的利用率使其催化效率增强,进一步提高对病毒等微生物的灭活能力一直是光催化技术的研究热点。TiO2光催化剂由于其良好的催化性能、经济性以及稳定性,是消毒灭菌领域应用最为广泛的光催化材料之一,已有大量研究报道围绕着TiO2光催化剂及其改性展开。此外,近年来学者发现对于不含TiO2的新型光催化剂的研究同样具有广阔的发展前景。因此,本文主要从TiO2及TiO2基光催化剂和不含TiO2的光催化剂两部分对光催化材料进行全面的综述。
2.1 TiO2及TiO2基光催化剂
TiO2是一种n型半导体,作为光催化剂的研究已有近百年历史[15],TiO2在自然界中有三种晶体结构:金红石型、锐钛矿型和板钛矿型。锐钛矿的禁带宽度为3.23eV (388nm),金红石为3.02eV(413nm),这两种结构具有较高的催化活性,锐钛矿型活性最佳。目前普遍使用的是市场上德国Degussa公司生产的P-25型TiO2(约80%的锐钛矿与20%的金红石)[16]。然而TiO2应用于光催化领域仍受到两个主要因素的限制:①由于TiO2的禁带较宽,只能吸收太阳光谱中4%左右波长较短的紫外光,无法有效利用太阳能;②其光生电荷和空穴复合率高,由光激发的电子和空穴在迁移至材料表面前易重组。因此,通过缩小半导体带隙或抑制光生电子/空穴的复合成为提高TiO2催化效率的关键。对TiO2的改性有许多方法,目前用于去除水中病毒的光催化剂改性主要研究集中在金属离子掺杂、非金属元素掺杂、多元共掺杂和复合半导体材料上。
2.1.1 金属离子掺杂
金属,尤其是贵金属(Au、Ag、Pt 或Pd 等)由于其独特的电子结构和光学性质,被广泛用于半导体催化剂的改性。金属离子的掺杂会改变TiO2的晶体结构和电子结构,从而提高光催化活性。一方面金属掺入TiO2的晶格后,导致其内部结构发生变化,产生可以使光生电子和空穴有效分离的局域电场;另一方面,金属掺入后在TiO2的带隙间产生杂质能级,成为捕获光生电子的陷阱,从而降低电子-空穴复合率,同时由于这些杂质能级的存在,降低了TiO2价带中的电子跃迁到导带所需的激发能量,使TiO2的吸收光谱扩展至可见光区,大大提高了TiO2对太阳光的利用率[17]。
Saran等[18]通过溶胶凝胶法制备Ag掺杂的TiO2,实验表明与纯TiO2和直接光解法相比,银离子的掺杂显著提高了所有微生物的灭活率。TiO2掺杂Ag后吸收光谱扩展至可见光区域,并且通过降低电子-空穴对的复合增加了ROS的生成。实验2h内完成了对屋顶收集雨水的消毒,结果显示在掺Ag 和纯TiO2固定光反应器中分别在太阳照射45min 和60min时,观察到MS2噬菌体的完全失活,这表明掺杂银离子相对提高了光催化失活效率。其中表现出的灭活效率依次为:大肠杆菌>MS2 噬菌体>黑曲霉。值得一提的是,2h 后释放的Ag 离子的总浓度约为0.009mg/L,远低于环境保护机构规定的允许标准水平0.1mg/L。Zheng等[19]采用静电纺丝法制备了一维Cu-TiO2纳米纤维用于噬菌体f2 的去除。在最佳掺杂比为n(Cu)∶n(Ti)=1∶8 和煅烧温度为450℃下,初始浓度为105PFU/mL 的f2 被50mg/L 的Cu-TiO2纳米纤维在可见光照射4h后完全灭活。其课题组随后的实验研究表明,噬菌体f2 的去除效率随着催化剂用量、光强度和温度的增加而增加,但随着初始病毒浓度和HA浓度的增加而降低。在酸性条件下,光催化剂和病毒之间的静电力得以增强,从而提高了病毒灭活效率[20-21]。
2.1.2 非金属元素掺杂
非金属元素(C、N、S等)的掺入使得TiO2价带宽化上移,禁带宽度相应减小,吸收光谱扩展至可见光区,即提高光催化活性。目前对N掺杂的研究较多,Asahi 等[22]研究表明,氮掺杂TiO2后在可见光下的光吸收和光催化活性均明显高于TiO2。为了解决阴离子掺杂后载流子复合问题,Li等[23]通过溶胶-凝胶法在介孔活性炭纤维模板上合成了钯改性的氮掺杂二氧化钛(TiON/PdO)光催化纤维,用可见光(波长大于400nm,平均强度为40mW/cm2)照射1h,通过结合黑暗条件吸附处理和可见光催化,噬菌体MS2 去除率达到99.75%~99.94%。Horovitz 等[24]通过溶胶凝胶法在200nm 孔径的氧化铝膜上制备了N 掺杂TiO2涂层光催化膜(PMR),研究了不同水质下其对噬菌体MS2 的去除效果。结果表明,制备的PMR 对MS2 的灭活具有很高的效率,碱性水的pH 通过静电排斥引起的病毒与催化剂的相互作用抑制了光催化消毒;NOM 对光催化失活表现出最显著的抑制作用;静电相互作用影响着地表水中的病毒灭活,然而当与光催化灭活结合时,病毒去除率达到大于99.99%。
2.1.3 多元共掺杂
多元共掺杂是指将两种及两种以上金属或非金属元素掺杂复合到半导体催化剂上对其改性,使光催化性能增强。Choi等[25]通过溶胶凝胶法制备了一种新型的可见光诱导光催化剂:基于几种掺杂过渡金属(铁、镁和锰)的TiO2对流感病毒H1N1进行灭活,结果表明在可见光条件下照射30min,对H1N1 的灭活率可达到99%。Venieri 等[26]利用共沉淀法制备了Mn、Co 和二元Mn/Co 掺杂的TiO2催化剂,在模拟和自然光照射下灭活污水样品中的MS2噬菌体。二元掺杂的催化剂在所有情况下均表现出最佳的光催化活性,不到20min 灭活率即达到99.9%,这表明复合掺杂剂诱导协同效应的作用。不同掺杂剂浓度对灭活率有一定的影响,最高的掺杂水平并不一定导致噬菌体完全或快速失活。
2.1.4 染料敏化
光敏剂吸附在半导体的表面上,吸收可见光后形成激发态,将电子有效地转移至半导体的导带上从而激活光催化,染料敏化能将半导体对光的吸收拓宽至可见光范围[27]。金属钌络合物染料稳定且激发态活性高,Mac Mahon 等[28]在连续流系统中利用Ru(bpy)3Cl2、TiO2、ZnO 和它们的组合作光催化剂分别对水中大肠杆菌和噬菌体MS2、ΦX174、PR772 进行光催化灭活。实验发现MS2 是Ru(bpy)3Cl2和TiO2光催化处理最敏感的噬菌体,引入Ru(bpy)3Cl2可以明显提高PR772和ΦX174的失活率,并导致在灭活的前15min 内将MS2 完全去除。Ru(bpy)3Cl2的存在显著改善了ZnO 和TiO2的性能,并且Ru(bpy)3Cl2和TiO2的组合比Ru(bpy)3Cl2和ZnO的效率更高。然而在组合试验中,钌络合物生成单线态氧和催化剂生成·OH 之间可能会形成对光子的竞争,影响光催化效率。因此对半导体进行染料敏化的改性仍需进一步研究。
2.1.5 复合半导体材料
半导体的复合材料分为两种:半导体与半导体复合是将另一种禁带宽度小、导带位置高的半导体与TiO2复合(如CdS-TiO2等),改变电子的转移,减小电子-空穴复合率;半导体与绝缘体复合利用绝缘体发达的孔结构和比表面积,增加自由基等与病毒的碰撞概率,从而提高催化率[29]。目前复合半导体材料对水中病毒的去除研究偏向于利用绝缘体与TiO2的复合。Liga 等[30]提出了将SiO2纳米粒子对TiO2进行改性的方法,尽管SiO2改性稍微减少了·OH 的产生,但是由于吸附密度的增强,复合SiO2-TiO2纳米材料对噬菌体MS2 灭活率有显著提高(比未改性的TiO2高出270%)。Langmuir吸附等温线表明,用5%SiO2改性的TiO2的最大吸附密度是未改性的37倍。Monmaturapoj等[31]采用固相反应法制备了羟基磷灰石与TiO2的复合材料(HA/TiO2),研究其对H1N1流感病毒的灭活效果。结果表明,在0.5mg/mL下,复合物对H1N1有很强的抗病毒活性,在紫外线照射60min下,病毒灭活率最高(超过2log/h)。这两种方法利用提高对病毒的吸附能力来增强光催化剂灭活能力,是一种简单、廉价且绿色的方法。
2.2 不含TiO2的光催化材料
目前,对于TiO2的改性有相当多的研究,然而不含TiO2的新型光催化剂也是光催化领域的研究热点,学者们开发了诸如金属氧化物和硫化物、无金属材料、等离子体光催化剂及核酸适配子修饰材料等,利用可见光驱动实现对水中病毒的去除。
2.2.1 金属氧化物和硫化物
Takehara 等[32]利用Pt 负载WO3制备的新型光催化剂,在照度为1000lx 的荧光灯照射下,2h 内H1N1 病毒灭活率达到5.3log。Akhavan 等[33]制备了具有片状表面形态的石墨烯-WO3复合薄膜(G-WO3),在对MS2 的光灭活中显示出优异的可见光催化性能。在室温下照射3h 后,MS2 在G-WO3复合膜表面的光催化作用导致病毒蛋白几乎完全破坏,包覆于其中的RNA 也大量流出。在20 个测量周期后,RNA 流出量的减少不到10%,这表明其长达60h 稳定的光催化性能。Yamaguchi等[34]利用掺杂Rh 的SrTiO3作为光催化剂对噬菌体Qβ进行灭活。在可见光照射下,Rh价态从3+变为4+,同时颜色从灰色变为紫色,在细菌存在下仍然观察到噬菌体的灭活,表明Rh4+离子有助于噬菌体的有效和选择性灭活。Giannakis等[35]用三种不同的铁氧化物(方铁矿、磁赤铁矿、磁铁矿)对水中的噬菌体MS2 进行灭活,实验表明与三价铁氧化物不同,方铁矿作为半导体光催化剂在无H2O2添加情况下表现出更好的失活动力学,超纯水中30min 内灭活率达到5log(99.999%),分析可能由于芬顿反应的介入,Fe2+与生成的H2O2反应产生更多的·OH。磁铁矿、纳米磁赤铁矿在光照射下加入H2O2后,非均相的光芬顿作用明显增强了对MS2的灭活,铁氧化物不仅作为半导体催化剂,同时Fe3+还原成Fe2+并与H2O2反应生成·OH氧化破坏病毒蛋白质外壳。铁氧化物不仅具有磁性可分离回收的经济性优势,加入H2O2后形成的光芬顿反应还增强了对病原微生物的灭活。Sarkar 等[36]开发了一种在单层二硫化钼(MoS2)纳米片上电喷雾沉积银离子制备纳米孔的新方法。利用电喷雾沉积的银离子与MoS2纳米片反应,生成的富钼缺陷在可见光下能高效地产生H2O2等ROS,对水中病原微生物进行有效的去除。对多种细菌菌株和病毒菌株进行了实验,这种多孔的MoS2纳米片的消毒效率比普通的提高了105倍,其在107CFU/mL 的细菌浓度和107PFU/mL 的病毒浓度下仍能提供抗菌和抗病毒活性。
2.2.2 无金属催化材料
石墨相氮化碳(g-C3N4)是杀菌消毒领域中无金属催化剂的研究热点,研究人员开发了许多改性和复合方法来提高光催化性能。Li 等[37]通过实验发现,g-C3N4在最佳浓度为150mg/L,360min可见光照射下将108PFU/mL 的MS2 完全灭活,最大达到8log 的灭活率。灭活过程中起主导作用的致使四种主要的RNA 基因泄露和破坏,最终导致病毒死亡。Cheng 等[38]采用水热法合成了Ag3PO4/g-C3N4复合材料对噬菌体f2 进行光催化消毒。复合材料在可见光照射80min 内达到了对3×106PFU/mL 的f2 完全失活,灭活率达到6.5log,H+和·OH 在光催化消毒过程中起着重要作用。Zhang 等[39]合成了一种由g-C3N4和低密度多孔膨胀珍珠岩(EP-520)的复合材料,其比表面积高达45.3m2/g。可见光照射下240min,MS2 的灭活率达8log。其课题组[40]还通过低温溶剂热-水热法,将氧掺杂的g-C3N4微球与水热碳化碳(HTCC)结合用于灭活人体腺病毒。 实验表明滴度为105MPN/mL 的病毒在可见光照射下可在120min 内完全失活(最高灭活率达5log)。此外,随着水温的升高、pH 的降低或盐的存在,都可能致使病毒的灭活效率得以提高。g-C3N4不仅灭活效率高且性能稳定,作为一种绿色、可持续且成本低的无金属光催化剂拥有广阔的应用前景。
2.2.3 等离子体光催化剂
等离子体金属纳米结构能够激发光催化剂表面等离子体效应,有效提高光催化效率。Hu 等[41]发现Ag-AgI/Al2O3等离子体能在可见光照射下催化灭活轮状病毒等肠道病原微生物。以中孔Al2O3为载体,表面沉积AgI 后将Ag 在其表面制备的Ag-AgI/Al2O3催化剂在可见光照射下,40min内能快速灭活3.2log 轮状病毒。研究表明该催化剂的光催化消毒主要是由Ag NPs 的等离子体共振效应引起的(特别是在波长大于450nm时),而不是Ag NPs捕获电子提高电子-空穴分离效率。其诱导产生的h+、无机阴离子自由基和是光催化消毒的主要活性物种,水中的无机阴离子自由基不但加强了电子转移,其基团还具有很高的杀菌活性。因此,等离子体光催化是一种非常有前景的消毒方法。
2.2.4 核酸适配子修饰
核酸适配子是一段单链的DNA 或RNA,适配子小、水溶性高且易于化学生成和修饰能与多种目标物质高特异性、高选择性地结合。Hu 等[42]合成了一种新型的光催化剂:核酸适配子修饰氧化石墨烯(GO-适配体),研究其在可见光照射下灭活病毒的能力。GO 没有与目标的特异性结合位点,容易聚集影响光催化效率,固定在GO上的适配子能与病毒的表面蛋白特异性结合,破坏噬菌体MS2 的蛋白质衣壳和核酸,可见光照射下灭活率达99.999%,明显优于相同条件下的纯GO。此外,在黑暗条件下,裸露的GO与光照条件下灭活能力相似,而边缘更钝的GO则灭活能力弱,可能是锋利的边缘物理破坏了病毒蛋白。GO 与适配子的结合有效提高了GO对病毒的灭活能力,作为一种智能的绿色光催化剂,可以在复杂的水基质下实现对病毒的选择性灭活,利用核酸适配子修饰在光催化消毒领域拥有极大的研究价值。然而制作复杂且成本高,因此也限制了它们的批量生产和工程应用。
目前,新型冠状病毒仍在全球范围内肆虐,WHO表示:“尚未在饮用水中检测到COVID-19病毒的存在,其对供水系统的安全隐患很低。”尽管美国国家环境保护局(EPA)认为,新型冠状病毒易被消毒剂灭活,常规污水处理和消毒工艺能够控制该病毒的传播。然而,新冠病毒对饮用水系统安全的威胁依然不容忽视,因此迫切需要更精确高效快速的消毒方法。近日,由美国莱斯大学的Pedro alvarez 教授和生物学家Yizhi Jane Tao 共同提出利用分子印迹结合石墨碳氮化物进行选择性的光催化灭活冠状病毒的假设。该项目已经获得美国国家科学基金会(NSF)的资金支持于近日启动。研究人员推测,具有常见冠状病毒附着因子的石墨化氮化碳分子印迹将病毒在活性位点附近选择性吸附,从而可靠地实现准确快速消毒[43]。这种“诱捕”消毒技术可以增强各种冠状病毒的表面识别能力,进而有助于浓缩病毒的工作,通过吸附剂进行更精确的分离,并提高诊断和检测工作中使用的传感器检测限。新型冠状病毒对人类饮用水安全依旧存在着潜在威胁,针对其光催化灭活的研究仍需进一步加大力度,消毒技术应向着更加准确高效的方向开发。
表1为灭活水中病毒的光催化材料汇总。
3 结语与展望
本文综述了近年来国内外学者对于光催化材料应用于去除水中病毒的研究进展。光催化作为一种最具潜力的消毒技术之一,不仅高效、绿色安全且成本低廉。对于光催化材料的设计开发目前主要集中于半导体材料及其改性,尤以TiO2基为主,为了克服其禁带较宽、光生电荷和空穴复合率高的限制,通过贵金属沉积、金属/非金属离子掺杂、染料光敏化、复合半导体材料以及多元共掺杂等方法能有效提高光催化活性。不含TiO2的光催化材料包括金属氧化物和硫化物、无金属材料、等离子体光催化剂及核酸适配子修饰材料等也具有很好的应用潜力,受到研究人员的广泛关注。
未来针对光催化材料的研究仍然是以可见光驱动为主,并提高其光催化效率。为实现光催化技术的商业化和工程化,降低光催化材料的制备成本以及加强其分离回收再利用,提高光催化材料的使用寿命仍需进一步研究设计。光催化消毒研究与实际大规模应用还存在着许多机遇和挑战,仍需进一步探索。

表1 灭活水中病毒的光催化材料总览表
