3种总大肠菌群和大肠埃希氏菌酶底物法检测试剂性能比较
2020-10-19孙杰
孙 杰
(上海城投水务〈集团〉有限公司,上海 200082)
酶底物法(defined substrate technology,DST)是指在选择性培养基上能产生β-半乳糖苷酶(β-D-galactosidase)的细菌群组分解色原底物、释放色原体,使培养基呈现颜色变化,来检测水中大肠菌群的方法[1]。与传统多管发酵法相比,该方法具有操作简便、检测时间短、无需确认试验、无菌要求低等优点,且大量文献证实,Colilert酶底物法试剂与多管发酵法在检测大肠菌群结果上没有显著性差异[2-3]。因此,该方法被广泛应用于大肠菌群的检测[4-6]。《生活饮用水标准检验方法》(GB/T 5750.12—2006)[1]和《水质 总大肠菌群、粪大肠菌群和大肠埃希氏菌的测定》(HJ 1001—2018)[7]中,均将酶底物法作为总大肠菌群和大肠埃希氏菌的标准检测方法。随着酶底物法应用的普及,市面上出现了各种不同品牌的酶底物法试剂,这些产品的质量良莠不齐,性能也不同,影响检测结果的准确性。为确定酶底物法试剂的性能,保证检测结果的真实有效,本文对市面上常见的3种酶底物法试剂进行了分析比较,检测定量质控、原水、二次供水、管网水等多种水样,并对其性能进行评价。
1 试验部分
1.1 主要试剂、设备
3种酶底物商品试剂(Colilert、LI、QT),程控定量封口机、无菌取样瓶、97孔定量盘、51孔定量盘、NSI定量质控菌株。试验使用国产恒温培养箱(SPX-250B-Z型),温控精度为±0.5 ℃,经计量部门校准合格。
1.2 试验步骤
(1)水样采集:原水水样为上海某水厂的进厂原水,二次供水水样为上海居民的龙头水,管网水水样取自上海某地区的管网监测点。参照GB/T 5750.2—2006进行采集和样品保存[8],采样容器使用一次性无菌含硫代硫酸钠采样瓶。水样采集后冷藏保存,并在4 h内进行检测。
(2)定量质控检测:NSI定量质控菌株从-10 ℃冰箱中取出,平衡温度10~15 min后,将质控菌株转移入预先准备好的100 mL无菌磷酸缓冲液中,轻轻振荡,待全部溶解后在30 min内进行检测。
(3)样品检测:样品使用酶底物法进行检测,检测项目为总大肠菌群、大肠埃希氏菌。检测步骤参照GB/T 5750.12—2006。
(4)实际水样阳性结果测序:对于定量盘阳性结果,送由金唯智生物科技有限公司测序,对菌种进行鉴定。
2 结果分析
2.1 混合质控阳性菌:饮用水和环境水定量质控检测
Colilert、LI、QT总大肠菌群和大肠埃希氏菌质控检测结果表明:3种试剂的检测结果均在质控样品结果可接受范围内;QT试剂总大肠菌群和大肠埃希氏菌结果相同,表明该试剂对大肠埃希氏菌的显色反应有误,未能区分大肠埃希氏菌和其他混合菌种。为进一步评价试剂性能和结果的准确性,计算检测结果与真值的相对误差[相对误差=(测定值-真值)/真值×100%],如表1、图1所示。结果表明,Colilert试剂检测结果与真值的相对误差最小,检测结果更接近于真值。计算3种试剂检测结果相对误差的标准差,可得总大肠菌群标准差:SD(Colilert)=5.54,SD(QT)=19.87,SD(LI)=34.30,大肠埃希氏菌标准差:SD(Colilert)=7.26,SD(QT)=14.27,SD(LI)=25.84。可知,Colilert试剂标准差最小,表明其检测结果与真值的相对误差离散程度较小,性能较为稳定;LI试剂的标准差最大,表明其性能不稳定,结果波动性较大。

表1 3种试剂检测NSI定量质控样品的结果Tab.1 Results of NSI Quantitative Quality Control Samples (QC) Detected by Three Reagents

图1 3种试剂检测结果真值的相对误差Fig.1 Relative Error between Test Samples and Trueth-Values
2.2 单一菌种质控及阴性菌:大肠埃希氏菌、铜绿假单胞菌检测
Colilert、 LI、 QT检测单一菌种质控及阴性菌。3种试剂的检测结果均在质控样品结果可接受范围内。QT试剂大肠埃希氏菌结果与总大肠菌群结果不一致,证明了2.1节的推断,即该试剂对大肠埃希氏菌的显色反应不稳定,不能用于大肠埃希氏菌的检测,如表2所示。3种试剂对阴性菌铜绿假单胞菌均能有效辨别。计算检测结果与真值的相对误差,结果表明, Colilert试剂检测结果与真值的相对误差最小,检测结果更接近于真值。
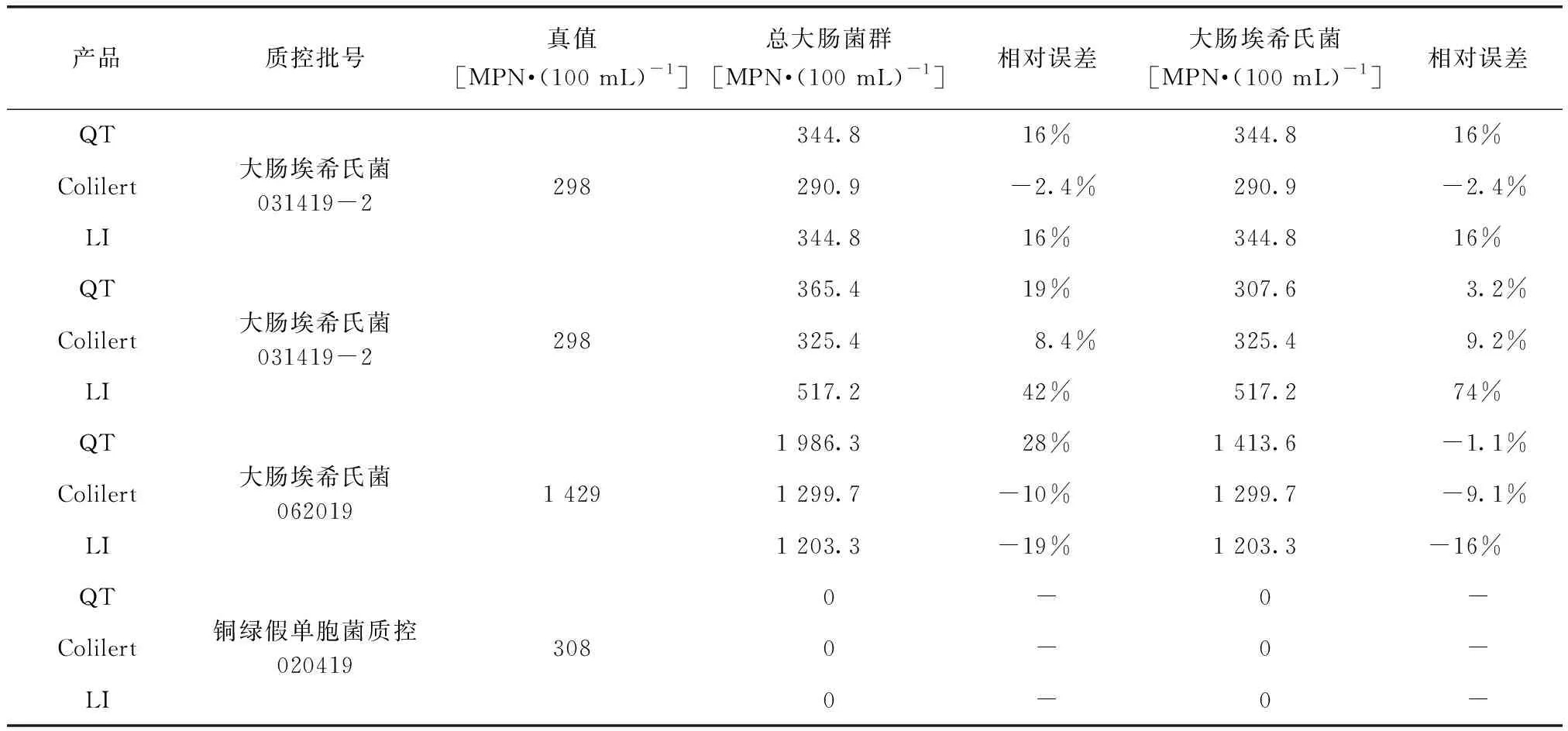
表2 3种试剂检测单一菌种质控及阴性菌结果Tab.2 Results of Single Strain QC and Non-Target Bacteria Detected by Three Reagents
2.3 实际水样
(1)3种试剂检测二次供水、管网水总大肠菌群,并对阳性结果进行16S rDNA测序,结果如表3所示。Colilert、LI和QT阳性检出率,二次供水分别为11.43%、5.71%和45.71%,管网水分别为0.00、3.33%、26.67%。提取二次供水和管网水阳性孔菌体的DNA,测定16S rDNA,进行菌种鉴定,确认阳性结果的真实性。测序结果表明,Colilert阳性结果的样品均含有总大肠菌群,即检测结果与测序结果吻合。LI阳性结果3组,E-31为真阳性,E-6和G-8两组结果为假阳性,假阳性率为66.6%,阳性样本漏检率为75%。QT检测阳性结果24组,1组为真阳性,其余23组均为假阳性,假阳性率为95.8%,阳性漏检率为75%。
(2)对原水总大肠菌群,Colilert、LI和QT的实际检测结果如表4所示。
运用软件SPSS Statistics 19,对Colilert、LI和QT检测结果进行配对t检验,为了使数据呈正态分布,对数据进行对数处理后再进行t检验,结果如表5所示。
由表3可知:Colilert 与LI、QT的泊松相关系数为0.495和0.319,属弱相关;P<0.05,具有统计学意义上的显著性差异。结果表明,LI、QT在检测原水总大肠菌群时,与Colilert的检测结果具有差异性。

表3 3种试剂对二次供水、管网水的检测及测序结果Tab.3 Testing and Sequencing Results of Three Reagents for Secondary Water Supply and Pipeline Water

序号水样类型Colilert[MPN·(100 mL)-1]16S rDNALI[MPN·(100 mL)-1]16S rDNAQT[MPN·(100 mL)-1]16S rDNAG-5管网水0-0-0-G-6管网水0-0-5假阳性G-7管网水0-0-0-G-8管网水0-1假阳性0-G-9管网水0-0-0-G-10管网水0-0-0-G-11管网水0-0-0-G-12管网水0-0-0-G-13管网水0-0-0-G-14管网水0-0-0-G-15管网水0-0-0-G-16管网水0-0-1假阳性G-17管网水0-0-1假阳性G-18管网水0-0-0-G-19管网水0-0-3假阳性G-20管网水0-0-0-G-21管网水0-0-0-G-22管网水0-0-0-G-23管网水0-0-0-G-24管网水0-0-0-G-25管网水0-0-0-G-26管网水0-0-0-G-27管网水0-0-1假阳性G-28管网水0-0-0-G-29管网水0-0-0-G-30管网水0-0-0-
3 讨论
3.1 混合质控检测
Colilert、LI、QT对3组混合质控总大肠菌群和大肠埃希氏菌检测结果真值相对误差绝对值的平均值分别为14.35%、36.55%、21.70%和15.51%、32.34%、72.26%。Colilert 检测定量质控结果真值的相对误差小,检测结果准确;LI和QT检测结果真值的相对偏差较大。标准差结果计算表明,Colilert试剂标准差最小,表明其检测结果与真值的相对误差离散程度较小,性能较为稳定;LI试剂的标准差最大,表明其性能不稳定,结果波动性较大。同时,总大肠菌群和大肠埃希氏菌的检测结果表明,QT不能辨别大肠埃希氏菌与非大肠埃希氏菌,检测大肠埃希氏菌时存在误判的可能。
3.2 单一质控及阴性菌检测
Colilert、LI、QT对3组单一菌种质控总大肠菌群和大肠埃希氏菌检测结果真值相对误差绝对值的平均值分别为6.92%、25.6%、20.7%和6.87%、35.02%、6.67%。但是,QT检测大肠埃希氏菌单一质控时,总大肠菌群和大肠埃希氏菌检测结果数值不一样,荧光颜色较弱或呈蓝绿色荧光,检测数值偏低,有假阴性风险。因此,判断QT不能有效辨别大肠埃希氏菌与非大肠埃希氏菌,检测大肠埃希氏菌时存在误判的可能。另外,LI培养基溶解后,显示淡黄色,增加了结果判读的难度。
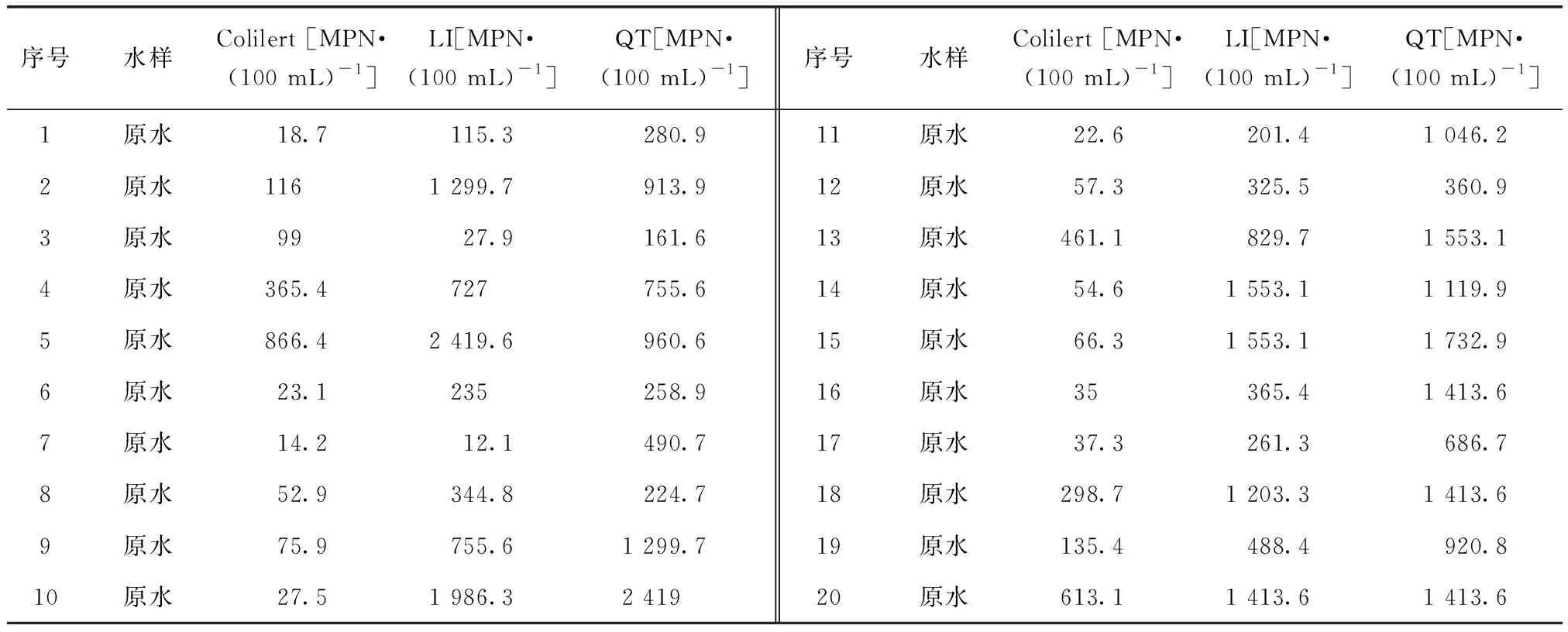
表4 3种试剂检测原水的结果Tab.4 Testing Results of Raw Water by Three Reagents
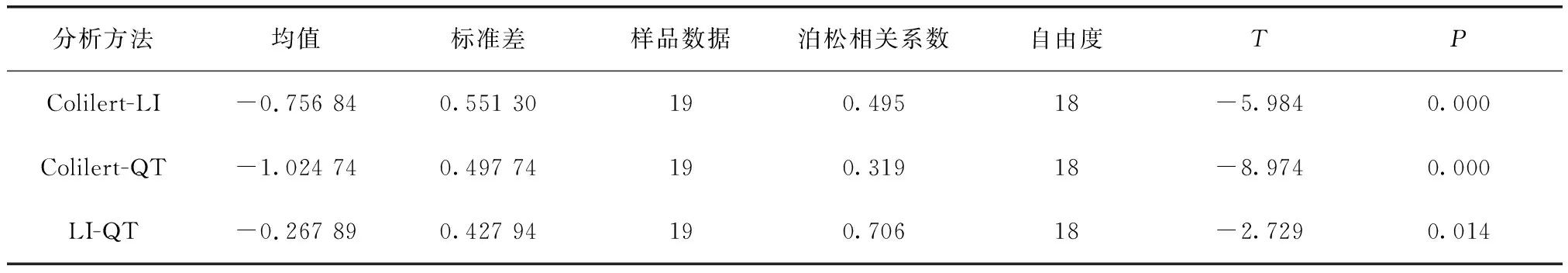
表5 3种试剂对原水检测结果的t检验Tab.5 Results of t-Test of Raw Water by Three Reagents
3.3 实际水样检测
对于二次供水和管网水,Colilert 阳性结果与16S rDNA测序结果吻合;LI假阳性率为66.6%,阳性样本漏检率为75%;QT检测假阳性率为95.8%,阳性漏检率为75%。因此,在检测实际水样的过程中,2种酶底物试剂有漏检阳性水样的风险,增加了水质实验室结果的不可信度;假阳性检测结果的出现,会增加水质实验室排查水质隐患的工作量。对于原水的检测,2种酶底物试剂与Colilert 具有弱相关性,具有统计学意义上的显著性差异,和管网与二次供水的结果可互相验证。
4 结论
Colilert 试剂质控样品检测结果与真值相对误差较小,实际水样检测未出现假阳性,结果真实可靠,性能稳定;LI和QT试剂在检测质控样品时,与真值相对误差较大,检测实际水样时,有假阳性和阳性漏检的风险;QT不能有效辨别大肠埃希氏菌与非大肠埃希氏菌,检测大肠埃希氏菌时存在误判的可能。因此,实验室在选择酶底物试剂时,应选择性能优良、口碑较好的品牌,确保检测结果的准确性。
