生物法制备丁二酸的研究及产业化进展
2020-10-15万屹东高有军马江锋
万屹东,高有军,马江锋
(1.常茂生物化学工程股份有限公司,江苏 常州 213034;2.江苏省生化手性工程技术研究中心,江苏 常州 213034;3.南京工业大学 生物与制药工程学院,江苏 南京 211800)
丁二酸作为重要的C4平台化合物拥有巨大的市场需求,可作为鲜味剂、食品铁质强化剂、分析试剂、配制电镀药水、清洗添加剂等应用于食品工业与化学工业,同时可作为聚合单体合成生物可降解材料聚丁二酸丁二醇酯(PBS)和耐高温特殊尼龙(PA-X4)[1]。此外,基于丁二酸线性的分子结构和二元羧酸特性,可作为前体进一步合成多个大宗化学品,如1,4-丁二醇(聚酯纤维和氨纶的单体)、γ-丁内酯(农药、除草剂和部分药物的前体)、四氢呋喃(聚四亚甲基醚二醇合成的前体和助剂)、己二酸(尼龙PA-X6的单体)和N-甲基吡咯烷酮(化工和锂电池工业中的重要溶剂),预计至2020年市场需求将达到70万t[2]。
目前丁二酸的生产主要以丁烷为原料,通过催化加氢等步骤进行化学合成,其生产工艺成熟,较生物基丁二酸的制备具有显著成本优势,但其依赖原油,因此成本受原油价格波动影响较大、原料不可再生且生产过程污染严重[3]。在石油危机及环境污染的双重压力下,微生物发酵生产丁二酸因具有利用可再生资源、固定温室气体CO2等优点,近年来成为国内外研究的热点而受到广泛关注。
美国能源部在20世纪90年代初提出了替代性原料计划,并联合了Argonne National Laboratory、OakRidge National Laboratory、Pacific Northwest National Laboratory和National Renewable Energy Laboratory(NREL)这4个国家级实验室联合进行丁二酸生物转化和提取技术的攻关。如今,已经有多家企业建立了商业化的生物基丁二酸生产线,并开始对外提供生物基丁二酸样品供下游产品的开发以满足丁二酸的市场需求。荷兰DSM和法国Roquette两家公司联合成立的Reverdia公司于2014年对外声明在意大利建立了采用酵母菌低pH发酵的10 000吨/年生产能力的商业化生物基丁二酸装置(http://www.reverdia.com/news-events/news/)。美国BioAmber公司于2015年声明其合资公司 Sarnia和日本三井公司合作,建成了基于低pH发酵工艺设计和建设的30 000吨/年生物基丁二酸生产装置(https://www.bio-amber.com/bioamber/en/company)。除此之外,美国Myriant也建立了采用铵盐法中性发酵工艺的14 000吨/年的生物基丁二酸装置(http://www.myriant.com/)。荷兰CorbionPurac和德国BASF联合成立的Succinity公司在西班牙建立了采用中性发酵工艺的14 000吨/年的生物基丁二酸装置(http://www.succinity.com/about-us)。国内中国石化扬子石油化工股份有限公司与南京工业大学合作,设计和建造了采用钠盐法中性发酵的1 000吨/年生物基丁二酸中试生产装置。
生物基丁二酸已经初步实现了产业化,但与生物基富马酸、苹果酸等生物炼制有机酸产品一样,其主要问题是比化学合成的制造成本要高。柠檬酸的生物制造是目前有机酸生物炼制中最成功的案例之一。20世纪末我国天津工业微生物所、上海工业微生物所以及企业家的联合攻关,在菌株、发酵过程及放大过程三方面取得了重大成果,目前柠檬酸发酵技术(柠檬酸的平均生产质量浓度、生产速率和总收率分别约为150 g/L、3 g/(L·h)和90%,车间成本在4 000元/吨左右)处于世界领先水平[4]。中国有柠檬酸生产厂近百家,总年产能力约100万t,是全球最大的柠檬酸生产国和出口国,如安徽丰原生化公司的柠檬酸生产能力达18万t,占世界柠檬酸生产额的17%,居世界第一位[4-5]。因此,利用先进的合成生物学、代谢工程等技术,结合分离工艺模拟、设计及优化,提高丁二酸的生产效率,将有助于实现生物基丁二酸的低成本制造,具备与石油基丁二酸相竞争的成本优势[6]。
本文中,笔者针对国内外生物基丁二酸生产成本偏高以及产品原料依赖粮食资源等问题,从生产菌株、非粮碳源、发酵工艺和分离工艺四方面进行综述,并预测未来具有经济性的工艺路线,为生物基丁二酸的绿色、高效和低成本制造提供借鉴。
1 丁二酸生产菌株
1.1 野生菌株
产丁二酸野生菌株主要包括产琥珀酸放线杆菌[7]、曼海姆产琥珀酸菌[8]、产琥珀酸厌氧螺菌[9]和钝齿棒杆菌[10]等(表1)。丁二酸是三羧酸途径(TCA)的终端产物之一,其合成途径如图1所示,因此在厌氧条件下诸多野生型菌株也能积累丁二酸。
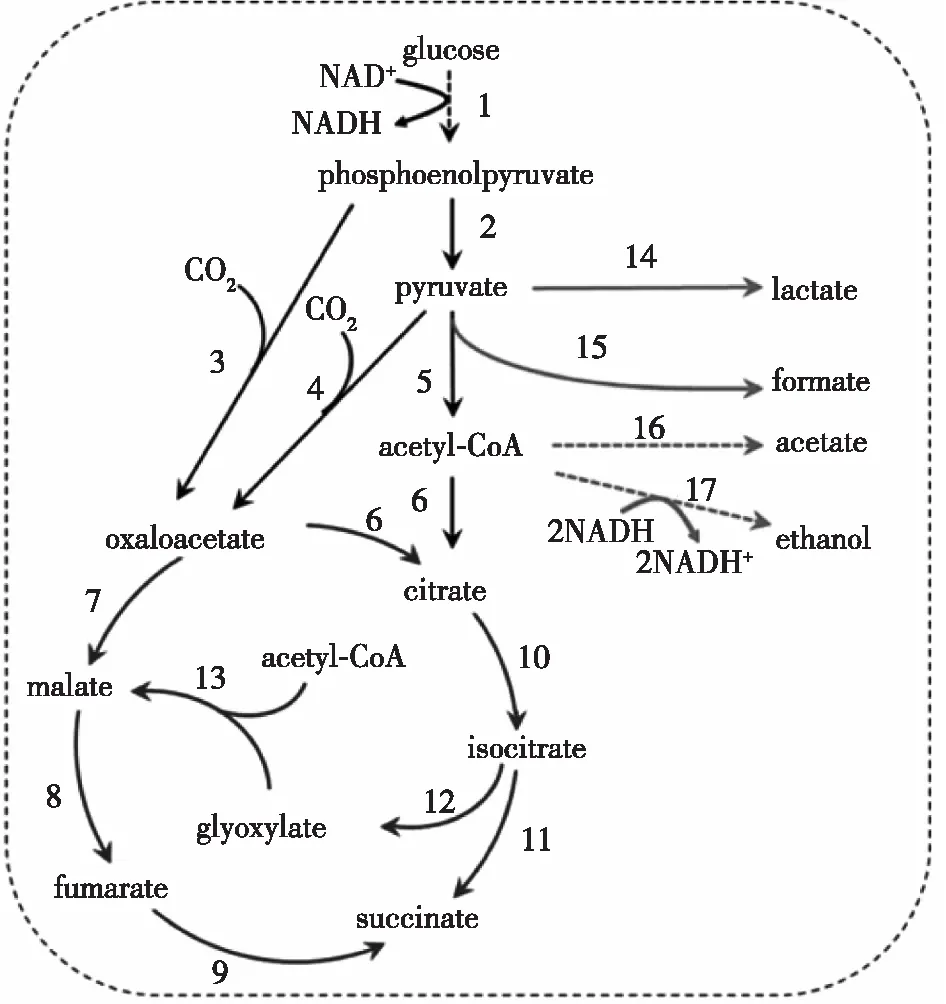
1—Embden-Meyerhof途径;2—丙酮酸激酶;3—磷酸烯醇式丙酮酸羧化酶;4—丙酮酸羧化酶;5—丙酮酸脱氢酶;6—柠檬树合成酶;7—苹果酸脱氢酶;8—富马酸酶;9—富马酸还原酶;10—顺乌头酸酶;11—异柠檬酸裂解酶;12—异柠檬树裂解酶;13—苹果酸合酶;14—乳酸脱氢酶;15—丙酮酸裂解酶;16—磷酸转乙酰化酶和乙酸激酶;17—乙醇脱氢酶和乙醛脱氢酶

表1 产丁二酸野生菌株
产琥珀酸放线杆菌最先是从牛瘤胃内容物中分离得到的一种兼性厌氧、不运动的革兰氏阴性杆菌,该菌在厌氧环境中可以利用广泛的碳源,如葡萄糖、乳糖、木糖、阿拉伯糖、纤维二糖和其他还原性糖[18]。研究人员考察了该菌对一些废弃生物质的利用情况,如乳清[12]、甘蔗糖蜜[14]、稻草[15]、玉米芯[11,16]、秸秆[13]、麸皮[19]和浮萍[20]等,结果发现,产琥珀酸放线杆菌具有利用多种生物质的天然特性,在低劣生物质综合利用方面具有显著优势,能够通过菌株原料预处理、发酵过程控制等策略实现全糖利用。
曼海姆产琥珀酸菌是从牛的瘤胃中分离筛选得到的另一株兼性厌氧嗜CO2革兰氏阴性菌。以葡萄糖为碳源,厌氧发酵时丁二酸是主要产物,乙酸和甲酸为主要副产物,比例为2∶ 1∶ 1。此外,利用乳清为底物,以玉米浸出物代替酵母提取物发酵生产丁二酸,收率71%,生产速率达到1.18 g/(L·h)[8]。
产琥珀酸厌氧螺菌是从小猎犬的口腔中分离得到的一株革兰氏阴性、严格厌氧菌,以葡萄糖为碳源厌氧发酵时,主产物为丁二酸和乙酸,同时生成少量的甲酸、乙醇和乳酸[21]。但产琥珀酸厌氧螺菌不能耐受高渗透压,最优底物葡萄糖为20~80 g/L,而且不能耐受高浓度的丁二酸盐。因此,Meynial-Salles等[9]通过耦合电渗析过程并结合膜生物反应器,产物丁二酸产量提高至83 g/L,且收率和生产速率分别达到1.35 mol/mol和10.4 g/(L·h),具有一定的应用前景。
钝齿棒杆菌是一株产谷氨酸菌,Chen等[10]筛选得到一株钝齿棒杆菌,该菌有氧发酵时能生产谷氨酸,回收细胞转厌氧发酵能够利用合成培养基发酵制备丁二酸,且细胞能够重复回收利用多次。当以麦麸水解液为碳源发酵时,丁二酸产量和生产速率分别达到43.6 g/L和4.36 g/(L·h)。
产琥珀酸放线杆菌和曼海姆产琥珀酸菌等野生菌株能够高收率、高浓度制备丁二酸,但这类菌多为营养缺陷型,往往依赖营养丰富的复合培养基,而高昂的培养基成本使得这类菌株的经济性大大降低。
1.2 基因工程菌株
随着基因测序、基因编辑技术及基因精细调控表达等技术的进步,从分子层面改造微生物代谢网络提高丁二酸生产效率的研究已经取得了一定的成果(表2)。综合各种代谢工程改造策略,丁二酸基因工程菌的构建主要包括:敲除或突变副产物合成途径相关基因、外源引入或超量表达丁二酸合成途径相关酶、提高底物利用效率及优化辅因子代谢。

表2 产丁二酸代谢工程菌株
1.2.1 敲除或突变副产物合成途径相关基因
为超量积累目标产物,首先需要解决副产物积累的问题,可以通过敲除或突变副产物合成途径中关键酶基因来减少副产物的合成。在丁二酸基因工程菌株中,主要包括有氧发酵和厌氧发酵两类生产菌。针对有氧丁二酸生产菌株,Lin等[28-29]通过失活大肠杆菌的sdhAB、poxB、ackA-pta、iclR和ptsG基因构建获得了重组菌E.coliHL27659k,该菌株发酵59 h积累58.3 g/L丁二酸,收率为0.56 g/g。Otero等[36]结合进化代谢选育并敲除酿酒酵母SDH3P和Ser3p/Ser33p基因,维持细胞生长与代谢合成丁二酸的过程,最终产物浓度比出发菌株提高了43倍。Yuzbashev等[33]敲除解脂耶氏酵母SUC2和SDH2基因并突变了SDH1基因,获得的重组菌在低pH下以甘油为碳源发酵制备丁二酸,产量达到45 g/L,该技术具有显著减少下游分离步骤的作用。针对厌氧丁二酸生产菌株,敲除ldhA、pflB、adh以及pta、ackA、poxB基因可以减少乳酸、甲酸、乙醇和乙酸的积累,而失活磷酸转移酶转运系统(PTS)中的葡萄糖专性转运蛋白编码基因ptsG可以减少丙酮酸的生成,促使更多的碳代谢流流向还原三羧酸途径。其中,重组大肠杆菌KJ073(ldhA、adhE、ackA、focA-pB、mgsA、poxB)利用合成培养基,以葡萄糖为碳源厌氧发酵,丁二酸的收率达到1.2 mol/mol[37]。Lee等[35]敲除曼海姆产琥珀酸菌中的ldhA、pflB、pta和ackA基因构建获得了重组菌M.succiniciproducensLPK7,该菌株在分批发酵过程中积累52.4 g/L丁二酸,收率为1.16 mol/mol,生产速率达到1.8 g/(L·h)。
1.2.2 外源引入或超量表达丁二酸合成途径相关酶
在敲除或突变与副产物合成相关基因的基础上,进一步强化丁二酸合成途径相关基因的表达是提高丁二酸合成效率的另一种策略。Wang等[38]通过敲除大肠杆菌中ldhA、pflB和ptsG基因并过量表达来源于蓝细菌的ppc基因获得重组菌株SD121,该菌株利用秸秆水解液厌氧发酵,丁二酸达到36.5 g/L,收率为0.83 g/g。另一方面,若在ppc基因缺失的菌株中超量表达pck基因,使得催化磷酸烯醇式丙酮酸(PEP)至草酰乙酸的反应能额外产生一分子ATP,可促进菌株在厌氧条件下的生长性能,进而提高丁二酸的生产效率[37]。Yang等[39]基于提高菌株产物合成速率的计算机模拟方法,在有氧丁二酸生产菌E.coliZJG13中超量表达pyc基因,结果表明重组菌E.coliZJG13/pT184pyc的平均生产速率比丁二酸的明显提高。Okino等[30]敲除了谷氨酸棒杆菌的ldhA基因并表达pyc基因,重组菌所产的丁二酸达到146 g/L,厌氧阶段收率0.92 g/g。在嗜乙酰乙酸棒杆菌(Corynebacteriumacetoacidophilum)中采用相同的策略也实现丁二酸的超量积累,丁二酸超过100 g/L,收率为1.34 mol/mol[31]。Yan等[32]在缺失pdc、fum1基因的酿酒酵母中过量表达pyc2和mdh3r基因并引入来源于大肠杆菌的fumC、frds1基因,构建获得的重组酿酒酵母在pH3.8的酸性环境下发酵也能积累12.9 g/L丁二酸。
1.2.3 提高底物利用效率
在野生型大肠杆菌中,葡萄糖的转运和磷酸化主要采用PTS系统完成,该转运系统每转运1分子葡萄糖需要消耗1分子磷酸烯醇式丙酮酸(PEP)[40]。PEP是厌氧丁二酸合成过程中重要的前体物质,为了提高还原三羧酸途径中PEP的供给,Lu等[41]失活了PTS系统使得葡萄糖的转运采用激酶途径,结果导致葡萄糖代谢速率显著下降,进一步构建启动子和mRNA稳定区文库精细调控半乳糖透性酶和葡萄糖激酶基因的表达,使得葡萄糖消耗速率达到1.64 g/(L·h),代谢速率提高了10倍。
木糖是纤维素水解液的主要成分之一,来源广泛,可作为微生物发酵的重要碳源。Liu等[42]研究发现,野生型大肠杆菌可以利用木糖进行厌氧有机酸发酵,但当敲除乳酸和甲酸、乙酸生成相关的编码基因pflB和ldhA后,菌株在厌氧条件下不能利用木糖生长和代谢。进一步通过敲除自身ppc基因并引入来源于枯草芽孢杆菌的pck基因,提高了胞内ATP的供给,从而恢复了菌株的木糖利用能力。在以秸秆水解液为碳源的发酵过程中,丁二酸的收率达到1.02 g/g,该研究证实了木糖代谢较葡萄糖代谢需要更多的ATP供给,供给不足将导致菌株生长及代谢受到抑制。
除单糖外,二糖、多糖等也可作为丁二酸发酵的碳源。Inokuma等[43]和Park等[44]研究发现,构建细胞表面展示系统将相关的水解酶固定在细胞表面,促使二糖、多糖在胞外水解并获得单糖,进而可作为细胞生长及代谢所需的碳源。Ma等[45]利用细胞表面展示技术以产丁二酸重组大肠杆菌AFP111为出发菌株,以OmpC为锚定蛋白将蔗糖水解蛋白锚定在细胞表面,最终菌株能够利用蔗糖发酵制备丁二酸。当以蔗糖和糖蜜为碳源时,发酵34 h时丁二酸的质量浓度分别达到41和36.3 g/L。
1.2.4 优化辅因子代谢
微生物胞内存在氧化还原平衡,其分子基础是NAD(P)+和NAD(P)H等辅因子对的比例。当对微生物胞内代谢途径进行重构后,往往会引起辅因子比例的变化,影响菌株生长及代谢。Vemuri等[46]敲除了大肠杆菌ldhA和pflB基因获得E.coliNZN111,该菌株由于降低了NAD+的再生效率,导致胞内辅因子失衡,因此在厌氧条件下不能以葡萄糖为碳源生长。针对NZN111生长抑制的问题,Liang等[47-49]先后采用两种策略恢复了其生长及代谢能力,一是通过mdh基因的超量表达强化NADH的消耗速率,二是从NAD+原始生物合成途径出发提高NAD+的总量使之不容易失衡。Zhou等[50]在枯草芽孢杆菌中引入来源于大肠杆菌的pntAB基因,其表达的酶能够催化NAD(H)和NADP(H)相互转化,以维持胞内辅因子的平衡,最终该重组枯草芽孢杆菌丁二酸收率和质量浓度分别提高了16%和57%。
2 底物碳源
2.1 主要非粮生物质碳源
淀粉质碳源是目前生物基丁二酸发酵的主要碳源,但在“不与民争粮,不与民争地”的方针原则下,开发其他低成本碳源迫在眉睫。根据扬子石油化工股份有限公司“1 000吨/年丁二酸中试生产装置”连续3批发酵数据(数据未公布)结果分析,碳源约占丁二酸生产成本的45%~50%。因此,如何降低碳源成本是建立经济性的丁二酸生产工艺需要重点考虑的问题之一。基于此,众多研究者考察了诸如纤维素水解液等低品位碳源在丁二酸发酵体系中的利用情况。
Chen等[51]通过营养定向补给策略,采用废酵母细胞水解液和玉米秸秆水解液复配的方法,A.succinogenesNJ113能积累70.3 g/L丁二酸,收率和生产速率达到67.7%和0.63 g/(L·h)。Liu等[42]以蔗渣水解液为原料,利用重组大肠杆菌BA204两阶段发酵,厌氧阶段丁二酸收率达到0.96 g/g。连续糖化发酵可减少预处理步骤,Zheng等[52]和Chen等[53]分别考察了A.succinogenes和E.coli连续糖化发酵制备丁二酸的可能性,结果发现,通过在发酵介质中添加纤维素酶和纤维二糖酶可以利用经过简单稀酸处理的纤维素物质,最高的丁二酸质量浓度达到47.7 g/L。
尽管水解秸秆等木质纤维素原料用于发酵制备丁二酸具有环境友好、来源广泛以及成本低廉等优点,但现有的半纤维素水解技术往往导致水解液中含有糠醛、羟甲基糠醛和甲酸等抑制物,若不经过脱毒处理,这类物质将在发酵过程中影响微生物的生长及代谢,并影响最终丁二酸产品品质[54-55]。为了提高菌株的发酵效率,Wang等[56]在大肠杆菌中过量表达糠醛降解基因获得重组菌E.coliXW36,该菌株能利用未脱毒半纤维素水解液发酵制备丁二酸,产物质量浓度和收率达到32 g/L和0.9 g/g。
2.2 气态碳源——CO2气体

除了过程中采用碳酸盐外,在发酵初始需要大量的CO2气体以使得发酵环境成为厌氧环境,因此厌氧发酵丁二酸工业生产必须具备直接的CO2气体供应能力。而采用纯CO2压缩气体成本较高,如果能与企业现有的排放CO2气体的生产装置(如环氧乙烷装置、生物乙醇装置、甲烷装置等)耦合或是进行过境处理,不仅能降低温室气体的排放,也能解决厌氧丁二酸发酵气态碳源的问题。Wu等[58]考察了环氧乙烷尾气(环氧乙烷装置实际的尾气中含氧量在1.2%以内)为CO2气态碳源厌氧发酵制备丁二酸的可行性,结果丁二酸终质量浓度为68.1 g/L,CO2气体固定速率达到4.7 mmol/(L·h),基本与纯CO2气体发酵性能基本一致,且环氧乙烷尾气含氧量在2%范围以内波动对发酵无影响。
3 丁二酸生产工艺
3.1 发酵工艺
针对生物基丁二酸的发酵工艺已经有大量的研究成果,除了常见的分批发酵和补料发酵[59]策略外,研究者还设计并形成了细胞循环利用技术、分阶段连续培养技术以及基于膜技术的发酵分离耦合工艺等[60-62]。Beauprez等[63]总结了现有的众多的发酵策略,在肯定了这些策略的优点之余,也提出了存在的问题。众所周知,丁二酸是大宗化学品,价格偏低,对生产成本控制要求高,因此需要进行大规模的生产,比较合理的发酵体积在100 m3左右。基于此,很多复杂的发酵策略因其投资和操作成本高、维护困难以及运转稳定性偏差等问题很难实施。比如,利用超滤膜进行细胞循环利用在大规模发酵过程中就存在易导致染菌、膜易被堵塞等问题[64]。因此,在诸如丁二酸这类大宗化学品的发酵策略的选择上必须考虑其对生产成本的影响以及在实际生产中的操作难度。
3.2 产品分离工艺
3.2.1 传统有机酸分离工艺-钙盐法
传统的有机酸工业化生产,如柠檬酸、乳酸、衣康酸均采用钙盐法[5,65-66]。该技术成熟,且生产成本低,但会产生大量的硫酸钙沉淀(即石膏),大量固废的产生对环境影响较大。同时,该技术只适合低pH(pH<5)发酵,对于中性发酵工艺,钙盐法缺点很多,如必须额外添加酸中和剂。
3.2.2 铵盐法
铵盐法是指在发酵过程中采用氨水调节pH并形成丁二酸二铵,在分离阶段经固液分离后采用硫酸或硫酸氢铵酸化生成丁二酸和硫酸铵并进化后续的纯化步骤。其中丁二酸可通过浓缩、结晶沉淀进行纯化,剩余的母液主要含有硫酸铵和约7%的丁二酸,该母液可直接作为化肥销售,也可采用热裂解的方法重新生成氨气和硫酸氢铵[67-68]。
该技术较钙盐法的优势是采用廉价的氨水为原料,且可利用循环闭合工艺回收氨气,同时产生的母液是含部分丁二酸的硫酸铵溶液,可直接作为化肥销售。其缺点是采用氨水调节发酵过程pH值,对微生物的发酵产生了一定的抑制作用[69],未来需要在菌株构建和驯化过程中提高其对铵盐的耐受性能和利用能力。同时,母液中损失的丁二酸降低了整个产品的分离收率。
3.2.3 电渗析法
电渗析法是指在发酵过程中采用NaOH作为酸中和剂形成丁二酸二钠,进而采用电渗析膜一步实现固液分离和浓缩丁二酸二钠[70]。Dunuwilla等[71]在丁二酸体系中采用双极膜电渗析,借助电势的作用分离获得丁二酸和NaOH。
该技术的优势是发酵过程采用了廉价的NaOH作为酸中和剂,且该物质能在下游分离过程中回收获得,且整个过程不会产生大量的盐。其缺点是钠盐对发酵过程同样存在抑制,尤其是采用NaOH时。同时双极膜电渗析的使用需要高昂的设备投资及相应的自动化装备投入,双极膜的寿命也是制约其普及的另一因素。
3.2.4 直接结晶工艺
与上述3种工艺不同,直接结晶工艺依赖低pH发酵过程,即在丁二酸整个发酵过程中不调节pH,因此发酵液中存在大量游离的丁二酸。该方法的优势显而易见,即简化了分离步骤,降低了下游设备投资,提高了分离收率。但该方法要求微生物具有较强的耐低pH性能,而提高细胞的耐受性能会消耗额外的能量[72],因而导致产物收率的下降。因此,需要对丁二酸生产菌株进行必要的基因工程改造并结合合适的胞外控制策略提高丁二酸的生产效率。
4 结论与展望
通过对现有丁二酸生产工艺与乳酸、酒精发酵工艺的比较,笔者认为微生物发酵法生产丁二酸的主要技术屏障包括:①现有丁二酸生产菌株未具备较高的鲁棒性,在厌氧条件下尤其是采用低品位生物质时,其生长及代谢性状较差。②下游过程分离步骤较多及三废排放偏高。③未考虑综合性工艺系统和工业化装备等问题。
因此,建立经济性的丁二酸发酵工艺需要具备的要素包括:①提高生产速率。可以减少发酵设备投资和发酵的运行成本。如果要在经济性上有竞争力,最小的生产速率应达到2.5 g/(L·h)。②减少营养需求。产业化生产过程要求在保证菌株生长及代谢性能的基础上,使用最少的营养。像酵母膏、生物素这样价格高的营养成分应当除去。营养需求应限制像玉米浸膏或价格相当的成分。③提高最终的产物浓度。产品最终的发酵浓度是影响整个工艺生产成本的重要因素,尤其是下游分离过程的能耗,因此较高的最终产物浓度将减少分离和浓缩的成本。④提高菌株对低pH的耐受性。理想的情况是发酵在低pH下运行,不需要任何的碱中和,否则发酵阶段的中和过程及下游分离阶段盐转换为游离酸的过程会大大增加生产成本。
预测两条经济性较高的丁二酸合成路线:①极低pH发酵(pH<3),发酵过程不中和,下游采用结晶工艺,该路线要求菌株具有较高的耐酸性能和在低pH环境下的代谢性能,同时生产设备也需要采用相应耐腐蚀性能的材质。②中性pH发酵(pH 6.5~7.5),发酵过程氨水中和,下游采用铵盐闭合循环工艺,该路线要求菌株具有耐高浓度铵根离子的性能。
