小儿磁共振成像检查中咪达唑仑口服复合右美托咪定滴鼻镇静的安全性和有效性
2020-10-13季莹莹张剑蔚
季莹莹,薛 彬,黄 悦,张剑蔚
上海交通大学医学院附属上海儿童医学中心麻醉科,上海200127
磁共振成像(magnetic resonance imaging,MRI)检查常用于儿童心脏疾病、脑部发育异常及其他脏器解剖结构异常的诊断,在儿科群体的应用越来越广泛。检查时一般需要患者保持制动10 ~30 min,甚至1 h。儿童由于与父母分离,对检查环境和设备的恐惧、不合作以及无法长时间制动等原因,需要施行镇静或者麻醉才能完成影像检查。MRI 系统的强磁场作用,要求配备特殊的麻醉机与监护仪,导致单次麻醉费用较昂贵。相较于麻醉,镇静可以节省近一半的人力与财力成本,不失为一个经济有效的方法[1]。成功的镇静能改善成像质量,有效降低错误诊断率[2]。理想的镇静方案应具有更高的镇静成功率和较低的不良反应发生率。然而目前镇静方案多种多样,并未就理想方案达成共识。
右美托咪定是一种高选择性α2肾上腺素能受体激动剂,经鼻给药刺激性小,且几无呼吸抑制作用,患者循环稳定,因此在儿童镇静的应用越来越广泛。研究[3-5]表明水合氯醛或右美托咪定单药镇静,小儿完成MRI 检查的成功率较低;需要补救用药的概率较高,导致设备的使用效率和患儿家属的满意度降低。我们既往研究[6]发现水合氯醛复合右美托咪定滴鼻可有效、安全地用于小儿MRI 检查时的镇静,成功率约90%。因此联合使用镇静药物可明显提高成功率,应视为可选方案。水合氯醛是一种常用的有效的小儿镇静药物,但其半衰期长且服用后恶心、呕吐发生率较高;近年来水合氯醛的心脏毒性与神经毒性也越来越受到关注,故不推荐多次重复使用水合氯醛镇静[7-8]。因此,有必要探索更安全有效的联合用药镇静方案。本研究将咪达唑仑口服复合右美托咪定滴鼻镇静用于小儿MRI 检查,拟探讨该联合用药方案的安全性及有 效性。
1 资料与方法
1.1 一般资料
选择2019 年3 月—2019 年7 月于上海交通大学医学院附属上海儿童医学中心拟行MRI 检查且需要镇静的186例患儿作为研究对象,年龄3 ~8 岁,美国麻醉师协会(American Society of Anesthesiologists,ASA)分级Ⅰ~Ⅲ级。排除标准:存在水合氯醛、右美托咪定或咪达唑仑过敏史,严重肝肾功能不全,过去48 h 内使用过镇静催眠药物,过度肥胖即体质量指数(body mass index,BMI) ≥28 kg/m2,存在严重呼吸道感染或鼻腔卡他症状的患儿。采用随机、单盲、对照的方法,通过计算机模拟产生随机数,将患儿分为2 组,每组93 例,分别为口服咪达唑仑复合右美托咪定滴鼻组(咪达唑仑组)、口服水合氯醛复合右美托咪定滴鼻组(水合氯醛组)。研究通过上海交通大学医学院附属上海儿童医学中心伦理委员会的批准(批准号SCMCIRB-K2018110-2),获得患儿监护人签署的知情同意书。
1.2 镇静方法
嘱咐患儿镇静前夜晚睡2 h,早起1 h,镇静前常规禁食6 h,禁饮2 h。镇静当日由麻醉医师进行评估,包括一般资料、现病史、诊断、过敏史、ASA 分级等。患儿随机分配至咪达唑仑组或者水合氯醛组。依据患儿分组情况给予相应镇静药物;由镇静室的护士负责患儿用药并记录心率、血压、血氧饱和度的基础值。咪达唑仑组患儿先口服0.3 mg/kg 咪达唑仑糖浆(咪达唑仑与单糖浆1:1 混合;咪达唑仑注射液5 mg/mL,生产批号20180202,江苏恩华药业股份有限公司),再给予2 μg/kg 右美托咪定滴鼻(100 μg/mL,生产批号1710211,四川国瑞药业有限责任公司)。水合氯醛组患儿口服给予50 mg/kg 水合氯醛(药剂科自配,质量体积浓度10%,10 mL/支),超过10 mL者给予10 mL,再给予2 μg/kg 右美托咪定滴鼻。口服药物后,记录患儿对药物的接受程度(是否哭泣)。右美托咪定滴鼻时平均滴入两侧鼻腔,给药后平躺1 ~2 min 以达到最大程度的药物吸收。另一位护士专职负责记录患儿的各项监测值和进行镇静评分,同时记录镇静起效时间、MRI 检查时间、苏醒时间及可能的不良反应。Ramsay 镇静量表(表1)用来评估镇静深度,每10 min 1 次;评分≥5 分者视为达到深度镇静,可以进行MRI 检查,完成检查则认为镇静成功;用药30 min 后评分≤4 分者或者患儿在检查过程中苏醒无法完成检查,则认为镇静失败,该情况下建议家属择日再镇静或静脉麻醉下完成检查。患儿苏醒后观察其呼吸、循环、血氧饱和度、意识及按指令活动情况(表2);改良Alderete 评分≥9 分,准许患儿离开医院。

表1 Ramsay 镇静评分Tab 1 Ramsay sedation score

表2 改良Alderete 评分Tab 2 Modified Alderete score

Continued Tab
1.3 安全性及有效性评估
以患儿镇静后完成MRI 检查的成功率作为评价有效性的主要指标,以不良反应发生率作为评价安全性的主要指标。不良反应包括心率异常、血压异常、血氧饱和度降低及呕吐。心率变化低于或高于正常值20%视为心率异常,血压低于或高于正常值20%视为血压异常,血氧饱和度低于90%视为低氧[9]。
1.4 统计学方法
采用SPSS 25.0 软件进行统计学分析。不符合正态分布的定量资料用M(Q1,Q3)表示,采用秩和检验进行组间比较;符合正态分布的定量资料用x—±s 表示,采用t 检验进行组间比较。定性资料用n (%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 患儿一般情况比较
本研究共纳入186 例患儿,水合氯醛组93 例,咪达唑仑组93 例。2 组患儿一般资料见表3,组间年龄、性别、体质量、BMI 比较,差异无统计学意义。
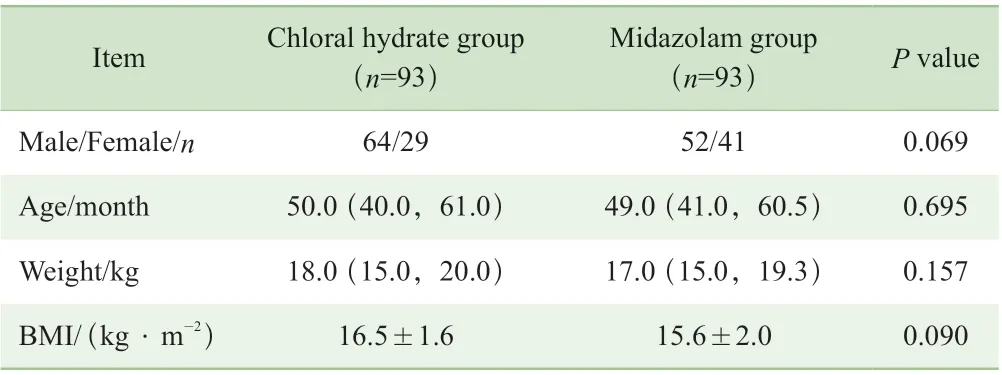
表3 患儿一般情况比较Tab 3 Comparison of baseline characteristics between the two groups
2.2 镇静安全性及有效性评估
水合氯醛组1 例患儿镇静失败,咪达唑仑组5 例患儿镇静失败,2 组镇静成功率差异无统计学意义(P=0.213)。水合氯醛组起效时间短于咪达唑仑组(P=0.000),但其苏醒时间和总镇静时间均明显长于咪达唑仑组(P=0.000,P=0.001),2 组之间差异有统计学意义。2 组MRI 检查时间差异无统计学意义(P=0.177)(表4)。

表4 镇静成功率及各项镇静时间比较Tab 4 Comparison of sedation success rate and sedation time
水合氯醛组出现9 例(9.7%)心动过缓,咪达唑仑组出现5 例(5.4%),2 组之间差异无统计学差异(P=0.266)。水合氯醛组低血压发生率高于咪达唑仑组(14.0% vs 3.2%),差异有统计学意义(P=0.009)。所有患儿血流动力学均稳定,未进行药物干预,通过加强监测,患儿苏醒后血压及心率均恢复至正常范围。2 组患儿均未发生血氧饱和度下降的情况。水合氯醛组1 例患儿出现呕吐,呕吐1 次,未予处理,之后未再出现呕吐;咪达唑仑组未出现呕吐。水合氯醛组21 例(22.6%)患儿给予口服药物时哭泣,咪达唑仑组仅有4 例(4.3%),2 组差异有统计学意义(P=0.000)。
3 讨论
儿童是一类特殊的医疗群体,难以像成人一样配合MRI 检查,常常需要镇静后才能完成检查。年龄对MRI检查的镇静成功率有较大影响,随着年龄增加,镇静成功率降低。大龄儿童的不合作仍然是MRI 检查中独特的挑战[10]。儿童镇静的药物较多,咪达唑仑是其中一种常见的镇静药物。咪达唑仑单独用于镇静检查成功率低,一般不作为常规药物,需要联合其他镇静药物以提高成功率[11-12]。咪达唑仑复合右美托咪定滴鼻能产生良好的中深度镇静效果。Li 等[13]颊黏膜给予咪达唑仑复合右美托咪定滴鼻用于自闭症患儿的CT 检查成功率达95%,未发生需要临床干预的呼吸抑制或血流动力紊乱。Cozzi 等[14]对108 例拟行MRI 检查的儿童使用0.5 mg/kg 咪达唑仑口服复合3 μg/kg 右美托咪定滴鼻镇静,其中91 例患儿完成检查,成功率达84%;该研究者认为咪达唑仑联合右美托咪定是一种安全有效的镇静方案,但该研究患儿年龄跨度较大,结论有待进一步证实。研究发现右美托咪定滴鼻镇静的有效剂量为1 ~2 μg/kg[15],高剂量右美托咪定可能引起心动过缓、呼吸抑制,但需要药物干预的较少[16]。因此,本研究通过0.3 mg/kg 咪达唑仑口服复合2 μg/kg 右美托咪定滴鼻用于小儿MRI 检查镇静,与传统水合氯醛复合右美托咪定的镇静方案对比,探讨前者联合用药方案的安全性及有 效性。
本研究发现水合氯醛组的镇静成功率为98.9%,略高于咪达唑仑组的94.6%,但差异无统计学意义。本研究的镇静成功率高于其他文献报道,可能与所实施的睡眠剥夺有关。大龄儿童睡眠剥夺联合使用右美托咪定能够产生良好的镇静效果[17]。咪达唑仑组镇静起效时间更长,但苏醒时间明显缩短,总镇静时间也短于水合氯醛组。右美托咪啶常见的不良反应是心动过缓。本研究2 组患儿均出现心动过缓,但差异无统计学意义,且患儿血流动力学均稳定,无需药物干预,苏醒后心率回升至正常范围。本研究中咪达唑仑组低血压发生率低于水合氯醛组,但2 组患儿的血压降低均为一过性降低,之后回升至正常范围,无需药物干预。有研究[18]显示咪达唑仑对血流动力学影响较小,用于镇静时安全性与右美托咪定相似。由于测量基础血压时患儿配合度低,且检查过程中缺少血压的连续监测,血压监测准确性较低,未来研究需要对其加强监测。研究过程中没有患者出现血氧饱和度下降的情况,这与既往文献认为右美托咪定对呼吸影响较小的研究结果一致[19-20]。 咪达唑仑注射液口感极苦,我们配制时混合单糖浆从而大大提升了口感,患儿耐受良好。与水合氯醛组比较,咪达唑仑组哭泣发生率明显降低,2 组间差异有统计学意义,且有1 例患儿口服水合氯醛后出现呕吐。考虑到不良反应的发生率一般均较低,因此有关不良反应研究需要进一步提高样本量。
本研究也有一些局限性:首先,口服给药无法实现完全双盲,采用第三方评价方式可尽可能减少主观偏倚;其次,缺少单纯水合氯醛或右美托咪定对照组,但以往有此类文献报道且使用单一镇静药物MRI 检查成功率低,考虑患者利益未设单一用药组;再次,患儿离院后随访缺乏,无法发现远期不良反应;最后,由于样本量有限,未设立不同年龄和不同药物剂量分组,研究结果仅能说明目前所选剂量的镇静药物组合是安全有效的,可能并非最佳剂量。
综上所述,0.3 mg/kg 咪达唑仑口服复合2 μg/kg 右美托咪定滴鼻可安全有效地用于3 ~8 岁儿童MRI 检查镇静。虽然该方案镇静起效时间较长,但苏醒时间明显短于水合氯醛复合右美托咪定,且未出现需要临床干预的血流动力学不稳定或血氧饱和度下降的情况,不失为小儿MRI 检查需要镇静时一个安全有效的联合用药 方案。
参·考·文·献
[1] Bailey MA, Saraswatula A, Dale G, et al. Paediatric sedation for imaging is safe and effective in a district general hospital[J]. Br J Radiol, 2016, 89(1061): 20150483.
[2] Stern KW, Gauvreau K, Geva T, et al. The impact of procedural sedation on diagnostic errors in pediatric echocardiography[J]. J Am Soc Echocardiogr, 2014, 27(9): 949-955.
[3] Ambi US, Joshi C, Ganeshnavar A, et al. Intranasal dexmedetomidine for paediatric sedation for diagnostic magnetic resonance imaging studies[J]. Indian J Anaesth, 2012, 56(6): 587-588.
[4] Tug A, Hanci A, Turk HS, et al. Comparison of two different intranasal doses of dexmedetomidine in children for magnetic resonance imaging sedation[J]. Paediatr Drugs, 2015, 17(6): 479-485.
[5] Delgado J, Toro R, Rascovsky S, et al. Chloral hydrate in pediatric magnetic resonance imaging: evaluation of a 10-year sedation experience administered by radiologists[J]. Pediatr Radiol, 2015, 45(1): 108-114.
[6] 卞勇, 姚莹, 王丹, 等. 水合氯醛复合右美托咪定滴鼻用于小儿核磁共振检查镇静的疗效及安全性评估[J]. 国际麻醉学与复苏杂志, 2015, 12(36):1080-1085.
[7] Kao SC, Adamson SD, Tatman LH, et al. A survey of post-discharge side effects of conscious sedation using chloral hydrate in pediatric CT and MR imaging[J]. Pediatr Radiol, 1999, 29(4): 287-290.
[8] Heistein LC, Ramaciotti C, Scott WA, et al. Chloral hydrate sedation for pediatric echocardiography: physiologic responses, adverse events, and risk factors[J]. Pediatrics, 2006, 117(3): E434-E441.
[9] Hartman ME, Cheifetz IM. Pediatric emergencies and resuscitation[M]//Kliegman RM, Stanton BF, St Geme JW, et al. Nelson textbook of pediatrics. 19th ed. Philadelphia: Elsevier Saunder, 2011: 279-296.
[10] 李波, 陈怡绮, 卞勇, 等. 小儿中深度镇静失败原因回顾性分析[J]. 国际麻醉学与复苏杂志, 2017, 38(4): 303-306.
[11] Majidinejad S, Taherian K, Esmailian M, et al. Oral midazolam-ketamine versus midazolam alone for procedural sedation of children undergoing computed tomography; a randomized clinical trial[J]. Emerg (Tehran), 2015, 3(2): 64-69.
[12] Stephen MC, Mathew J, Varghese AM, et al. A randomized controlled trial comparing intranasal midazolam and chloral hydrate for procedural sedation in children[J]. Otolaryngol Head Neck Surg, 2015, 153(6): 1042-1050.
[13] Li BL, Yuen VM, Zhang N, et al. Intranasal dexmedetomidine with and without buccal midazolam for procedural sedation in autistic children: a double-blind randomised controlled trial[J]. Lancet, 2017, 390: S26.
[14] Cozzi G, Monasta L, Maximova N, et al. Combination of intranasal dexmedetomidine and oral midazolam as sedation for pediatric MRI[J]. Paediatr Anaesth, 2017, 27(9): 976-977.
[15] Zhang WH, Wang ZX, Song XR, et al. Comparison of rescue techniques for failed chloral hydrate sedation for magnetic resonance imaging scans: additional chloral hydrate vs intranasal dexmedetomidine[J]. Paediatr Anaesth, 2016, 26(3): 273-279.
[16] Mason KP, Lönnqvist PA. Bradycardia in perspective-not all reductions in heart rate need immediate intervention[J]. Paediatr Anaesth, 2015, 25(1): 44-51.
[17] Tenney JR, Miller JW, Rose DF. Intranasal dexmedetomidine for sedation during magnetoencephalography[J]. J Clin Neurophysiol, 2019, 36(5): 371-374.
[18] Barends CR, Absalom A, van Minnen B, et al. Dexmedetomidine versus midazolam in procedural sedation. A systematic review of efficacy and safety[J]. PLoS One, 2017, 12(1): e0169525.
[19] Fantacci C, Fabrizio GC, Ferrara P, et al. Intranasal drug administration for procedural sedation in children admitted to pediatric Emergency Room[J]. Eur Rev Med Pharmacol Sci, 2018, 22(1): 217-222.
[20] Sulton C, McCracken C, Simon HK, et al. Pediatric procedural sedation using dexmedetomidine: a report from the pediatric sedation research consortium[J]. Hosp Pediatr, 2016, 6(9): 536-544.
