过氧化物酶体增殖激活物受体γ辅激活因子1α rs8192678位点单核苷酸多态性与非酒精性脂肪性肝病发病风险的关系
2020-09-28刘守胜孙宝凯辛永宁
张 青,刘守胜,孙宝凯,张 梅,辛永宁
青岛大学附属青岛市市立医院 a.感染性疾病科; b.感染性疾病与肝病研究室,山东 青岛 266011
非酒精性脂肪性肝病(NAFLD)是由肝脏内脂质堆积过多造成的一种病理结果,被认为是代谢综合征在肝脏中的表现[1]。最新一项包含了237项研究的Meta分析[2]显示亚洲NAFLD总患病率为29.62%。NAFLD已成为肝移植最常见的原因之一[3-4]。我国NAFLD发病率不断增加,一项Meta分析[5]显示其患病率已达29.2%。NAFLD是一种复杂的多因素疾病,涉及久坐、肥胖、不良的饮食习惯、肌肉减少、胰岛素抵抗、遗传易感性、肠道菌群等多种因素[6-9],与糖尿病、心血管疾病以及肾脏疾病等多种疾病密切相关[10-12]。NAFLD的遗传因素较复杂,现已经证明跨膜蛋白6超家族成员2、Patatin样磷酯酶结构域蛋白3、溶血脂酰肌醇酰基转移酶1与NAFLD的发生发展有密切关系,但其具体发病机制仍在不断的研究和完善中[13]。
过氧化物酶体增殖激活物受体γ辅激活因子1α(PPARGC1A)是一种蛋白质编码基因,通过转录形成辅助激活因子来调节参与能量代谢的基因[14]。其功能涉及胰岛素抵抗、脂质合成及转运、氧化应激以及炎症[15-18]。多项研究表明PPARGC1A单核苷酸多态性(SNP)在NAFLD发生发展过程中起着重要作用。2008年日本的一项研究[19]检测了PPARGC1A rs2290602 SNP,最先发现PPARGC1A SNP是NAFLD的遗传危险因素之一。2018年伊朗的一项研究[20]招募了288例超重或肥胖的女性,发现受试者总胆固醇(TC)和胰岛素水平与 PPARGC1A rs2970847的T等位基因携带呈正相关。此外,在PPARGC1A rs11290186中,不携带A等位基因的受试者具有较高的三酰基甘油和胰岛素水平。我国尚无PPARGC1A SNP与NAFLD关系的研究。本研究旨在探索PPARGC1A rs8192678 SNP与NAFLD的关联,探讨该位点SNP对NAFLD发生风险的影响,从而完善NAFLD的遗传学研究。
1 资料与方法
1.1 研究对象 选取2017年12月-2018年12月在青岛市市立医院就诊的NAFLD患者(NAFLD组)和健康体检者(对照组)。NAFLD由彩色超声仪进行诊断,其诊断标准符合《非酒精性脂肪性肝病诊疗指南》[21]。排除标准:有过量的饮酒史(男性饮酒折合乙醇量≥30 g/d,女性≥20 g/d);病毒性肝炎、自身免疫性肝炎、肝豆状核变性等可以引起脂肪肝的肝脏疾病;近期服用引起肝损伤的药物(如他莫昔芬、甲氨喋呤等),以及其他能引起脂肪肝的全身性疾病(如炎症性肠病、甲状腺功能减退症等)。
1.2 数据采集 在抽血前,获取受试者性别、年龄、身高、体质量等基本信息,并计算BMI。NAFLD组和对照组均在禁食12 h后于正中静脉抽取静脉血4 ml,并分到2个EDTA抗凝管中进行后续的研究:一管血液样本利用市立医院检验科的自动生化分析仪进行生化指标的检测,包括空腹血糖(FPG)、甘油三酯(TG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、游离脂肪酸(FFA)、TC、ALT、AST、GGT、ALP、TBil;一管血液样本存于-80 ℃冰箱内待提取DNA后进行基因型鉴定。
1.3 基因型鉴定 血液基因组DNA使用TIANGEN公司基因组纯化试剂盒并按照说明书进行DNA提取,放置于-20 ℃冰箱进行保存。PPARGC1A rs8192678位点SNP首先采用PCR扩增出含有待检SNP位点的目的片段,PCR上游引物:ACGTTGGATGTACTGAAATCACTGTCCCTC,下游引物:ACGTTGGATGAACAAGCACTTCGGTCATCC。首先94 ℃预变性5 min,之后进行45个循环的扩增反应,每次循环的程序为:94 ℃变性20 s,56 ℃退火30 s,72 ℃延伸1 min。PPARGC1A rs8192678的基因型及等位基因分布运用质谱检测(MALDI-TOF MS)的方法进行鉴定。
1.4 伦理学审查 本研究方案经由青岛市市立医院伦理委员会的审批[批号:2017临审字第20号(快)],所纳入受试者均签署了知情同意书。
1.5 统计学方法 采用SPSS 22.0统计软件进行数据分析。评价样本的群体性,采用χ2检验判断样本的基因型分布是否符合Hardy-Weinberg平衡法则。正态分布的计量资料用表示,两组间比较采用t检验;非正态分布的计量资料用M(P25~P75)表示,两组间比较采用Wilcoxon秩和检验。计数资料两组间比较采用χ2检验。采用二元logistic回归分析NAFLD发生的危险因素。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 本研究纳入NAFLD患者119例,其中女38例,男81例,平均年龄43岁;健康体检者213例,其中女77例,男136例,平均年龄44岁。两组性别、年龄比较差异无统计学意义(P值均>0.05)。与对照组相比,NAFLD组BMI、FPG、TC、TG、LDL、ALT、GGT水平较高,HDL水平较低,差异均有统计学意义(P值均<0.05)(表1)。
2.2 两组PPARGC1A rs8192678基因型及等位基因分布
基因测序分析后经χ2检验结果显示,两组PPARGC1A rs8192678的基因型分布均符合Hardy-Weinberg平衡定律(P值分别为0.905、0.934)。两组CC和CT基因型及C、T等位基因分布差异均无统计学意义(P值均>0.05)(表2)。二元logistic回归分析显示,PPARGC1A rs8192678位点CT基因型不是NAFLD发生的危险因素(比值比=0.951,95%可信区间:0.368~2.457,P=0.918)。
2.3 不同基因型受试者生化指标的比较 为进一步分析PPARGC1A rs8192678位点SNP与NAFLD相关指标的关系,分别在所有受试者、对照组及NAFLD组中比较不同基因型携带者各生化指标的差异。结果显示,在所有受试者及对照组中,CT与CC基因型各生化指标差异均无统计学意义(P值均>0.05)(表3、4);在NAFLD组中,CT基因型受试者GGT水平较高(P=0.020)(表5)。

表1 两组基线资料及生化指标比较

表2 两组受试者PPARGC1A rs8192678基因型及等位基因分布

表3 所有受试者中不同基因型携带者各生化指标比较

表4 对照组中不同基因型携带者各生化指标比较
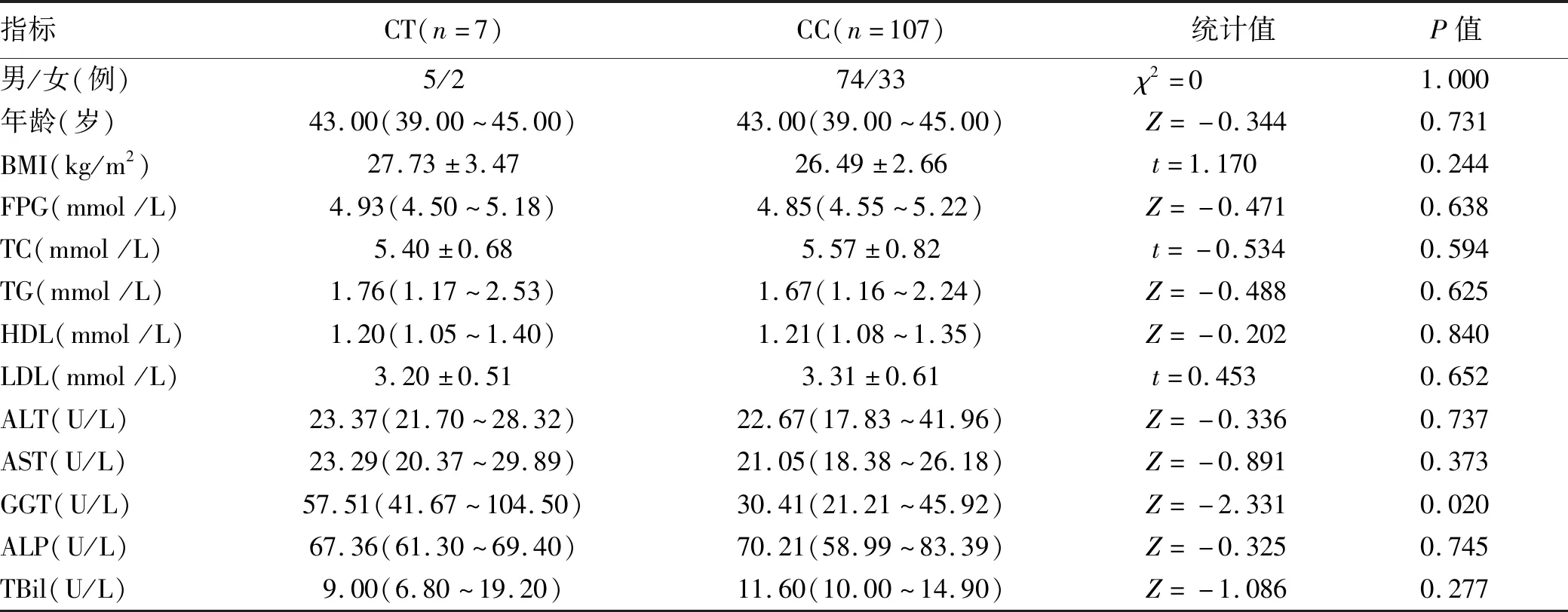
表5 NAFLD组不同基因型携带者各生化指标比较
3 讨论
NAFLD是一种环境与遗传共同作用的代谢性疾病,以往研究[13]已经显示多种基因在NAFLD的发生发展中起着非常重要的作用,参与脂质合成、分泌,载脂蛋白的合成与分解,胰岛素抵抗,氧化应激等多种生理病理过程。本研究着眼于与能量代谢密切相关的PPARGC1A,研究该基因rs8192678 SNP对NAFLD的影响。
Piccinin等[22]发现PPARGC1A在NAFLD中表达降低,且PPARGC1A的表达与NAFLD严重程度呈负相关。但PPARGC1A rs8192678 SNP在NAFLD中的意义尚有争议。PPARGC1A rs8192678位点的突变发生于外显子区域,导致PPARGC1A编码蛋白的第482位氨基酸由甘氨酸(Gly)变为丝氨酸(Ser)。有研究[23]显示PPARGC1A rs8192678导致Gly482Ser,但不影响PPARGC1A蛋白的功能完整性。而Besse-Patin等[24]研究显示PPARGC1A rs8192678位点改变会导致PPARG1A蛋白的半衰期缩短,PPARGC1A减少会促进小鼠NAFLD的发生。另一项在H4IIE细胞脂质堆积模型中的研究[25]显示PPARGC1A Gly482Ser会减弱由PPARGC1A过表达引起的肝细胞脂质堆积减少,促进NAFLD发生。本研究对NAFLD患者和健康人群的PPARGC1A rs8192678 SNP进行检测,发现在两组中该基因位点的SNP无显著性差异,可能是由于本研究受试者均为青岛地区汉族人群,人种及环境单一,故需要进一步扩大样本,进行多中心研究。
本研究结果显示在NAFLD组中,CT基因型携带者相比于CC基因型携带者血清中GGT水平更高。GGT已被证明与NAFLD相关。Kozakova等[26]研究显示血清GGT可能与脂肪肝和早期动脉粥样硬化的发生有关。GGT水平还与代谢综合征、肥胖相关。一项包含5404例上海社区人员的横断面研究[27]显示,在中国成年人中,GGT与代谢综合征存在显著而独立的相关性,且发生代谢综合征的风险以GGT剂量依赖性方式增加;Botton等[28]对8~17岁儿童的研究显示,超重及腹部脂肪增加与GGT水平升高有关。NAFLD被认为是代谢综合征在肝脏中的表现,肥胖亦是其重要的发病因素之一,在本研究中,PPARGC1A rs8192678 SNP可能导致NAFLD患者血清GGT改变,提示PPARGC1A rs8192678可能通过GGT影响NAFLD的发病风险,值得更进一步的探索。
综上所述,PPARGC1A rs8192678 SNP未增加NAFLD的发病风险,但在NAFLD患者中会提高血清GGT水平。本研究用超声检查来确定NAFLD,缺乏肝活检,且仅对血液标本中的基因及生化指标进行了检测,尚未对肝组织标本进行检测。下一步的研究需要招募更多的受试者,增加对心血管相关指标的检测并完善肝活组织检查,探索相关机制,进一步研究PPARGC1A SNP对NAFLD的影响。
