3D腹腔镜与2D腹腔镜在儿童食管裂孔疝修补及胃底折叠术中的应用对比
2020-09-18张雁冰高红强刘朝阳
张雁冰 张 甜 高红强 刘朝阳 尹 强
儿童食管裂孔疝多由先天性因素所致,大多需手术治疗。近年来,腹腔镜下食管裂孔疝修补+胃底折叠术逐步变成医治儿童食管裂孔疝的首选术式[1]。随着腹腔镜手术经验的积累,腹腔镜手术的缺点也逐渐受到关注,其中最突出的是二维(2-dimensional,2D)画面缺乏景深感,且空间定位不足,导致术中操作失误和重复动作增加,而三维(3-dimensional,3D)腹腔镜正好弥补了2D腹腔镜的上述不足,提高了手术效率[2,3]。在临床应用方面,3D腹腔镜已被相关临床实验证实具备诸多优势[4-6]。本研究对儿童食管裂孔疝修补及胃底折叠术中2D腹腔镜与3D腹腔镜的应用效果展开评估。
材料与方法
一、临床资料
对2016年1月至2019年6月间在湖南省儿童医院普外一科接受腹腔镜辅助食管裂孔疝修补与胃底折叠术治疗患儿的临床资料进行回顾性分析,共纳入38例。纳入标准:年龄>1岁;明确诊断食管裂孔疝。排除标准:食管裂孔疝复发;术中需要使用补片修补食管裂孔。按照术中使用腔镜种类的不同分为3D组(17例)和2D组(21例)。两组基本资料差异无统计学意义(P>0.05),见表1。
二、研究方法
(一)手术方法
2D组所应用的腹腔镜系统为STORZ(德国),术者不要求佩戴眼镜;3D组所应用的腹腔镜系统与2D组相同,但术者需佩戴特制3D眼镜。2组手术均由同一术者主刀完成。实施全身麻醉后,均采用经典四孔法:脐轮上穿刺Trocar(2D组Trocar直径为5 mm,3D组Trocar直径为10 mm),气腹压力8~12 mmHg,置入腹腔镜观察食管裂孔,于右肋缘下锁骨中线及腋前线分别置入5 mm Trocar,左侧脐上2 cm锁骨中线的Trocar于剑突下3 cm处腹壁经食管裂孔上缘和肝圆韧带予以2-0线悬吊左半肝。借助无损伤钳通过左侧的Trocar(5 mm)抓持胃底,同时将疝内容物牵拉至左下方,充分暴露食管裂孔。使用超声刀进行分离操作,先完全游离双侧膈肌脚和食管之间的连接,再构建“食管后窗”,用粗绳经 “食管后窗”牵拉食管下段显露食管后方,完全切除疝囊。进入纵隔后将食管周围的粘连完全松解,至腹段食管(≥3 cm)无张力回纳入腹腔时为止。将食管裂孔疝裂孔右侧膈肌脚及其反折部予2-0不可吸收线缝合,松紧适度,经过食管后窗用无损伤钳抓取胃底大弯外缘胃壁浆肌层,根据术中情况决定是否松解脾胃韧带,拉至食管右方,用3-0不可吸收线对胃底与左侧胃壁实施间断缝合,共3针,以此方式结束整个胃底360°折叠操作。
(二)观察指标及随访
记录手术总时间、术中出血量、术后随访情况(包括呕吐、吞咽障碍、气胸、腹部感染和纵隔感染等在内的术后并发症)。术后12个月通过门诊随访,掌握相关并发症与复发状况。
三、统计学方法
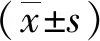
结 果
3D组患者总手术时间明显缩短,且术中出血更少(P<0.05),两组术后住院时间及术后并发症发生率差异无统计学意义(P>0.05)。术后随访过程中两组各有2例进食后出现轻度呕吐,调整进食方案后(流质饮食为主,逐渐进食团块状食物)1个月左右呕吐症状消失。两组均无一例消化道穿孔、胸腹腔感染以及气胸等其他严重并发症,详见表2。

表2 3D腹腔镜组和2D腹腔镜组各手术指标对比Table 2 Comparison of observation items between 3D and 2D laparoscopic groups组别手术时间(x±s,min)术中出血量(x±s,mL)住院时间(x±s,d)并发症发生率(%)3D组82.4±17.711.6±8.25.8±1.711.72D组102.1±20.419.2±6.56.4±2.39.5P值0.0310.0430.7540.087
讨 论
3D腹腔镜系统在临床领域的首次应用虽可追溯至上世纪90年代早期,但受制于设备和当时的技术条件未得到广泛应用,直到2010年,新一代的3D腹腔镜系统才再次进入临床并得到认可。国内3D腹腔镜的报道集中于成人普外科、泌尿外科及妇科等疾病的治疗并取得了显著效果,也已经完成3D腹腔镜应用专家共识并予以推荐[5,6]。通过文献检索尚未发现3D腹腔镜应用于儿童食管裂孔疝手术的报道,因此我们进行了本次研究。
2D腹腔镜仅有一个摄像头,其显示的是平面图像,缺少景深和空间距离感。术者在操作时需要不断地尝试或重复动作以获得距离感和方向感,尤其是在腹腔镜下进行分离、缝合或打结等精细操作时[7]。因此早期腹腔镜手术时间较开腹手术长,而长时间的手术容易导致术者视觉疲劳。要想获得腹腔镜下熟练的操作,必须通过长时间的训练,形成学习曲线,而这在一定程度上限制了腹腔镜技术的开展。3D腹腔镜的出现恰好打破了这一僵局,它采用人眼产生立体视觉的原理,最终呈现出高清且具有立体视觉的图像,使术者有开放手术的感觉,可直接减少镜下过多重复的动作及误损伤的可能性。因此,3D腹腔镜的直接优势是手术持续时间、术中出血量及术中并发症的减少,其他皆为间接优势。
本研究结果显示,相对于2D腹腔镜组,3D腹腔镜组在总手术时间更短、术中出血量更少的情况下,住院时间未见显著增加(P>0.05)。食管裂孔疝修补+胃底折叠术被认为是复杂的腹腔镜手术之一,具体体现在: ①手术区域狭小,且周围血管、神经分布紧密。主要操作区域位于胃-食管连接处双侧膈肌脚周围,其前方由左肝覆盖,后方为脊柱和腹主动脉,右侧为肝尾叶和下腔静脉,左侧为脾脏。此外,该操作围绕食管裂孔分布区双侧膈下动脉、迷走神经,因此术中误损伤和能量器械的副损伤概率较其他手术增加。②分离操作多,操作范围广(包括腹腔和下纵隔)。食管裂孔疝的手术目标要求:充分游离食管,保证腹段食管>3 cm,为此绝大多数病例均需在纵隔内游离食管;彻底离断食管和双侧膈肌脚之间的疝囊,尽可能切除纵隔内的疝囊。③解剖结构辨认困难。部分滑疝或混合型疝的疝囊显著增厚,导致在分离过程中与食管及胃壁分辨困难,有可能导致穿孔。而在食管后窗的建立过程中,增厚的疝囊与迷走神经粘连紧密,极有可能离断迷走神经。④腹腔镜下缝合多,耗时长。为达到手术设计的目标,需要缝合食管裂孔(缝合双侧膈肌脚),缝合食管与膈肌,并做好胃底折叠。
有报道显示3D腹腔镜肝切除相较2D腹腔镜手术用时大幅减少,本研究结果与已有报道一致[8]。而Hanna等[9]研究发现,3D腹腔镜辅助和2D腹腔镜辅助下行胆囊切除治疗的病人手术时间及疗效方面无显著差异,可能是因为3D腹腔镜应用过程复杂、需要精细的操作过程中才能体现其优势。
本研究中两组均有2例出现术后早期进食哽咽感,予以保守治疗现已恢复正常。进食有哽咽感与食管裂孔疝复发是常见的并发症,而食管裂孔修补的松紧度不当是其主要原因,缝合过紧容易导致吞咽困难,反之容易导致复发[10-12]。我们的经验是在完成食管裂孔修补后间隙内可顺利通过5 mm器械为宜,而3D腹腔镜在判断缝合的松紧度上并无显著优势。
本研究虽然基本达到了预期的研究目的,但存在以下局限性:首先,病例的选择上有意识地排除了婴儿、需要使用补片的患儿和复发的患儿,主要是考虑到婴儿的腹腔容积小、肝脏相对较大、手术操作空间狭小;3D腹腔镜的镜头直径是2D腹腔镜的2倍,在纵隔内分离食管时器械的“筷子效应”显著增加,使得手术操作困难。此外,复发病例因为粘连严重分离时间过长,使得食管裂孔疝分离和修补裂孔时间过长[13]。但是上述病例均较为罕见,不具有代表性,笔者拟在后续的研究中集中分析特殊病例。
综上所述,3D腹腔镜因其类似开放手术的立体图像,可显著减少镜下的重复动作,降低误损误伤的可能性,与2D腹腔镜相比可显著缩短手术时间和术中出血量[14,15]。
