Fenton 氧化-混凝沉淀处理电镀废水中重金属镍的研究①
2020-09-14蔡文良谢艳云
蔡文良, 谢艳云
(重庆水利电力职业技术学院,重庆402160)
我国电镀企业规模小、数量多、废水排放量大[1-3]。由于镍质地坚硬且具有耐腐蚀等优点,在电镀行业中被广泛使用;电镀废水中重金属镍和有机物浓度都较高,去除困难[4-6]。 Fenton 氧化是一项广泛使用的氧化技术,反应迅速、操作过程简单,无二次污染物质产生[7-9];混凝沉淀法可使水中胶体颗粒混凝进而沉淀去除[10]。 本文以某电镀厂废水处理站原水为对象,利用Fenton 氧化除镍后再利用混凝沉淀进行深度处理,研究了各工艺条件对废水处理效果的影响。
1 实验材料及方法
1.1 实验用水
实验用废水为某电镀厂废水处理站的原水,废水水质如表1 所示。

表1 某电镀厂废水水质
1.2 实验方法
取电镀厂含镍废水100 mL,用氢氧化钠调节废水pH 值后,加入Fenton 试剂(H2O2和FeSO4·7H2O),用磁力搅拌器进行搅拌,反应后再以氢氧化钠调节pH值,静置一段时间后取上清液,用原子吸收光谱仪测定上清液中的总镍含量。
2 实验结果和讨论
2.1 Fenton 氧化研究
2.1.1 H2O2投加量对镍去除效果的影响
在6 个烧杯中分别加入100 mL 废水水样,用氢氧化钠调节pH=5,设置H2O2浓度分别为0.5,1.0,1.5,2.0,2.5,3.0 mmoL/L,并按照FeSO4/H2O2(摩尔比)=1加入FeSO4,用磁力搅拌器搅拌,反应时间90 min,反应后再用氢氧化钠调节pH =9 ~12,沉淀30 min 后取上清液,用原子吸收光谱仪测定其中总镍含量。 实验结果如图1 所示。
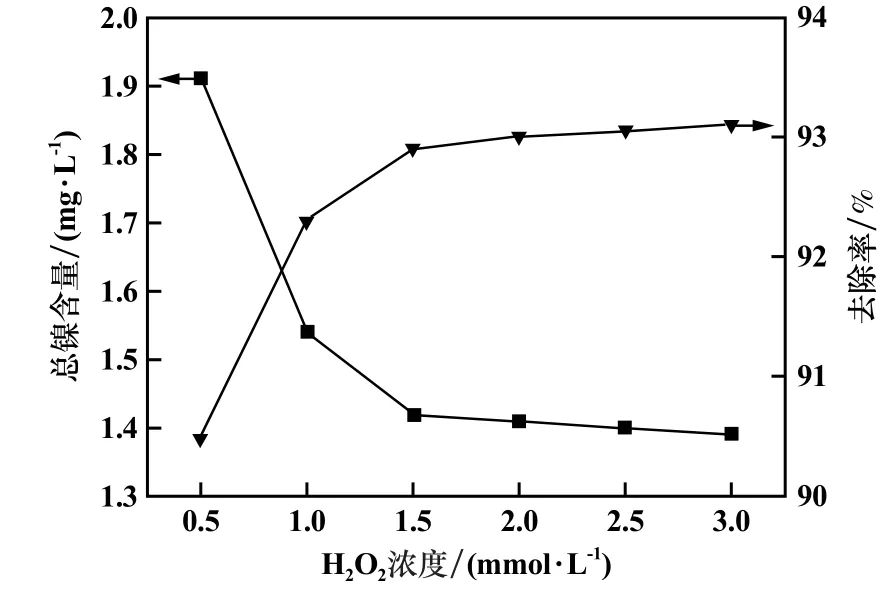
图1 H2O2 浓度对去除总镍的影响
由图1 可知,当H2O2浓度较低时,随着H2O2浓度增加,上清液中残留总镍含量逐渐减少,去除率不断增大;当H2O2浓度为1.5 mmoL/L 时,镍去除率达到92.9%;此后再继续增加H2O2浓度,镍去除率不再明显增加。 H2O2投加量过大,反而会消耗反应系统中的羟基自由基,对镍去除效果不再有增益,从反应效果以及经济成本综合考虑,选择H2O2投加量为1.5 mmoL/L。
2.1.2 FeSO4/H2O2摩尔比对镍去除效果的影响
固定H2O2投加量为1.5 mmoL/L,以不同FeSO4加入量调整FeSO4/H2O2摩尔比,其他条件不变,FeSO4/H2O2摩尔比对镍去除效果的影响如图2 所示。由图2 可知,在FeSO4/H2O2摩尔比为0.05~0.5 时,上清液中残余镍浓度逐渐下降,对镍的去除率不断升高;随着FeSO4/H2O2摩尔比增加到0.5 ~2 时,上清液中镍浓度上升,去除率明显下降。 这是因为当反应系统中FeSO4较少时,催化H2O2分解的速度较慢,随着FeSO4加入量增加,反应速度增加,对镍的去除效果加大;FeSO4继续增加,过多的Fe2+会与羟基自由基反应生成Fe3+,使羟基自由基被消耗,镍去除率下降。 综合考虑,选择FeSO4/H2O2摩尔比为0.2~0.5。

图2 FeSO4/H2O2(摩尔比)对去除总镍的影响
2.1.3 初始pH 值对镍去除效果的影响
在推进地下水超采治理试点工作中,始终牢牢把握五条基本原则:一是政府引导、全民行动,发挥好政府和群众两个积极性;二是规划统领、科学治理,年度实施方案与中长期规划有机衔接,集中连片规模实施,务求治理一片、见效一片、巩固一片;三是创新机制、示范带动,探索建立地下水超采治理的有效途径,力求取得可示范、可复制、可推广的经验;四是因地制宜、积极稳妥,根据实际情况,科学确定治理模式和工程规模;五是竞争立项、绩效考核,依据项目前期工作和压采效果择优实施,严格把关、严格奖惩。
固定FeSO4/H2O2摩尔比为0.5,其他条件不变,初始pH 值对镍去除效果的影响如图3 所示。 由图可知,随着pH 值升高,镍去除率逐渐增加,在pH =4 时去除率达到最大;pH 值再继续增加,镍去除率则快速下降。 这是因为羟基自由基主要在Fe2+的催化下生成,而pH 值影响反应系统中Fe2+与Fe3+间的平衡关系,pH 值过低时,溶液中大量存在H+,阻碍Fe2+的生成,不足以催化H2O2产生羟基自由基,而pH 值过高,Fe2+与氢氧根形成沉淀,难以达到催化效果。 因此选择初始pH=4。

图3 初始pH 值对去除总镍的影响
2.1.4 反应时间对镍去除效果的影响
初始pH=4,其他条件不变,反应时间对镍去除效果的影响如图4 所示。 随着反应时间增加,上清液中残留镍快速下降;当反应时间超过90 min 后,去除率变化不再明显。 因此,反应时间选择90 min。

图4 反应时间对去除总镍的影响
2.1.5 Fenton 氧化综合实验
根据Fenton 氧化单因素实验结果,配合正交实验及结果,确定Fenton 氧化工艺最佳条件为:H2O2投加量2 mmoL/L,FeSO4/H2O2摩尔比0.6,初始pH 值5,反应时间80 min。 在最佳工艺条件下处理废水后,出水水中总镍含量1.19 mg/L,镍去除率94.1%。 虽然Fenton氧化工艺能去除废水中大部分镍,但仍不满足《电镀污染物排放标准》(GB21900—2008 )表Ⅲ要求。
2.2 混凝沉淀研究
Fenton 氧化工艺可以将废水中的大部分镍去除,但出水中的镍浓度依然超过0.1 mg/L 的排放标准,因此还需进一步深度处理。 本文以PAC 为混凝剂,研究其深度处理含镍废水效果。
2.2.1 pH 值对混凝沉淀的影响
在9 个烧杯中分别加入经Fenton 氧化最佳条件下反应所得废水水样100 mL,分别调节pH 值为4,5,6,7,8,9,10,11,12,加入PAC 10 mg/L,用磁力搅拌器搅拌,反应20 min 后加入助凝剂PAM 10 mg/L,继续搅拌反应20 min 后静置90 min,取上清液测定总镍含量,初始pH 值对混凝沉淀效果的影响如图5 所示。由图可知,在pH 值4 ~7 范围内,镍去除率快速增加;在pH=7 时,镍去除率达到99.6%;pH>7 后,镍去除率没有明显变化。 因此,确定混凝沉淀的pH 值为7。
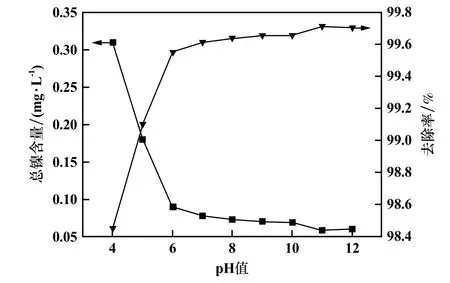
图5 混凝沉淀pH 值对总镍去除率的影响
2.2.2 PAC 用量对混凝沉淀的影响
pH 值为7,其他条件不变,PAC 用量对混凝沉淀的影响如图6 所示。 由图可知,随着PAC 投加量增加,上清液中镍含量先快速减少之后缓慢波动;在投加量为0~12 mg/L 时,随着PAC 投加量增加,镍去除率快速增加;PAC 用量为12 mg/L 时,镍去除率达到99.8%;再继续增加PAC 投加量,去除率缓慢波动。 因此确定PAC 投加量为12 mg/L。2.2.3 混凝时间对混凝沉淀的影响

图6 PAC 用量对去除总镍的影响
固定PAC 用量为12 mg/L, 其他条件不变,混凝时间对混凝沉淀的影响如图7 所示。 由图可见,随着混凝时间增加,镍去除率先上升后下降;混凝时间为10 min 时,去除率最高,达到99.7%。 因此确定混凝时间为10 min。

图7 混凝时间对去除总镍的影响
2.2.4 沉降时间对混凝沉淀的影响
固定混凝时间为10 min,其他条件不变,沉降时间对混凝沉淀的影响如图8 所示。 由图可知,随着沉降时间增加,镍去除率逐渐升高,沉降时间60 min 时,镍去除率达到最大,为99.7%。 因此选择沉降时间为60 min。
2.2.5 助凝剂用量对混凝沉淀的影响

图8 沉降时间对去除总镍的影响
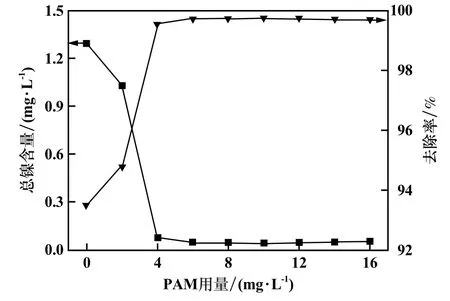
图9 PAM 用量对去除总镍的影响
固定沉降时间为60 min,其他条件不变,助凝剂PAM 用量对混凝沉淀的影响如图9 所示。由图可见,随着PAM 用量增加,镍去除率先快速下降,在PAM 用量为6 mg/L 时,镍去除率最高,为99.7%;之后再增加PAM 用量,去除率基本无变化。 因此确定助凝剂PAM用量为6 mg/L。
2.2.6 混凝沉淀综合实验
根据混凝沉淀工艺单因素实验结果,并结合正交实验及结果,确定混凝沉淀工艺最佳条件为:pH =9,PAC 用量12 mg/L,混凝时间12 min,助凝剂用量6 mg/L,沉降时间60 min。 在最佳工艺条件下,废水处理后水中总镍含量为0.029 mg/L,镍去除率为99.8%,出水满足《电镀污染物排放标准》(GB21900—2008)表Ⅲ要求。
3 结 论
1) Fenton 氧化反应的最佳实验条件为:H2O2投加量2 mmoL/L,FeSO4/H2O2摩尔比0.6,初始pH =5,反应时间80 min。 最佳工艺条件下处理废水,出水总镍含量为1.19 mg/L,镍去除率为94.1%。
2) 电镀废水经Fenton 氧化最佳工艺条件处理后,进行混凝沉淀反应,最佳条件为:pH =9,PAC 用量12 mg/L,混凝时间12 min,助凝剂用量6 mg/L,沉降时间60 min。 最佳工艺条件下处理废水,出水总镍含量为0.029 mg/L,镍去除率为99.8%。
3) 应用Fenton 氧化-混凝沉淀工艺处理该电镀厂废水,有效去除了废水中的镍,出水水质满足《电镀污染物排放标准》(GB21900—2008 )表Ⅲ要求。
