头孢呋辛酯在丙酮溶液中的降解动力学研究
2020-09-10张哲凡刘宝树韩康张军立孙华
张哲凡 刘宝树 韩康 张军立 孙华
摘 要:为了研究头孢呋辛酯丙酮溶液的稳定性,应用高效液相色谱,采用单因素方式考察初始溶液pH值、温度、氧化剂种类等条件下,头孢呋辛酯在溶液中的含量随时间的变化规律,依据化学反应动力学方法建立得到了头孢呋辛酯在不同条件下的降解反应动力学模型,回归得到了模型参数、预测半衰期(t1/2)。利用Materials Studio模拟软件从分子尺度对头孢呋辛酯的降解机理进行了分析。结果表明:头孢呋辛酯丙酮溶液的降解符合一级反应动力学;pH值<9.54时头孢呋辛酯丙酮溶液基本稳定,pH值≥9.54时其化学稳定性变差,随着pH值的增大降解速率迅速加快、溶液颜色加深;头孢呋辛酯丙酮溶液的化学稳定性随温度的升高而变差。研究结果可为相关产品的生产过程、结晶工艺设计、存储和应用提供数据支撑。
关键词:化学动力学;高效液相色谱;头孢呋辛酯;稳定性;降解
中图分类号:TQ465.9;R978.1 文献标识码:A
文章编号:1008-1542(2020)04-0341-08
doi:10.7535/hbkd.2020yx04007
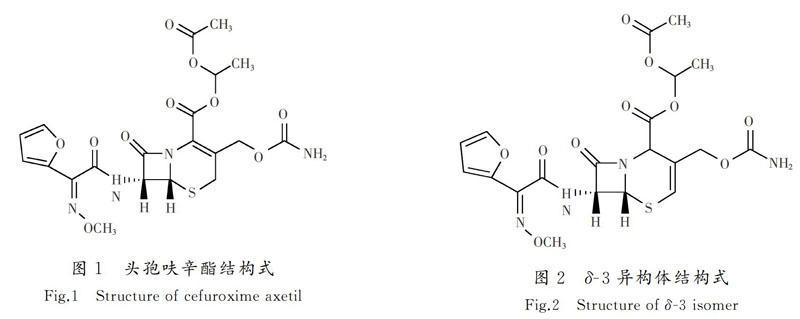
头孢呋辛酯,化学名为(6R,7R)-7-[2-呋喃基(甲氧亚氨基)乙酰氨基]-3-氨基甲酰氧甲基-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-羧酸,1-乙酰氧基乙酯,CAS No:6544-07-6,结构式见图1。头孢呋辛酯易溶于丙酮,略溶于甲醇和乙醇,微溶于乙醚,不溶于水,呈白色或类白色粉末,几乎无臭[1]。作为头孢呋辛的前体药物,头孢呋辛酯在酯酶作用下水解可以发挥抗菌疗效,具有广谱、抗菌性强、疗效高、副作用小等优点。目前临床上主要用于治疗由感染引起的疾病,如呼吸道感染[2]、淋病和尿道感染等[3]。
头孢呋辛酯主要成分是一对非对映异构体[4],称为δ-2异构体;其他杂质多为成对非对映异构体,其中主要杂质为δ-3异构体,可能来源于原料、合成生产过程及储存运输中,结构式见图2。由构效关系可知,δ-3异构体无生物活性,所以要降低其含量以提高药物质量。
有研究表明,头孢菌素发生碱水解或胺解时,通常会生成以7位侧链为主的降解产物[5]。头孢呋辛酯也有类似性质,碱性条件会加速其降解。有学者证实:头孢呋辛酯对光、热和水分比较敏感[6],易发生异构化反应及β-内酰胺环开环[7-8],侧链易水解,紫外灯照射24 h会产生头孢呋辛酯E异构体。
已有文献采用HPLC法研究了头孢呋辛酯水溶液在254 nm下的光致异构化动力学,结果表明,整体降解是烷氧基亚氨基的异构化与β-内酰胺环的光解之间竞争的结果[9]。在有关头孢呋辛酯溶液稳定性的研究中发现:头孢呋辛酯溶液需在配置3 h内使用,否则会产生更多的δ-3异构体;温度会影响溶液的稳定性,温度越高,稳定性越差;样品溶液是否在其稳定性范围内进行实验会影响最终的实验结果[10]。文献[11]和文献[12]报道了运用LC-MS确定原料中所含的8个未知杂质;还有学者运用HPLC研究了头孢呋辛酯原料药的成分,测定了其含量及高分子聚合物的含量等[13-14]。
药物的化学、物理和生物学3部分基本涵盖了药物的稳定性内容。药物的稳定性见表1。药物的内在结构和客观的外界环境等均会对药物的稳定性产生影响,有学者[15-17]认为可以采用化学反应动力学方法研究药物的稳定性,建立化学反应过程中反应速率与时间的关系,研究影响药物降解的因素并探讨药物的降解机理以及预测药物制剂的有效期等。在研究药物稳定性中,药物有效期通常是指药物降解10%所需的时间,以t0.9表示。
本文拟通过HPLC分别考察溶液初始pH值、温度及不同氧化剂对头孢呋辛酯稳定性的影响,得到各个因素下的降解动力学方程,计算其表观速率常数,解析不同处理条件下头孢呋辛酯的降解规律,为准确测定其浓度或含量、处方设计以及储存运输条件提供科学支撑,指导头孢呋辛酯结晶工艺的研究。
1 实验部分
1.1 材料
实验所用头孢呋辛酯经HPLC分析,其纯度≥96.77%;甲醇为色谱纯;其他试剂均为分析纯。
1.2 装置
实验降解装置见图3,主要由试管、温度计、恒温水浴槽及泡沫板组成。
1.3 色谱条件
依据ChP2015版。
1.4 实验过程
准确称量1.000 0 g原料于试管中,向其加入10 mL丙酮并密封好,配制初始浓度c0=0.195 9 mol/L的头孢呋辛酯丙酮溶液,置于恒温水浴槽中水浴,向其緩慢滴加稀释后的酸或碱,用pH计检测pH值(探究氧化剂对其降解影响时需向溶液中再滴加一定量的氧化剂)。用移液枪定时取样,先加甲醇,再用流动相稀释并定容至25 mL,0.45 μm有机膜过滤,得到0 h样品。借助HPLC分析该条件下头孢呋辛酯的含量,连续追踪40 h内的变化趋势。
1.5 浓度计算方法
依据物质组分的含量与其峰面积成正比来计算不同时刻的取样浓度,采用式(1)和式(2)进行计算。
2 结果与讨论
2.1 初始pH值对头孢呋辛酯降解的影响
在初始浓度c0=0.195 9 mol/L、温度T=298.15 K条件下,头孢呋辛酯随pH值变化的降解规律如图4所示。从图4可知:头孢呋辛酯丙酮溶液在pH值<9.54时比较稳定,P值基本维持不变,表明该条件下溶液几乎不发生降解;pH值=9.54,P值开始减小,表明该条件下溶液开始发生降解;pH值≥10.76,P值骤降,表明该条件下溶液的降解速率加快,其降解速率远大于pH值<10.76条件下的降解速率。因此,pH值≥9.54条件下液体药会失去原有疗效,甚至增加药物毒性。可见在丙酮中提纯原料过程中须保证pH值<9.54,否则会引入更多杂质。
以时间t对-ln c/c0作图,头孢呋辛酯残留浓度随时间变化的降解规律如图5所示。斜率为反应速率常数k,依次为k9.54=0.012 76 h-1,k10.76=0.015 25 h-1和k11.23=0.031 84 h-1。由图5可知:在实验所考察的温度和pH值范围内,头孢呋辛酯的降解基本表现为一级反应,即降解速率与浓度的一次方成正比;随着pH值的升高k值显著增大,即碱性越强降解速率越快。
pH值对头孢呋辛酯降解速率常数k和t0.9的影响如图6所示。由图6可知,碱性越强,头孢呋辛酯丙酮溶液的有效期越短。
图7是初始溶液pH值=11.23时不同时刻的降解液相图,经HPLC检测可知,在碱性条件下引入新的杂质峰,δ-3杂质峰组分的量随时间的延长逐渐变多。目前普遍认为双键异构是C-3位上的氢受到碱进攻而脱落;双键发生重排,从2,3位移至3,4位[18-19]。
降解体系的颜色可体现pH值对头孢呋辛酯降解的快慢。初始溶液pH值<9.54,溶液呈现淡黄色;pH值>9.54,溶液颜色随pH值的增大逐渐加深,呈现深红棕色。
2.2 温度对头孢呋辛酯降解的影响
选择初始浓度c0=0.195 9 mol/L,pH值=5.90~11.23,研究头孢呋辛酯丙酮溶液随温度变化的降解规律。首先在318.15 K,pH值=5.90和7.24条件下进行实验,溶液浓度随时间的变化如图8所示。
由图8可知,头孢呋辛酯丙酮溶液在40 h内比较稳定,溶液依然呈现出透明的淡黄色。因此,没有进一步研究278.15 K、酸性条件下头孢呋辛酯在丙酮中的降解规律。以初始浓度c0=0.195 9 mol/L,pH值=11.23为条件,研究了温度对头孢呋辛酯降解速率常数k的影响,结果见图9。由图9可知:随着温度不断升高,头孢呋辛酯变得越来越不稳定,其降解速率常数lg k呈指数上升,表明头孢呋辛酯在该条件下的降解速率比在碱性或加热条件下更大。因此,在头孢呋辛酯的生产过程和工艺设计中,须避免溶液处于高温环境,否则药物在短时间内会产生更多的杂质。
将pH值=11.23下的降解速率常数k与温度的关系用Arrhenius方程进行拟合,得到该条件下降解反应的表观活化能Ea,约为19.79 kJ/mol。
同样,降解体系的颜色体现了温度对头孢呋辛酯降解速率的快慢。相同pH值下,随着温度的升高,降解体系的颜色逐渐加深,由浅红棕色到深红棕色,最终变为黑红色。
2.3 氧化剂种类对头孢呋辛酯降解的影响
初始浓度不同的头孢呋辛酯在H2O2的作用下几乎不会降解(见图10),而在
KMnO4和四水过硼酸钠的作用下,会发生明显降解,如图11、图12所示。其中KMnO4的降解作用更为明显。
3 降解机理探析
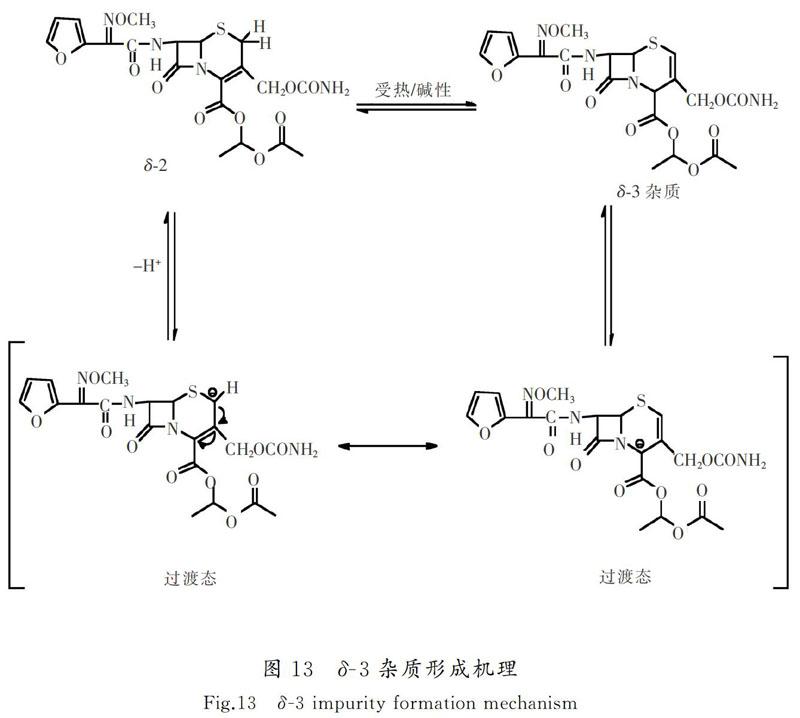
依据头孢呋辛酯丙酮溶液在碱性条件下的液相图可以看出:出现了2个新的杂质峰,δ-3杂质含量变多,相对地δ-2异构体含量减少。因此,在该条件下部分δ-2异构体转化为δ-3杂质。研究[18-19]表明头孢呋辛酯在碱性条件下会发生双键重排,过程机理如图13所示,但没有说明具体pH值。因此,应用MS中的DMol3模拟δ-2异构体转化为δ-3杂质的机理。
过渡态理论是1935年由A.G.埃文斯和M.波拉尼提出的,是解释反应物和生成物之间反应过程的理论[20]。搜索任何一个反应势能面都需知道反应进程中每一步的结构和能量,尤其是决定反应速率的一步,这就要求确定过渡态结构。常用的搜索过渡态结构的方法有线性同步度越(linear synchronous transit,LST)和四極同步度越(quadratic synchronous transit,QST)。
本文使用DMol3模块中的LST/QST工具搜索δ-2转化为δ-3进程中的过渡态结构。主要内容如下:
1\*GB3建立反应物和产物的计算模型结构;
2\*GB3对结构式进行几何优化;
3\*GB3定义反应物的生成物原子配对;
4\*GB3用LST/QST方法计算过渡态。
3.1 建立反应物和产物模型
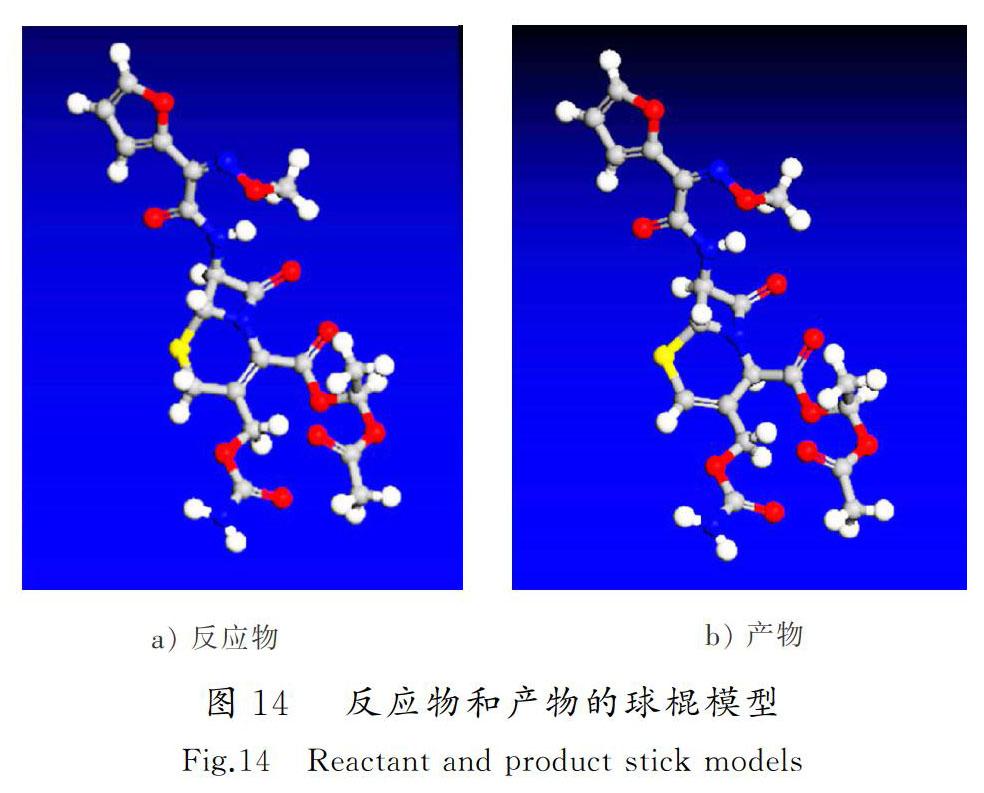
寻找化学反应过渡态结构,首先要确定反应物和产物,所以使用MS软件建立了两者的球棍模型,如图14所示。
3.2 几何优化结构
DMol3使用密度泛函理论(DFT)对头孢呋辛酯的分子结构和能量进行建模。常用泛函理论有GGA,LDA,B3LYP及m-GGA,其中GGA模型下的结果具有最高可靠性。故实验选取泛函理论GGA下的BP,以此对反应物和产物建模,如图15所示。再对建模结构进行几何优化,如图16所示,反应物经过48步优化结束。由图17可知,反应物优化时对应每一步结构的变化。
3.3 定义原子配对
使用反应预览功能对反应物和产物中所有原子进行配对,需要在反应物和产物之间建立一条通道。
3.4 用LST/QST的方法计算过渡态
LST/QST计算结束得到过渡态结构,如图18所示。图19表示过渡态搜索的进程。
由图18可知:反应物的双键位置发生了转移。图19显示了LST和CG的路径坐标变化曲线,LST线监测了过渡态搜索的进程。其中,横坐标为0时代表反应物,横坐标为1时代表产物,横坐标为0.616 55时代表一个过渡态位置,相应的能量在纵坐标上。
由TS.outmol中的的数据可知:反应物能量为-5.632 393×106 kJ/mol,产物能量为-5.632 393×106 kJ/mol,过渡态能量为-5.632 130×106 kJ/mol,反应能量为1.06 kJ/mol。综上所述,实现这一过渡态搜索,可确定过渡态结构。pH值≥9.54的环境中,头孢呋辛酯δ-2异构体形成了不稳定的过渡态,最终转变为δ-3杂质。
4 結 语
头孢呋辛酯丙酮溶液的降解符合一级反应动力学规律。在pH值<9.54条件下比较稳定;pH值=11.23条件下的降解速率与温度的关系符合阿仑尼乌斯方程,表观活化能约为19.79 kJ/mol。头孢呋辛酯丙酮溶液的降解程度受氧化剂种类的影响。
使用HPLC确定了初始溶液pH值、温度以及氧化剂种类变化对丙酮溶液中头孢呋辛酯降解动力学的影响,以优化新的生产工艺操作参数。在头孢呋辛酯生产过程中,要适当降低溶液温度,并使溶液尽可能处在pH值<9.54的环境中。
由HPLC图可知,头孢呋辛酯丙酮溶液的降解使δ-3杂质变多。采用MS模拟软件的LST/QST工具搜索得到了δ-2异构体转化为δ-3杂质进程中的过渡态结构,并对部分头孢呋辛酯的降解机理进行了分子层面的分析。
不同氧化剂对溶液的降解研究还不够全面,不同氧化剂对初始溶液不同pH值的影响尚未研究,未来将对其进行更加深入的探讨。
致谢:感谢天津大学国家工业结晶工程技术研究中心陈巍博士在MS分子模拟方法的帮助。
参考文献/References:
[1] 国家药典委员会.中华人民共和国药典[M].北京:中国医药科技出版社,2015.
[2] 孟雅杰,李应瑞,侯栩.法罗培南钠片和头孢呋辛酯片治疗呼吸道细菌性感染成本-效果分析[J].武警医学,2008,19(8):698-700.
MENG Yajie,LI Yingrui,HOU Xu.Cost-effectiveness analysis of faropenem sodium tablets and cefuroxime axetil tablets in treatment of respiratory tract bacterial infections[J].Armed Police Medicine, 2008,19(8):698-700.
[3] 韩润凤,袁恒杰,张洪香,等. 4厂家头孢呋辛酯片的质量评价[J].中国药房,2010,21(9):845-847.
HAN Runfeng,YUAN Hengjie,ZHANG Hongxiang,et al.Quality evaluation of cefuroxime axetil tablets from four manufacturers[J]. Chinese Pharmacy,2010,21(9):845-847.
[4] 刘浩,王红武,仇仕林.头孢呋辛酯HPLC含量测定方法的改进[J].中国抗生素杂志,2003,28(11):659-662.
LIU Hao,WANG Hongwu,QIU Shilin.Improvement of HPLC determinationmethod of cefuroxime axetil[J].Chinese Journal of Antibio-tic, 2003,28(11):659-662.
[5] 江晓玲,刘昆,邓俊丰,等.头孢菌素类抗生素中高分子杂质的研究进展[J].国外医药(抗生素分册),2007,28(6):264-269.
JIANG Xiaoling,LIU Kun,DENG Junfeng,et al.Research progress of high molecular impurities in cephalosporin antibiotics[J]. Foreign Medicine (Antibiotic Volume),2007,28(6):264-269.
[6] 屈海涛.头孢曲松钠中有机杂质的研究[D].沈阳:沈阳药科大学,2006.
QU Haitao.Study on Organic Impurities in Ceftriaxone Sodium[D].Shenyang:Shenyang Pharmaceutical University,2006.
[7] 梁晟,胡娟妮,吴琦琦,等.头孢呋辛酯中有关物质的LC-MS/MS分析[J].中国新药杂志,2014,23(4):480-485.
LIANG Sheng,HU Juanni,WU Qiqi,et al.Analysis of related substances in cefuroxime axetil by LC-MS/MS[J].Chinese Journal of New Drugs,2014,23(4):480-485.
[8] 罗顺德,于星,尹武华,等. 头孢泊肟酯的体内过程[J].中国药学杂志,1996(2):110-112.
LUO Shunde,YU Xing,YIN Wuhua,et al.The in vivo process of cefpodoxime ester[J].Chinese Journal of Pharmacy, 1996(2): 110-112.
[9] FABRE H,IBORK H,LERNER D A.Photoisomerization kinetics of cefuroxime axetil and related compounds[J].Journal of Pharmaceutical Sciences,1994,83(4):553-558.
[10]吴宏伟,黄赐煌.头孢呋辛酯的稳定性研究[J].海峡药学,2006,18(1):78-80.
WU Hongwei, HUANG Cihuang.Study on the stability of cefuroxime axetil[J].Strait Pharmaceuticals, 2006,18(1):78-80.
[11]胡娟妮. 头孢呋辛酯原料药的有关物质研究[D].长沙:中南大学,2014.
HU Juanni.Research on Related Substances of Cefuroxime Axetil API[D].Changsha:Central South University, 2014.
[12]曹卫凯.头孢呋辛酯的合成研究[J].合成技术及应用,2016,31(2):4-8.
CAO Weikai.Synthesis of cefuroxime axetil [J]. Synthesis Technology and Application, 2016,31(2):4-8.
[13]陈慧.HPLC法测定头孢呋辛酯中高分子聚合物含量[J].广东微量元素科学,2016,23(3):22-24.
CHEN Hui.Determination of high molecular polymer in cefuroxime axetil by HPLC[J].Guangdong Elemental Science,2016, 23(3):22-24.
[14]李裕基,张璇,闫小华.HPLC测定头孢呋辛酯片的含量及有关物质[J].中国医药指南,
2014(19):17-18.
LI Yuji, ZHANG Xuan, YAN Xiaohua.
Determination of cefroxime axetil tables and related substances by HPLC
[J].Chinese Medicine Guide, 2014(19):17-18.
[15]SU Min,BAI Yuxing,HAN Jian,et al.Adhesion of gypsum crystals to polymer membranes:Mechanisms andprediction[J].Journal of Membrane Science,2018,566:104-111.
[16]王貴芳,任晓亮,欧阳慧子,等. 化学动力学法研究4种光源对二苯乙烯苷稳定性的影响[J].药物分析杂志,2011,31(3):458-462.
WANG Guifang,REN Xiaoliang,OUYANG Huizi,et al.Study on the effect of four light sources on the stability of stilbene glycosides by chemical kinetics[J].Journal of Pharmaceutical Analysis,2011,31(3):458-462.
[17]丁彦蕊,蔡宇杰,孙培冬,等.青霉素G阴离子态的稳定性影响因素研究[J].中国抗生素杂志,2003,28(1):6-9.
DING Yanrui,CAI Yujie,SUN Peidong,et al.Study on the factors affecting the stability of penicillin G anion state[J].Chinese Journal of Antibiotics,2003,28(1):6-9.
[18]SAAB A N,DITTERT L W,HUSSAIN A A.Isomerization of cephalosporin esters: Implications for the prodrug ester approach to enhancing the oral bioavailabilities of cephalosporins[J].Journal of Pharmaceutical Sciences,1988,77(10):906-907.
[19]BENTLEY P H,BROOKSG,ZOMZYA I I.Phthalidyl Esters of Cephalosporins[J].Tetrahedron Letters,1976,17(41):3739-3742.
[20]EVANS M G,POLANYIM.Some applications of the transition state method to the calculation of reaction velocities,especially in solution[J].Transactions of the Faraday Society,1935,31(1):1965-1967.
