MAE-HPLC-HG-AFS同时测定洛克沙砷及其8种代谢物
2020-09-10崔颖姜涛倪松逯玉凤
崔颖,姜涛,倪松,逯玉凤
(1.天津海关动植物与食品检测中心,天津300461;2.北京海光仪器有限公司,北京100015)
洛克沙砷(roxarsone,ROX)属于有机砷类制剂,曾广泛用作猪、鸡的促生长剂,有预防疾病、促进生长、提高饲料利用率和改善肉的色泽等作用[1]。但是ROX进入动物体内经吸收、分布、代谢后,通过排泄物进入外界环境,如果在环境中进一步富集,通过食物链传递,最终会对人类构成危害。2018年1月11日,我国农业部《中华人民共和国农业部公告第2638号》明确规定:为保障动物产品质量安全,维护公共卫生安全和生态安全,开展了风险评估和安全再评价。评价认为ROX的原料药及各种制剂可能对动物产品质量安全、公共卫生安全和生态安全存在风险隐患。根据《兽药管理条例》第六十九条规定,决定停止在食用动物中使用ROX。
受形态分析方法的限制,早期对ROX代谢研究工作主要集中在禽类的排泄物上。在鸡的排泄物中ROX占主要成分[2-5],动物体内吸收较少,大多数随粪便直接排出[6]。已有研究[7-12]在鸡的组织样品中发现了多种砷形态,包括砷甜菜碱(arsenobetaine,AsB)、亚砷酸盐[arsenite,As(III)]、砷酸盐[arsenate,As(V)]、一甲基砷酸(monomethyl arsenic,MMA)、二甲基砷酸(dimethyl arsenic dimethyl arsenic,DMA)、3-氨基-4-羟基苯胂酸(3-amino-4-hydroxybenzene arsenic acid,3-AHPAA)、4-氨基苯胂酸(4-aminophenylarsonic acid,4-APAA)、N-乙酰-4-羟基苯胂酸(N-acetyl-4-hydroxy-m-arsanilic acid,N-AHAA)、洛克沙砷(roxarsone,ROX)和一些未知形态[2,5,13-17]。
砷形态分析前处理方法应该既有良好的回收率又能保持砷在样品中的原始形态[18]。按提取仪器不同,可分为萃取提取、振摇提取、离心提取、超声辅助提取、微柱辅助提取和微波辅助提取等[19-23];按提取液不同,可分为水提取、甲醇-水提取、氯仿-甲醇-水提取和酶提取等[24-25]。目前主要的检测联用技术有高效液相色谱与原子荧光光谱(atomic fluorescence spectrometry,AFS)[26]、电感耦合等离子体发射光谱(inductively coupledplas ma-atomic emission spectrometry,ICP-AES)[27-28]、电感耦合等离子体质谱(inductively coupled plasma-mass spectrometry,ICP-MS)[9-10,29]等联用。本研究运用微波辅助萃取-高效液相色谱-氢化物发生-原子荧光光谱(microwave assisted extraction-high performance liquid chromatography-hydride generation-atomic fluorescence spectrometry,MAE-HPLC-HG-AFS)联用技术对动物样品中ROX及其代谢物进行了同时检测,可为ROX的代谢转化及其代谢物在环境中累积和迁移的研究提供技术支撑,为研究动物对ROX代谢物的吸收累积以及毒性砷形态进入人体的途径提供科学依据。
1 材料与方法
1.1 标准品与试剂
洛克沙砷(CAS 编号:121-19-7,C6H6AsNO6,纯度≥97.5%):ehrenstorfer gmbh公司;3-氨基-4-羟基苯胂酸(CAS 编号:2163-77-1,C6H8AsNO4,纯度≥98.1%):sigma aldrich公司;砷甜菜碱(CAS编号:64436-13-1,C5H11AsO2,纯度≥98%):tri chemical laboratories公司;4-氨基苯胂酸(CAS 编号:98-50-0,C6H8AsNO3,纯度≥99%)、N-乙酰-4-羟基苯胂酸(CAS编号:97-44-9,C8H10AsNO5,纯度≥98.1%):pfaltz and bauer公司;亚砷酸根溶液标准物质(Na3AsO3,GBW08666)、砷酸根溶液标准物质(Na2HAsO4·12H2O,GBW08667)、一甲基砷酸溶液标准溶液(CH4AsNaO3·1.5H2O,GBW08668)、二甲基砷酸溶液标准溶液(C2H6AsNaO2·2H2O,GBW08669):国家标准物质中心。
甲醇(HPLC级):德国Merck公司;盐酸、硼氢化钾、磷酸二氢钾、过硫酸钾(优级纯):国药集团化学试剂有限公司;氢氧化钠(优级纯):北京化工厂;四丁基溴化铵(优级纯):天津光复精细化工研究所;三氟乙酸(优级纯):上海天莲精细化工有限公司。其他试剂均为分析纯及以上。
1.2 仪器与设备
1260型号高效液相色谱仪(包括液相色谱泵和进样装置):美国agilent公司;9560型原子荧光光谱仪:北京海光公司;multiwave PRO型微波消解系统:奥地利AntonPaar公司;T18组织匀浆机:德国IKA公司;Alpha 1-4/LD-plus型冻干机:德国 christ公司;Milli-Q reference型超纯水仪:德国millipore公司;VORTEX型涡轮混合器:美国scientific industries公司;3-30K型高速冷冻离心机:美国sigma公司;N-EVAP-24型水浴氮吹仪:美国organomation associates Inc公司;PL303分析天平(Max=210 g,d=0.001 g):梅特勒-托利多仪器(上海)有限公司;SQP电子天平(Min=10mg,Max=220g,d=0.1mg):赛多利斯科学仪器(北京)有限公司;滤膜(0.45 μm,直径47 mm,有机系):agela technologies公司。
1.3 试验方法
1.3.1 液相色谱参考条件
色谱柱:阴离子交换色谱柱PRP X-110S(7 μm,150 mm×4.10 mm,Hamilton)。流动相:(A)5%甲醇;(B)5%甲醇-60 mmol/L碳酸氢铵溶液,pH 8.75。流速:2.0 mL/min。洗脱程序:0~2 min,流动相A从100%线性递减到50%,流动相B从0%线性递增到50%;2 min~5 min,50%A 和 50%B;5 min ~8 min,流动相 B从50%递增到100%;8 min~17 min,100%B;17 min~18 min,流动相B从100%线性递减到0%,流动相A从0%递增到100%;18 min~20 min,100%A。进样体积:100 μL。
1.3.2 原子荧光检测参考条件
负高压:330 V;灯电流:100 mA;载气流量:400 mL/min;屏蔽气流量:900 mL/min;载流:7%HCl溶液;载流流速:110 r/min;还原剂:5 g/L KOH-20 g/L KBH4;还原剂流速:110 r/min;过硫酸钾溶液浓度:3%;过硫酸钾溶液流速:100 r/min;读数模式:峰面积。
1.3.3 样品处理方法
准确称取1 g(精确到0.001 g)鸡和猪组织匀浆于微波辅助萃取内罐中,加10 mL甲醇-水提取液(1∶1,体积比),按照微波辅助萃取仪的操作步骤进行提取,提取温度80℃,提取时间60 min。提取完毕,取出冷却至24℃,10 000 r/min离心5 min,将上清液转移至25 mL容量瓶中。残渣再加5 mL提取液于25 mL容量瓶中。重复“残渣再加5 mL提取液,在涡旋混合器上充分混合,10 000 r/min离心5 min,将上清液转移至25 mL容量瓶中”操作一次。合并上清液于25 mL容量瓶中,定容。取10 mL上清液,氮气吹扫,用提取液定容至2 mL,经0.45 μm有机滤膜过滤,供HPLC-AFS测定。按同一操作方法作空白试验。
2 结果与分析
2.1 HPLC-AFS试验条件的确定
对9种砷形态进行分析,包括ROX和它可能的代谢产物,如3-AHPAA、4-APAA和N-AHAA以及一些常见的砷形态,如 As(III)、DMA、MMA、As(V)和 AsB。这9种砷形态用于建立砷形态分析方法。
2.1.1 高效液相色谱分离条件的确定
应用9种混合标准溶液优化HPLC条件。在这9种砷形态中,有7种砷形态的酸度系数(protein kinase A,pKa值)低于7.0,在碱性条件下,它们会带上负电荷。因此,这里选用了一种强阴离子交换柱(PRP X-110S)来实现对9种砷形态的分离。基于对HPLC-AFS进样的考虑,选用了碳酸氢铵溶液和5%甲醇作为流动相,适用于两个仪器。采用梯度洗脱的方式可以达到对全部9种砷形态的基线分离,缩短N-AHAA和ROX的保留时间。而对于两性离子AsB和As(III)(pKa=9.2)则可以通过调节pH值为8.75来实现分离。在优化好的条件下,ROX、As(III)、DMA、MMA、As(V)、AsB、3-AHPAA、4-APAA和N-AHAA能在12 min内完全分离。9种砷形态经过HPLC的分离情况见图1。
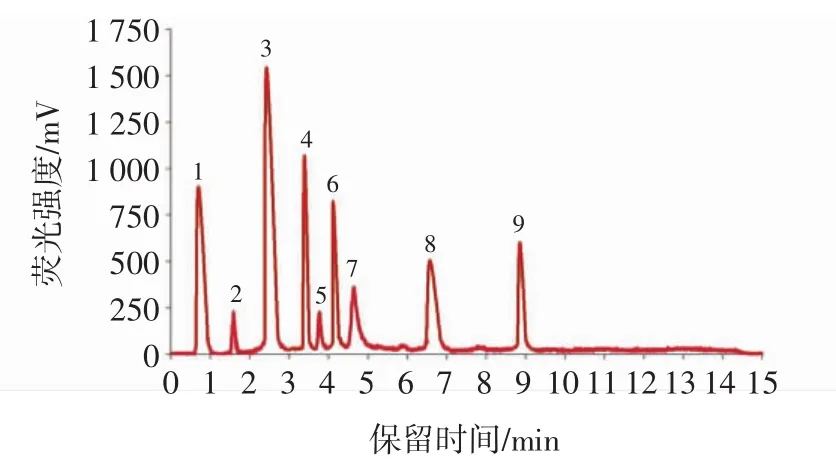
图1 HPLC-AFS测定9种砷形态的强阴离子交换色谱图Fig.1 Chromatograms showing strong anion exchange separation of nine species with HPLC-AFS detection
2.1.2 氢化物发生条件的优化
砷形态混标经过色谱柱分离后,与过硫酸钾混合,在紫外灯的照射下,有机砷形态被消解为无机砷,最后在载流和还原剂的作用下,被还原为砷的氢化物,由氩气载入原子化器加热分解为原子态,空心阴极灯的发射光激发产生原子荧光。为了使有机态完全消解成无机态,确定过硫酸钾浓度为3%。载流和还原剂的流速和浓度直接影响着氢化反应效率,通过采用单变量方法,每次变化其中一个变量,研究载流和还原剂的最优化组合。
2.1.2.1 蠕动泵流速优化
还原剂由蠕动泵来驱动,在泵管确定的条件下,蠕动泵的转速决定了各种试剂的流速。试验中首先研究了还原剂不同流速对于试验结果的影响,确定HCl的蠕动泵转速为110 r/min,研究不同还原剂流速对于试验结果的影响。改变KBH4的蠕动泵转速由80 r/min梯度增大,不同还原剂流速下荧光强度的检测结果如图2所示。

图2 还原剂流速优化试验Fig.2 Optimization of reducing agent flow rate
由图2可见,当KBH4流速较小时,由于还原剂不足,导致被测氢化元素氢化反应不完全,所以检测信号强度不高,检测灵敏度较低。不断增大还原剂流速,检测谱峰强度逐渐增大,谱峰面积增大,灵敏度增大。但是,随着还原剂流速的增大,氢化反应愈加强烈,反应剧烈,气液分离器中出现泡沫,检测信号噪声增大,信噪比下降。当蠕动泵转速为110 r/min时,灵敏度较高,此时氢化反应强度适中,信号噪声不高,所以选择KBH4蠕动泵转速为110 r/min。
2.1.2.2 还原剂浓度优化
氢化反应中,还原剂应该适当过量,以保证氢化元素最大程度的发生氢化反应。选定HCl浓度5%,改变KBH4的浓度,通过一系列试验来确定KBH4的最佳浓度。检测样品均采用浓度100 μg/L的9种砷形态混标。分别改变KBH4的浓度为15、20、25 g/L和30 g/L,利用原子荧光光谱仪检测谱峰面积的结果如图3所示。

图3 硼氢化钾浓度优化试验Fig.3 Optimization of potassium borohydride concentration
试验中发现,刚开始时,随着KBH4浓度的增加,各个成分的灵敏度均上升,至浓度为20 g/L时达到最大,随着KBH4浓度的增加,9种成分的检测灵敏度开始下降,其原因可能是随着KBH4浓度的增加,氢化反应变得越来越剧烈,产生的氢气越来越多,经气液分离器分离后送入AFS检测器的气流流速过大,对砷的氢化物具有一定的稀释作用,从而降低了砷形态的原子荧光信号,导致了检测灵敏度的下降。所以,还原剂KBH4的浓度选为20 g/L。
2.1.2.3 HCl浓度优化
还原剂采用含5 g/L KOH的20 g/L KBH4溶液,改变HCl的浓度,通过一系列试验来确定HCl的最佳浓度。检测样品均采用浓度100 μg/L的9种砷形态混标。分别改变HCl的浓度为4%、5%、7%和10%,利用原子荧光光谱仪检测谱峰面积的结果如图4所示。
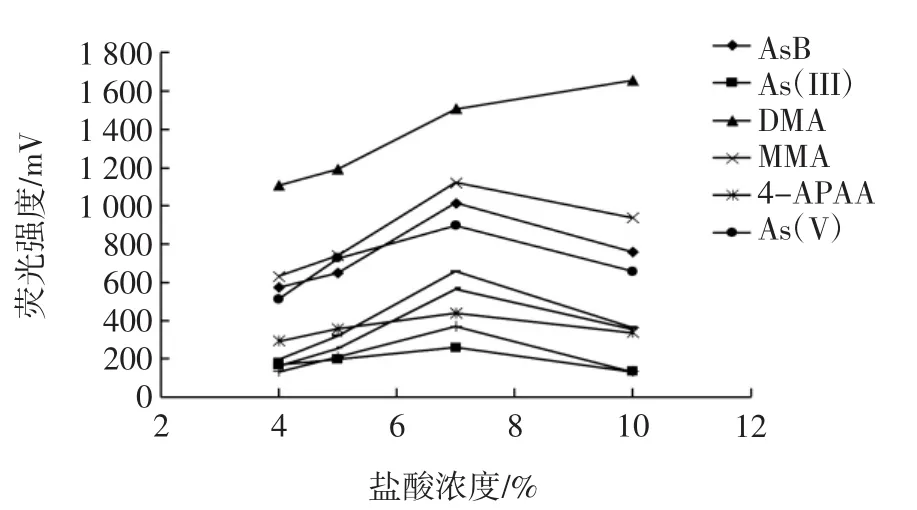
图4 盐酸浓度优化试验Fig.4 Optimization of hydrochloric acid concentration
图4中,在HCl浓度达到10%时,ROX及其他砷形态的灵敏度继续减小,但是DMA反而有所上升,其原因可能是此时氢化反应比较剧烈,进入AFS检测的气体流速很大,造成原子荧光检测器中原子化器的火焰跳动特别厉害,使得谱图噪声很大,在计算谱峰面积时,造成了误差。所以,在还原剂采用含5 g/L KOH的20 g/L KBH4溶液的条件下,HCl的浓度选为7%。
2.1.3 原子荧光条件的优化
在原子荧光检测器中,光电倍增管电压、空心阴极灯电流、载气及屏蔽气流量都会影响到最终的检测灵敏度,通过一系列试验研究了原子荧光检测器主要参数的优化条件,检测样品均为浓度100 μg/L的9种砷形态混标。评定各种参数条件下的信噪比,信噪比较高的为其最优值。
2.1.3.1 光电倍增管高压
光电倍增管主要对检测到的荧光信号进行放大,加到它上面的负高压的大小决定了其放大倍数。试验中,分别选择 300、310、320、330 V 和 340 V 5个梯度值,各参数下检测信号的信噪比如图5所示。
由图5可见,当光电倍增管负高压较小时,荧光信号较弱,谱峰强度较低,部分谱峰甚至淹没在噪声信号中,此时,信噪比较低;随着负高压的增大,荧光信号的放大倍数增大,而噪声信号的强度也增大,信噪比提升较快。虽然各种砷形态的谱峰强度增大,但是当负高压不断增大时,信号本底值、各种噪声信号的强度也一直增大,至330 V以后,虽然继续增大负高压,荧光信号强度继续增大,但是信噪比却开始下降,因为此时噪声信号增大的程度变得越来越大,所以,选择330 V为光电倍增管负高压的最优值,因为此时信噪比最大,信号强度较高,而本底值也相对较低。
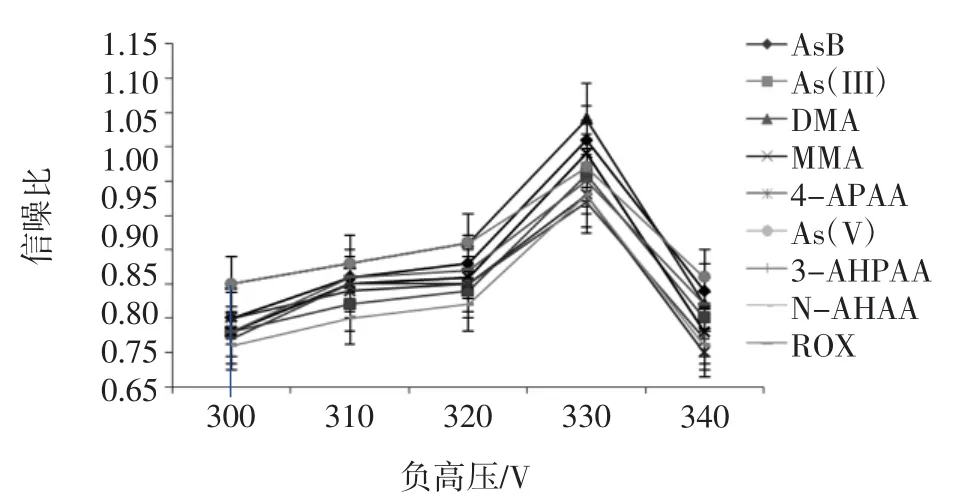
图5 不同负高压下的信噪比Fig.5 Signal to noise ratio under different negative high voltage
2.1.3.2 空心阴极灯电流优化
空心阴极灯用来激发荧光信号,被测元素原子吸收空心阴极灯辐射的能量,跃迁到较高能级,当回到基态时,便发出荧光信号,所以,空心阴极灯辐射强度的大小会影响到吸收辐射能量的原子数量,继而影响到辐射的荧光信号的强度。空心阴极灯采用集束脉冲式供电,脉冲电流的大小决定了辐射能量的高低。试验中,不断增强空心阴极灯的灯电流,从80 mA梯度增大,如图6所示。
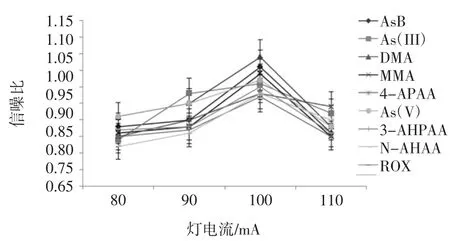
图6 不同灯电流下的信噪比Fig.6 Signal to noise ratio under different lamp current
从图6中可以看出,当空心阴极灯电流较小时,激发的荧光信号较弱,谱峰强度较低,部分谱峰甚至湮没在噪声信号中,此时,信噪比较低;随着空心阴极灯电流的逐渐增大,检测信号的强度也逐渐增大,当增大到100 mA时,信噪比达到最大,而后随着灯电流的增大,信噪比反而开始下降,其原因可能是灯电流在100 mA后发生了自吸,从而使得荧光信号反而减弱,且灯电流越大,自吸现象越严重,而谱峰信号越弱;另外,过大的灯电流可能会影响空心阴极灯的使用寿命,甚至造成损坏。所以,本试验采用100 mA空心阴极灯电流。
2.1.3.3 载气流速优化
载气的作用是一方面吹扫反应过程中产生的被测元素氢化气,将其送到原子化器中被原子化后实现检测;另一方面与反应生成的氢气一起在原子化器中形成氩氢火焰,使被测元素氢化物形成原子蒸气。所以载气会影响到原子化效率以及氩氢火焰的稳定性,继而影响到信噪比的大小。试验中,使流速从300 mL/min不断增大,比较不同载气流速下荧光强度的大小,所得结果如图7所示。

图7 载气流速优化试验Fig.7 Optimization of flow velocity of carrier gas
从图7中看出,一开始时荧光强度较小,因为在流速较小时,氩气吹扫能力不足,反应生成的氢气流量不稳定,使得氩氢火焰不稳定,造成火焰抖动,从而使得检测信号抖动,噪声增大,所以信噪比较低。不断增大载气流量,在流量达到500 mL/min后,随着载气流量的增大,吹扫速度增大,但是谱峰强度却降低得较多,使得被测元素氢化物未能完全原子化即被排出,所以荧光强度开始减小。当载气流速为400 mL/min时,荧光强度最大,此时吹扫速度适中,而氩氢火焰也比较稳定,噪声较小,所以最终选定400 mL/min为载气流速的最优值。
2.1.3.4 屏蔽气流速优化
屏蔽气主要是在原子化器中用来保护原子化蒸气不被氧化,易吸收空心阴极灯的辐射能量,使得荧光信号增强,所以屏蔽器的流量选择主要从经济方面考虑,选择最小的屏蔽气流量,达到最佳的屏蔽作用。如图8所示,使屏蔽气流速从800 mL/min不断增大,比较不同屏蔽气流速下荧光强度大小。
由图8中可以看出,在屏蔽气流速较小时,所检测得到的荧光强度较小,而噪声信号较强,说明空气中的氧气与部分原子化后的气体发生了氧化反应,受激荧光辐射不足。不断增大屏蔽气流速,谱峰面积逐渐增大,噪声信号强度减小,当流速达到900 mL/min~1 000 mL/min时,荧光强度达到最大,从经济方面考虑,选择900 mL/min为屏蔽气流量。

图8 屏蔽气流速优化试验Fig.8 Optimization of flow velocity of shield gas
2.2 线性方程及检出限
ROX及其代谢物在不同的线性范围内的线性方程、相关系数R2见表1。由表1可得,各砷形态的浓度与峰面积呈线性相关,相关性R2>0.997,符合定量要求。
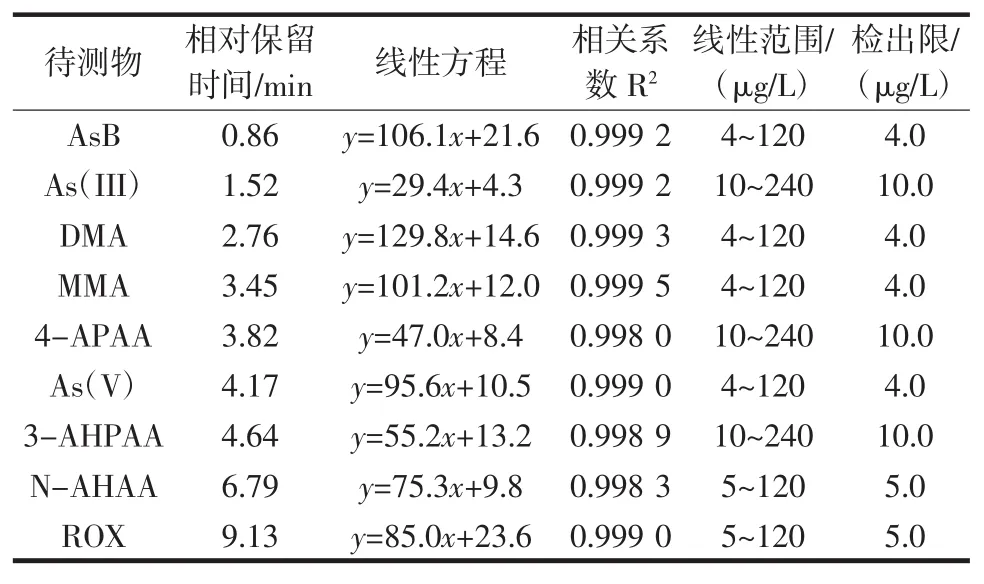
表1 ROX及其代谢物的一元线性回归方程及相关系数Table 1 Linearity regression and coefficient of correlation for ROX and its metabolites
2.3 精密度和回收率
采用上述方法检测这9种不同的砷形态,重复6次,计算相对标准偏差(relative standard deviation,RSD)和添加回收率,如表2所示。
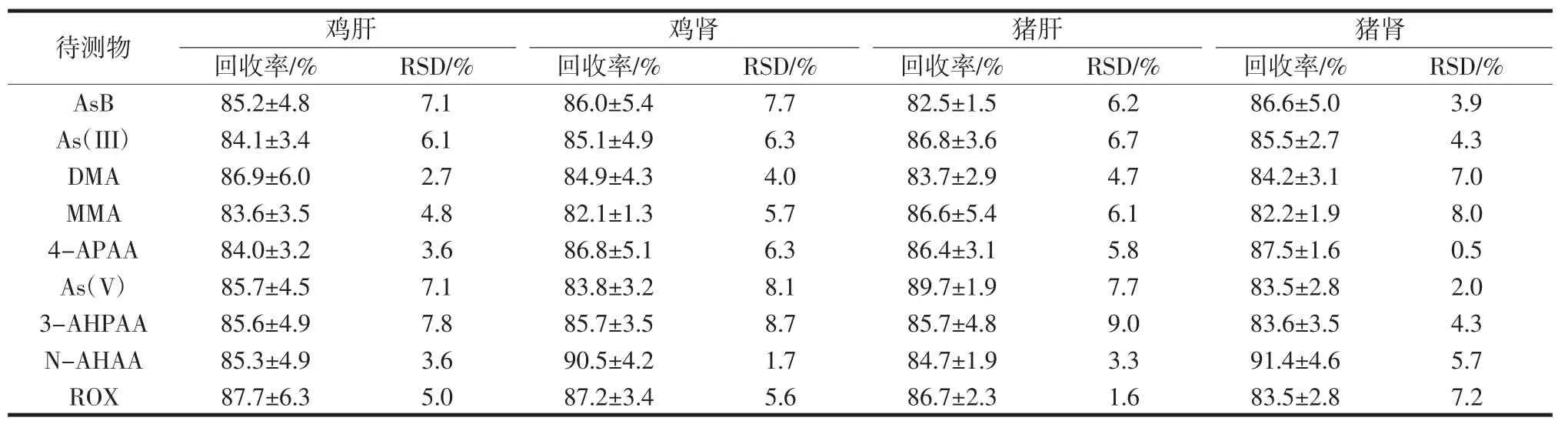
表2 ROX及其代谢物的回收率和相对标准偏差Table 2 Recoveries and inter-day relative standard deviation of ROX and its metabolites
由表2可知,试样中9种砷形态的加标回收率在80.1%~96.0%范围内,RSD都控制在9%以内,说明该方法能较好的保持形态稳定性,可靠性和可重复性良好。
2.4 样品分析
实验室对猪和鸡连续饲喂ROX,对饲喂第28天的鸡肝、鸡肾、猪肝、猪肾样品的砷形态进行MEAHPLC-HG-AFS分析,结果见表3。

表3 鸡肝、鸡肾、猪肝、猪肾中ROX及其代谢物的含量Table 3 Content of ROX and its metabolites in chicken liver,chicken kidney,pig liver and pig kidney μg/kg
本方法分别检测到了 ROX、As(III)、DMA、MMA、As(V)、AsB、3-AHPAA 和 N-AHAA。其中 3-AHPAA是ROX的还原产物,而N-AHAA则是进一步乙酰化的产物。
3 结论
本文介绍了采用微波辅助萃取-高效液相色谱-氢化物发生-原子荧光光谱法同时测定洛克沙砷及其8种代谢物残留量,探讨了试验条件的优化和试验方法的验证。最终优化结果为流动相:(A)5%甲醇;(B)5%甲醇-60 mmol/L碳酸氢铵溶液,pH 8.75;负高压:330 V;灯电流:100 mA;载气流量:400 mL/min;屏蔽气流量:900 mL/min;载流:7%HCl溶液;载流流速:110 r/min;还原剂:5 g/L KOH-20 g/L KBH4;还原剂流速:110 r/min。提取试剂:甲醇-水提取液(1 ∶1,体积比);提取温度:80℃。验证结果表明建立的方法具有良好的回收率,并且方法稳定性高、重复性好,将应用于后续的工作,以实现对动物体内ROX的分布以及代谢途径的分析。
