六种传代细胞系的致瘤性研究
2020-09-10王磊杨承槐王团结刘莹
王磊,杨承槐,王团结,刘莹
(中国兽医药品监察所,北京 100081)
原代细胞用于生物制品的生产已有50多年的历史,但是其存在传代次数有限、组织来源很难保证均一稳定、生产成本较高等诸多制约因素。传代细胞系作为理想的替代用生产基质可以很好地克服以上缺点。为确保生物制品的安全性,在进行生物制品研发生产前,应对作为生产用的传代细胞系进行致瘤性检验[1-3]。用于研发和生产的传代细胞系致瘤性与否会直接关系到相关生物制品的种类、生产用细胞最高代次的限定以及相关质量标准的制定等诸多方面[4-5]。目前WHO和我国药典对于细胞致瘤性检验推荐的方法主要是动物体内接种法[1-3]。体内法具有检验敏感性好、判定结果直观、结果重复性好等诸多优点,是针对细胞致瘤性检验的“金标准”。
中国兽医微生物菌种保藏管理中心(国家兽医微生物资源平台)保藏的羊睾丸细胞系(OA3.Ts)、牛肾细胞系(MDBK)、小鼠成纤维细胞系(McCoy)、猪睾丸细胞系(ST)、猪肾细胞系(PK-15)、猴肾细胞系(Marc-145)均是兽用生物制品研发生产中的常见传代细胞系。其中OA3.Ts、MDBK对羊痘病毒、羊口疮病毒、牛病毒性腹泻病毒等牛羊病病毒易感,可作为草食动物疫病疫苗研发生产用细胞[6-7]; McCoy是针对导致猪回肠炎的劳森菌的最佳体外宿主,可用于猪回肠炎疫苗的研发生产; ST、PK-15和Marc-145均对多种病毒易感并已用于疫苗生产[8]。
鉴于目前对上述非禽源细胞系的致瘤性研究报道较少,本研究采用动物体内接种法对上述6种常见生产用传代细胞系的基础代次进行致瘤性研究,为生产用传代细胞系的安全性评价提供试验依据。
1 材料与方法
1.1 材料及试剂
1.1.1 细胞 BHK-21细胞第55代、Marc-145细胞第18代、McCoy细胞(原始代次不明)第18代、ST细胞第125代、OA3.Ts细胞第29代、MDBK 细胞第9代、PK-15 细胞第135代,上述使用的细胞均为基础种子库细胞,由中国兽医微生物菌种保藏管理中心保藏。鸡胚成纤维细胞(CEF)为中国兽医微生物菌种保藏管理中心细胞实验室使用SPF鸡胚自行分离的原代细胞。
1.1.2 实验动物 Nu-Nu品系裸鼠,雌性,6~8周龄,共80只,购于北京维通利华实验动物技术有限公司,饲养于中国兽医药品监察所大兴生物实验基地。饲养期间各组裸鼠饮用水均为高压灭菌纯净水,饲料及垫料均为辐照灭菌产品,由中国兽医药品监察所基础保障处提供。饲养环境:昼夜各半循环照明,湿度恒定,温度控制在22~25 ℃。所有操作均符合中国兽医药品监察所实验伦理要求。
1.2 方法
1.2.1 实验分组 将80只裸鼠随机分为8组,处理组分为MDBK细胞组、OA3.Ts细胞组、Marc-145细胞组、McCoy细胞组、PK-15细胞组、ST细胞组,每种细胞培养物注射10只裸鼠。BHK-21细胞阳性对照组和鸡胚成纤维细胞阴性对照组各注射10只裸鼠。
1.2.2 细胞培养物收集与接种 每种细胞培养10个175 cm2培养瓶的细胞量。按《中国兽药典》方法消化、收集每种细胞系的细胞培养物悬液进行细胞计数后,1000 r/min离心10 min收集细胞沉淀,用无血清DMEM重悬。每只裸鼠颈背部消毒后,于皮下注射约0.3 mL细胞培养物。处理组每只裸鼠注射107以上个细胞。BHK-21细胞阳性对照组和鸡胚成纤维细胞阴性对照组注射106以上个细胞(表1)。
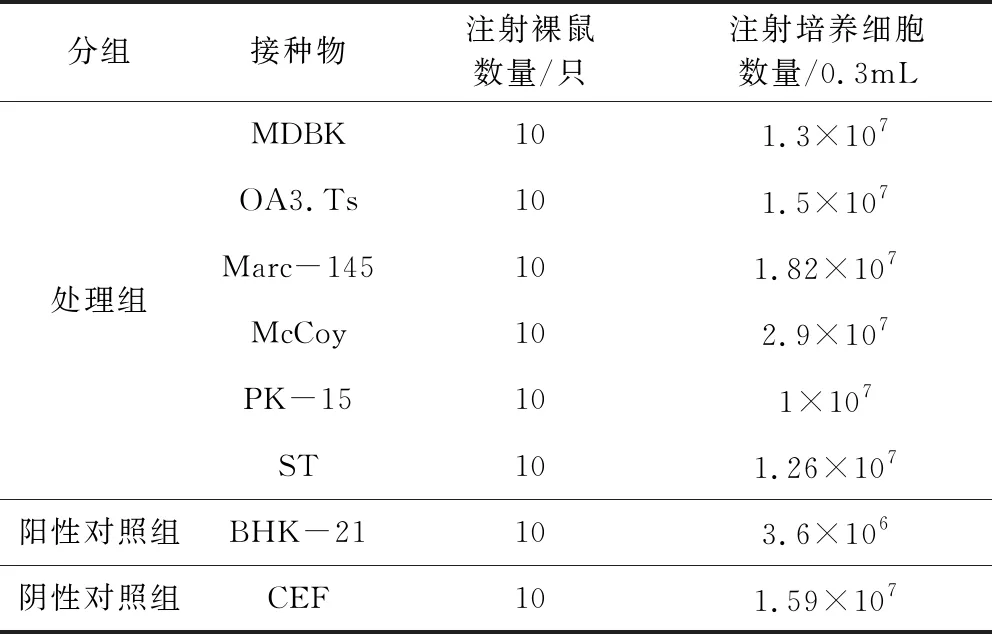
表1动物分组Tab 1 Experimental animal grouping
1.2.3 接种后观察与剖检 接种后的裸鼠连续观察35日,检查有无结节或肿瘤形成。如有结节或可疑病灶需进行剖检。对未发生结节的动物,取一半数量进行剖检。对另一半未发生结节的动物继续观察至12周,对接种部位进行剖检,观察有无结节形成。BHK-21细胞阳性对照组和鸡胚成纤维细胞阴性对照组35日后全部进行剖检。
1.2.4 组织切片取材、制备及病理学检查 断颈处死裸鼠,所有处理组和对照组裸鼠剖检后均需进行组织病理学检查。取注射部位附近皮肤组织、肝脏组织、肾脏组织、脾脏组织,如处理组和阳性对照组剖检发现结节或可疑病灶,则取出裸鼠皮下结节及可疑病灶,均放入4%多聚甲醛固定24~48 h。将固定后的样品制备石蜡包埋切片后,经H-E染色后镜检。
2 结果与分析
2.1 阳性、阴性对照组结果 经观察35日后,BHK-21细胞阳性对照组的裸鼠颈背部接种部位均发现有明显肿块(表2),且结节直径4~10 mm左右,精神萎顿、采食量下降;经剖检发现,全部小鼠的肝脏、肾脏、脾脏、肺脏均无明显结节(图1A)。对小鼠肿块、肝脏、肾脏、脾脏、肺脏进行组织切片检测发现:结节组织肿瘤细胞体积偏大,细胞核与细胞质的比例增大,细胞核形态大小不一,染色质粗糙,出现病理性核分裂象,肝脏、肾脏、脾脏组织未发现肿瘤细胞(图2A)。此外,阳性对照组中一只裸鼠在肺脏部位发现有病理性核分裂象的存在,疑似发生了肿瘤细胞肺部转移的现象(图2B)。由图1B可知,注射CEF细胞的阴性对照组小鼠未见结节或可疑肿瘤组织,精神、饮食未出现异常表现。取10只裸鼠进行剖检并对注射部位皮肤、肝脏、肾脏、脾脏进行组织切片检测,未发现有肿瘤细胞。
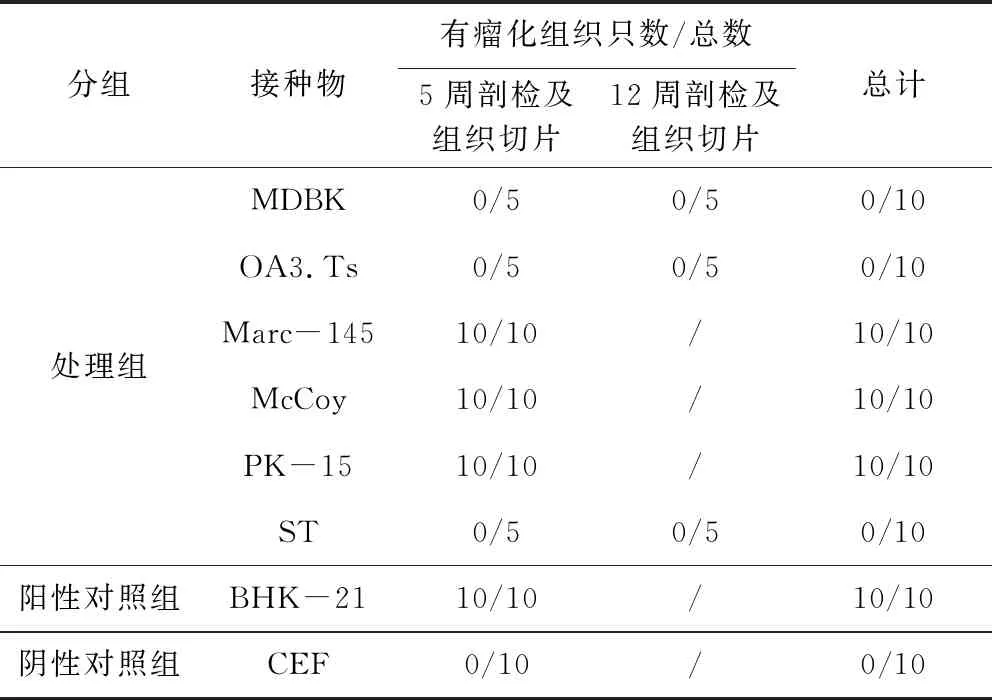
表2 各组裸鼠成瘤数量统计Tab 2 Experimental animal grouping
2.2 实验处理组结果 实验处理组,注射ST、MDBK、OA3.Ts细胞的3组裸鼠,观察35日精神、饮食未出现异常表现,均未见结节或可疑肿瘤组织(图1C、图1G、图1H)。各组取各5只裸鼠进行剖检,并对注射部位皮肤、肝脏、肾脏、脾脏、肺脏进行组织切片检测,未发现有肿瘤细胞。继续饲养观察

箭头所指位置为结节或可疑病灶 A:BHK-21细胞阳性对照组;B:CEF细胞阴性对照组;C:ST细胞处理组 D:PK-15细胞处理组; E:McCoy细胞处理组;F:Marc-145细胞处理组;G:MDBK细胞处理组;H:OA3.Ts细胞处理组 A: Positive control (BHK-21 group); B: Negative control (CEF cell group); C: ST cell group; D: PK-15 cell group; E: McCoy cell group; F: Marc-145 cell group; G: MDBK cell group; H: OA3.Ts cell group图1 裸鼠大体解剖学检查Fig 1 The gross anatomy examination of the nude mice
至12周,对各组剩余裸鼠进行剖检并对注射部位皮肤、肝脏、肾脏、脾脏、肺脏进行组织切片检测,均未发现有肿瘤细胞。在35日观察期内,注射Marc-145、McCoy、PK15细胞的3组裸鼠均出现精神萎顿、采食量下降,接种部位有可疑肿块组织。PK15、Marc-145接种组肿块直径2~8 mm(图1D、图1F);McCoy细胞接种组肿块直径5~15 mm,有丰富的血管组织且部分表皮破溃(图1E)。对3个处理组的取样肿块分别进行组织切片检测,均发现广泛病理性核分裂象,为鳞状细胞癌细胞(图2C、图2D、图2E)。此外,3个处理组裸鼠肝脏、肾脏、脾脏、肺脏均无明显结节和病理变化。

A:BHK-21细胞阳性对照组注射部位肿块;B:BHK-21细胞阳性对照组肺部转移瘤;C:Marc-145细胞处理组 注射部位肿块 D:McCoy细胞处理组注射部位肿块;E: PK-15细胞处理组注射部位肿块 A: Positive control (BHK-21 group); B: BHK-21 cell positive control group lung metastasis; C: Mass at injection site in Marc-145 cell treatment group; D: Mass at injection site in McCoy cell treatment group; E: Mass at injection site in PK-15 cell treatment group图2 阳性对照组、处理组可疑肿块病理切片检查 HE 400×Fig 2 Histopathological examination of suspicious mass in positive control group and treatment group
3 讨论与结论
传代细胞系一般是由人或动物肿瘤组织或正常组织的细胞转化而来[2],在转化的过程中会获得与原始细胞不同的生物学特性,如:细胞中染色体的数量或是结构发生改变;细胞锚定依赖性的消失以及细胞致瘤性的发生。根据以上特性,可将转化可分为一般转化和恶性转化。一般转化细胞培养时伸展良好、有方向性、接触抑制且具有锚定依赖性,无致瘤性。恶性转化细胞培养时细胞伸展性差、接触抑制消失,并不具备锚定依赖性,可在软琼脂内增殖,接种裸鼠皮下可致瘤[9-10]。随着传代细胞系在生物制品领域的广泛应用,致瘤性阳性的传代细胞系能否作为生产用细胞基质及其对生物制品安全性的影响逐渐成为疫苗研发、评审、监管机构关心和讨论的问题[11]。
2015版《中华人民共和国兽药典》在使用动物体内接种法评价生产用细胞基质的致瘤性时,主要检查接种待检细胞的活培养物在动物体内是否成瘤,其目的是为了确定细胞基质接种动物后形成(肿)瘤的能力,检查细胞系动物体内成瘤的特性。本研究针对6种细胞的基础代次进行了致瘤性检查,结果表明:MDBK细胞、OA3.Ts细胞、ST细胞不会引起裸鼠发生肿瘤,具有良好的安全性。由于某些细胞传代次数增加会增加致瘤风险[1],因此以上三种细胞用于生物制品的研发或生产时,还应对其限定的生产最高代次细胞进行致瘤性检查,以确保传代的过程不会增强细胞致瘤性。McCoy细胞、PK-15细胞、Marc-145细胞基础代次致瘤性检查呈阳性,用于兽用灭活疫苗的生产时,应进行适当处理,如冻融或超声波裂解细胞[12],使用β-丙内酯或二乙烯亚胺降解细胞核酸[13],超滤去除细胞碎片等,以减低细胞致瘤风险。
为了保证疫苗的安全性,应尽可能使用低代次的细胞用于疫苗生产,参考WHO 相关指南、《欧洲药典》、《中国药典》三部,建议在细胞系生产的疫苗质量标准中增加细胞DNA 残留量限定标准,降低细胞性致瘤性和致癌性的风险。从长远来讲,解决问题的最佳办法是开发无致瘤性细胞系。
