超声引导细针抽吸细胞块免疫组化对BI-RADS 4类乳腺结节的诊断
2020-09-08王川予王飞亮贾静怡陈秀华何淑蓉陆旭戴维德
王川予,王飞亮,贾静怡,陈秀华,何淑蓉,陆旭,戴维德*
1.北京医院超声科、国家老年医学中心,北京 100730;2.北京医院病理科、国家老年医学中心,北京 100730;3.北京医院乳腺外科、国家老年医学中心,北京 100730;*通讯作者 戴维德 Dai.weide@126.com
超声引导下粗针穿刺组织学检查(coarse needle biopsy,CNB)是临床诊断乳腺恶性肿瘤最常用的方法,广泛用于乳腺结节的鉴别诊断。粗针穿刺可获取较多的细胞学组织,可得到明确的病理结果[1]。细针抽吸(fine needle aspiration,FNA)细胞学检查创伤面积较小,所获得的样本量不足。粗针穿刺创伤程度较FNA 大,不适用于高龄体弱、凝血机制差的患者。本研究拟应用超声引导FNA 结合细胞块免疫组化检测诊断乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS)4 类乳腺结节,与CNB 进行对比,探讨其对乳腺结节的临床诊断价值。
1 资料与方法
1.1 研究对象 收集2018年1月-2019年6月于北京医院就诊的女性乳腺结节患者160例,年龄19~95岁,平均(51.9±7.3)岁;结节大小约1.0~4.5 cm。取材标准:①FNA 及CNB 的细胞量或病灶组织充足;②FNA涂片血细胞过多造成干扰、出现细胞干片、抽取细胞量少导致蜡块制作不成功、抽取细胞为少量导管上皮细胞及纤维细胞判定为取材失败;CNB 抽取组织为少许乳腺组织、皮肤组织或坏死组织为取材失败。将疑似恶性和非典型病变归为恶性结果,排除标本不符合要求者。
1.2 仪器与方法 采用Toshiba Apllo型彩色多普勒超声诊断仪,探头频率5~12 MHz。患者取仰卧位或侧卧位,选择最佳穿刺点并完成定位。穿刺部位消毒铺巾,采用2%利多卡因局麻,行超声引导下FNA 穿刺,采用10 ml 注射器25G 针头,于彩色多普勒超声引导下进针,沿结节长轴进入,提拉注射器针芯至2 ml 处,使注射器保持负压状态,反复旋转抽吸3~5 次后改变进针方向,使针头在结节内呈扇形朝不同方向抽吸,当注射器内出现红色吸取物后,去负压退针。使用吸取物涂片2~3 张,置入95%乙醇固定液中;部分吸取物送液基薄层细胞学检测(图1)。在相同穿刺点行超声引导下粗针穿刺,根据超声提示达至结节边缘,推按内针手柄将内针插入病变区至止动点,迅速按压内针手柄闭合外套管,退针完成活检后迅速使用福尔马林溶液固定并送病理检查。穿刺部位使用无菌纱布覆盖并按压20 min。将FNA 和CNB 诊断为疑似恶性及恶性结节者均进行石蜡切片病理检查。
1.3 免疫组化检查 选用 CK5/6、34 βE 12、E.cadherin、P120、P53、P63 等鉴别乳腺腺病、乳腺浸润癌、导管/小叶增生及导管/小叶原位癌等;calponin、p63、CD31、CD40、S100 等可判断肿瘤有无浸润及侵犯;雌激素受体(ER)、孕激素受体(PR)、人类表皮生长因子受体-2(HER-2)指导乳腺癌治疗,判断预后。
1.4 统计学方法 采用SPSS 25.0 软件,计数资料组间比较采用χ2检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 CNB 和FNA 结合细胞蜡块免疫组化取材结果比较 FNA 取材成功率为94.3%(151/160),其中9 例失败,涂片有大量红细胞,未能做出诊断。CNB取材成功率为95%(152/160),其中8 例抽取物为凝血块或纤维脂肪组织,未能做出诊断。160 例患者行FNA 联合细胞块免疫组化与CNB 检查,均未见明显并发症。两种方法诊断差异无统计学意义(P>0.05),见表1。

表1 FNA 联合细胞块免疫组化与CNB 病理结果比较[例(%)]
2.2 CNB 和FNA 结合细胞蜡块免疫组化与病理及随访结果比较 151 例FNA 取材成功患者中,恶性病变92 例,其中90 例细胞学检查、细胞块免疫组化联合诊断结果与随访结果相符,阳性符合率为97.8%(90/92)。152 例粗针穿刺取材成功者中,恶性病变99 例,其中93 例组织学检查结合免疫组化联合诊断结果与随访结果相符,阳性符合率为94%(93/99)。两组穿刺成功率和阳性符合率比较,差异无统计学意义(χ2=0.803、0.281,P>0.05)。见图1、2。
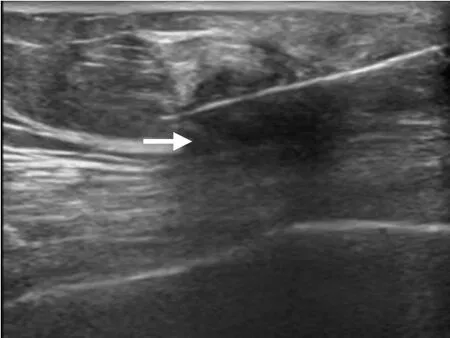
图1 女,38 岁,浸润性乳腺癌。右乳疑似实性结节超声引导下细针穿刺显示结节边界欠清,形态欠规则(箭)

图2 女,65 岁,乳腺基底细胞样癌。超声引导下细针穿刺病变部位细胞免疫组化染色(两步法,×400)示ER(-)(A)、PR(-)(B)、HER-2(-)(C)、Ki-67(+)(D)
3 讨论
超声引导下穿刺活检可早期诊断疑似BI-RADS 4 类乳腺恶性结节[2]。本研究显示FNA 结合免疫组化检测和CNB 检查诊断乳腺结节性质无显著差异,穿刺成功率和阳性符合率比较有显著差异,提示超声引导FNA 细胞学检查联合细胞块免疫组化技术诊断疑似恶性乳腺结节与组织学检查具有相同的诊断效果。
超声引导下细针穿刺细胞学检查可通过检测细胞有无异型性获得病理诊断,临床上广泛用于乳腺结节的良恶性诊断,但因取材标本不足未能充分显示病变组织结构导致假阴性率偏高[3-4]。超声引导下粗针穿刺活检获得的标本在组织学异型性和核异型性上可获得准确的病理诊断。然而,粗针穿刺活检较细针穿刺创伤大,受到患者年龄、部位、凝血状态及结节大小限制等因素的影响,故临床应用受限。
细胞蜡块免疫组化检测是一种基于涂片细胞学诊断基础上的病理诊断方法[5],可连续切片,避免细胞涂片脱片;标本易于保存;同时避免了细胞重叠堆积、薄厚不等现象[6]。细胞蜡块免疫组化和超声引导下FNA 结合后进行细胞学或组织学检查的优势为:①较粗针穿刺创伤更小、适用人群范围更广、操作过程简便快捷、检查后对后续治疗无不良影响,拓宽了老年和不能耐受组织活检患者乳腺结节疾病诊断路径[7];②免疫组化检测仅需较短时间即可获得病理学诊断[8-9];③CNB 对直径<1 cm 的结节容易取材不准确,而FNA 可多角度取材,更容易获得病变组织;④降低了漏诊率和误诊率,可达到与粗针组织学穿刺相同的病理诊断符合率;⑤血供丰富的恶性结节可通过结合免疫组化检测方法,避免因针吸出血造成有效细胞收集不足[10];⑥免疫组化检测可同时获得P53、ER、PR 及HER-2 等病理诊断和疾病分期的指标,有助于鉴别乳腺腺病及浸润性乳腺癌,区分普通型增生和不典型增生与原位癌[11],同时为临床治疗提供了依据,使患者得到准确的诊断和治疗[12-13]。
既往研究显示,CNB 的诊断敏感度明显高于FNA,在诊断疑似乳腺癌方面更具优势,而两者诊断假阴性率均较高[4,14-15]。王金祥等[16]在超声引导下穿刺活检对BI-RADS 分级诊断中发现,乳腺肿块直径<1 cm 和导管内乳头状肿瘤的假阴性率较高。本研究显示将细胞学穿刺与免疫组化检测相结合可降低单纯进行FNA和CNB 的假阴性率,提高了临床诊断率。
总之,超声引导FNA 细胞学检查联合细胞块免疫组化技术诊断疑似恶性乳腺结节与组织学检查的诊断效果相同,与粗针穿刺相比体现了特殊的优势。
