ox-LDL诱导的Raw264.7细胞炎症因子表达变化及PPARγSer273磷酸化调控作用观察
2020-09-08沈娜方涛苏卫东刘勇李焕明
沈娜,方涛,苏卫东,刘勇,李焕明
天津市第四中心医院,天津 300140
动脉粥样硬化(AS)是一种脂质异常触发的动脉内膜慢性炎症性疾病,巨噬细胞所介导的炎症反应在AS的发生发展中发挥关键作用。既往研究[1,2]表明,氧化低密度脂蛋白(ox-LDL)可诱导巨噬细胞发生炎症,细胞中TNF-α、IL-1β等促炎因子呈高表达。研究[3,4]显示,PPARγ对心血管疾病具有一定的保护作用,具有减轻氧化应激、抑制炎症反应、改善糖脂代谢、拮抗细胞凋亡等功能,与AS的发生发展呈负相关。此外还有研究发现,PPARγ磷酸化对AS也具有调节作用,CDK5介导的PPARγSer273磷酸化可调节多种与AS相关的脂肪因子的释放,如脂联素、瘦素、抵抗素、内脂素等[5~8],间接促进了AS发生发展,拮抗了PPARγ的抗AS作用。然而,PPARγSer273磷酸化对AS的直接作用仍不明确。2018年9月~2019年12月,我们观察了ox-LDL诱导后小鼠单核巨噬细胞白血病细胞株Raw264.7中炎症因子表达变化和PPARγSer273磷酸化情况,探讨PPARγSer273磷酸化是否通过促进ox-LDL诱导的巨噬细胞炎症反应起到促进AS的作用。
1 材料与方法
1.1 细胞、主要试剂及仪器 Raw264.7细胞(中国科学院上海细胞库),293T细胞(南开大学分子病毒学实验室惠赠)。DMEM培养基(美国Gibco公司),标准胎牛血清(美国Hyclone公司),EDTA-胰蛋白酶消化液(北京Solarbio公司),氧化低密度脂蛋白(广州奕元生物技术有限公司),pPPARγ(美国New England Peptide公司),PPARγ、β-actin(美国Abcam公司),辣根过氧化物酶标记的羊抗兔、羊抗鼠IgG(北京Solarbio公司),TNF-α酶联免疫吸附试剂盒(美国R&D Systems公司),IL-1β酶联免疫吸附试剂盒(加拿大Anogen-Yes Biotech公司),LipofectamineTM2000转染试剂(美国Thermofisher公司),总RNA提取试剂盒(美国Qiagen公司),cDNA合成试剂盒(日本Takara公司),qPCR试剂盒(美国Promega公司),引物(上海生工生物工程股份有限公司)。CO2培养箱、生物安全柜(美国Thermo Fisher公司),电泳仪(美国Bio-Rad公司),PCR仪(瑞士Roche公司),酶标仪(瑞士Tecan公司)。
1.2 ox-LDL诱导后Raw264.7细胞炎症因子和PPARγSer273磷酸化检测 ①Raw264.7细胞炎症因子TNF-α和IL-1β分泌量检测:取对数期生长的Raw264.7细胞,以5×105个细胞/孔接种于6孔板中,每孔加入2 mL完全培养基(90%DMEM培养基+10%标准胎牛血清),于37 ℃、5%CO2的环境的培养箱中培养。待细胞融合至70%左右进行分组,将实验分为ox-LDL组和对照组,ox-LDL组加入50 mg/L的ox-LDL诱导,对照组则不予任何处理,24 h后,采用ELISA法检测细胞培养液中炎症因子TNF-α和IL-1β的浓度。收集上述两组细胞的培养液,置于EP管中,以3 000 r/min速度离心5 min,分别按照TNF-α和IL-1β试剂盒说明书进行操作,每个样品设置2个复孔。于酶标仪450 nm处读取各孔吸光度值,以标准品吸光度值为横坐标,浓度为纵坐标绘制标准曲线,计算各孔样品浓度值(pg/mL),每组重复3次,取平均值。②Raw264.7细胞中PPARγSer273磷酸化水平检测:Raw264.7细胞培养、分组和干预方法同“①”。采用Western blot法检测PPARγ和PPARγSer273磷酸化蛋白的相对表达量。将各组细胞收集至1.5 mL的EP管中,使用含1%PMSF的RIPA裂解液,于摇床上4 ℃裂解30 min,裂解结束后,离心吸取上清,即为细胞总蛋白。以BCA法测定各组蛋白浓度,加入适量蛋白上样缓冲液。样品蛋白经SDS-PAGE电泳后转印至PVDF膜上,将PVDF膜置于10%脱脂奶粉中室温封闭1 h,一抗(兔抗pPPARγ、PPARγ均为1∶1 000,鼠抗β-actin为1∶10 000)室温孵育3 h,HRP偶联的二抗(1∶10 000)室温孵育45 min,ECL法显色后于凝胶成像仪中成像,以β-actin作为内参,使用Image Lab软件分析各组蛋白条带的灰度值,计算PPARγSer273磷酸化与PPARγ蛋白相对表达量的比值,作为PPARγSer273磷酸化水平,每组重复3次,取平均值。
1.3 PPARγSer273位点突变后Raw264.7细胞炎症因子分泌量、mRNA检测 ①构建并筛选PPARγ缺陷型Raw264.7细胞:a.使用293T细胞构建逆转录病毒颗粒。取对数期生长的293T细胞,以5×105个细胞/孔接种于6孔板中,待细胞融合至60%时进行分组,实验分为实验组和无关对照组,实验组取水泡型口炎病毒G蛋白包膜蛋白质粒、莫罗尼白血病病毒包装质粒和PPARγ缺陷型重组质粒稀释至1 μg/μL,以1∶2∶2的比例与lipo2000混匀共转染293T细胞,48 h后收集上清,以12 000 r/min速度离心20 min获得PPARγ缺陷型病毒颗粒;无关对照组重组质粒为无关对照质粒,其余处理方式同实验组。b.用上述病毒颗粒感染Raw264.7细胞。取对数期生长的Raw264.7细胞,以5×105个细胞/孔接种于6孔板中,待细胞融合至70%时进行分组,实验分为实验组、无关对照组和未处理组。实验组取出1 mL培养基后,加入含PPARγ缺陷型病毒颗粒的培养基(500 μL病毒颗粒+1 μL polybrene+499 μL DMEM完全培养基),以3 000 r/min离心10 min提高感染效率。24 h后,加入2 μg/mL嘌呤霉素筛选出稳定表达PPARγ缺陷型细胞系;无关对照组加入含无关对照的病毒颗粒,其他处理方法同实验组;未处理组不予任何处理。c.观察PPARγ沉默情况。取“①b”中的3组细胞,利用“1.2”中的方法提取蛋白并检测PPARγ蛋白的相对表达量,与无关对照组和未处理组比较,实验组未检出PPARγ表达,表明PPARγ沉默成功。②构建并筛选PPARγSer273突变型和PPARγ野生型Raw264.7细胞:a.制备PPARγSer273突变型和PPARγ野生型病毒颗粒,方法同“①a”。b.用上述病毒颗粒感染PPARγ缺陷型Raw264.7细胞。取对数期生长的PPARγ缺陷型Raw264.7细胞,以5×105个细胞/孔接种于6孔板中,待细胞融合至70%时进行分组,S273A+ox-LDL组细胞经PPARγSer273突变型质粒转染,并以50 mg/L ox-LDL诱导;S273A组细胞经PPARγSer273突变型质粒转染,但不予50 mg/L ox-LDL诱导;WT+ox-LDL组经PPARγ野生型质粒转染,并以50 mg/L ox-LDL诱导;WT组组经PPARγ野生型质粒转染,但不予50 mg/L ox-LDL诱导;其余处理方式同“①b”。c.观察PPARγSer273突变型和PPARγ野生型Raw264.7细胞构建情况。取上述“②b”中的S273A组和WT组细胞,利用“1.2”中的方法进行蛋白提取并检测各组细胞PPARγ和PPARγSer273磷酸化蛋白的相对表达量,两组PPARγ蛋白相对表达量无差异,而与WT组相比,S273A组不再检测出磷酸化,说明细胞系构建成功。③PPARγSer273位点突变后Raw264.7细胞炎症因子分泌量检测:取对数期生长的PPARγSer273突变型和PPARγ野生型Raw264.7细胞,分别以5×105个细胞/孔接种于6孔板中,待细胞融合至70%左右进行分组,实验分为S273A+ox-LDL组、S273A组、WT+ox-LDL组、WT组。S273A+ox-LDL组和WT+ox-LDL组分别加入50 mg/L的ox-LDL诱导,S273A组和WT组不予任何处理,24h后,采用ELISA法检测各组细胞培养液中炎症因子TNF-α和IL-1β的浓度,方法同“1.2”。④PPARγSer273位点突变后Raw264.7细胞中TNF-α、IL-1β mRNA检测:细胞培养、分组和干预方法同“③”。采用PCR法检测各组细胞中TNF-α和IL-1β的mRNA的相对表达量,首先使用RNeasy Mini Kit提取各组细胞总RNA,随后用PrimeScript RT-PCR Kit将其反转录为cDNA。引物:TNF-α:上游5′-GATCGGTCCCCAAAGGGATG-3′,下游5′-GTGGTTTGCTACGACGTGGG-3′,IL-1β:上游5′-ATGCCACCTTTTGACAGTGATG-3′,下游5′-TGATGTGCTGCTGCGAGATT-3′。按照Promega GoTaq qPCR Master Mix试剂盒说明书进行目的基因扩增,反应体系:RNase Free Water 7.2 μL,上游引物0.4 μL,下游引物0.4 μL,GoTaq qPCR Master Mix 10 μL,模板cDNA 2 μL。反应条件:95 ℃预变性2 min,循环反应设置为95 ℃、15 s,60 ℃、1 min,50个循环。反应结束后,得出各组样品的Ct值,以β-actin为内参,利用2-ΔΔCt法计算目的基因的相对表达量,每组重复3次,取平均值。

2 结果
2.1 ox-LDL诱导后Raw264.7细胞TNF-α、IL-1β分泌量、PPARγSer273磷酸化水平比较 ox-LDL诱导后Raw264.7细胞TNF-α、IL-1β分泌量、PPARγSer273磷酸化水平比较见表1。
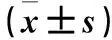
表1 ox-LDL诱导后Raw264.7细胞TNF-α、IL-1β分泌量、PPARγSer273磷酸化水平比较
2.2 PPARγSer273位点突变后Raw264.7细胞TNF-α、IL-1β分泌量、mRNA表达水平比较 PPARγSer273位点突变后Raw264.7细胞TNF-α、IL-1β分泌量、mRNA表达水平比较见表2。
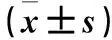
表2 PPARγSer273位点突变后Raw264.7巨噬细胞TNF-α、IL-1β分泌量和mRNA比较
3 讨论
心血管疾病是威胁人类健康的主要疾病,随着生活水平的迅速提高和生活方式的巨大改变,心血管疾病的发病率和死亡率显著上升[9],AS是多种心血管疾病的病理基础,巨噬细胞作为AS核心细胞,在AS整个疾病过程中都发挥重要作用,包括单核巨噬细胞募集、巨噬细胞泡沫化、巨噬细胞增殖、凋亡、极化、坏死等,这些功能的综合作用决定了疾病的进展与消退。小鼠单核巨噬细胞白血病细胞株Raw264.7是一种常见的AS模型细胞,在泡沫细胞形成、炎症反应、氧化应激、巨噬细胞迁移等方面均有研究[10~12]。此外,Raw264.7细胞易于培养,转染效率高,因此本研究选择此细胞作为研究对象,进行后续实验。
TNF-α和IL-1β是AS相关炎症因子,AS患者外周血中TNF-α、IL-1β均呈高水平状态[13]。研究[14]显示,TNF-α可通过增加LDL跨内皮细胞的转运使其在血管壁滞留,促进AS的发生。Yuan等[15]也指出TNF-α加速了巨噬细胞向泡沫细胞的转化,诱导AS脂纹形成。IL-1β也被证明具有促AS的作用,一项大型双盲研究中指出IL-1β抗体卡那奴单抗可通过降低IL-1β活性改善心肌梗死患者的预后,并降低炎症标志物水平[16],细胞和动物实验均证实,靶向IL-1β抗体能够抑制AS炎症因子的分泌,减小病变面积[17]。因此,针对于TNF-α和IL-1β的机制研究越来越受到关注。ox-LDL是一种诱发斑块炎症的标志物[18],一方面其通过启动TLRs信号通路使巨噬细胞产生TNF-α[19],另一方面通过激活炎症小体NLRP3,产生IL-1β[20]。炎症反应可受多种潜在机制的调节,PPARγ作为AS的保护因子,其抗炎作用早已得到证实,研究显示PPARγ通过调节TNF-α、IL-1、IL-6、细胞间黏附分子-1(ICAM-1)、血管细胞黏附分子-1(VCAM-1)等因子改善内皮功能,从而发挥抗AS的作用[21]。Yao等[22]研究指出,PPARγ可诱导巨噬细胞分化为M2抗炎表型,从而改善了细胞炎症状态,起到抑制斑块形成,维持斑块稳定性的作用。PPARγ的作用受翻译后修饰的调节,如磷酸化、乙酰化、泛素化等,不同的生物学修饰可发挥不同功能,其中PPARγSer273磷酸化主要参与肥胖相关胰岛素抵抗相关机制,本课题组前期研究证实,PPARγ部分激动剂替米沙坦通过降低PPARγSer273磷酸化来改变脂联素、瘦素、FABP4、GLUT4和CAP的表达,促进脂联素分泌,从而增加胰岛素敏感性[23]。另有研究表明脂肪细胞中的PPARγSer273磷酸化可诱导TNF-α、IL-1β等炎症因子表达[24],因此我们推测在巨噬细胞中,PPARγSer273磷酸化也可能具有相同作用。本研究发现,ox-LDL刺激后,PPARγSer273磷酸化水平增加,同时炎症因子释放增加,提示PPARγSer273磷酸化可能促进了巨噬细胞炎症反应。为进一步验证其作用,我们将PPARγSer273位点进行突变,并以WT型PPARγ作为对照,检测细胞中炎症因子分泌和表达水平,结果显示PPARγSer273位点突变后该位点不再检测出磷酸化水平,且随着磷酸化水平的消失,两种促炎因子的分泌和表达水平也下降,验证了PPARγSer273磷酸化对巨噬细胞炎症因子的促进作用。
总之,PPARγSer273磷酸化促进了ox-LDL诱导的巨噬细胞炎症反应,进一步加速了AS进程。
