氟尼辛葡甲胺掩味口腔崩解片的质量标准研究
2020-09-07颜国庆徐杨峰彭健波邓锐涵吴莉芩陈海兰黄宏业何家康
颜国庆,徐杨峰,彭健波,邓锐涵,吴莉芩,陈海兰,2,黄宏业,何家康,2
(1.广西大学动物科学技术学院,广西 南宁 530005 ; 2.广西兽药制剂工程技术研究中心,广西 南宁 530003 ; 3.广西北斗星动物保健品有限公司,广西 南宁 530003)
氟尼辛葡甲胺(Flunixin meglumine,FM)是一种动物专用的非甾体抗炎药(Nonsteroidal antiinflammatory drugs,NSAIDs),具有良好的抗炎、解热和镇痛效果,在国内外已被广泛应用于牛、马、猪、犬、猫等动物的解热、肌肉疼痛、关节炎等病症[1]。
氟尼辛葡甲胺广泛应用于兽医临床[2-4],但其剂型较为单一,主要以颗粒剂、注射剂为主。氟尼辛葡甲胺具有较强的刺激性气味和苦味,动物口服适口性差,因此研制掩味口服制剂有重要意义。氟尼辛葡甲胺掩味口腔崩解片是本课题组利用热熔挤出技术制备FM掩味固体分散体,经制粒后加以辅料通过直接压片法制备而成的片剂,解决了普通口服制剂动物的顺应性差、传统的注射剂对注射部位刺激性大等问题[5]。为科学有效的控制产品质量,保证临床疗效,本试验参照《中华人民共和国兽药典》、《兽药研究技术指导原则汇编》(2006-2011年)等[6-7],对氟尼辛葡甲胺掩味口腔崩解片建立了薄层鉴别、崩解时限、重量差异、脆碎度、溶出度、含量测定等考察项目的检查方法,为氟尼辛葡甲胺掩味口腔崩解片质量标准的制定奠定基础。
1 材料与方法
1.1 材料
1.1.1 仪器设备 高效液相色谱仪:Waters e2695,美国Waters公司;紫外分光光度计:UV-1750,日本岛津公司;智能溶出试验仪:ZRS-8LD、脆碎度仪:FT-2000SE、智能崩解仪:ZBS-6E,天津天大天发科技有限公司;全自动薄层板器:939,重庆南岸贝尔德仪器技术厂;电子天平:EL204,梅特勒-托利多仪器(上海)有限公司;色谱柱:Phenomenex luna C18(250 mm×4.6 mm,5 μm),美国Waters公司。
1.1.2 主要试剂 氟尼辛葡甲胺对照品(98%,批号:H0611604),购自中国兽医药品监察所;磷酸二氢钾、甲苯、乙酸乙酯、醋酸钠、冰醋酸、盐酸、硝酸、氯化钙 (CaCl2·2H2O)、氯化镁(MgCl2·6H2O)、氯化钠(NaCl)、碳酸钾(K2CO3·1.5H2O)、磷酸氢二钠(Na2HPO4·7H2O)、磷酸二氢钠(NaH2PO4·H2O)、异丙醇,均为分析纯,均购自成都科龙化工试剂公司;乙腈(色谱纯)、甲醇(色谱纯),均购自美国ThermoFisher Scientific公司。
1.1.3 试验药物 3批FM掩味口腔崩解片样品(批号:20170308、20170315和20170322),400 mg/片(约相当于氟尼辛20 mg),经热熔挤出掩味技术-直接压片法制备而得,为本实验室自制。
1.2 方法
1.2.1 鉴别方法
1.2.1.1 氟尼辛葡甲胺掩味口腔崩解片的鉴别 称量本品适量(约相当于氟尼辛25 mg),研磨成粉末,置于50 mL离心管中,加磷酸盐缓冲液(取无水醋酸钠4.1 g,加水500 mL使溶解,加冰醋酸2.9 mL,用水稀释至1 000 mL,摇匀,即得)10 mL,振摇,再加入乙酸乙酯25 mL,振摇,静置分层,取上层清液作为供试品提取液。此外,取氟尼辛葡甲胺对照品,加甲醇制成每1 mL含1.5 mg氟尼辛葡甲胺的对照品溶液。按照薄层色谱法试验,吸取10 μL上述溶液,分别点于同一硅胶GF254薄层板上,以甲苯-乙酸乙酯-冰醋酸-水(65∶30∶10∶1)为展开剂,展开,取出,晾干,置紫外灯(254 nm)下检视。
1.2.1.2 专属性考察 配制缺氟尼辛葡甲胺的阴性样品,按照标准规定的薄层鉴别检测,考察该方法的专属性。
1.2.1.3 重复性考察 取3批氟尼辛葡甲胺掩味口腔崩解片样品,进行薄层鉴别检测,考察该方法的重复性。
1.2.2 崩解时限检查 按照相关规定,采用改良崩解仪法测定:取本品1片,置崩解仪中进行检查,应在60 s内全部崩解并通过筛网,但无硬心者,可作符合规定论。重复测定6片,均应符合规定。如有1片不符合规定,应另取6片复试,均应符合规定。
1.2.3 重量差异检查[6]精密称定样品20片,计算重量差异限度。每片重量与平均片重比较,平均片重或表示片重在0.30 g以下,重量差异限度应在±7.5%以内;0.30 g及0.30 g以上,重量差异限度应在±5%以内。超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。
1.2.4 脆碎度检查[6]称取样品片约为6.5 g,吹风机吹去粉末,精密称重,置圆筒中,转动100次。取出,吹去粉末,精密称重,减失重量不得过1%,且不得检出断裂、龟裂及粉碎的片,计算样品脆碎度。
1.2.5 溶出度检查
1.2.5.1 溶出介质的制备 人工唾液:取氯化钙 0.228 g,氯化镁 0.061 g,氯化钠 1.017 g,碳酸钾 0.603 g,磷酸氢二钠 0.204 g,磷酸二氢钠 0.273 g,加水800 mL溶解后,用盐酸调节pH值至6.8,用水稀释至1 000 mL,即得;pH值4.5的醋酸缓冲液:取醋酸钠2.99 g,加水500 mL溶解后,加入2 mol/L醋酸溶液14.0 mL,用水稀释至1 000 mL,即得。
1.2.5.2 溶出度标准曲线的制备 精密称取FM对照品52.12 mg,用适量超纯水溶解后,转移至50 mL容量瓶中,并以超纯水稀释至刻度,即得1 mg/mL的对照品贮备液,备用。用介质将氟尼辛葡甲胺对照品贮备液稀释成一系列标准工作液。然后以介质为空白对照,以紫外-可见光分分光度法在282 nm处测定吸光度,每个浓度设3个重复,以吸光度为横坐标,浓度为纵坐标,进行线性回归。
1.2.5.3 溶出度条件的设定 缓冲液中溶出度:pH值4.5的醋酸缓冲液900 mL,注入溶出杯中,温度保持(37±0.5)℃,转速100 r/min。称取本品适量(约相当于氟尼辛12.5 mg),投入转篮中,于5 min、10 min、20 min、30 min、50 min、60 min、90 min、120 min取样,取样经0.8 μm微孔水相滤膜过滤,平行3次。以pH值4.5的醋酸缓冲液为空白对照,于紫外282 nm波长处测定样品吸光度。
人工唾液中溶出度:人工唾液300 mL,注入溶出杯中,温度保持(37±0.5)℃,转速100 r/min。称取本品适量(约相当于氟尼辛12.5 mg),每隔10 s取样至1 min,经0.8 μm微孔水相滤膜过滤,平行3次。以人工唾液为空白对照,于紫外282 nm波长处测定样品吸光度。
1.2.5.4 溶出度计算 将各个样品的吸光度带入标准曲线,吸光度超出标准曲线的范围,则用相应介质将样品稀释后再测定吸光度,计算FM的累积溶出百分比。
1.2.6 含量测定
1.2.6.1 色谱条件 色谱柱:Phenomenex luna C18(250 mm×4.6 mm,5 μm);紫外检测器,检测波长:282 nm;柱温:30 ℃;流动相:甲醇∶0.1%磷酸二氢钾溶液=80∶20(V∶V);流速:1.0 mL /min;进样量:20 μL。
1.2.6.2 对照品药液的制备 称取氟尼辛葡甲胺52.12 mg,置于50 mL容量瓶中,用超纯水溶解并稀释至刻度,制成1 mg/mL对照品贮备液。
1.2.6.3 供试品溶液的配制 称取本品适量(约相当于氟尼辛葡甲胺10 mg),并研磨成粉,置于100 mL容量瓶中,加入适量流动相,超声溶解15 min,取出,放冷,用流动相稀释至刻度,即得。
1.2.6.4 阴性样品液的制备 按处方10倍量称取空白辅料,按照供试品溶液配制方法,制备阴性样品液。
1.2.6.5 方法的专属性 取对照品药液、供试品溶液、阴性样品液按色谱条件测定,考察方法专属性。
1.2.6.6 标准曲线的制作和线性关系的考察 精密吸取适量对照品药液,用流动相稀释制成一系列浓度的工作液,按照色谱条件进行高效液相色谱测定,以浓度为横坐标,峰面积为纵坐标,进行线性回归,绘制氟尼辛葡甲胺标准曲线,考察氟尼辛葡甲胺在规定范围内的线性关系。
1.2.6.7 精密度试验 重复性试验:取同一批样品6份,照供试品溶液配制方法制备,按照色谱条件测定,记录峰面积,计算相对标准偏差RSD(%)。中间精密度试验:于同一实验室由不同人员用不同设备完成样品测定。
1.2.6.8 加样回收率试验 称取已知含量的片剂适量,充分研碎,置于100 mL容量瓶中,加入已知浓度对照品溶液适量,按供试品制备方法处理,按照色谱条件测定,计算加样回收率和相对标准偏差(%)。
1.2.6.9 稳定性试验 取同一批号的氟尼辛葡甲胺掩味口腔崩解片样品,按1.2.6.3下方法制备供试品溶液,分别在0、4、8、12、16、20 h和24 h进样20 μL,考察其稳定性。
1.2.6.10 样品测定 取3批氟尼辛葡甲胺掩味口腔崩解片样品,按色谱条件测定,计算氟尼辛葡甲胺含量。
2 结果
2.1 氟尼辛葡甲胺的薄层鉴别 3批氟尼辛葡甲胺掩味口腔崩解片,按标准规定的薄层鉴别方法检测,结果显示,3批供试品色谱与FM对照品色谱相应位置上,显相同颜色的荧光斑点,而配制的缺FM的阴性样品无干扰,薄层色谱图见图1。
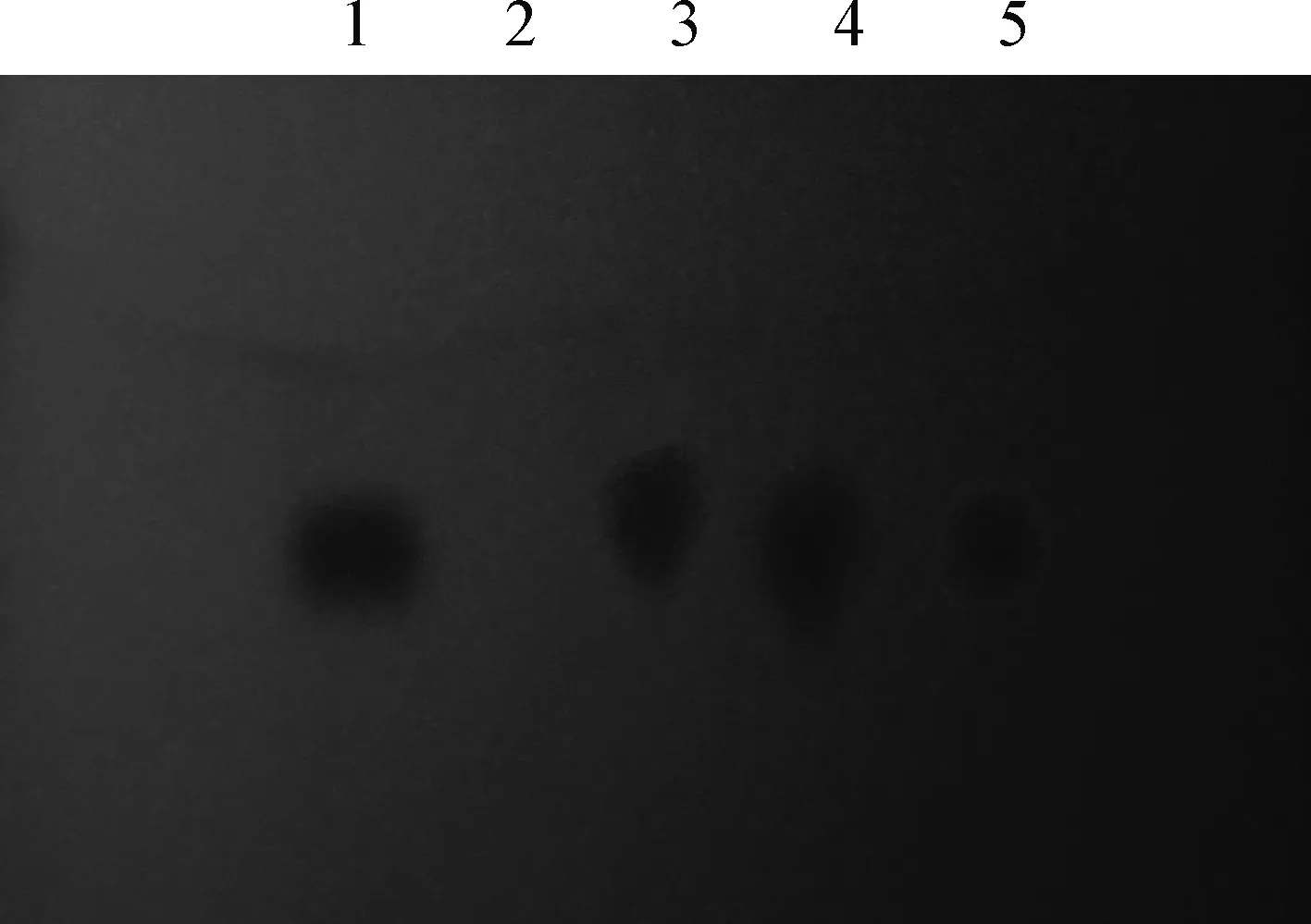
图1 氟尼辛葡甲胺掩味口腔崩解片中氟尼辛葡甲胺薄层色谱图Fig. 1 The thin layer chromatogram of FM identification on FM ODT1:FM对照品; 2:阴性样品; 3:供试样品(批号:20170308);4:供试样品(批号:20170315); 5:供试样品(批号:20170322)1:The standard of FM; 2:Negative sample; 3:Test sample (Batch number:20170308); 4:Test sample (Batch number:20170315); 5:Test sample (Batch number:20170322)
2.2 崩解时间检查 取3批样品,进行崩解时间检查。3批样品的崩解时间分别为(17.52±1.44)s、(16.58±1.73)s、(18.13±1.02)s,均小于30 s,结果符合规定。
2.3 重量差异检查 取3批样品,进行重量差异检查。3批样品重量差异结果分别为(2.72±1.02)%、(3.13±1.12)%、(3.13±1.14)%,均小于重量差异限度±5%,结果符合规定。
2.4 脆碎度检查 取3批样品,进行脆碎度检查。3批样品的脆碎度分别为(0.88±0.08)%、(0.87±0.06)%、(0.82±0.02)%,均小于1%,结果符合规定。
2.5 溶出度检查 取3批样品,进行溶出度检查。口崩片在人工唾液中60 s内溶出低于10%(图2),在pH值4.5缓冲液中10 min内溶出超过80%(图3),表明氟尼辛葡甲胺掩味口腔崩解片具有掩味效果及速释特性。

图2 制剂在人工唾液中的溶出度Fig. 2 Dissolution of the FM taste-masked ODTs in artificial saliva
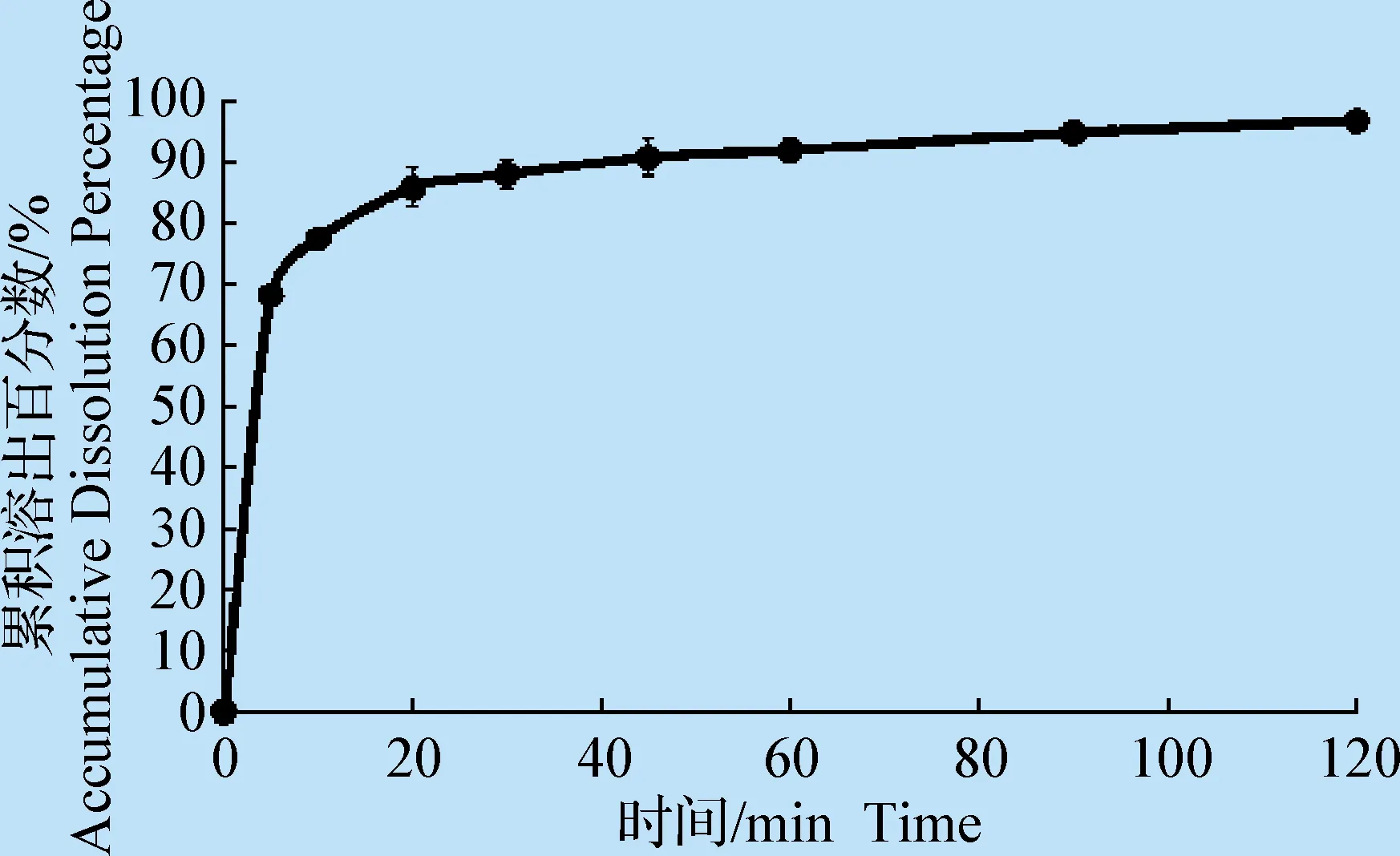
图3 制剂在pH值4.5缓冲液中的溶出度Fig. 3 Dissolution of the FM taste-masked ODTs in pH 4.5 buffer solution
2.6 含量测定
2.6.1 专属性试验 结果表明,供试品溶液中FM与相邻峰的分离度良好,氟尼辛葡甲胺的测定无干扰(图4)。
2.6.2 标准曲线的制作 氟尼辛葡甲胺回归方程(图5)为y=48 647x-56 582,R2=0.999 8,在24.5~245 μg/mL范围内线性关系良好。
2.6.3 精密度试验
2.6.3.1 重复性试验 样品中药物的平均含量为4.97%,RSD为0.04%,仪器精密度良好。
2.6.3.2 中间精密度试验 样品中药物的平均含量为4.90%,RSD为2.44%,仪器精密度良好。
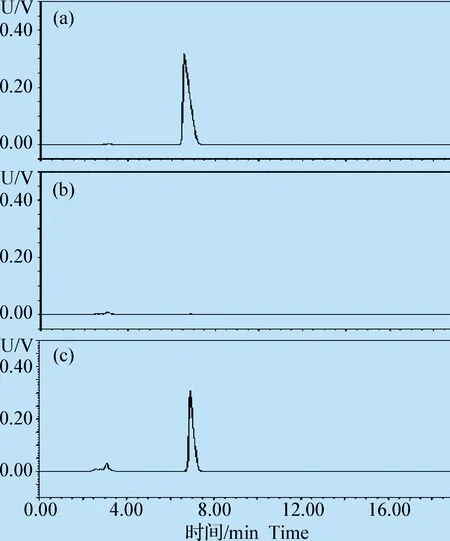
图4 系统适应性试验及方法专属性考察色谱图Fig. 4 The chromatogram of system suitability test and method specificityA:FM对照品; B:阴性样品; C:氟尼辛葡甲胺掩味口腔崩解片供试品溶液A:The standard of FM; B:Negative sample; C:Test sample

图5 氟尼辛葡甲胺标准曲线Fig. 5 The standard curve of FM
2.6.4 稳定性试验 24 h内氟尼辛葡甲胺掩味口腔崩解片供试品中药物的平均含量为4.90%,RSD为1.29%。结果表明,供试品溶液在室温下24 h内稳定。
2.6.5 加样回收率试验 结果如表1。氟尼辛葡甲胺平均回收率为99.45%,RSD为0.58%(n=6)。结果表明方法准确度良好。
2.6.6 样品测定 3批氟尼辛葡甲胺掩味口腔崩解片样品含量测定见表2。201703008、20170315、20170322三个批次样品的含量分别为(4.876±0.102)%、(4.959±0.066)%和(4.960±0.053)%。

表1 加样回收率试验结果Table 1 The results of sample recovery rate test (%,n=6)

表2 3批氟尼辛葡甲胺掩味口腔崩解片的含量Table 2 The content of three batches sample of FM taste-masking ODT (%,Mean±SD,n=6)
3 讨论
3.1 高效液相色谱条件的确定 对氟尼辛葡甲胺对照品的紫外吸收光谱(200~400 nm)测定结果表明,FM在281.5 nm处有最大吸收,为了保证灵敏性,色谱波长选择282 nm。其他色谱条件参照《中华人民共和国兽药典》(2015年版一部)[6]收载的氟尼辛葡甲胺的含量测定方法,进行多次的筛选、验证,最终确定上述色谱条件。结果显示,在该色谱条件下,氟尼辛葡甲胺色谱峰分离度良好,且阴性样品色谱图相同保留时间中未出现干扰峰。
3.2 氟尼辛葡甲胺掩味口腔崩解片的重点考察项目 口腔崩解片主要的质控标准为崩解时限和溶出度[8],因此,根据本试验片剂的掩味、速释效果和口腔崩解等特性,拟定了薄层鉴别、崩解时限、重量差异、脆碎度、溶出度、含量测定考察项目并建立了相应的检查方法。其中溶出度和崩解时限项目同普通片剂检查方法略有不同。
本制剂为掩味口腔崩解片,目的是使药物在口腔中尽量少溶解达到掩味效果,而在胃肠道中尽量快溶解以快速发挥效果,但是主药氟尼辛葡甲胺在酸性环境中属于微溶状态,且辅料Eudragit®E PO在小于pH值为5的溶液中会形成盐而迅速溶解,因此参考相关文献[7,9-11]对氟尼辛葡甲胺掩味口腔崩解片在人工唾液和pH值4.5缓冲液的溶出度进行考察,体外溶出度结果表明本制剂具有掩味特性,但要最终确定该片剂的掩味效果,仍需进行电子舌、志愿者和动物试验等方面的评价。
对于崩解时限,目前口腔崩解片的崩解时间的测定尚没有法定的标准方法。本试验参阅相关文献[12-14],对不同测定方法进行比较,其中改良崩解仪法有标准仪器,重现性好且易于操作,因此最终选择改良崩解仪法作为崩解时间的测定方法。结果表明,本制剂崩解迅速,崩解时限满足口腔崩解片的要求。
