高校生活饮用水软化研究
2020-08-26叶祥桔黎少君李子荣汪徐春
刘 川,贡 飞,叶祥桔,杨 梅,黎少君,李子荣,汪徐春
(安徽科技学院 化学与材料工程学院,安徽 凤阳 233100)
水质硬度是指水中钙、镁、铁、铝、等离子的含量多少,通常以Ca2+、Mg2+含量计算。单位有两种,一种用mg/L表示,一种用度表示。硬水是指水质中含有大量Ca2+、Mg2+等离子的水,而软水是指水质中含有少量或者不含Ca2+、Mg2+等离子的水。此外,硬水又有暂时性硬水和永久性硬水之分。暂时性硬水是指水质中的钙、镁离子主要以碳酸氢盐形式存在,当水被煮沸时这些碳酸氢盐变为碳酸盐沉淀析出,水质转变为软水。永久性硬水是指水质中的钙、镁离子以氯化物或者硫酸盐形式存在,通过烧煮不能将其除去,水质不会转变为软水[1]。我国《生活饮用水卫生标准》(GB 5748-2006)明确指出生活饮用水总硬度不能高于450 mg/L(以CaCO3计)[2]。当前,随着工业化的发展,水资源正遭受严重污染,水质中Ca2+、Mg2+等离子严重超标[3]。长期饮用硬水会使人体肠胃系统功能紊乱,且肾结石发病率升高。用硬水洗脸、沐浴,会堵塞皮肤腺体开口,影响正常代谢,使皮肤过早萎缩老化[4-5]。测量水质硬度的方法非常多,其中EDTA测水质硬度的方法运用最为普遍,该方法操作准确可靠,相关仪器设备价格较为低廉[6-10]。
高校人口密集,水质的优劣直接影响师生的身心健康。安徽科技学院地处安徽凤阳,因地处石英砂产地,饮用水硬度较高,学校师生患肾结石现象时有发生。本研究以安徽科技学院凤阳校区生活饮用水为研究对象,利用EDTA测水质硬度的方法测定水质总硬度,并运用持续煮沸法、药剂软化法、离子交换法对水样进行软化研究,旨在为有效软化高校生活饮用水提供依据。
1 材料与方法
1.1 供试材料
乙二胺四乙酸钠(EDTA,99%,Alfar Aesar);碳酸钙(CaCO3,99%,国药集团化学试剂有限公司);氢氧化钠(NaOH,96%,国药集团化学试剂有限公司);碳酸钠(Na2CO3,99.8%,国药集团化学试剂有限公司);732型离子交换树脂(95%,廊坊拓豪树脂有限公司);三乙醇胺(C6H15NO3,98%,Alfar Aesar);氯化铵(NH4Cl,99.5%,国药集团化学试剂有限公司);钙指示剂(Alfar Aesar);铬黑T(Alfar Aesar)。
仪器:FA2104B分析天平(上海越平科学仪器制造有限公司);DZS-706型多参数水质分析仪(上海仪电科学仪器股份有限公司)。
1.2 实验方法
1.2.1 EDTA标准溶液的配制及标定 称取13.5 g EDTA,溶于温水后稀释至5 L;准确称取一定量的CaCO3,用1∶1盐酸溶解后稀释至250 mL容量瓶中;取25 mL钙标准液于锥形瓶中,用10% NaOH调节pH至12并加入钙指示剂,用EDTA标准溶液滴定至终点,平行测定3次。
1.2.2 水样总硬度的测定 取100.00 mL水样,加少量三乙醇胺溶液和NH3-NH4Cl缓冲溶液,铬黑T少许,用EDTA标准溶液滴定至终点,平行测定3次。
1.3 测定项目及分析方法
1.3.1 持续煮沸法软化效果研究 取11份100 mL水样于11个250 mL锥形瓶中,对11组水样分别做煮沸0、1、2、3、4、5、6、7、8、9、10 min处理。待水样温度降至室温后用EDTA标准溶液测定水样总硬度,重复3次[11]。
1.3.2 药剂软化法软化效果研究 在室温及沸腾条件下,取9份100 mL水样于9个250 mL锥形瓶中,分别加入5、10、15、20、25、30、35、40、45 mL浓度为0.01 mol/L的碳酸钠溶液,用EDTA标准溶液测定水样总硬度,重复3次[12]。
1.3.3 离子交换法软化效果研究 用饱和食盐水浸泡732型离子交换树脂20 h,然后用蒸馏水过滤清洗至排出的水清澈,再用2%氢氧化钠浸泡4 h,放干氢氧化钠溶液后用蒸馏水洗至中性,最后用5%的盐酸溶液浸泡6 h,放干溶液后用蒸馏水洗至中性,烘干放置备用。用移液管量取100 mL水样,加适当质量的预处理后的732树脂,在水温25 ℃的条件下用恒温振荡器振荡(振荡速度设为45 r/min)至水样和树脂接触充分后测定水样的硬度[13]。
2 结果与分析
2.1 持续煮沸对水硬度软化结果及分析
利用EDTA测定水硬度方法,测得待测水样总硬度为138.02 mg/L(以CaCO3计)。图1考察了持续煮沸对水样总硬度的影响。

图1 持续煮沸对水硬度的影响
根据图1得出,持续煮沸使水样总硬度降低,持续煮沸3 min后水样总硬度持续较大幅度下降,持续煮沸6 min后水样总硬度没有显著变化,水样总硬度维持在110 mg/L左右,软化率为20.27%。持续煮沸使水样总硬度下降原因在于加热可使水样中钙等离子的碳酸氢盐分解为CaCO3析出,MgCO3变为更加难溶的Mg(OH)2,虽然持续煮沸自来水的方法对其总硬度的软化效率并不高,但是该方法操作简单,在日常生活中具有一定使用价值。
2.2 药剂软化对水硬度软化结果及分析
利用纯碱法,向水样中投加碳酸钠降低其总硬度,根据实验确定药剂添加量以及酸碱度最佳条件。从图2可以得知,在室温条件下,水样总硬度随碳酸钠投加量的增加而降低,当碳酸钠溶液投加量大于20 mL后,水样总硬度没有显著变化,软化率为25.16%。在投加碳酸钠溶液条件下,水样中的钙、镁等离子与碳酸根离子结合形成碳酸盐沉淀析出,从而造成水样总硬度降低,相关反应如下:

图2 室温条件下碳酸钠加入量对总硬度的影响
当碳酸钠投加量大于20 mL后,水样中钙、镁离子被完全沉淀,因此,继续增加碳酸钠的投放量对水样总硬度不会有显著影响。
根据第一部分的结果及分析得知,沸腾条件下可以降低水样总硬度。因此,考察了在沸腾条件下碳酸钠加入量对总硬度的影响,实验结果如图3所示。

图3 沸腾条件下碳酸钠加入量对总硬度的影响
从图3得知,在沸腾条件下水样总硬度随碳酸钠投加量的变化趋势与室温下相似,碳酸钠投加量大于20 mL后,水样总硬度无明显变化,软化率为77.56%。然而,在沸腾条件下水样总硬度下降量明显大于室温条件下水样总硬度下降量。这主要是因为在沸腾条件下,水样中以碳酸氢盐形式存在的钙、镁离子被析出,从而进一步降低了水样的总硬度。另外,对比图3与图1以及图3与图2数据可知,沸腾条件下加入碳酸钠对水样的软化效果要优于单独煮沸方法与室温下加入碳酸钠方法的加和。
2.3 离子交换技术对水硬度软化结果及分析
分别取100 mL水样于10个锥形瓶中,分别加入1~10 g不同质量的732型离子交换树脂,在25 ℃条件下振荡5 h并分别测定其总硬度,测定结果如图4所示。

图4 树脂投加量对总硬度的影响
从图4得知,水样总硬度随732型离子交换树脂投加量的增加而降低,当732型离子交换树脂投加量超过5 g时,水样总硬度无显著变化,水样软化率为88.78%。在732型离子交换树脂投加量为5 g时,对水样中钙、镁离子吸附量达到最大值,因此选定5 g为32型离子交换树脂最佳投加量。
分别取100 mL水样于6个锥形瓶中,分别加入5 g 732型离子交换树脂,在25 ℃条件下振荡1~6 h并分别测定其总硬度,测定结果如图5所示。
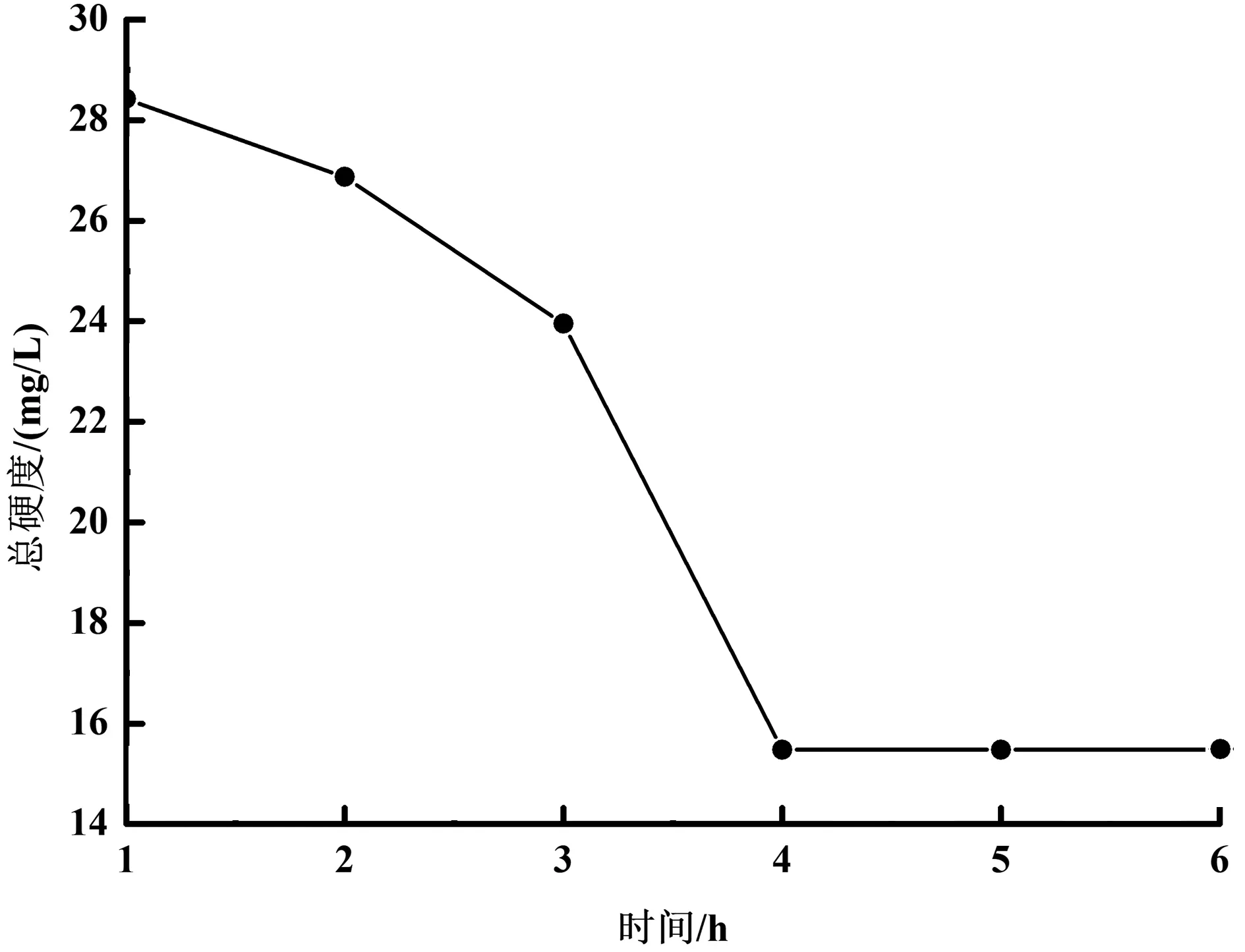
图5 吸附时间对总硬度的影响
从图5得知,在投放5 g 732型离子交换树脂后,水样总硬度随振荡时间的增加而降低,当振荡时间为4 h时水样总硬度无显著变化,水样软化率为88.78%。
3 结论与讨论
本文分别采用了持续煮沸法、药剂软化法、离子交换法降低安徽科技学院凤阳校区自来水硬度的过程进行了实验研究。通过实验得出以下结论:待测自来水水样总硬度为138.02 mg/L(以CaCO3计),持续煮沸水样6 min后其总硬度无显著变化,软化率为20.27%;通过向水样中投加碳酸钠以实现水样软化,室温下软化率为25.16%,沸腾条件下软化率为77.56%;通过732型离子交换树脂对水样进行静态实验,确定100 mL水样的最佳树脂投加量为5 g,最佳吸附时间为4 h,软化率为88.78%。
