脐血单核细胞移植治疗慢性完全性脊髓损伤Ⅱ期临床试验的安全性和疗效评估
2020-08-26封亚平WiseYoung朱辉封雨邓洵鼎谢佳芯张社敏方芳石静陈永和郑爽
封亚平 Wise Young 朱辉 封雨 邓洵鼎 谢佳芯 张社敏 方芳石静 陈永和 郑爽
脊髓损伤(spinal cord injury,SCI)严重危害人类健康,在美国每年大约新增1 万SCI 患者,其中大多数是健康的青壮年,其高致残率给社会和家庭造成了沉重的负担,美国每年SCI 的治疗经费超过10亿美元。我国目前没有具体的统计数据,但不会低于这个数字。SCI 的治疗一直是医学界的难题,也是全球神经科学领域研究的热点和具有挑战性的课题。近年来,急性脊柱脊髓损伤早期固定与髓内外显微减压联合手术取得了可喜的疗效,科学家们采用不同类型的细胞[常用的5 种细胞:骨髓间充质细胞、胎儿神经前体、嗅鞘细胞、雪旺氏细胞和脐血单核细胞(umbilical cord blood mononuclear cell,UCBMC)]移植到损伤的脊髓内,细胞移植可以为轴突生长穿过损伤部位提供一个良好的环境,并取得了良好效果[1-9]。尤其是动物实验研究表明,UCBMC 移植能恢复大鼠和犬SCI 模型的行走功能[10-13]。本研究将该动物实验结果转化于临床进行Ⅱ期临床试验,评估人类白细胞抗原(human leukocyte antigen,HLA)≥4∶6配型的UCBMC 移植治疗慢性完全性SCI 的安全性、可行性、有效性和最佳细胞剂量,以及联合使用甲基强的松龙(methylprednisolone,MP)和碳酸锂对细胞移植的作用,现报道如下。
资料与方法
一、纳入与排除标准
纳入标准:(1)18~60 岁的受试者;(2)慢性SCI(SCI 初次手术后12 个月或以上),且神经学检查结果稳定至少6 个月;(3)美国脊髓损伤协会(American Spinal Injury Association,ASIA)评分为A 级;(4)SCI平面为C3~T12;(5)MRI 显示SCI 部位在3 个脊柱节段以内;(6)受试者必须能够阅读、理解和完成视觉模拟量表;(7)受试者自愿签署伦理委员会批准的知情同意书;(8)如果受试者同意参与但由于身体原因无法签署知情同意书,则应由受试者口头同意、由其直系亲属代签名,并请1 位参与了知情同意全过程的见证人同时签名。
排除标准:(1)有明显的心、脑、血管、肝、肾和精神性疾病;(2)严重的内科或感染性疾病(包括但不限于乙肝病毒携带者和人类免疫缺陷病毒携带者);(3)怀孕或哺乳期妇女;(4)有怀孕能力又不愿意避孕的女性;(5)MRI 显示SCI 长度超过3 个节段;(6)成像技术无法判断SCI 的边缘;(7)无法提供符合HLA 配型的UCBMC;(8)具有椎板切除术、MP 和(或)碳酸锂的任何禁忌证;(9)受试者目前正参与其他研究或者在本研究的筛选访视前4 周内服用了研究药物;(10)研究者的意见认为受试者不符合研究方案和(或)不适合参与本研究。
二、一般资料
选取联勤保障部队第九二〇医院神经外科自2011 年2 月至2014 年1 月收治的20 例SCI 患者作为受试者,均为初次损伤后2 年以上(2~20 年),平均(7.2±1.2)年。其中女性4 例,男性16 例;年龄范围18~53 岁,年龄(36.9±2.4)岁。19 例受试者SCI平面分别位于C5-T11 神经水平,1 例受试者为C3神经水平。所有受试者都有明确的脊柱骨折,18 例受试者均行脊柱骨折钉棒内固定手术。
1.治疗分组:将20 例患者按随机数字表法分为5 组,每组4 例。A 组:在损伤上下缘脊神经背根入处的4 个点(上下各2 点)注射UCBMC(100 000 细胞/μL),每点注射4 μL;B 组:每点的细胞注射量为8 μL;C组:每点的细胞注射量为16 μL;D 组:依据C 组注射细胞量且移植后静脉注射30 mg/kg MP;E组:依据D 组疗程(细胞+MP),手术后服用6 周碳酸锂片(750 mg/d),剂量通过检测血清锂浓度进行调整,使浓度到达0.6~1.0 mmol。
2.UCBMC 提取:HLA≥4∶6 配型人源脐血(美国Stemcyte)解冻后进行Ficoll 梯度离心,取“淡黄薄衣(buffy-coat)”层进行细胞分离。细胞用人工血浆制成混悬液,取少量进行台盼兰染料排斥检验细胞活性。细胞装入含CIM 培养剂的洁净密封袋,以室温运送。细胞分离后须在5 d 内进行移植。移植前,细胞液离心(相对离心力为400 g)浓缩至100 000/μL 活性细胞。细胞以伊思考夫改良DMEM 混悬液(100 万细胞/mL),密封于50 mL Teflon 袋中室温运送至手术室。
三、手术方式
所有患者行全麻,取俯卧位。对于椎板未减压者行损伤节段椎板咬除,暴露硬脊膜;对于已行椎板减压者,分离硬脊膜外疤痕组织;悬吊、切开硬脊膜后在显微镜下行UCBMC 注射。采用28 号手术针头、以45°角针尖向上刺入损伤边缘脊神经背根入处,将细胞混悬液缓慢注入脊髓背侧灰质内,注射速度为1 μL/min(图1),上下各2 点,共注射4 点,为了防止细胞从注射针眼溢出,细胞注射完成后留针5 min,缝合蛛网膜、硬脊膜,放置引流管,然后缝合肌肉和皮肤。A~C 组的细胞注射量分别为每点注射4、8 或16 μL(100 000/μL 活细胞),细胞总量大约为160 万、320 万和640 万活细胞。如每组发现有2例或以上受试者因脊髓内注射而出现神经功能丢失,则前一组的剂量为最高安全剂量,用于D 和E 组。D、E 组除了注射320 万活细胞外,静脉注射30 mg/kg MP。E 组进行为期6 周的口服碳酸锂片,250 mg,2~3 次/d,调整剂量达到0.6~1.0 mmol/L 血药浓度。

图1 显微镜下行脐血单核细胞注射(箭头示进针点)
四、术后处理
1.术后常规使用抗生素预防感染,定期复查血、大便、小便常规和血液肝功能、生化等。术后24~48 h拔除引流管。
2.碳酸锂口服剂量从750 mg/d(250 mg tid)开始,每3 天检测一次血清锂浓度,以碳酸锂250 mg 递增(或递减),即250 mg bid、250 mg tid、500 mg bid 等,直至血清锂浓度达到0.6~1.0 mmol,6 周为1 个疗程。
3.术后2 周,受试者参加为期3 个月的强化昆明十级步行训练[1,3,14]:Ⅰ级:仅能坐轮椅;Ⅱ级:扶助行车站立,需要一人扶双膝;Ⅲ级:扶助行车独立站立;Ⅳ级:扶助行车,需要一人用绷带拉住双膝行走;Ⅴ级:扶助行车,独立行走;Ⅵ级:扶四角架独立行走;Ⅶ级:拄双拐独立行走;Ⅷ级:拄四点拐独立行走;Ⅸ级:蹒跚步态,独立行走;Ⅹ级:正常行走。受试者每天步行训练6 h,每周训练6 d,为期3~6 个月,上午、下午各3 h,住院3 个月或6 个月后出院,如果在3个月时病情仍在好转,1 年的随访时间为41~87 周。
五、临床疗效观察指标及随访
分析比较患者在基线与移植后1、2、6 及14 周的改变。此外,进行6 个月和1 年的随访检查确定疗效和持续性。
主要研究指标:神经学评分,包括运动评分、轻触评分和针刺评分:(1)ASIA 运动评分和感觉评分[15];(2)ASIA 残损分级:简明损伤分级(abbreviated injury scale,AIS)[16]。
次要评分指标:(1)脊髓磁共振成像/密散张量成像分析;(2)脊髓损伤步行指数(walking index of spinal cord injury,WISCI)评分[17];(3)脊髓独立量表(spinal cord independence measure,SCIM)评分[18]:包括生活自理、呼吸和括约肌控制、活动3 个方面,共19 项评分,总分100 分;(4)昆明步行量表(Kunming locomotor scale,KLS)[1,3,14];(5)痉挛改良Ashworth量 表(modified Ashworth scale,MAS)评分[19];(6)疼痛模拟视觉量表(visual analogue scale,VAS)评分[20]。安全性指标为已知的和未知的临床不良事件发生率、神经学评估基线水平的改变、生命体征、心电图和实验室检查结果。
六、统计学分析
采用SPSS11.5 统计软件进行分析处理,ASIA 评分、SCIM 评分和VAS 评分使用重复测量方差分析;KLS 分级、AIS 分级、WISCI 评分使用Kruskal-Wallis H 检验进行分析。以P<0.05 为差异有统计学意义。
结果
一、不良事件统计
本研究中9 例患者出现术后伤口肿胀和疼痛,采用常规方法处理得到解决。无一例出现运动或感觉丧失。出现4 例不良事件:A 组中1 例受试者伤口愈合慢,血红蛋白低,给予高蛋白饮食得到解决;1例受试者出现了CSF 漏及切口裂开,予以CSF 漏修补、切口清创后愈合,后来被检查出左侧胫骨陈旧性骨折,停止运动训练。C 组中1 例受试者左下肢肿胀,B 超检查为左下肢深静脉血栓形成,于腔静脉内放置滤网。E 组中1 例受试者左侧胫骨骨折。
二、MAS 评分和VAS 评分结果
MAS 评分:治疗前5 例患者有轻度痉挛(MAS 1分),2 例患者有中度痉挛(MAS 2 分);治疗后(41~87周),有7 例患者的MAS 评分增加1 分,而2 例患者减少1 分,治疗前后患者MAS 评分差异无统计学意义(χ2=2.977,P=0.562)。VAS 评分:在治疗前,5 例患者的VAS 评分为12~50 分(满分为100 分)。治疗前和治疗后(41~87 周),3 例患者VAS 评分有所增加(增加范围:15~69 分),而4 例患者有所减少(减少范围:5~43 分),其治疗前后及组间差异无统计学意义(时间:F=0.015,P=0.905;组别:F=0.0470,P=0.757;组别×时间:F=1.232,P=0.339)。详细信息见表1。

表1 各组治疗前后疼痛模拟视觉量表评分变化
三、ASIA 评分和AIS 分级结果
ASIA 评分:轻触觉和针刺觉较治疗前略有提高(1.7、2.6),差异均无统计学意义(P>0.05),运动评分无明显提高(1 例提高2 分,1 例提高4 分,其余受试者运动评分无变化)。AIS 分级:AIS A 转为AIS B 有2 例(10%),转为AIS C 有3 例(15%),其余受试者AIS 分级无变化,差异具有统计学意义(P=0.038)。
四、KLS 分级结果
20 例患者术前KLS 分级中4 例为Ⅰ级,15 例为Ⅱ级,1 例为Ⅳ级。治疗后14~24 周,20 例患者中16例(80%)KLS 达到Ⅳ级,9 例在14 周内出院回家,因为其中6 例达到了平稳期,3 例(2 例胫骨骨折,1 例左下肢深静脉血栓形成)停止强化步行训练,回家后有4 例患者没有继续步行训练。治疗后41~87 周,20例患者中11 例(55%)KLS 达到Ⅳ级,2 例(10%)达到Ⅵ级,41~87 周的KLS 与治疗前差异具有统计学意义(Z=3.532,P<0.0005)。详细信息见图2A。
五、WISCI 评分结果
治疗前,20 例患者中16 例(80%)不能行走(WISCI 0 分),1 例行走<10 m(WISCI 1 分),1 例在助手协助下通过双杠行走10 m(WISCI 2 分),2 例在使用绷带及没有助手协助下行走10 m(WISCI 9分)。治疗后41~87 周,20 例患者中5 例WISCI 0分,2 例WISCI 2 分,6 例(30%)在1 个助手协助下行走10 m(WISCI 6 分),7 例(35%)在没有助手协助下行走10 m(WISCI≥7 分)。治疗后41~87 周的WISCI 评分与治疗前有明显提高(Z=3.315,P=0.001)。详细信息见图2B。
治疗组中步行评分比较显示,A 组、B 组、C 组的WISCI 平均评分变化从3.5 增加到6.1~9.1,在D组下降到2.9,E 组下降到0.4。B 组和C 组的8 例患者的WISCI 评分提高了6 分以上;在A 组和D 组中,只有2 例患者表现出明显改善,E 组中只有1 例参与者。虽然这在统计学上并不显著,但数据并不支持MP 或锂对细胞移植的协同效果。在5 个治疗组中,出现不良事件的3 个组差异无统计学意义。
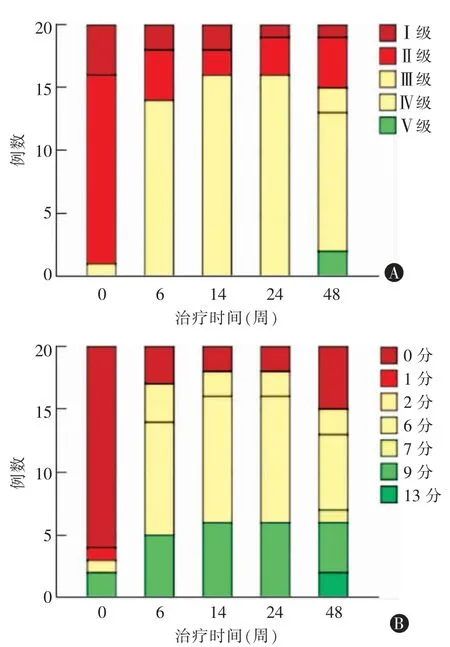
图2 脊髓损伤患者治疗前后KLS 分级及WISCI 评分结果
六、SCIM 评分结果
治疗48 周后,14 例(70%)患者的SCIM 评分都有不同程度的提高。重复测量的方差分析显示,患者的SCIM 评分在治疗后显著提高(表2),其差异具有统计学意义(F=51.194,P<0.001)。SCIM 的19 项评分中有14 项(即除了进食、梳洗、呼吸、户外活动>100 m、上下楼梯)在治疗后41~87 周有显著提高。在治疗前,只有2 例(10%)患者不需要协助膀胱和肠道控制,但治疗后41~87 周,12 例(60%)受试者能够进行独立膀胱和肠道控制。治疗前仅有6 例(30%)在没有帮助的情况下完成从床到轮椅转移,从轮椅到洗手间和浴缸转移,而治疗后增加到14 例(70%)患者。在治疗后41~87 周,6 例(30%)受试者可以在不需要帮助或需要看护的情况下在室内行走,而在中等距离的情况下则可以达到100 m;对于行走距离>100 m 时,只有2 例受试者无需辅助步行,其余受试者需要使用轮椅。
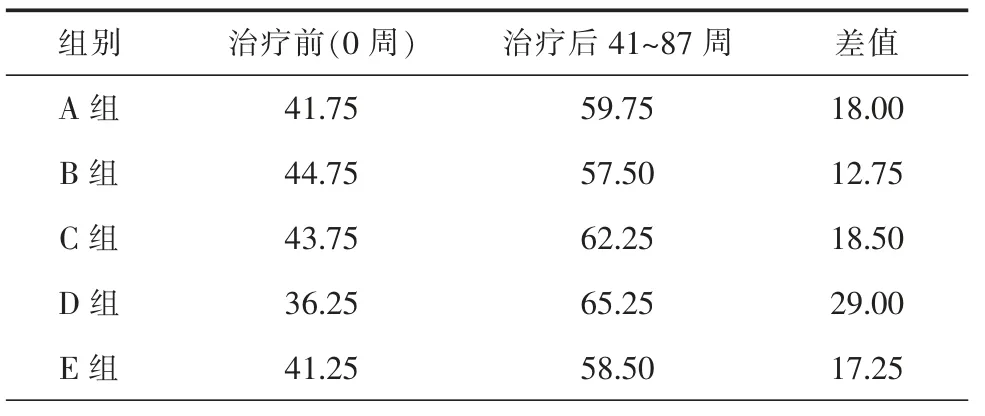
表2 各组治疗前后脊髓独立量表总分(均数)变化统计
讨论
HLA 决定了移植组织和细胞的免疫排斥,尽管HLA 类型众多,但对免疫排斥起决定作用的主要有3 种抗原:HLA-A、HLA-B、和HLA-Dr。每个人都有2套这类HLA 抗原,一套来自母亲,一套来自父亲。如果供给单位六个抗原都吻合,就称为6/6 或者 “完全”吻合,移植成功的机会大于90%。与骨髓移植需要移植物6/6 HLA 吻合不同,UCBMC 移植治疗SCI 4/6 HLA 吻合即可[21,22]。
常用的细胞移植治疗SCI 的方法有静脉输注、鞘内注射、脊髓内直接注射或囊腔切开等移植细胞[1,6,7,9]。大多数外科医生采用脊髓后正中沟注射方法移植细胞,因薄束位于后柱的后正中线,传递腿部的体感信息,该方法可能导致薄束损伤。一般外科医师注入脊髓的细胞量为10~35 μL,根据注射脊髓内细胞的直径与体积计算公式,该细胞注射量的直径约为2.6~4.0 mm,而人类脊髓的直径约为2 cm,则该注射细胞的直径可达脊髓直径的10%~20%,显而易见,注射到脊髓内细胞的体积过大,可能会导致SCI。本临床试验采用28 号不锈钢注射针,以45°角在脊神经背根入区进针约3 mm 深,这种操作可避开脊髓后柱和侧柱白质束,细胞注入背侧灰质内1 μL 为1 mm3,1 μL 体积的小球直径>1 mm,选择4、8 和16 μL 注射体积进行研究,直径分别为1.7、2.5 和3.0 mm,这样注射细胞的直径与脊髓的相对大小及注射细胞的方法是避免脊髓后柱和侧柱白质束损伤的方法之一。经临床试验证明,采用28 号不锈钢注射针,以45°角在脊神经背根入区进针约3 mm深,分别以4、8、16 μL UCBMC 注入脊髓内,无一例出现神经功能丢失,说明该注射细胞量及注射方法是安全的。在UCBMC 移植后进行强化运动训练6~12 个月,50%以上的受试者在几乎或没有任何帮助下恢复了步行及日常独立生活能力,包括生活自理、肠道和膀胱控制以及室内和户外活动。这种治疗慢性完全性SCI 的功能恢复是罕见的。
慢性完全性SCI 患者步行得到康复的研究很少见[23-25]。本研究结果显示,在治疗后41~87 周,有6 例(30%)患者的步行能力得到显著恢复,可以在不需要帮助或需要看护的情况下于室内行走,而在中等距离的情况下则可以达到100 m。
从AIS A 后期转变到ASI B 或C 级也很少见。Kirshblum 等[26]研究表明,在987 例1 年后神经系统检查为完全性(AIS A)的受试者,5 年后,3.5%的患者恢复到AIS B,而仅有1.05%的患者恢复到AIS C或D。在本研究中,治疗后有2 例患者从AIS A 恢复到ASI B (10%),3 例患者从AIS A 恢复到ASI C(15%),改善率为25%。表明UCBMC 移植和积极康复治疗对患者的AIS 等级改善有明显作用。此外,本研究中SCIM 评分的变化及分析表明经治疗后膀胱和肠道自主控制能力有显著改善。
本研究结果显示WISCI 评分的变化随着细胞剂量的增加而增加。A、B、C 组WISCI 评分的变化呈递增趋势,但D 组和E 组中均有所下降,提示C 组和E 组有差异。在5 个治疗组中有3 组出现不良事件,A 组有2 例,C 组1 例,D 组1 例。
虽然大多数受试者ASIA 运动评分没有改善,但是恢复了行走功能和其他脊髓功能,如排尿和排便功能。笔者推测UCBMC 移植刺激了轴突的生长,这些轴突激活了腰骶中枢模式产生器,改善行走、排尿和排便等功能,但仅限于接受高强度运动训练的受试者。这就解释了为什么大多数受试者在治疗1年后,其下肢肌肉没有自主收缩和轻触觉及针刺觉,却能步行。一些受试者以后将有可能恢复更多的自主运动和感觉功能。
综上所述,UCBMC 移植到慢性SCI 的方法和剂量是安全可行的,同时,高强度的运动训练对受试者运动恢复至关重要。UCBMC 移植结合高强度的运动训练对运动、肠道、膀胱等功能的恢复更加明显。下一步可通过多中心的临床试验来对UCBMC 移植治疗SCI 做进一步深入的研究,以期为SCI 治疗提供一种安全有效的治疗方法。
