HPLC同时测定附子理中丸(大蜜丸)中果糖和葡萄糖的含量
2020-08-22武红娜王晓琦潘海霞
武红娜,王晓琦,潘海霞
(沧州市食品药品检验所,河北 沧州 061000)
附子理中丸是甲类非处方药,出自宋代《惠民药局方》,具有温中健脾的功效,用于脾胃虚寒、脘腹冷痛、手足不温等症[1-4],临床应用广泛。目前,附子理中丸有大蜜丸、小蜜丸、水蜜丸和浓缩丸4种剂型,其中大蜜丸、小蜜丸和水蜜丸3种剂型均收载于《中国药典》2015年版一部 ,由附子(制)、干姜、炒白术、党参和甘草5味药加炼蜜制成[1]。
炼蜜是由蜂蜜炼制而成,作为蜜丸中常用的辅料,据调查目前市场上不排除存在劣质蜂蜜制丸的现象[5-6]。现行标准中未对辅料蜂蜜质量进行控制,故拟建立高效液相色谱法(HPLC)同时测定附子理中丸(大蜜丸)辅料蜂蜜中葡萄糖和果糖成分,以期为附子理中丸及同类药品的质量控制提供参考依据。
1 仪器与试药
1.1 仪器
LC20AT型 HPLC仪,RID-10A检测器(日本岛津公司);LC350A型超声波处理器(济宁市鲁超仪器有限公司);CP225D型十万分之一电子天平(德国赛多利斯公司); Milli-Q Advantage A10型超纯水仪(美国Millipore公司)。
1.2 试剂与试药
果糖对照品(批号:100231-201807),D-无水葡萄糖对照品(批号110833-201707,中国食品药品检定研究院);乙腈(色谱纯),醋酸(色谱纯),磷酸(纯度85 %,默克公司);其他试剂均为分析纯,水为纯化水(自制)。附子理中丸(大蜜丸)15批次,来自我省11个地市,产自全国各地不同企业。
2 方法与结果
2.1 色谱条件
流动相:乙腈-水(85:15),流速0.8 ml/min,以Prevail Carbohyrate ES为色谱柱,柱温25 ℃,示差折光检测器检测。理进样体积15 μl。理论板数:按果糖峰计应不低于2000。
2.2 溶液的制备
2.2.1 对照溶液的制备 取果糖、D-无水葡萄糖对照品适量,精密称定,加40 %乙腈,分别制成每1 ml含果糖15 mg、D-无水葡萄糖16 mg的溶液,摇匀,滤过,作为对照品溶液。
2.2.2 供试品溶液的制备 取本品剪碎,取约2.0 g,精密称定;置具塞锥形瓶中,精密加入40 %乙腈50 ml,密塞,称定重量,超声处理20 min,放冷,用40 %乙腈补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按附子理中丸的处方比例和生产工艺制备缺炼蜜的阴性样品,并按2.2.1项下方法制成阴性对照溶液。
2.3 方法学考察
2.3.1 专属性试验 精密量取2.2项下对照品溶液、供试品溶液、阴性对照溶液各适量,按2.1 项下色谱条件进样测定,记录色谱(见图1)。由图1可见,供试品溶液主峰与对照品溶液主峰保留时间一致,阴性对照溶液无干扰,说明本方法专属性良好。
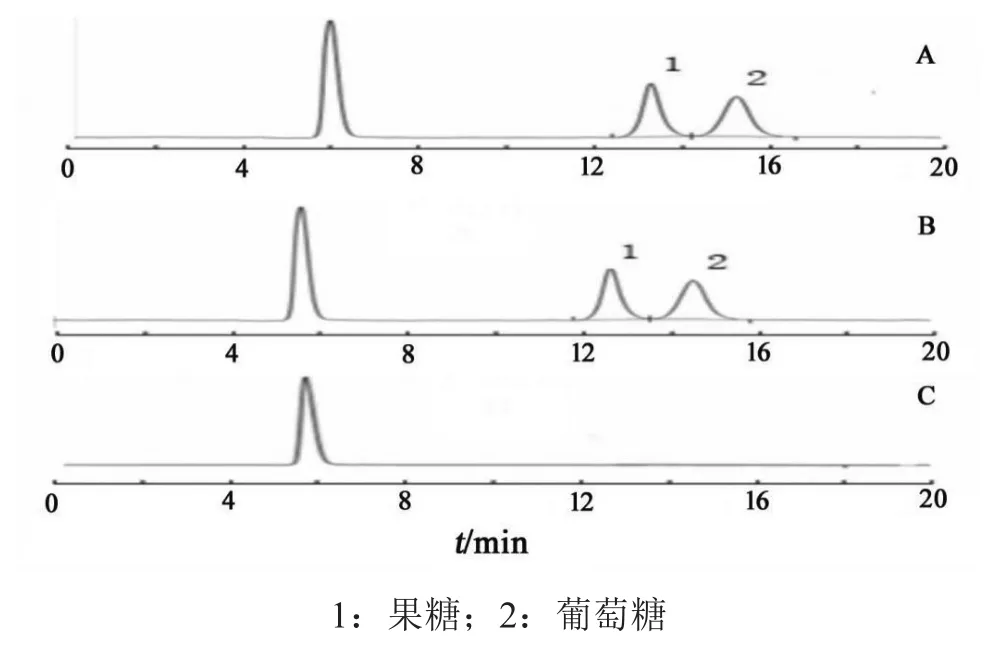
图1 HPLC图谱
2.3.2 线性关系考察 分别配制果糖、D-无水葡萄糖系列浓度混合对照品溶液,使其每1 ml分别含果糖5.0001,10.0002,15.0005,20.0073,25.0013 mg,D-无水葡萄糖5.3337,10.6669,16.0002,21.3341,26.6673 mg。精密吸取系列浓度混合对照品溶液各15 μl,按上述色谱条件测定,记录色谱图,以峰面积(Y)对进样量(X,μg)进行线性回归。果糖回归方程为:Y=3.07523X+0.18501,相关系数r=0.9998,结果显示果糖在75.0015~375.0150 μg范围内线性关系良好。葡萄糖回归方程为:Y=3.2692X+0.1175,相关系数r=1.0000,结果显示葡萄糖在80.0015~400.0075 μg范围内线性关系良好。
2.3.3 精密度试验 精密吸取2.2.1项下同一对照品溶液15 μl,连续进样6次,按2.1项下色谱条件测定,结果果糖、葡萄糖峰面积RSD分别为0.5 %,0.9 %,说明本方法精密度较高。
2.3.4 稳定性试验 按2.2.2项下方法制备附子理中丸(2号企业,批号为180101)的供试品溶液,进样分析。于2,4,8,12,24 h后分别再次进样分析,记录并比较果糖、葡萄糖含量的变化,评价样品溶液中果糖、葡萄糖室温放置不同时间的稳定情况。结果6个检测点果糖、D-无水葡萄糖峰面积的RSD分别为0.3 %,0.1 %,表明果糖、葡萄糖在室温放置24 h内稳定性良好。
2.3.5 重复性试验 取同一批号样品附子理中丸(2号企业,批号:180101)6份,按2.2项下方法制备对照品和供试品溶液,进样分析,记录并比较果糖、葡萄糖含量的变化。结果6份样品的果糖、D-无水葡萄糖的RSD为分别为0.6 %,0.5 %(均小于2 %),表明该方法重复性良好。
2.3.6 回收率试验 取已知含量的附子理中丸(2号企业,批号:180101)样品约1.5 g,精密称定,置50 ml具塞锥形瓶中,共9份,按样品含量的50 %,100 %,150 %,分别加入3个不同浓度果糖、D-无水葡萄糖的混合对照品溶液(每个浓度 3 份),按2.2.2项下方法制备供试品溶液,依法测定,计算回收率。结果平均回收率分别为100.03 %,99.34 %,RSD分别为1.33 %,1.42 %,表明该方法回收率良好,结果见表1。
2.4 样品测定
精密称取15批次附子理中丸 (大蜜丸)样品各2份,分别按2.2项方法制备对照品溶液和供试品溶液,分别按2.1项色谱条件测定果糖和葡萄糖的含量,以外标法计算样品含量,结果见表2。附子理中丸果糖与葡萄糖总量在23.9 %~50.8 %之间,果糖与葡萄糖比值分别在0.65~2.11之间。
3 讨论
蜂蜜是附子理中丸(大蜜丸)的主要辅料,具有润肠降压、保护肝脏、增强免疫力的效果[7],主要成分有蛋白质、糖类、维生素、多酚类和矿物质等。作为一个复方药物,附子理中丸成分复杂,因此本研究对提取方式和指标成分均进行了优化选择。
3.1 指标成分的选择
2015年版《中国药典》一部规定,蜂蜜中果糖和葡萄糖的总含量不得低于60 %,果糖与葡萄糖含量比值不得小于1.0[1]。因此,糖类成分为蜂蜜质量考察的重要指标[8-9]。本研究根据上述标准及样品测定结果,结合制剂工艺等因素,拟定附子理中丸(大蜜丸)果糖、葡萄糖总量(%)不得少于31.4 %,比值不得小于1.0 %,与药典标准统一。
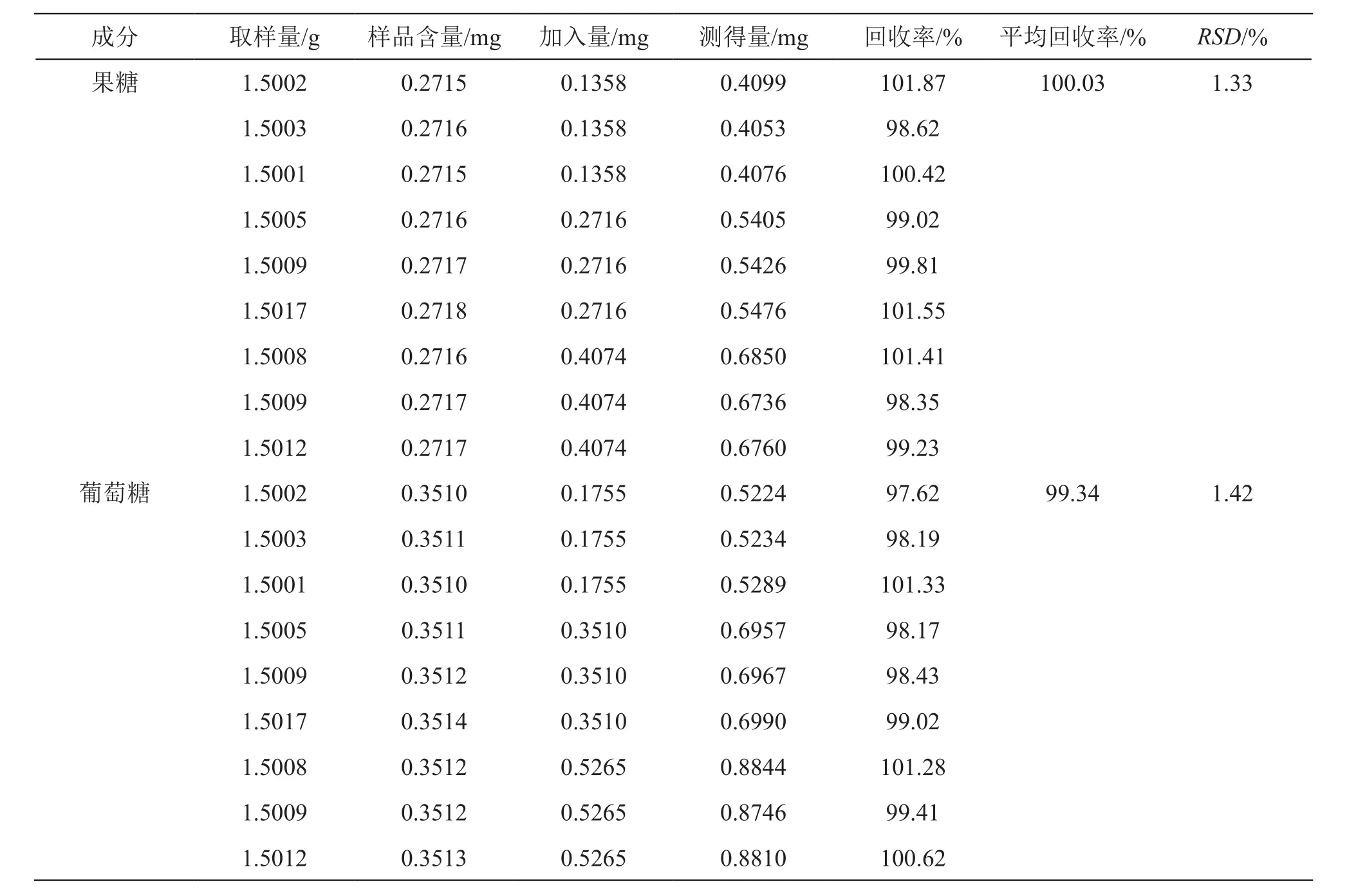
表1 加样回收率测定结果(n=9)
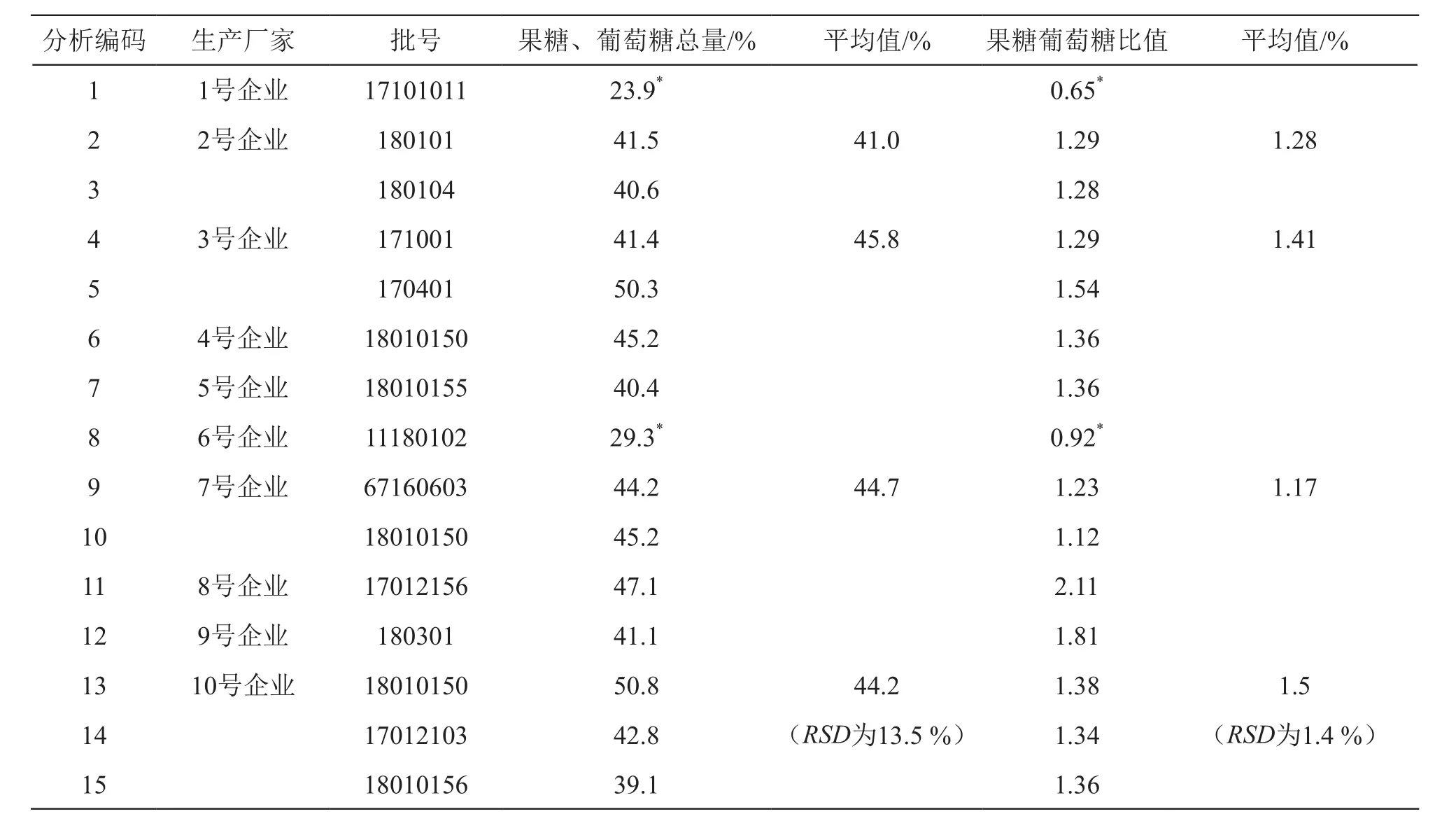
表2 样品测定结果
3.2 柱温考察
分别设置柱温20,25,30,35,40 ℃,测定供试品溶液,结果温度在30 ℃以上色谱峰的保留时间有严重漂移,考虑到环境温度等综合因素,最终确定试验温度为25 ℃。
综上所述,该方法科学、可靠,能在短时间内同时检测附子理中丸中果糖和葡萄糖含量,最大限度地排除其他化学成分的干扰,具有快速、灵敏和准确的优点,为该药辅料的质量控制提供了依据。
