酮洛芬注射液对靶动物奶牛的安全性研究
2020-08-19寇贺红付良凯焦晓军周淑贞李成应
寇贺红,付良凯,焦晓军,周淑贞,李成应
(佛山市南海东方澳龙制药有限公司,广东佛山528234)
酮洛芬(ketoprofen)属于芳基丙酸类非甾体类抗炎药(non-steroids anti-inflammatory drugs,NSAIDs),在水中几乎不溶,极易溶于甲醇,易溶于乙醇、丙醇或乙醚,具有解热、镇痛、抗炎的作用。它主要通过可逆性抑制环氧合酶(COXs)、促炎肽或脂氧化酶(LOXs) 的活性,从而抑制致炎性物质前列腺素(PGs)、白三烯(LTs) 及血栓素(TXs) 的生物合成,使缓激肽释放减少,进而发挥其良好的抗炎、镇痛和解热作用。研究发现,酮洛芬的抗炎、镇痛和解热作用强于阿司匹林、萘普生、消炎痛、布洛芬、双氯芬酸和炎痛喜康等药物,抗炎作用比阿司匹林强 150 倍,解热作用比消炎痛强 4 倍,毒性仅为消炎痛的 1/20,且不良反应与布洛芬相似且较轻[1]。酮洛芬于1967年首次合成,首个人药制剂于1973年在法国上市。兽用制剂也在多个国家广泛应用,如西班牙辉瑞公司生产的 15%酮洛芬注射液(商品名:Danidol/Ederal)[2],加拿大梅里亚公司生产的10%酮洛芬注射液(商品名:Anafen®)[3],治疗牛呼吸道感染、乳腺炎、乳腺水肿、躺卧母牛综合征、内毒血症、关节炎和肌肉骨骼外伤等引发的发烧、疼痛和炎症等相关疾病。目前国内尚无酮洛芬注射液对靶动物奶牛安全性的相关研究。本试验选用健康泌乳奶牛进行酮洛芬注射液的靶动物安全性试验,以期为临床用药提供科学依据。
1 材 料
1.1 试验药品 酮洛芬注射液,规格 100mL∶15g;批号:20160503,由佛山市南海东方澳龙制药有限公司提供。
1.2 仪器设备 全自动动物血细胞分析仪:XFA6130型,南京普朗医用设备有限公司;全自动生化分析仪:BS300,深圳迈瑞生物医疗电子股份有限公司;牛奶体细胞计数仪:MINI5700型,北京康达智信科技有限公司。
1.3 试验动物 20头泌乳期健康荷斯坦奶牛(胎次:2~3胎),体重为400~450 kg,由三门峡市合源奶牛养殖场提供。按奶牛场常规饲养,试验期间奶牛不使用其他任何抗菌药物、生殖激素等。
2 方 法
2.1 试验分组及给药 20头健康试验奶牛随机分为4组,每组5头,设1倍推荐剂量(3 mg/kg·bw)、3倍推荐剂量(9 mg/kg·bw)、5倍推荐剂量(15 mg/kg·bw)3个受试药物组(分别编号为1倍组、3倍组、5倍组)以及空白对照组(注射生理盐水)。颈部肌肉注射,每日1次,连续给药9 d。试验持续至末次给药后第15天,试验期间按照牛场管理规程做好消毒防疫和防病工作,保证自由采食和饮水。
2.2 试验评价指标 参照“VICH兽药靶动物安全性研究指导原则概述”[4]和“靶动物安全试验指导原则(征求意见稿)”[5],从临床表现和健康状况、直肠温度、血液学检测、血清生化学检测等方面进行观察,判定结果。
2.2.1 临床观察 试验期间观察动物是否有与药物相关的不良反应,如行为异常、精神抑郁、呼吸加深加快及粪尿排泄异常等变化情况。
2.2.2 血液学检测 分别于给药前第0天和末次给药后第1天、第7天、第15天的同一时间尾静脉采集血液3~5 mL,加入EDTA-2K,制备抗凝血用于血常规检查,检查参数主要有:红细胞计数(RBC)、血红蛋白(HGB)、红细胞平均体积(MCV)、平均血红蛋白含量(MCH)、白细胞计数(WBC)、血小板计数(PLT)等指标。
2.2.3 血清生化学检测 分别于给药前第0天和末次给药后第1天、第7天、第15天的同一时间尾静脉采集血液5~6 mL,制备非抗凝血,分离血清,进行血清生化指标测定,检查参数有:丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、总蛋白(TP)、白蛋白(ALB)、球蛋白(GLB)、乳酸脱氢酶(LDH)、肌酐(CREA)、尿素(Urea)、间接胆红素(DBIL)、总胆固醇(TC)等指标。
2.2.4 奶产量和乳汁体细胞数 分别于给药前第0天和末次给药后的第1天、第7天、第15天统计奶牛奶产量,并采集奶样20~30 mL进行乳汁体细胞数检测。
2.2.5 直肠温度 分别于给药前第0天和末次给药后的第1天、第7天、第15天,用电子体温计检测奶牛直肠温度。
2.2.6 数据统计分析 观察记录各剂量组和空白对照组试验奶牛用药前后的临床症状,记录各试验组奶牛的血常规和血清生化指标数值,使用 SPSS20.0 统计软件计算各指标的平均值与标准差,采用单因素方差分析,比较各组组内给药后不同时间点数据与给药前第0天数据的差异性,如药物产生不良反应,对其原因进行分析,并提出注意事项。
3 结果与分析
3.1 临床症状变化 给药期间各剂量组奶牛未表现异常反应,如抵抗、兴奋等。整个试验期间,各剂量组奶牛精神状态、直肠温度、呼吸、采食、饮水和粪尿排泄均正常,与对照组相比,未观察到有不同临床表现。整个试验过程奶牛全部存活,且未观察到任何不良反应。
3.2 血液学检测 分别于给药前第0天和末次给药后第1天、第7天、第15天的同一时间静脉采集抗凝血,进行血常规检测,结果见表1-表4。数据显示,各指标在给药期间与给药前相比差异不显著(P>0.05),均在文献报道的范围内[6-13],说明酮洛芬注射液以推荐剂量(3 mg/kg·bw)至5倍推荐剂量(15 mg/kg·bw)应用于奶牛对其血液指标无明显影响。
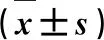
表1 空白对照组给药前第0天和末次给药后第1天、第7天、第15天的血常规检测Tab 1 The hematology of the control group on day 0,1,7,15 after
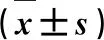
表2 1倍组给药前第0天和末次给药后第1天、第7天、第15天的血常规检测Tab 2 The hematology of the recommended dosage group on day 0,1,7,15 after
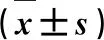
表3 3倍组给药前第0天和末次给药后第1天、第7天、第15天的血常规检测Tab 3 The hematology of three times of recommended dosage group on day 0,1,7,15 after
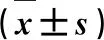
表4 5倍组给药前第0天和末次给药后第1天、第7天、第15天的血常规检测Tab 4 The hematology of five times of recommended dosage group on day 0,1,7,15 after
3.3 血清生化指标检查 分别于给药前第0天和末次给药后第1天、第7天、第15天的同一时间静脉采集非抗凝血,分离血清,进行血液生化指标测定,结果见表5-表8。数据表明,1倍剂量组的TC浓度在末次给药后第1天和第15天显著低于给药前水平(P≤0.05);3倍剂量组的UREA浓度在末次给药后第15天显著低于给药前水平(P≤0.05);5倍剂量组的ALP浓度在末次给药后第15天显著低于给药前水平(P≤0.05);其余各指标在给药期间与给药前相比差异不显著(P>0.05)。虽然上述试验组的某些指标在给药后与给药前第0天数据相比存在差异性改变,但所有检测值均在文献报道的正常范围内[6-13]。试验结果说明酮洛芬注射液以推荐剂量(3 mg/kg·bw)至5倍推荐剂量(15 mg/kg·bw)应用于奶牛对其血清生化指标无明显影响。
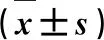
表5 空白对照组给药前第0天和末次给药后第1天、第7天、第15天的血清生化指标Tab 5 The blood chemistry of the control group on day 0,1,7,15 after
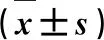
表6 1倍组给药前第0天和末次给药后第1天、第7天、第15天的血清生化指标Tab 6 The blood chemistry of the recommended group on day 0,1,7,15 after
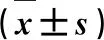
表7 3倍组给药前第0天和末次给药后第1天、第7天、第15天的血清生化指标Tab 7 The blood chemistry of three times of recommended dosage group on day 0,1,7,15 after
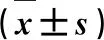
表8 5倍照组给药前第0天和末次给药后第1天、第7天、第15天的血清生化指标Tab 8 The blood chemistry of five times of recommended dosage group on day 0,1,7,15 after
3.4 奶产量和乳汁体细胞数统计 分别于给药前第0天和末次给药后的第1天、第7天、第15天统计奶牛奶产量,并采集奶样20~30 mL进行乳汁体细胞数检测,结果见表9和表10,各组受试奶牛在给药前后日产奶量无明显差异(P>0.05),给药前后受试奶牛的乳汁体细胞数均小于20万,各组受试奶牛在给药前后乳汁体细胞数无显著差异(P>0.05),显示酮洛芬注射液对泌乳期奶牛的产奶性能无影响。

表9 给药前后奶牛日产量统计表Tab 9 Milk production of dairy cattles before and after dosing kg/d

表10 给药前后奶牛乳汁体细胞数统计表Tab 10 SCC of dairy cattles before and after dosing 10000/mL
3.5 直肠温度 分别于给药前第0天和末次给药后的第1天、第7天、第15天,用电子体温计检测奶牛直肠温度。奶牛正常体温在37.5 ℃~39.5 ℃之间[11-13]。本试验中受试奶牛的直肠温度检查结果见表11,各试验组直肠温度无明显差异(P>0.05),均在正常值范围内,表明酮洛芬注射液对泌乳期奶牛的体温无明显影响。

表11 给药前后奶牛直肠温度统计表Tab 11 The rectal temperature of dairy cattles before and after treatment ℃
4 小 结
靶动物安全性试验是新兽药临床试验研究的重要内容,主要用于研究受试药物在治疗范围或治疗范围以上剂量时对生理功能潜在的不良影响[14]。本研究结果表明,酮洛芬注射液以推荐剂量(3 mg/kg·bw)至5倍推荐剂量(15 mg/kg·bw)
应用于奶牛是安全的。鉴于目前国内尚无酮洛芬注射液在奶牛上使用的安全性研究,因此本试验为酮洛芬注射液在奶牛临床中的使用提供了科学依据。
