肾小球滤过率与肾脏替代治疗启动的相关性研究
2020-08-18刘伟俊吴锡信
刘伟俊,吴锡信
1.广东医科大学研究生院,广东 湛江 524023;2.广东省第二人民医院肾内科,广东 广州 510317
慢性肾脏病(chronic kidney disease,CKD)已经发展成为一个全球性的公共卫生问题,影响着10%~15%的成年人[1]。而据过去十年中发表的几项流行病学研究表明,CKD在普通人群中的患病率仍在上升[2-3]。与一般人群相比,CKD患者具有更高的死亡风险。若进展至终末期阶段,其死亡风险将大大提高。据报道,终末期肾脏病血液透析患者的死亡率(主要与心血管并发症和感染有关)高于许多癌症或心力衰竭患者。在透析治疗启动后的第1年,其死亡率高达19.2%[4]。更值得重视的是,许多CKD患者在透析启动前没有明确的计划,导致因迫切需要而进入透析,这些患者的死亡风险将进一步升高。大量研究已表明,基础肾小球滤过率(GFR)及其年下降率与心血管并发症、全因死亡及肾脏替代治疗(renal replacement therapy,RRT)启动等CKD不良结局的发生风险独立相关[5-7]。然而,这些研究均基于估算肾小球滤过率(eGFR)进行探讨。鲜有研究探讨初始实测肾小球滤过率(mGFR)与RRT启动的相关性。故可假设初始mGFR与CKD 3~4期患者在2年内进展至RRT相关,能为CKD 3~4期患者的RRT启动风险提供重要信息。本文旨在探讨CKD 3~4期患者的初始mGFR与2年RRT启动的相关性,以期指导临床实践工作,有计划地做好透析前准备。
1 资料与方法
1.1 研究人群
1.1.1 纳入标准 选择2012年1月至2018年1月期间在广东省第二人民医院肾内科就诊并检测99m锝-二亚乙基三胺五乙酸(99mTc-DTPA)清除率评估GFR为CKD 3~4期的患者。
1.1.2 排除标准 18岁以下;患有重度血液系统、肝脏和心脏疾病或恶性肿瘤患者;mGFR资料缺失;因意外事故导致死亡者;失访患者。
1.2 研究方法
1.2.1 研究设计 单中心回顾性研究。
1.2.2 终点事件 血液透析治疗、腹膜透析治疗、肾移植及因拒绝RRT而导致死亡的患者,后者以拒绝RRT的时间点作为随访终点。
1.2.3 随访 自首次mGFR检查结果回报日期起,通过翻阅电子病历资料或电话随访,获取2年内患者是否出现终点事件。
1.2.4 临床资料 完成首次mGFR检查患者入院时的年龄、性别、吸烟史、BMI、收缩压、舒张压、高血压病病史、糖尿病病史、心脑血管病病史、肾脏疾病的病因(良性小动脉性肾硬化症、糖尿病肾病、原发性肾脏病、其他)、是否并发充血性心力衰竭等临床资料。完成首次mGFR检查的最近1次实验室检测资料(尿蛋白定性、血红蛋白、二氧化碳结合力(carbon dioxide combining power,CO2-CP)、尿酸、肌酐、尿素氮、β2微球蛋白(β2-microglobulin,β2M)、胱抑素C、白蛋白、铁、钾、钙、磷、同型半胱氨酸、总胆固醇(cholesterol,CHO)、低密度脂蛋白(low density lipoprotein,LDL)、高密度脂蛋白(high density lipoprotein,HDL)、甘油三酯(triglyceride,TG)、NT-proBNP、proBNP等)。
1.2.5 定义 (1)高血压病:收缩压≥140 mmHg和(或)舒张压≥90 mmHg(1 mmHg=0.133 kPa),或需使用降压药物治疗。(2)糖尿病:入院后检查符合糖尿病诊断,或需口服降糖药和/或胰岛素。心脑血管病史:有心绞痛、急性心肌梗死、血管成形术或心肌血运重建史的患者被认为是冠状动脉缺血;有脑卒中史、短暂性脑缺血发作史或行颈动脉内膜切除术者均为脑血管病;有肢体缺血导致跛行、溃疡或截肢史的患者或接受周围血管重建的患者被诊断为周围动脉疾病(peripheral arterial disease,PAD)。(3)充血性心力衰竭(congestive heart failure,CHF):患者有呼吸困难、水肿、颈静脉淤血、肝肿大、体力活动受限,体检或胸透检查发现肺充血,或使用抗心衰药物时被诊断为CHF。
1.3 统计学方法 采用SPSS25.0及Empower-Stats软件包进行统计分析。通过Shapiro-Wilk进行正态性检验。正态分布资料以均值±标准差(±s)表示,采用独立t检验比较发生终点事件组和未发生终点事件组之间的差异,非正态分布计量资料以中位数(25和 75百分位数)[M(P25,P75)]表示,采用Mann-Whitney U检验进行组间比较。分类变量以例(%)表示,采用χ2检验进行差异性分析。利用单因素Cox回归对各个单变量与2年RRT启动的关系进行单因素分析,得出各自效应值,将有统计学意义的变量(P<0.05)纳入多元回归分析。剔除数据缺失大于50%的指标[8],采用多重插补法进行缺失数据插补,并通过敏感性分析评估插补后的完整数据集是否与原始数据分布一致。若差异无统计学意义(P≥0.05),则利用插补后数据集进行多元Cox回归分析得出各个数据集在调整混杂因素后的mGFR效应值,进而通过罗宾法则合并5组插补后数据集的效应值。与2年RRT启动相关的风险根据mGFR每下降5 mL/(min·1.73 m2)来报告,以P<0.05为差异有统计学意义。
2 结果
2.1 患者的临床及实验室资料分析结果 本研究最终共纳人153例符合纳排标准的CKD 3~4期[15 mL/(min·1.73 m2)≤mGFR<60 mL/(min·1.73 m2)]患者,患者的临床及实验室资料特征见表1。其中,CKD 3期患者60例(39.2%),CKD 4期患者93例(60.8%)。随访2年后,72例患者发生终点事件(47.1%),有60例患者行血液透析治疗(39.2%),5例患者死亡(3.3%),2例患者接受了肾移植(1.3%),5例患者(3.3%)行腹膜透析治疗,平均随访时间510 d。
表1 153例患者基本临床及实验室资料[例(%),±s,M(P25,P75)]
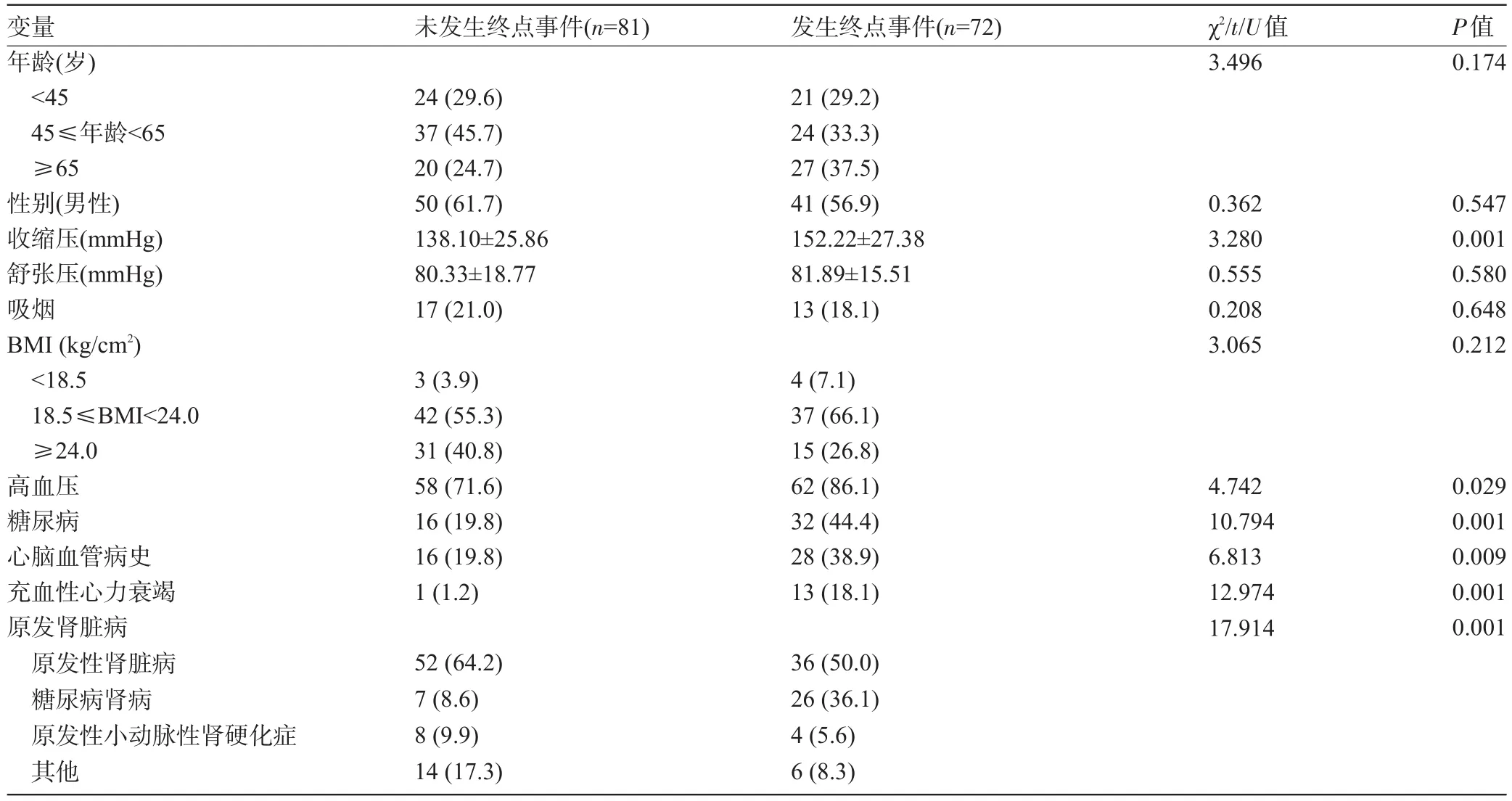
表1 153例患者基本临床及实验室资料[例(%),±s,M(P25,P75)]
变量年龄(岁)<45 45≤年龄<65≥65性别(男性)收缩压(mmHg)舒张压(mmHg)吸烟BMI(kg/cm2)<18.5 18.5≤BMI<24.0≥24.0高血压糖尿病心脑血管病史充血性心力衰竭原发肾脏病原发性肾脏病糖尿病肾病原发性小动脉性肾硬化症其他未发生终点事件(n=81)发生终点事件(n=72)24(29.6)37(45.7)20(24.7)50(61.7)138.10±25.86 80.33±18.77 17(21.0)3(3.9)42(55.3)31(40.8)58(71.6)16(19.8)16(19.8)1(1.2)52(64.2)7(8.6)8(9.9)14(17.3)21(29.2)24(33.3)27(37.5)41(56.9)152.22±27.38 81.89±15.51 13(18.1)4(7.1)37(66.1)15(26.8)62(86.1)32(44.4)28(38.9)13(18.1)36(50.0)26(36.1)4(5.6)6(8.3)χ2/t/U值3.496 0.362 3.280 0.555 0.208 3.065 4.742 10.794 6.813 12.974 17.914 P值0.174 0.547 0.001 0.580 0.648 0.212 0.029 0.001 0.009 0.001 0.001

续表1

表2 单因素回归分析结果
2.2 单因素回归分析结果 在未调整其他变量的情况下,初始mGFR与2年RRT启动风险显著相关,风险比(HR)为0.75(0.66,0.86),P<0.001。收缩压、充血性心力衰竭、高血压病病史、糖尿病病史、心脑血管病史、糖尿病肾病、蛋白尿定性、血红蛋白、CO2-CP、β2M、胱抑素C、钾、钙、铁、磷、白蛋白、同型半胱氨酸也与2年RRT启动风险显著相关,见表2。
2.3 缺失数据的多重插补 原始数据集数据缺失情况见表3。其中,同型半胱氨酸、NT-proBNP、proBNP数据缺失超过50%,故予以剔除。采用多重插补补齐余下各变量缺失数据,对插补前后的共6套数据(1组原始数据和5组插补后的完整数据集)进行敏感性分析,结果表明插补后的5组数据集与原始数据集分布基本一致,差异均无统计学意义(P>0.05),见表4、表5。
2.4多元回归分析结果 利用插补后数据集,纳入收缩压、高血压病病史、糖尿病病史、心脑血管病史、原发肾脏病、蛋白尿定性、血红蛋白、β2M、胱抑素C、血肌酐、尿素氮、钾、钙、铁、磷、白蛋白等一系列混杂因素得出调整后模型。结果提示初始mGFR与2年RRT启动风险呈显著负相关(HR=0.71,95%CI为0.52~0.98,P=0.039)。即初始 mGFR 每下降 5 mL/(min·1.73 m2),CKD患者2年RRT启动风险将增加29%。而且,该结果与单因素回归分析的未调整模型(HR=0.75,95%CI为0.66~0.86,P<0.001)较一致。

表3 各变量数据缺失情况[例(%)]
表4 插补前后各数据集连续性变量的数据分布情况[±s,M(P25,P75)]

表4 插补前后各数据集连续性变量的数据分布情况[±s,M(P25,P75)]
变量血红蛋白(g/L)CO2-CP(mmol/L)β2M(mg/L)胱抑素C(mg/L)血钙(mmol/L)血磷(mmol/L)铁(mmol/L)白蛋白(g/L)CRP(mg/L)CHO(mmol/L)LDL(mmol/L)HDL(mmol/L)TG(mmol/L)原始(n=153)98.49±22.84 22.00(20.50,24.00)7.02(5.34,10.87)3.41(2.69,4.42)2.19(2.08,2.36)1.58(1.38,1.87)11.20(8.00,15.30)34.30±6.64 2.80(0.10,12.50)4.67(3.93,5.63)2.47(1.88,3.30)1.02(0.88,1.32)1.56(1.11,2.58)插补1(n=153)98.46±22.76 22.00(20.00,24.00)6.18(3.35,8.70)3.87(2.86,4.98)2.19(2.08,2.36)1.58(1.38,1.87)11.20(8.00,16.00)34.23±6.67 2.30(0.05,9.70)4.59(3.86,5.60)2.45(1.80,3.34)1.02(0.86,1.32)1.60(1.10,2.69)插补2(n=153)98.48±22.76 22.00(20.00,24.00)5.65(3.31,9.57)3.82(2.81,5.18)2.19(2.08,2.36)1.58(1.38,1.88)11.00(7.67,16.00)34.28±6.62 2.37(0.09,11.25)4.61(3.74,5.80)2.43(1.72,3.32)1.00(0.80,1.27)1.60(1.08,2.70)插补3(n=153)98.52±22.76 22.00(20.50,24.00)5.68(3.18,8.70)3.92(2.74,5.23)2.19(2.08,2.36)1.61(1.38,1.88)11.50(8.00,16.00)34.32±6.62 2.30(0.04,9.70)4.53(3.74,5.66)2.47(1.76,3.30)1.00(0.80,1.23)1.60(1.08,2.70)插补4(n=153)98.71±22.92 22.00(20.07,24.00)5.76(3.13,9.38)3.87(2.89,5.52)2.19(2.08,2.36)1.58(1.38,1.87)11.20(8.00,16.00)34.21±6.72 2.80(0.10,12.50)4.59(3.74,5.73)2.38(1.69,3.30)1.00(0.82,1.24)1.62(1.11,2.70)插补5(n=153)98.52±22.76 22.00(20.00,24.00)5.76(3.22,9.24)3.96(2.97,5.43)2.19(2.08,2.36)1.58(1.38,1.87)11.20(8.00,15.25)34.19±6.77 2.60(0.09,13.85)4.61(3.77,5.73)2.38(1.69,3.29)1.02(0.83,1.31)1.65(1.17,2.79)F/H值0.002 0.129 10.660 8.092 0.074 0.019 0.841 0.100 0.776 0.219 1.418 2.483 1.433 P值1.000 1.000 0.059 0.151 1.000 1.000 0.974 1.000 0.979 0.999 0.922 0.779 0.921

表5 插补前后各数据集分类变量的数据分布情况[例(%)]
3 讨论
本研究通过调整一系列混杂因素后得出初始mGFR与CKD患者2年RRT启动风险呈显著负相关(HR=0.71,95%CI为 0.52~0.98,P=0.039)。 即 初 始mGFR每下降5 mL/(min·1.73 m2),CKD患者2年RRT启动风险将增加29%。同时,该结果与未调整模型的HR值(0.75)大小相当,方向一致,表明无论是否考虑其他因素的影响,初始mGFR与CKD 3~4期患者2年RRT启动的相关关系都是稳定的。
事实上,GFR的下降将加重残余肾单位肾小球高滤过和高灌注,进而导致肾小球硬化及残余肾功能进一步丧失,加速CKD进展,这是得出本研究结果的重要原因。而Cochrane数据库系统回顾分析了40项研究的结果,纳入63 887例患者,结果表明早期转诊至肾脏病专科可防止CKD患者进展为终末期肾脏病[9]。本研究的mGFR为CKD 3~4期患者首次评估值,故接受肾脏病专科治疗的时期可能为本研究结果的重要潜在原因。因此,本研究结果提示临床工作中应早期检测mGFR,尽早做好RRT前准备。
ELAINE等[10]研究表明CKD患者的GFR每2年下降5 mL/(min·1.73 m2)将增加心血管事件及终末期肾脏病发生风险。故GFR每5 mL/(min·1.73 m2)的变化量可能是一个与CKD进展相关的变化,本研究结果再次验证了这一点。KABASAWA等[5]研究发现,基础eGFR与社区人群的全因死亡率显著相关。CORESH等[11]研究表明eGFR在2年内下降超过30%可能预示着CKD的进展。多项研究发现,CKD患者eGFR年下降率与心血管并发症、全因死亡及RRT启动等CKD不良结局的发生风险独立相关。这些研究均为GFR与CKD进展的相关性提供有力证据[6-7,12-13]。这与本研究结果相一致。然而,既往研究更多地集中于eGFR。事实上,eGFR的波动在CKD患者中是常见的。近期研究讨论了超过70项研究,结果表明,eGFR与mGFR的差异通常在±30%或更多,eGFR值在30%~60%的患者中错误地分期CKD[14]。mGFR一直被认为是衡量肾脏功能的金标准。因此,为准确量化GFR的独立相关作用,本研究利用mGFR严格分期,探讨CKD 3~4期患者的初始GFR与2年RRT启动的相关性。显然,在准确性及可靠性上有明显优势。
本研究单因素回归分析结果提示收缩压、钾、磷、β2M、胱抑素C、尿素氮的升高,高血压病病史、糖尿病病史、心脑血管病史、糖尿病肾病、充血性心力衰竭、高蛋白尿,CO2-CP、血红蛋白、钙、铁、白蛋白的降低与2年RRT启动显著相关。该结果与既往研究基本一致。高血压病、糖尿病是传统的CKD进展危险因素[1]。糖尿病肾病是导致的终末期肾脏病的主要原因[15]。蛋白尿能增加CKD患者全因死亡率及RRT发生率[16]。心血管疾病(CVD)是导致一般人群和CKD患者死亡的主要原因[17]。贫血增加CKD患者住院率、死亡率及心血管事件发生率,促进CKD进展[18]。钙磷代谢紊乱增加CKD患者的心血管事件发生率及死亡风险[19-20]。血钾与CKD患者全因死亡率相关[20]。CO2-CP水平与GFR呈显著正相关[21]。β2M、胱抑素C是较血清肌酐更好的CKD心血管事件风险预测因子[22]。白蛋白为营养指标,营养不良直接导致CKD患者死亡率和住院率的增加[23]。此外,血脂异常通过促进动脉粥样硬化性心血管疾病的发展而加速CKD进展[24],年龄、吸烟亦为CKD进展危险因素[1],但本研究中均与2年RRT启动无显著相关性,考虑可能与样本量不足相关或可能需更长的随访时间才有显著性意义。
本研究为单中心回顾性研究,样本量有限,可能存在选择偏倚。当然,本研究尽量弥补不足,为扩大样本量,避免直接排除缺失值带来的统计效能减少和偏性,使用了多重插补来估计缺失值。然而,仍有部分变量由于数据缺失巨大,未能纳入分析(如同型半胱氨酸、NT-BNP、24 h尿蛋白定量等),因此尚不能评估这些变量与RRT启动的相关程度。
本研究表明初始mGFR能为CKD 3~4期患者2年RRT启动风险提供重要信息,可用于指导临床实践工作,有计划地做好透析前准备。然而,这还需要进一步扩大样本量,进行多中心研究,以更深入地评估初始mGFR与RRT启动的相关程度。
