气氛对氧化物吸附气相砷的影响及机理分析
2020-08-07何梓谦余圣辉方庆艳
何梓谦,余圣辉,张 成,许 豪,方庆艳,陈 刚
(华中科技大学 煤燃烧国家重点实验室,湖北 武汉 430074)
0 引 言
燃煤烟气中的砷是造成环境污染的主要物质之一,具有严重的生物毒性[1]。煤中砷在煤燃烧过程中挥发进入大气,在环境中易形成剧毒氧化物 As2O3和As2O5,污染环境且通过呼吸道、皮肤接触等进入人体,并在人体中富集引发慢性中毒,危害人体健康[2]。Tian等[3]对燃煤电厂Hg、As、Se的大气排放量计算发现,2007年大气中砷总排放量达到550.08 t。2011年中国发布《重金属污染综合防治“十二五”规划》,提出到2015年重点区域重点重金属污染物(铅、汞、铬、镉、砷等)排放量比2007年减少15%。生态环境部于2015年12月陆续发布了《砷污染防治技术政策》,对含砷燃煤使用、燃煤电厂与燃煤工业锅炉的污染防治和管理工作提出明确要求。因此对燃煤电厂烟气中砷排放进行控制是火电行业的迫切需求。
O2/CO2燃烧作为一种新型的燃烧方式,具有成本低、易规模化、可改造存量机组等优势[4],不仅可使NOx排放量降至常规空气气氛下燃烧的2/3左右,还可控制SO2排放[5],是在技术上、经济上均具有竞争力的CO2减排方法。O2/CO2燃烧技术是以CO2替代N2,大量CO2与碳颗粒反应生成CO,使碳粒表面形成短暂的还原性气氛,这是与空气气氛燃烧的最大区别,因此煤中砷的挥发和迁徙也会受到影响[5]。Bithi等[6]发现,随着O2/CO2燃烧环境中氧浓度增加,固体砷和铬含量均增加,而灰中最易挥发的微量元素硒含量减少。此外,煤粉在管式炉富氧燃烧试验中表明,温度低于900 ℃时,O2浓度是影响砷挥发的主要因素;高于900 ℃时,CO2浓度是影响砷挥发的主要因素[5]。
煤中砷属于半挥发性重金属,主要以硫化物形态存在[7]。煤粉燃烧时,砷发生气化、均相凝结和异相吸附等过程[8],最终分布在尾部烟气、飞灰以及底渣中,其中飞灰中砷的占比可达92%[9]。Mahuli等[10]研究了Ca(OH)2、高岭土、Al2O3和SiO2对As2O3的吸附性能,发现Ca(OH)2的吸附效果远高于其他3种矿物。Bartoňov等[11]研究发现,在旋转飞灰中,砷含量与CaO、Fe2O3含量呈正相关,与Al2O3呈负相关,且与CaO的相关性最高。张月等[12]研究了金属氧化物吸附剂CaO、Fe2O3、Al2O3对砷的吸附性能,发现在吸附温度范围内,Fe2O3比其他2种吸附剂吸附性能更好。
此外,烟气组分对气相砷的吸附也有影响。张月等[13-14]在富氧条件下研究了NO、H2O、SO2、CO2对Fe2O3/γ-Al2O3吸附气相砷的影响,发现高浓度CO2、高浓度SO2对Fe2O3/γ-Al2O3吸附气相砷有抑制作用,低浓度SO2对Fe2O3/γ-Al2O3吸附气相砷有促进作用,且O2含量增加在一定程度上减轻了高浓度SO2对吸附的抑制作用。H2O促进气相砷的吸附,NO对气相砷的吸附影响不明显。Huang等[15]研究了SO2、NO对γ-Al2O3吸附模拟烟气中As2O3能力的影响,发现SO2极少吸附于γ-Al2O3,对γ-Al2O3吸附砷能力的影响较小,而NO与砷竞争占据带正电的铝离子的反应位点,降低了γ-Al2O3对砷的吸附能力。
目前,矿物质氧化物吸附气相砷的研究主要集中在300 ℃低温区域,而700/900 ℃高温区烟气气氛对气相砷的吸附研究较少。本文采用恒定的砷源发生装置,探究模拟烟气下HCl、SO2对CaO、Fe2O3、MgO吸附气相砷的影响特性,以及富氧条件下CaO、Fe2O3、MgO吸附气相砷的特性,并对吸附机理进行分析。
1 试 验
1.1 试验材料
试验用块状CaO(天津大茂化学试剂厂)、块状Fe2O3(鼎鑫耐磨金属材料有限公司)、块状MgO(营口久丰镁制品有限公司)采用球磨研磨机均匀研磨,研磨样品经筛分至粒径为0.2~0.3 mm备用。吸附剂颗粒样品X射线荧光光谱(Shimadzu公司XRF-1800)分析结果见表1。可知,所用吸附颗粒样品的纯度高于98%,可认为吸附剂颗粒与纯氧化物的吸附效果一致。
1.2 试验装置和样品制备
气相砷吸附试验在两段式固定床反应器中进行,试验系统如图1所示。系统包括AsH3(g)发生和As2O3吸附2部分,其中可移动式反应器中间可流通烟气,底部安装不锈钢滤网,作为吸附剂颗粒气相砷吸附室,试验时,取出可移动式反应器,将称量好的吸附剂颗粒平铺于可移动式反应器底部,待试验系统稳定至设定条件,将可移动式反应器放入管式炉上段加热部位中间位置,保障吸附试验在恒温区进行。为了模拟电厂实际烟气(SFG),根据某电厂烟气测量结果,设定烟气中N2、O2、CO2、H2O的流量分别占77%、4.8%、13%、5.2%,总气体流量为1.5 L/min。试验中KBH4完全反应,H2O来自所生成H2的氧化。为了模拟富氧燃烧条件下吸附剂颗粒吸附气相砷的特性,设置O2、CO2流量为21%、79%,HCl和SO2由气瓶提供,且控制HCl和SO2含量为500 μL/L。总气体流量为1.5 L/min。砷源为NaAsO2[15],通过与KBH4和HCl反应生成AsH3,AsH3在700 ℃恒温条件下氧化,烟气中实际As2O3流量为120 μg/g。吸附温度设置为700和900 ℃,吸附剂0.5 g,吸附时间30 min,吸附完成后将吸附剂颗粒样品取出,在空气中冷却至室温并收集,每组试验重复3次。
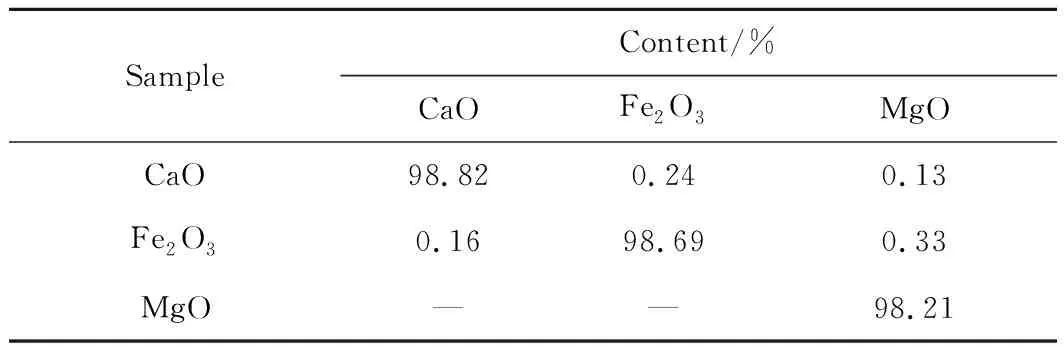
表1 氧化物成分XRF分析
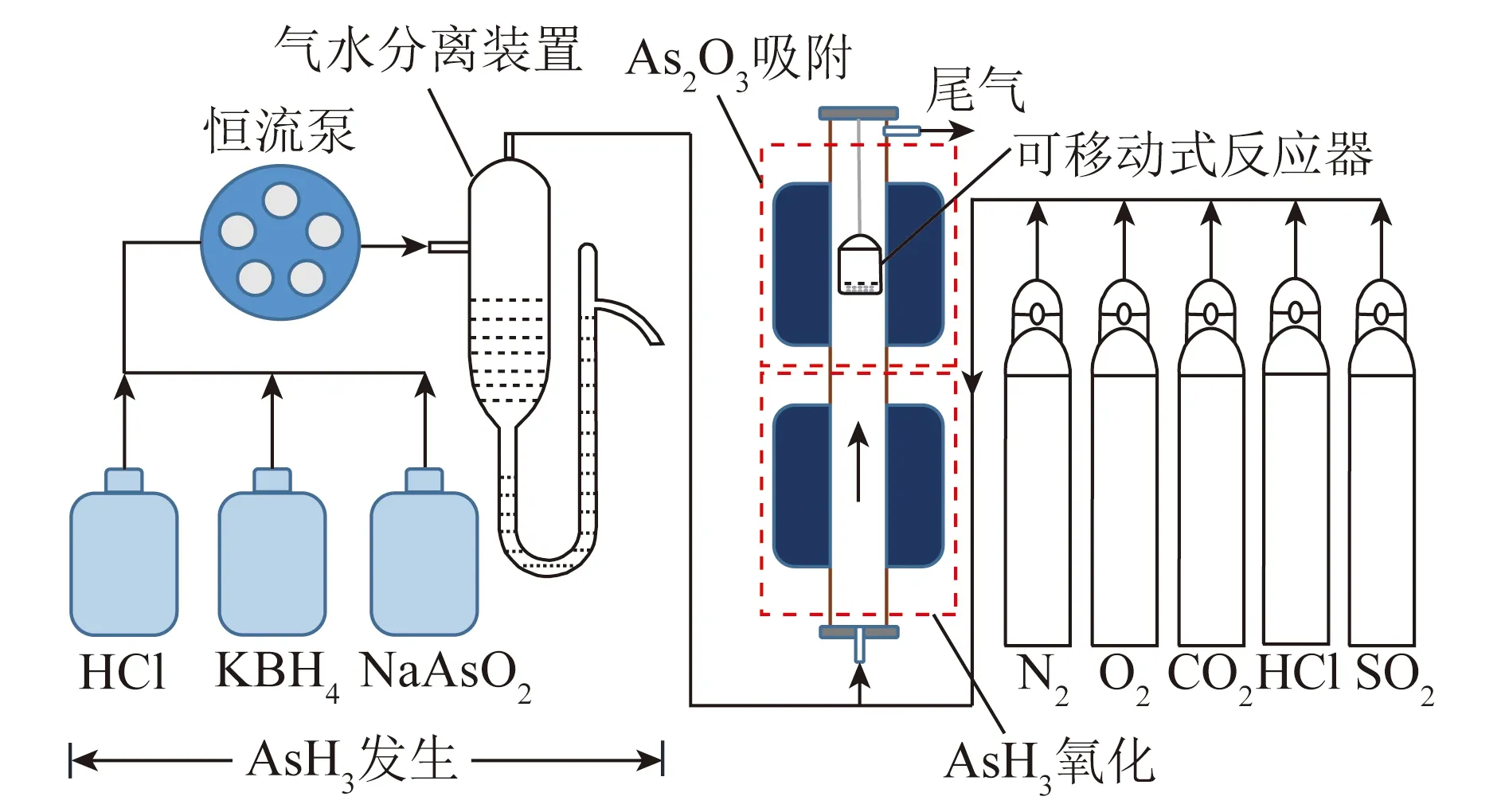
图1 气相砷吸附反应试验系统Fig.1 Gas-phase arsenic adsorption experimental system
1.3 样品分析
取40 mg吸附剂样品,用10 mL 20% 盐酸在80 ℃消解40 min,消解液经定容、过滤、稀释[15-16]后,稀释液采用吉天AFS-8220 原子荧光光度计测定。样品孔隙结构采用美国Micromeritics公司的ASAP2020测定仪测定,采用液氮(77 K)等温吸附法,比表面积采用BET(Brunauer-Emmett-Teller)法测定,平均孔径通过BJH(Barrett-Joyner-Halenda)公式计算获得,吸附剂样品颗粒的微观形貌通过扫描电子显微镜(ZEISS,Sigma300)分析。
2 结果与讨论
2.1 不同气氛CaO、Fe2O3、MgO对砷的吸附特性
图2对比了不同气氛下氧化物对气相砷的吸附特性。可知,900 ℃时MgO在4种气氛下对气相砷的吸附量均高于700 ℃,而900 ℃时Fe2O3在4种气氛下对气相砷的吸附量均低于700 ℃。O2/CO2气氛下,MgO和CaO对气相砷的吸附量少于相应燃烧气氛,而Fe2O3的气相砷吸附量高于燃烧气氛。HCl、SO2存在时,MgO和CaO对气相砷的吸附量明显少于相应燃烧气氛,且700 ℃时含HCl气氛更明显,900 ℃时含SO2气氛更明显;700 ℃下HCl抑制Fe2O3对气相砷的吸附,900 ℃则表现出促进作用;SO2对Fe2O3吸附气相砷无明显影响。整体来看,CaO对气相砷的吸附效果最好,其次是MgO,燃烧烟气中CaO吸附气相砷量最多。
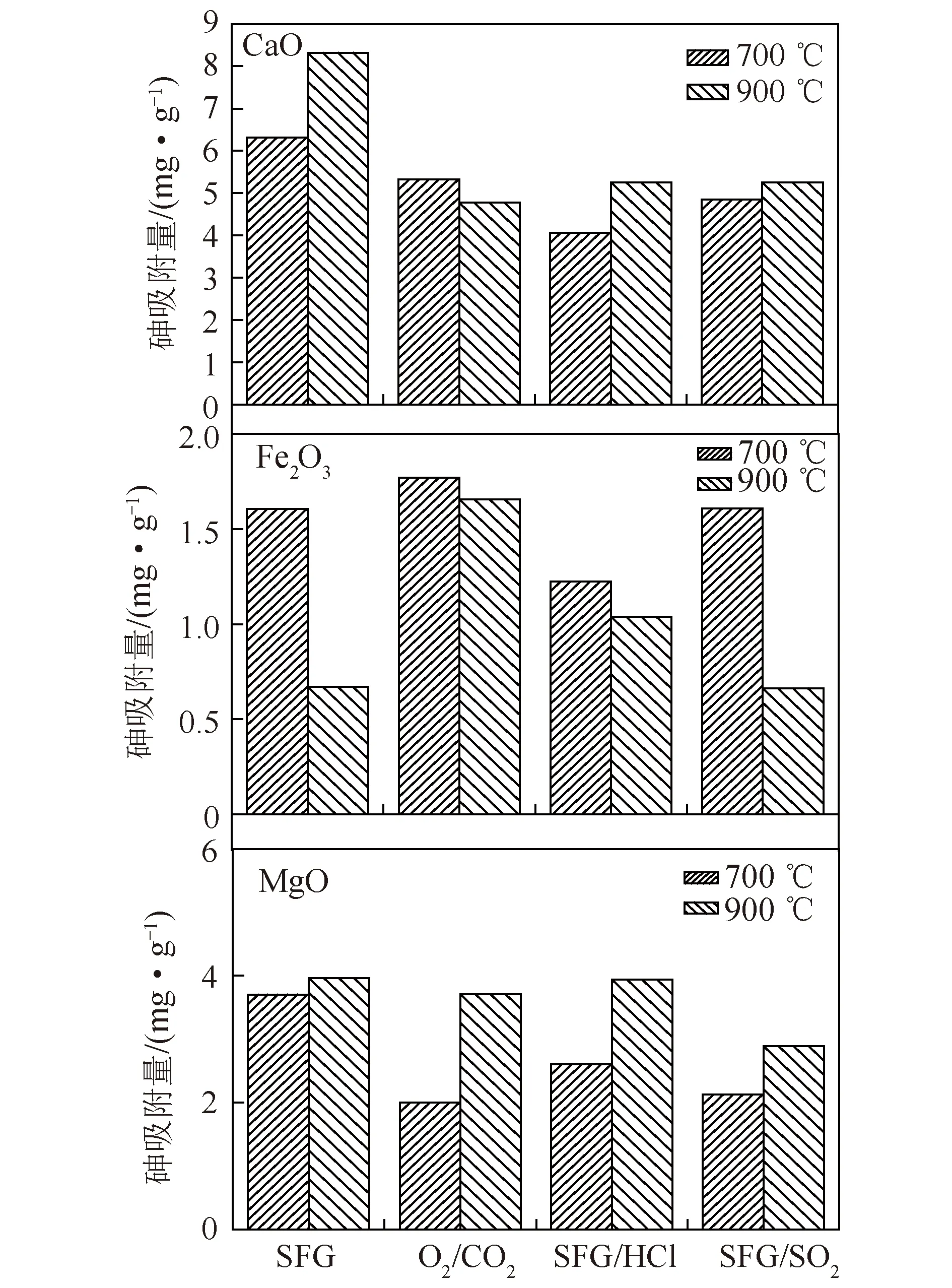
图2 不同气氛下砷的吸附量Fig.2 Arsenic adsorptionunder different atmosphere
定义P为相对于O2/N2气氛吸附砷的促进率,其计算公式为
(1)
其中,m0,t为模拟烟气气氛下样品对气相砷的吸附量;mx,t为O2/CO2、HCl、SO2气氛下气相砷的吸附量;t为测试温度。式(1)可用来评价相对于模拟烟气,其余3种气氛对气相砷吸附的作用效果。P>0,表现促进作用;P<0,表现抑制作用,计算结果如图3所示。
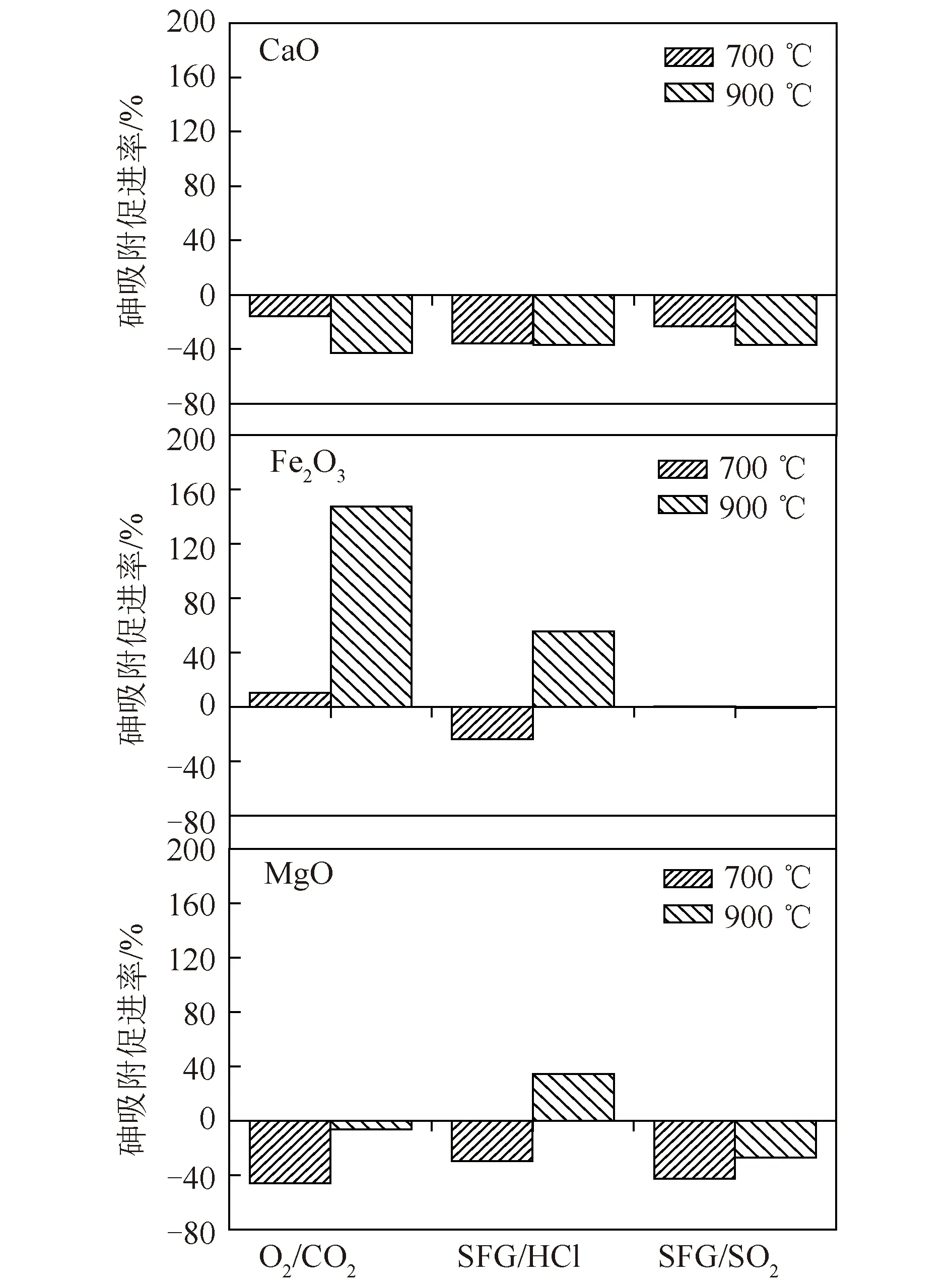
图3 气氛对样品吸附气相砷的影响Fig.3 Effect of atmosphere on the adsorptionof gas-phase arsenic in samples
由图3可知,O2/CO2气氛对CaO和MgO为抑制作用,900 ℃时CaO的砷吸附促进率为-42.63%,相对于700 ℃时的-15.70%,抑制作用明显;700 ℃时对MgO的砷吸附促进率为-45.99%,相比于900 ℃时的-6.29%,抑制作用较明显,这可能与碳酸化反应有关,CaO和MgO均为碱土金属氧化物,化学性质相似,而CaO与CO2反应生成性质比MgCO3稳定的CaCO3。O2/CO2气氛下,900 ℃时Fe2O3砷吸附促进率为147.12%,促进效果最明显。HCl对CaO吸附气相砷起抑制作用,700、900 ℃时砷的吸附促进率分别为-35.66%、-36.78%;700 ℃时,HCl对MgO和Fe2O3吸附气相砷起抑制作用,其吸附促进率分别为-29.73%、-23.68%,可见HCl对MgO的抑制作用更明显;900 ℃时,HCl对MgO和Fe2O3吸附气相砷起促进作用,其吸附促进率分别为34.26%、55.31%。SO2气氛对CaO和MgO吸附气相砷起抑制作用,700、900 ℃时CaO吸附促进率分别为-23.29%、-36.90%,MgO为-42.43%、-27.02%,可见700 ℃时对MgO抑制作用更明显,900 ℃时对CaO抑制作用更明显,SO2对Fe2O3吸附气相砷无明显影响。
2.2 吸附剂比表面积和孔隙结构
各吸附剂比表面积和孔隙结构见表2。可知,氧化物吸附剂比表面积较小,这与吸附剂制备方式有关,本试验吸附剂为粒径0.2~0.3 mm的颗粒状氧化物,均通过块状氧化物研磨筛选得到;Fe2O3比表面积最大,CaO和MgO次之。通常认为,比表面积越大,可为吸附反应提供更多的活性位点,吸附效果越好。结合图2和表2可知,比表面积不是决定气相砷吸附的唯一因素,氧化物对气相砷的吸附能力与表面活性位点数量有关,但是氧化物与气相砷结合的化学键键能强度对高温时氧化物吸附气相砷的影响更显著。研究认为,煤中痕量砷元素多富集于硫铁矿等硫酸盐,其中富集于无机盐周围的砷在燃烧过程以烟气形式与烟气颗粒、水蒸气等碰撞、吸附,当遇到表面发达的吸附剂时,由于吸附剂表面存在化学键,与砷相结合成稳定的砷酸盐[17-19]。此外,吸附剂表面形貌结构影响烟气流通,颗粒微观结构决定了气相砷吸附于吸附剂表面还是内部孔隙。
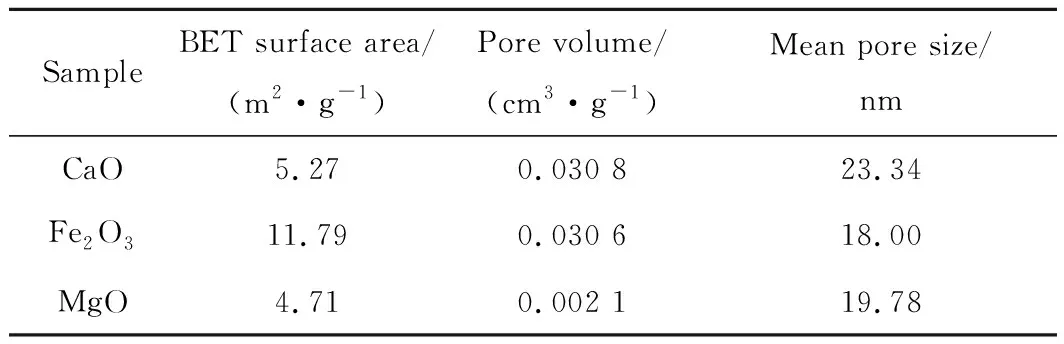
表2 样品的比表面积、孔容、孔径
2.3 吸附剂微观形貌
图4为CaO、MgO、Fe2O3吸附剂样品颗粒的微观形貌。可知,CaO和Fe2O3表面粗糙、孔隙发达,MgO表面较平滑。从化学性质看,MgO强于CaO,而从图2吸附效果看,CaO明显好于MgO,这与SEM结果一致。CaO颗粒松散,孔隙发达,能够过滤更多烟气中气相砷,除了表面能够吸附气相砷外,颗粒内部孔隙表面活性位点也可吸附气相砷;MgO较为密实,除了暴露在表面的吸附位点外,颗粒物内部对烟气中气相砷几乎无吸附作用。结合表2和图4,Fe2O3具有较大的比表面积,能够暴露更多的活性位点,但Fe2O3吸附酸性气体的活性低于MgO和CaO,因此吸附效果最差,说明气相砷的吸附量主要取决于吸附剂化学性质。通过测量流经吸附剂的烟气量发现,流经CaO和Fe2O3的气流量明显大于MgO。MgO和Fe2O3吸附剂颗粒的堆积密度大于CaO,因此MgO和Fe2O3吸附剂颗粒置于可移动式反应器时,填充厚度小于CaO,结合图4中CaO颗粒表面形貌,可推断CaO吸附剂颗粒参与实际反应的接触面积比MgO和Fe2O3吸附剂颗粒大。综合来看,CaO吸附剂颗粒吸附气相砷的通道面积大于Fe2O3和MgO。

图4 吸附剂微观形貌SEM图Fig.4 SEM pictures of adsorbents microstructure
2.4 吸附机理
CaO吸附气相砷的机理与MgO一致,因此分析CaO吸附气相砷机理,便可以理解CaO和MgO吸附气相砷过程。CaO吸附气相砷,一般认为以化学吸附为主,在700/900 ℃下,气相砷的物理吸收极少。张军营等[1]认为,CaO会与煤中砷化合物形成砷酸盐,从而起到固砷作用(式(2))。本文发现,O2/CO2气氛、HCl、SO2抑制CaO吸附气相砷,研究认为,CO2与CaO反应生成CaCO3,使CaO表面碱性活性位点减少,HCl、SO2相对于CO2更易与CaO反应,因此对CaO吸附气相砷的抑制作用更加明显[14]。通常认为,CO2与CaO发生碳酸化反应温度在600~800 ℃,而本文在900 ℃的O2/CO2气氛下,高浓度的CO2促进CaO碳酸化,该现象与Yu等[20]研究结果相符,说明CO2气化、O2/CO2气氛等高CO2气氛能够促进CaO在高温条件下发生碳酸化反应,进而抑制气相砷的吸附[21-22]。文献[23]研究表明,模拟烟气条件下,大量Fe2O3生成FeO和Fe3O4,温度和烟气酸性成分影响Fe2O3中Fe的价态。本文中Fe2O3的气相砷吸附效果低于CaO和MgO,Fe2O3吸附As2O3为化学作用,且弱于CaO(式(3))。Fe2O3比表面积大,但颗粒表面缺少团状颗粒,主要为细小的片状结构,且吸附As2O3的化学作用弱于CaO。O2/CO2气氛和HCl能够改变Fe2O3的存在形式,进而改变Fe2O3表面化学位点性质,由于Fe2O3高温时的存在形式具有易变性,气氛对Fe2O3吸附气相砷的影响随温度变化无定性规律。在测试温度条件下,SO2几乎不与Fe2O3发生反应,因此试验结果与模拟烟气一致。

(2)

(3)
3 结 论
1)在模拟锅炉烟气气氛下,CaO、MgO和Fe2O3对气相砷的吸附以化学吸附为主。
2)700、900 ℃下,模拟烟气、富氧、HCl及SO2四种气氛中,CaO对气相砷吸附量最高,这与CaO为强碱性氧化物和比表面积较大有关;MgO对气相砷的吸附次之,主要因为MgO颗粒表面较平整、吸附剂的比表面积较小;Fe2O3对气相砷的吸附最少。
3)O2/CO2气氛中,CO2及烟气中HCl、SO2为酸性气体,易与CaO和MgO表面碱性位点结合,从而抑制气相砷的吸附;但Fe2O3在O2/CO2气氛下气相砷吸附明显高于其他气氛,这可能与Fe2O3中Fe的存在形式有关,不同Fe的氧化物对气相砷吸附的作用效果不同,温度影响Fe2O3的存在形式,O2/CO2气氛和HCl能够改变Fe2O3的存在形式,进而改变Fe2O3表面化学位点性质,影响吸附强度。
