柠檬酸解离钛配位络合药物在4AA 制备中的应用
2020-07-28莫德欢叶敏张雁毕鸿亮张所德
莫德欢 叶敏 张雁 毕鸿亮 张所德*
(1.广东省科学院,广东 广州 510070;2.广东省生物医药技术研究所,广东 珠海 519090)
0 引言
随着元素化学的不断发展,有机Na、Li、Cu、Ti、Mg、Zn 等金属化合物被广泛应用于有机合成领域。手性配体与过度金属络合物催化提高合成过程的选择性,加速了不对称催化手型药物研发进程,常用过渡金属Sn、Ti、Cu、Ni、Rn 配体催化以多见报道。短效静脉麻醉药2,6-二异丙基酚,以TiCl4为催化剂,酰氯直接取代二异丙基酚邻位,在经过羰基还原,三氟乙酸脱羟基得到目标产物[1]。钛试剂可催化Sharpless 环氧化反应,参与烯丙醇的环氧化,该反应在合成抗HIV 药物、抗真菌药物、抗生素等药物合成中应用广泛[2]。钛离子极易与O、N 这类配位原子配位,形成钛络合物,可作为有机合成试剂、催化剂、抗肿瘤药物等,但Ti4+易与产物形成溶于水络合物,造成药物合成收率降低,药物产品纯化困难,影响药品质量,生态负荷严重。
β-内酰胺类抗生素是抗菌药物研究热点之一。(3R,4R)-3-[(R)-1-叔丁基二甲基硅氧乙基]-4-乙酰氧基-2-氮杂环丁酮(4AA)是合成培南类药物的关键中间体,应用广泛。而合成4AA的关键中间体(3S,4S)-4-乙酰基-3-[(1R)-1-羟乙基]-1-(4-甲氧苯基)-2-氮杂环丁酮(化合物B)是通过TiCl4催化(2R,3R)-N-(2-氧代丙基)-N-(4-甲氧基苯基)-2,3 环氧丁酰胺(化合物A)成环,但TiCl4极易与化合物B 形成溶于水的钛络合物,产物B 收率极低。本研究利用柠檬酸与Ti4+的强配位性,在醇溶剂下,与药物分子(化合物B)竞争配位钛离子,将药物分子释放,提高药物分子的收率。
1 实验部分
1.1 主要试剂与仪器
(2R,3R)-N-(2-氧代丙基)-N-(4-甲氧基苯基)-2,3 环氧丁酰胺(自制合成);TiCl4、柠檬酸、异丙醇、二氯甲烷等均为国药分析纯;紫外灯(ZF-20D);旋转蒸发仪(RE2000A);低温冷却液循环泵(上海科升仪器有限公司);真空泵(SHZ-D,上海科升仪器有限公司);三口烧瓶、分液漏斗、玻璃杯(欣维尔);电动搅拌(IKA)。
1.2 (3S,4S)-4-乙酰基-3-[(1R)-1-羟乙基]-1-(4-甲氧苯基)-2-氮杂环丁酮合成[3]
向1000mL 三口玻璃瓶中加入30g 0.114mol(2R,3R)-N-(2-氧代丙基)-N-(4-甲氧基苯基)-2,3 环氧丁酰胺(A,M 263.3g/mol),二氯甲烷500mL,N2保护,开启搅拌,用干冰/丙酮冷却液降温至-20℃,加入25g TiCl4,反应体系温度应<-15℃;原料反应完全即结束反应,向体系内加入150mL 4wt%HCl 溶液的冰水混合物粹灭,搅拌30min 后,静置2h 分层,水相用适量二氯甲烷萃取3 次,合并有机相和萃取相,150mL 饱和NaCl 溶液分次洗涤有机相3 次,无水MgSO4干燥5h 后过滤,滤液经减压旋蒸去除二氯甲烷,干燥24h,得到(3S,4S)-4-乙酰基-3-[(1R)-1-羟乙基]-1-(4-甲氧苯基)-2-氮杂环丁酮(化合物B)15.9g。
1.3 柠檬酸解离钛-药物分子络合物
依据1.2 小结化合物B 的合成方法,实际收率仅为53%,还有大量的化合物B 与过渡金属催化剂TiCl4形成络合进入水相。收集1.2 小节合成药物中间体B 过程中的4wt%HCl 粹灭液及饱和NaCl 洗涤液(300mL),此为解离反应的原料液。
1.3.1 解离反应
向300mL 原料液中加入适量的醇溶剂,开启搅拌,加入40wt%柠檬酸(CA)水溶液,继续搅拌1h;反应完毕后静置分层,水相用200mLCH2Cl2分次萃取,合并萃取相和醇溶剂相,减压旋蒸除有机溶剂,干燥后,得到钛络合物解离产物化合物B,反应历程如图1 所示。

图1 钛络合物解离反应历程
1.3.2 解离反应醇溶剂筛选
对解离反应醇溶剂种类进行单因素试验:向原料液中加入150mL 1%醇溶剂,醇溶剂的种类可为甲醇、乙醇、乙二醇、异丙醇、丁四醇。开启搅拌,加入40wt%柠檬酸(CA)水溶液150g,继续搅拌1h;反应完毕后用200mL CH2Cl2分次萃取,合并萃取相减压旋蒸除有机溶剂,得到钛络合物解离产物化合物B,选择收率最高的醇作为解离反应的醇溶剂。
1.3.3 解离反应酸溶液筛选
对解离反应所用酸的种类进行单因素试验:向原料液中加入150mL 1%异丙醇。加入适量(1+1)HCl溶液调整pH至4以下,pH 调节酸可选择HCl、H2SO4、H3PO4、CH3COOH、C2H5COOH;开启搅拌,加入40wt%柠檬酸(CA)水溶液150g,继续搅拌1h;反应完毕后用200mL CH2Cl2分次萃取,合并萃取相,减压旋蒸除有机溶剂,得到钛络合物解离产物化合物B,选择收率最高的酸作为解离反应的pH 调节用酸。
1.3.4 解离反应优化
在单因素试验基础上,为提高钛-化合物B 络合物解离效率,以反应中所使用的异丙醇溶液用量、浓度,柠檬酸的用量(以与化合物B 的摩尔比表示)、解离反应时间为影响因素,解离原液中化合物B 的收率为评价指标,选择L9(34)正交表,进行钛-化合物B 络合物解离反应优化实验,正交表设计见表1。
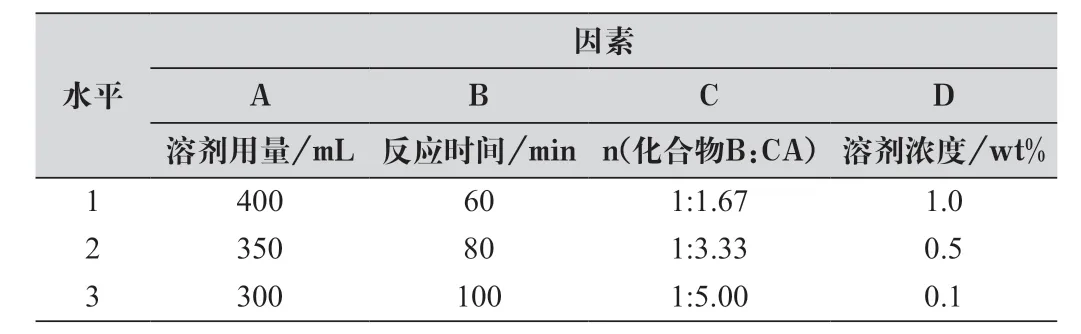
表1 解离反应表头设计
2 结果与分析
2.1 钛-化合物B解离机理
在有机合成领域中,钛试剂可作为多种有机反应催化剂,以提其合成反应性能。但钛离子特殊配位极易与目标产物形成较稳定的水溶性络合物,产物收率受到影响。若钛-产物分子络合物作为杂质进入有机相,有机相的纯化难度会显著增加,影响成药品质[4,5]。通过研究发现,柠檬酸的强配位性可与药物分子(目标产物)竞争配位金属离子,形成极其稳定的柠檬酸-钛络合物,释放药物分子,提高目标产物收率[6],历程如图2 所示。
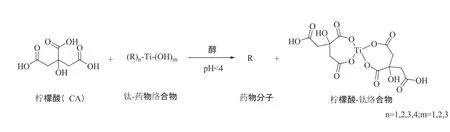
图2 柠檬酸-钛络合物生成历程
2.2 钛-化合物B络合物解离反应
2.2.1 醇溶剂筛选
筛选解离反应醇溶剂种类单因素试验结果,如图3 所示。五种醇为溶剂进行解离反应,化合物B 收率均在60%以上,大小依次为:异丙醇>丁四醇≈乙二醇>乙醇>甲醇。因此选择异丙醇为优选醇溶剂进行解离反应。
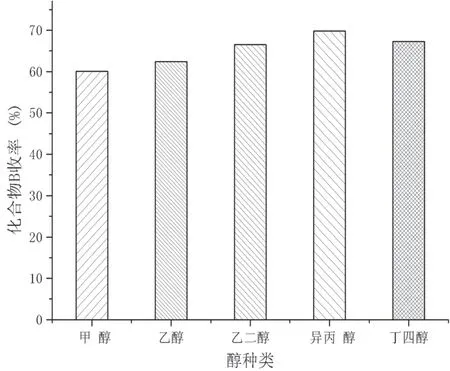
图3 醇种类筛选
2.2.2 酸种类筛选
筛选解离反应酸种类单因素试验结果,如图4 所示。五种酸分别为酸度调节剂,将pH 调至4 以下进行解离反应,化合物B 收率依次为:盐酸≈磷酸>硫酸>乙酸>丙酸。盐酸和磷酸在化合物收率上相当,因此可选择盐酸或磷酸为优选酸溶液进行解离反应。
2.2.3 正交试验极差分析
以1.2 小节化合物B 合成过程的水相为解离的原料液,在pH<4 的酸性条件,由柠檬酸解离钛-化合物B 络合物,得到单体化合物B,通过正交试验对异丙醇用量及浓度、柠檬酸的用量、解离反应时间进行分析,考察其对化合物B 收率的影响趋势,确定最佳解离条件。表2 为正交实验设计、结果和极差分析。
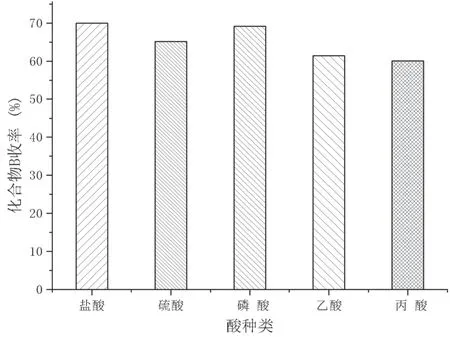
图4 酸种类筛选
极差分析可知,影响化合物B 收率因素主→次关系:柠檬酸用量>异丙醇浓度>异丙醇用量>反应时间。最佳实验方案:以络合物形式进入水相的化合物B 为14g 计算,柠檬酸用量60g,即40%柠檬酸溶液150g;异丙醇浓度为0.5%,用量200mL,反应时间60min。验证此方案,从水相中解离得到化合物B 收率为76.7%。
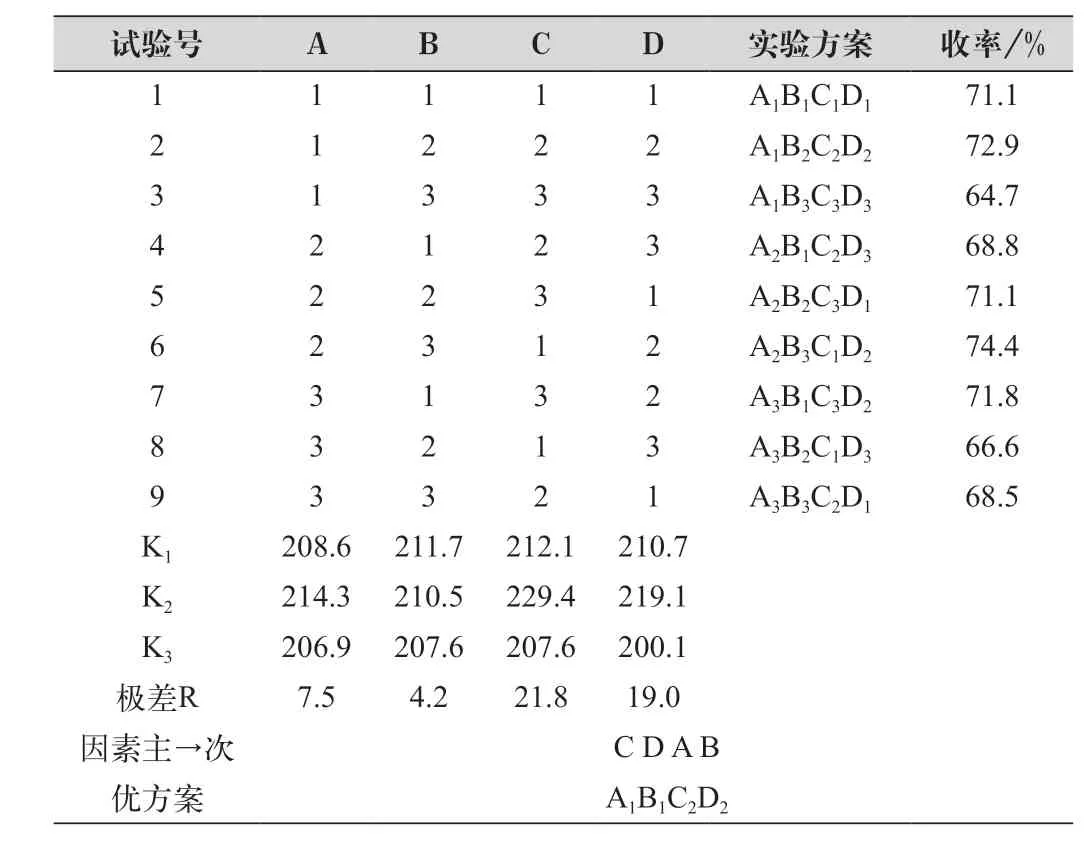
表2 正交实验极差分析
3 结语
TiCl4成环制备(3S,4S)-4-乙酰基-3-[(1R)-1-羟乙基]-1-(4-甲氧苯基)-2-氮杂环丁酮(化合物B),化合物B 与TiCl4形成水溶性络合物,致使目标产物收率极低。利用柠檬酸与Ti4+的强配位性,在醇溶剂下,与化合物B 竞争配位钛离子,将其解离进入有机相,提高药物分子的收率。通过单因素试验筛选解离过程的醇溶剂为异丙醇,酸溶液可选择盐酸或磷酸,最佳解离条件:40%柠檬酸溶液48.0g;异丙醇浓度为0.5%,用量400mL,反应时间30min,化合物B 收率76.7%。
