超声造影诊断肝包膜下小肝癌的临床价值*
2020-07-27毛枫袁海霞范培丽曹佳颖王文平
毛枫 袁海霞 范培丽 曹佳颖 王文平
小肝癌的早期诊断及肝癌术后复发是影响肝癌患者生存的一大因素[1],而部分小肝癌可位于肝包膜下,而肝包膜下小肝癌常规灰阶超声常常显示欠清或不清,为超声诊断及后续治疗带来一定的困难[2]。本研究拟通过分析肝包膜下小肝癌的超声特点及超声造影特征,旨在提高临床对超声造影诊断肝包膜下小肝癌的认识。
1 材料与方法
1.1 材料
对2017年1月至2019年7月间临床或影像学检查诊断或怀疑肝包膜下小肝癌的51例患者进行常规灰阶超声和超声造影检查。51例患者中,男37例,女14例,年龄25~78岁,平均(45.8±11.9)岁。共53个病灶,单发49例,多发2例;原发性45个,继发性8个。51例患者中乙肝或丙肝阳性者42例,阴性者9例;甲胎蛋白升高者30例,正常者21例;51例中经手术病理证实18例,介入治疗证实20例,穿刺病理证实3例,其他影像学检查及临床表现诊断10例。
1.2 方法
采用百胜Mylab Twice 超声诊断仪,探头选用CA541,频率1.5~5.0 MHz,均具有超声造影谐波成像功能。造影剂选用SonoVue,注射前用5 mL 0.9%生理盐水稀释,充分摇匀后震荡配置成混悬液。造影时用团注法快速推入肘正中静脉2.0 mL,然后用5 mL 生理盐水冲管。每次造影持续观察5~8 min,同时数字录像记录造影全过程。
常规灰阶超声仔细扫查肝脏,观察记录是否存在可疑区域灶,若发现病灶,记录其位置、大小、形态及回声特征,做出初步印象。若常规灰阶超声未发现明确的病灶,即在MRI及其他影像学检查的提示下,对可疑病灶及区域进行超声造影检查,切换至造影模式,机械指数设为0.06~0.10,观察动脉期、门脉期及延迟期病灶的增强时间、达峰时间、等回声时间及或消退情况,对病灶超声表现进行描述,并进行定位、定性及鉴别诊断,总结其增强类型。病灶动脉期快速增强呈高回声或同步增强呈等回声,门脉期减退呈低回声的定义为“快进快出”型;病灶动脉期快速增强或同步增强,门脉期呈等回声者定义为“快进慢出”型。病灶动脉期快速增强或同步增强,门脉期及延迟期均呈等回声者定义为“快进不出”型。检查结束后,所有病例均由2位高年资具有腹部超声及超声造影诊断经验的医师进行资料回放分析确认,出现分歧时由协商解决,确保一致性,并统一做出诊断。
1.3 统计学分析
采用SPSS 17.0 软件进行统计学分析。患者年龄、病灶大小、超声造影时间等计量资料采用于表示。用χ2检验比较常规超声与超声造影对肝包膜下小肝癌诊断检出率的差异,以P<0.01为差异有统计学意义。
2 结果
2.1 超声造影结果
51例患者,共53个病灶,35个病灶经手术病理证实,18个病灶经介入、临床表现或其他影像学检查共同确诊。所有病灶均位于肝脏包膜下,45个病灶紧贴肝包膜,8个病灶位于肝包膜下10 mm以内。位于肝膈面47个,位于脏面6个。病灶最小为7 mm×6 mm,最大为18 mm×15 mm,平均最大直径为(11±3.8)mm。常规超声声像图上描述为等回声病灶28个,稍低回声12个,稍高回声8个,低回声2个,高回声3个;描述肿块边界不清30个,边界欠清20个,边界尚清或边界清楚的共3个。
肝包膜下病灶以等回声和稍高或稍低回声为主,占90.6%(48/53),肿块以边界不清和欠清为主,占94.3%(50/53)。
超声造影显示所有病灶开始增强时间为(15.3±6.1)s,达峰时间为(25.2±8.8)s,减退呈低回声时间为(95.7±57.8)s。
2.2 两种检查方法对比
53个病灶中48个表现为动脉期快速增强,占90.6%(48/53),同步增强5个,占9.4%(5/53)。38个病灶门脉期减退呈低回声,占71.7%(38/53),15个病灶呈等回声,占28.3%(15/53),50个病灶延迟期减退呈低回声,占94.3%(50/53),3个病灶延迟期仍基本呈等回声改变,占5.7%(3/53)(表1)。图1A~1D示女性患者63岁,肝癌术后11年,随访至今,增强MRI发现肝左叶包膜下增强灶。图2A~2D显示67岁患者男,乙肝史40年,发现肝右叶下角包膜下小结节病灶。
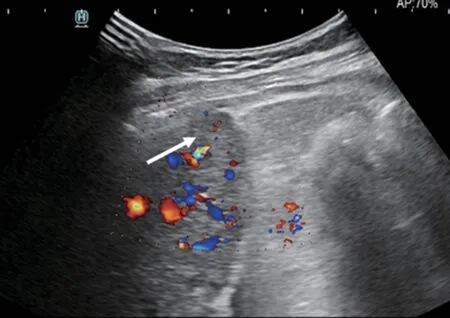
图1A 增强MRI 发现肝左叶包膜下增强灶,常规超声扫查隐约可见肝左叶包膜下一稍低回声区(白色箭头),边界不清,CDFI可见点状彩色血流

图1B 注射造影剂后,显示病灶动脉期明显强化(箭头所示),大小约13 mm×10 mm,病灶位于肝左叶包膜下
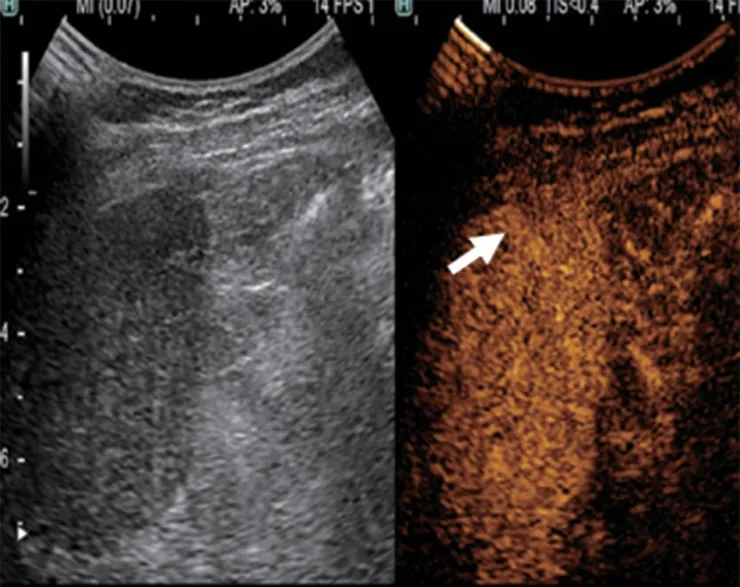
图1C 病灶门脉期基本呈等回声改变,未见明显减退(箭头所示)

图1D 病灶延迟期200s后仍呈等回声改变,病灶符合“快进不出”的超声增强模式

表1 53个病灶超声造影的增强表现
常规超声检出15个病灶,检出率为28.3%(15/53),其中低回声2个,高回声3个,稍低回声6个,稍高回声4个。超声造影检出53个病灶,检出率为100%(53/53),两种方法检出率比较差异有统计学意义(P<0.01)(表2)。
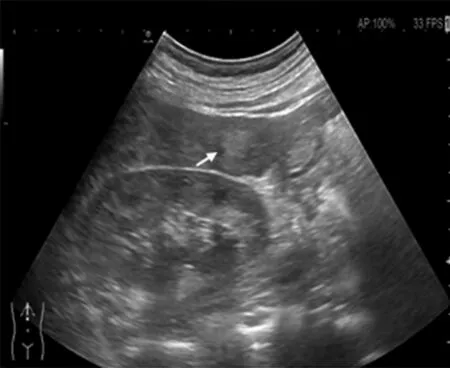
图2A 肝右叶下角包膜下占位1个月,病灶呈稍高回声(白色箭头),与周围肝硬化结节较难鉴别,边界欠清,大小约12 mm×10 mm

图2B 注射造影剂后,该病灶动脉期明显强化,病灶边界尚清晰
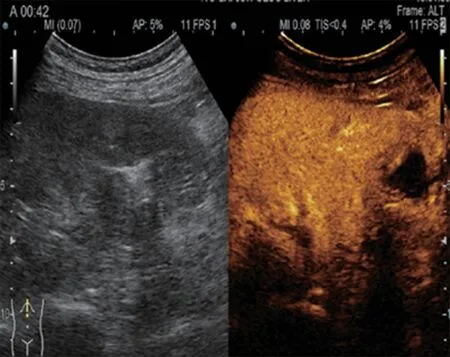
图2C 该病灶在门脉期呈稍低及等回声改变,此时边界欠清晰
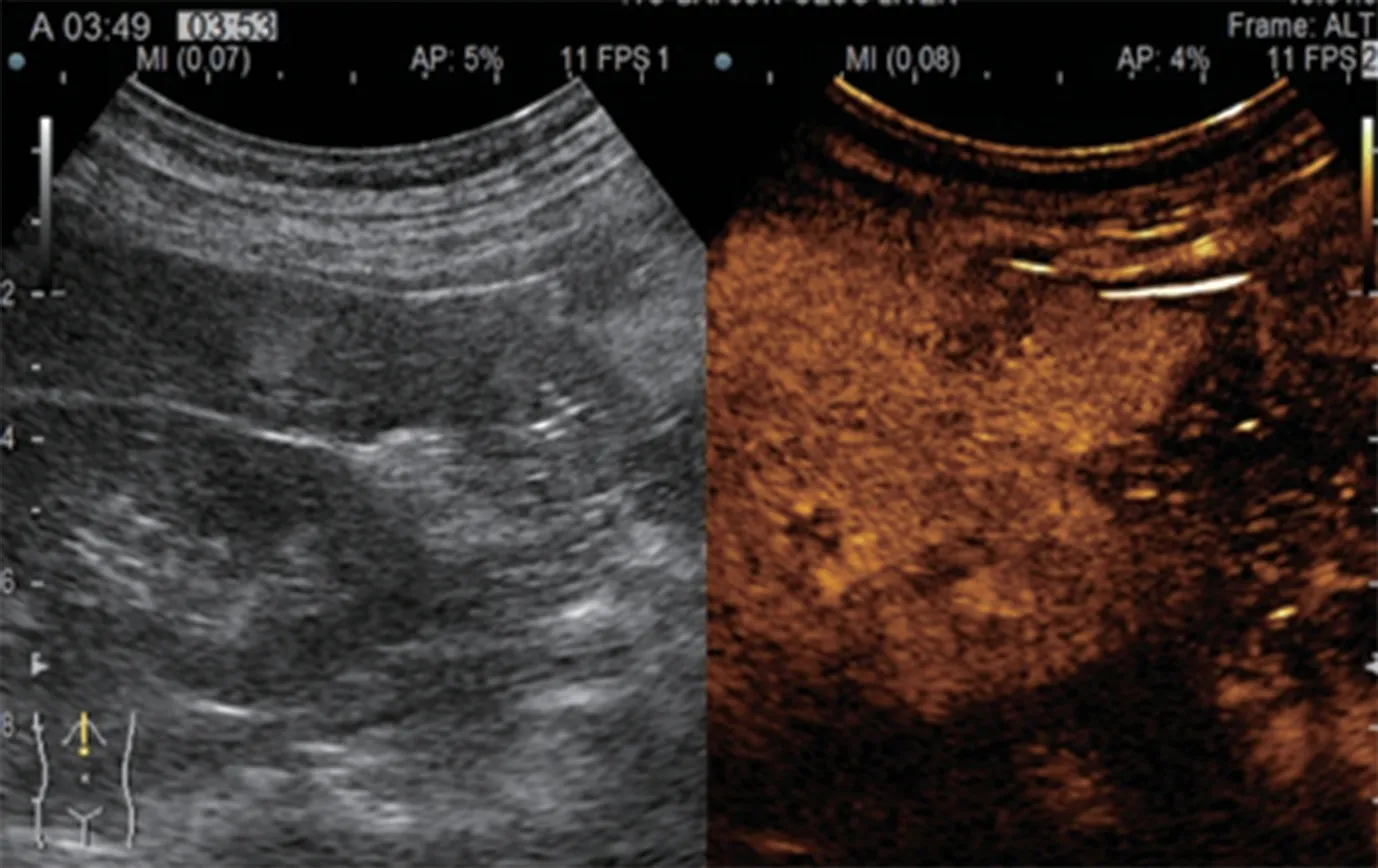
图2D 随着时间延长,该病灶在延迟期120s后呈低回声改变,此时边界显示较清,病灶符合“快进慢出”超声增强类型
53个病灶中,符合“快进快出”类型38个,占71.7%(38/53),“快进慢出”类型12个,占22.6%(12/53),“快进不出”类型3个,占5.7%(3/53)。

表2 常规超声与超声造影对肝包膜下小肝癌的检出率对比
3 讨论
原发性肝癌是危害我国人民健康的主要肿瘤,近年来,随着医学影像技术的发展及局部消融治疗的逐步推广,小肝癌局部消融治疗的有效性得到了较大提高[3]。然而,随着临床肝癌病例的增多,发现位于肝包膜下的小肝癌也逐年增多,且其在常规灰阶超声上表现越来越不典型,例如病灶较小,病灶呈等回声或病灶边界不清,病灶被肋骨或气体所遮盖及超声伪像等因素影响,使得病灶常常被常规灰阶超声漏诊,延误了最佳的治疗时机。
在本组资料中,常规灰阶超声发现15个病灶,占28.3%(15/53),且多为边界尚清、体积相对较大病灶,均建议超声造影检查以明确诊断。常规灰阶超声对肝包膜下小病灶容易漏诊的原因主要有:1)肝包膜下肝癌一般体积较小时,常呈等回声改变,边界不清,导致常规灰阶超声不易显示,容易漏诊。本组53个病灶,<15 mm 的病灶有40个,占75.5%,病灶呈等回声或稍高稍低回声的病灶,占90.%(48/53),边界欠清和边界不清的病灶有50个,占94.3%。2)病灶位于肝脏包膜下,易受到肺内气体或肋骨遮盖,容易遗漏,在检查中发现,较多病灶位置较高,位于膈顶区域,被肺内气体遮盖而不易显示;同时,由于病灶较小,常位于肋骨正下方而遗漏,此时往往需要患者呼吸配合进行反复扫查并侧动探头才能显示病灶。3)肝包膜下小肝癌常常受前方腹壁组织混响伪像影响而显示欠清,导致遗漏,此种情况高频表浅探头可以使病灶显示更加清晰,以避免此时伪像的发生。4)在肝硬化背景下,肝脏背景回声增粗,表面不平呈结节状,而小肝癌混杂其中,有时与硬化结节及肝表面凹凸不平较难鉴别[4]。
然而,随着技术的发展,超声造影可显著提高小病灶的显示率,并可全程观察病灶的增强方式、增强类型和减退情况,不仅可对大部分病灶做出定性和定位诊断,还可观察到肿块的形态学以及血供情况,并可在实时引导下进行肝癌的微创治疗,更好地为微创局部治疗提供可靠的影像依据。文献报道[5-6],超声造影可检查发现15 mm 以下微小肝癌。本组资料显示,超声造影对于肝包膜下病灶的显示率为100%,与文献基本一致[7]。对于肝包膜下的小肝癌,其在超声造影上也具有一定的特征性表现[8-9],即动脉期快速增强,门脉期及延迟期仍呈等回声的比例较高,本资料中符合此特征的有15个,占28.3%(15/53)。分析原因可能为肝包膜下病灶一般较小,肿块血供常以门静脉为主,且部分病灶为复发病灶,经过化疗及介入等治疗后,血供常减少或血供类型改变等因素,导致造影增强方式及类型改变。结合文献[10],对于肝包膜下小病灶,尤其是复发病灶,只要造影显示动脉期出现增强,仍可诊断为肝癌。
当然,超声造影同样也存在一些不足:1)某些特殊位置的病灶,如位于肝左外叶外侧缘、肝右叶膈顶、肝右后叶背侧以及肝尾状叶较深处时,由于肺脏及胃肠道气体的干扰、肋骨的遮盖、患者呼吸的配合不佳、脂肪肝以及各种原因导致的衰减等因素,导致超声造影亦存在一些易漏区及盲区,此时需要仔细扫查,微调探头,提高操作者水平,并参考其他影像学检查,才能做出正确的诊断;2)每次注射超声剂后,造影观察的病灶数目相对较少,多个病灶时需多次反复注射造影剂,且病灶动脉期增强时间往往较短,亦需要提高操作者熟练度以免漏诊。
总之,对于临床怀疑肝癌或肝癌复发的患者,应用常规灰阶超声仔细扫查肝脏及肝脏包膜下,同时对病灶进行超声造影检查,不仅可以观察病灶动脉期增强表现,还可以在门脉期及延迟期对肝脏进行反复扫查,更加明确肿块的性质及数目[7]。因此,超声造影对于肝包膜下肝癌的诊断具有一定的优势,可显著提高肝包膜下小肝癌的检出率,具有很大的临床应用价值。
