18F-NaF PET/CT对多发性骨髓瘤的诊断价值及其影像学特征的回顾性研究
2020-07-27张瑜张晓琳黄占文张伟陈跃
张瑜 张晓琳 黄占文 张伟 陈跃
西南医科大学附属医院,核医学与分子影像四川省重点实验室(四川泸州646000)
多发性骨髓瘤(multiple myeloma,MM)是一种发生于B 细胞的恶性血液系统肿瘤,其特征是浆细胞克隆恶性增殖,病变可以累及人体多个器官、系统,临床表现复杂多样,无特征性,常被误诊[1-2]。MM 骨骼病变主要是全身骨骼多发的溶骨性改变和广泛的骨质疏松。骨骼受累的后果是严重的疼痛、脊髓压迫和骨折,这些对患者的生存质量和最终的生存时间都有重大影响[3-4]。MM 骨病变的检出主要依靠传统影像学如CT、MRI 以及99mTc-MDP SPECT/CT 骨显像等,这些检查方法因自身的技术限制,仍不能完全满足临床诊断需求。近年来随着PET/CT 的广泛应用,关于MM 的18F-FDG PET/CT研究国内也陆续有报道[5-6]。18F-FDG 是一种非特异性肿瘤显像剂,在MM 诊断方面仍存在一定的不确定性。而18F-NaF 是一种用于探测骨骼病变的高灵敏亲骨性PET 显像剂,对于MM 骨病变的检出有更大的优势[7]。该研究意在探究18F-NaF PET/CT 在MM 诊断中的价值,以期为MM 的临床诊断提供一个新的影像学检查方法。
1 资料与方法
1.1 一般资料选取2015年7月到2018年12月期间到本院就医的53 例临床高度怀疑为MM 患者。该组病患中男34 例,女19 例,病患年龄45 ~81岁,平均年龄(59.1±11.6)岁。所有患者均在7 d内完成99mTc-MDP SPECT/CT 骨显像与18F-NaF PET/CT 检查。所有病患均依照国际卫生组织(WHO)诊断多发性骨髓瘤标准(2001年),通过病理组织活检、骨髓检查、血生化常规检查及影像学检查确诊或排除MM。
1.2 显像检查方法
1.2.1 18F-NaF PET/CT 显像方法检查设备采用飞利浦PET/CT(Gemini TF 16 型),显像剂18F-NaF由西门子回旋加速器自行生产,放化纯≥95.0%。18F-NaF 按照3.7 MBq(0.1 mCi)/kg(体质量)剂量计算,经静脉注射入病患体内,1 h 后进行检查。病患仰卧位平躺,双手放于身旁,检查范围从头顶到足底。先进行CT 采集(管电压100~120 kV,管电流100~110 mA,矩阵512×512,层厚3.8 mm),再进行PET 扫描,使用3D 模式采集,每个床位1.5~2.0 min。数据采用有序子集最大期望值迭代法(OSEM),经飞行时间(TOF)技术重建后,获得横断面、冠状面、矢状面的PET 图像 及PET 与CT 的融合图像。
1.2.2 99mTc-MDP SPECT/CT 显像方法检查设备采用西门子SPECT/CT(Sybia16T 型),准直器采用低能高分辨型。从99mo-99mTc 发生器淋洗获得99mTcO4,再与亚甲基二膦酸盐(MDP)合成显像剂99mTc-MDP,放化存纯≥95.0%。99mTc-MDP 的注射剂量为20 ~30 mCi,经静脉注射入病患体内,3~4 h后进行检查。检查前排空膀胱,病患仰卧位平躺,双手放于身旁,检查范围从头顶到足底。常规扫描速度18~20 cm/min,扫描矩阵256×1 024,必要时对病灶部位加做局部断层显像。
1.3 图像分析方法及诊断标准
1.3.1 图像分析方法99mTc-MDP SPECT/CT 图像和18F-NaF PET/CT 图像分别由2 位副高级及以上核医学医师独立、双盲法阅片,对两种检查方法的结果分别作出是否为MM 的定性诊断,并对所有出现的病灶作出定性诊断,分别对于两种检查方法诊断的MM 病灶计数,汇总分析。
1.3.2 图像诊断标准99mTc-MDP SPECT/CT 及18FNaF PET/CT 图像分析中,病变部位出现异常显像剂摄取增高区或稀疏缺损区为阳性表现,其中必须排除SPECT/CT 和PET/CT 上显像剂异常分布灶位于手术或有创伤部位、非病理性骨折、关节四周和椎体的骨赘、退变以及明显的骨良性病变。
CT 扫描的阳性表现是以穿凿状或虫蚀状为主的多发性溶骨性骨质破坏以及广泛的骨质疏松,包括四肢长骨近端的溶骨性骨质破坏,肋骨、四肢长骨等部位出现的皂泡样膨胀性骨质改变等均为阳性表现。
1.4 统计学方法统计分析采用SPSS 21.0 软件包,对于两种显像结果进行灵敏度、特异度、准确度等指标的运算,比较上述两种核素显像方法对于多发性骨髓瘤的诊断效能有无差异;统计方法采用配对χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 患者的最终诊断结果依据国际卫生组织(WHO)诊断MM 标准(2001年),通过病理组织活检、骨髓检查、血生化常规检查及影像学检查,53 例可疑患者中,最终42 例患者确诊为MM,11 例患者排除MM。
2.2 两种显像方法对多发性骨髓瘤的诊断效能比较见表1。99mTc-MDP SPECT/CT 与18F-NaF PET/CT 两种检查方法基于临床最终诊断结果,各自对MM 患者的诊断效能通过统计分析结果显示:99mTc-MDP SPECT/CT 全身骨显像诊断MM 的灵敏度为88.1%(37/42),特异度为81.82%(9/11),准确度为86.79%(46/53);18F-NaF PET/CT 诊断MM 的灵敏度为97.62%(41/42),特异度为81.82%(9/11),准确度为92.45%(49/53);18F-NaF PET/CT 诊断MM 的灵敏度明显高于99mTc-MDP SPECT/CT 全身骨显像,其差异有统计学意义(χ2=3.896,P=0.048);它们的特异性相同;准确度差异无统计学意义(χ2=1.504,P=0.220)。42 例MM 患者99mTc-MDP SPECT/CT、18F-NaF PET/CT 发现病灶数分别为238、351,其差异有统计学意义(χ2=20.441,P<0.001)。相比99mTc-MDP SPECT/CT 全身骨显像,18F-NaF PET/CT能检出更多的MM 患者、发现更多的MM 病灶、图像质量更佳(图1)。

表1 与金标准比较两种检查方法对MM 诊断效能Tab.1 Comparison between the two examination methods and the gold standard in the effectiveness of MM diagnosis 例

图1 多发性骨髓瘤SPECT/CT 及PET/CT 图像Fig.1 SPECT/CT and PET/CT images of multiple myeloma
2.3 多发性骨髓瘤18F-NaF 分布特征和骨质改变特征42 例MM 患者18F-NaF PET/CT 共发现351 处病灶,其中位于脊柱骨占37.89%(133/351),病灶形态多样,主要表现为粗横条形或细线形显像剂摄取增高;胸廓骨占31.91%(112/351),表现为结节状或点状显像剂摄取增高,形似“散弹”样分布;骨盆骨占17.09%(60/351),以团片状或结节状显像剂摄取增高为主;颅骨占7.12%(25/351),表现为“花斑”状显像剂摄取增高;四肢骨占5.98%(21/351),病灶主要分布在长骨两端,表现为点状或竖条状显像剂摄取增高。351 处病灶中共发现19 处(5.41%)显像剂摄取增高与稀疏缺损并存的“炸面圈”样改变,主要分布于肩胛骨、脊柱及骨盆等处。多发性骨髓瘤的18F-NaF PET/CT 特征性图像见图2。
MM 骨骼病变的CT 图像表现:颅骨、四肢骨病变表现为穿凿状或颗粒状骨质破坏;肋骨病变主要表现为髓腔膨大并骨皮质破坏、缺失及不连续;脊柱病变主要表现以多发的大小不等的虫蛀状骨质破坏或广泛的骨质疏松。
3 讨论
多发性骨髓瘤是一种中老年人比较常见的血液系统恶性肿瘤,在我国的发病率约为2~3/10 万,仅次于淋巴瘤位居血液系统恶性肿瘤的第2 位,男性多于女性,该组研究病例男女比例为1.8∶1。其病因与发病机制尚不清楚,可以与遗传、理化因素(长期接触离子放射、化学毒物等)、慢性炎症、EB 病毒感染、染色体异常和肿瘤基因突变等有关[8]。其骨骼病变发病机制可能是:肿瘤细胞促进破骨细胞分化和功能的信号因子上调,如RANKL、趋化因子(CCL3、CCL20)和白细胞介素(IL-1、IL-6),激活破骨细胞;肿瘤细胞通过直接分泌Wnt 拮抗剂(如DKK1)或诱导间质细胞和骨细胞(如硬骨素和激活素)释放成骨细胞抑制剂,改变周围的微环境以抑制成骨,这些因素最终导致骨质破坏和骨质疏松的发生[9-11]。
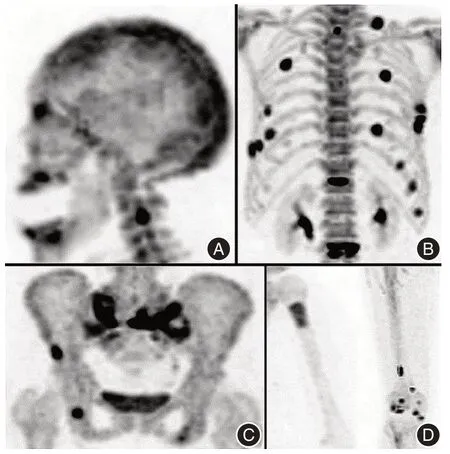
图2 多发性骨髓瘤患者的18F-NaF PET/CT 特征性图像Fig.2 Characteristic image of18F-NaF PET/CT in patients with multiple myeloma
目前诊断MM 的用影像学诊断方法有X 线、CT、MRI、SPECT 或SPECT/CT 骨显像以及18F-FDG PET/CT 显像等。X 线、CT 是MM 的常用影像学检查方法,但是X 线只有在局部骨无机盐丢失达30%~50%时才会出现异常,因此不能发现早期病变,诊断率低,漏、误诊率较高;CT 对骨病变检出率相对较高,但通常是局部检查,容易遗漏对诊断有帮助的重要骨病变;MRI 对MM 的髓外侵犯更加敏感,而对骨骼病变的显示不如CT 准确和敏感[12-13];18F-FDG PET/CT 在MM 骨骼病灶检出中对于溶骨性病灶更敏感,对于成骨性病灶的敏感性较差,相比MRI 或CT 更有益于髓外病变的检出[14-16]。相比以上检查方法,99mTc-MDP SPECT 或SPECT/CT骨显像对MM 骨病变的诊断具有较高检出率[17]。18F-NaF 是一种用于探测骨骼病变的高灵敏亲骨性PET 显像剂,其在体内的摄取机制类似于99mTc-MDP,但具有更好的药代动力学特性:(1)18F-NaF血浆蛋白结合低,骨摄取更快,显像更早;(2)更快的血液清除速度和更高的骨骼摄取(相当于99mTc-MDP 的2 倍),病灶/本底值高,图像质量更佳[18]。这使得它对于早期、轻微骨病变能够更好的检出。本研究表明对于MM 的诊断18F-NaF PET/CT灵敏度高于99mTc-MDP SPECT/CT,对于MM 病灶数目的探索18F-NaF PET/CT 更是明显高于99mTc-MDP SPECT/CT,这些主要体现在前者可以检出更多MM 患者,发现更多、更小、更早期的MM 病灶,这得益于18F-NaF 更好的药物理化性质、PET 更高的分辨率以及PET/CT 更多的图像信息。由于骨的良性病变(如外伤、炎症、退变等)18F-NaF 也会出现显像剂摄取的假阳性,这会影响18F-NaF 的特异性,但是PET/CT 显像中的CT 可以很好的弥补这一缺点,PET 功能成像和CT 形态成像的融合在一定程度上解决了假阳性的问题,进一步提高了诊断的准确率。本研究结果显示18F-NaF PET/CT与99mTc-MDP SPECT/CT 对于MM 诊断的特异性两者一致,18F-NaF PET/CT 的准确度高于99mTc-MDP SPECT/CT,但差异无统计学意义,分析原因为病例数较少,进一步扩大病例样本数,将会有不同的统计学价值。
MM 骨病变的好发部位以椎体、肋骨和骨盆骨最为常见,与这些部位的骨骼富含红骨髓有关[19]。本研究中42例MM患者18F-NaF PET/CT共发现351处病灶:脊柱骨占37.89%、胸廓骨占31.91%(主要为肋骨)、骨盆骨占17.09%、颅骨占7.12%、四肢骨占5.98%。MM 骨病变的18F-NaF PET/CT 显像剂分布具有一定的特征:(1)脊柱病灶形态主要以粗横条形或细线形显像剂摄取增高;(2)肋骨主要表现为结节状或点状显像剂摄取增高,形似“散弹”样分布;(3)骨盆骨以团片状或结节状显像剂摄取增高为主;(4)颅骨表现为“花斑”状显像剂摄取增高;(5)四肢骨病灶主要分布在长骨两端,显像剂呈竖条状或点状摄取增高。其中19 处(5.41%)病灶出现显像剂摄取增高与稀疏缺损并存的“炸面圈”样改变,主要分布于肩胛骨、脊柱及骨盆等处,可能与这些病变骨骼处既有破骨细胞参与的骨质吸收、破坏,又有成骨细胞参与的新骨正在修复形成有关[20]。
传统的99mTc-MDP 骨显像由于价格低廉、技术成熟已经成为部分骨骼病变首选检查方法。但它的显像原理是病变部位骨骼局部血流和骨代谢与正常骨骼的差异,而对于病变部位血流量及骨代谢改变不明显的病灶则很难发现,这就降低了其灵敏度。而随着SPECT/CT 断层融合技术的应用在一定程度上有所改善。但由于SPECT 空间分辨率较低、图像反映的信息量小(即计数率低)、断层显像的视野限制等,使得这种改善非常有限,不能为临床提供更多的影像信息。18F-NaF PET/CT凭借着18F-NaF 药物更好的理化性质、PET 更高的分辨率以及PET/CT 提供更多的图像信息,较传统的99mTc-MDP 骨显像、99mTc-MDP SPECT/CT 骨显像,18F-NaF PET/CT 对于MM 的检出,特别是早期检出具有更大的优势;其显像剂异常分布的特征性表现,在与恶性肿瘤骨转移及其他疾病的鉴别诊断中具有很好的价值;与传统的99mTc-MDP 骨显像、99mTc-MDP SPECT/CT 相比,18F-NaF PET/CT 能检出更多MM 患者、发现更多MM 病灶、图像质量更佳,势必会在更大程度上满足临床的需要。
本研究旨在探究18F-NaF PET/CT 诊断多发性骨髓瘤MM 的影像特征及应用价值,病例数尚不足,有待于扩大样本量研究。18F-NaF PET/CT 中CT为全身低剂量CT,而99mTc-MDP SPECT/CT 中CT 为局部CT 扫描,故18F-NaF PET/CT 中CT 存在优势,由于操作的复杂性,统计分析中未能将该优势排除在外。本研究中仅分析了MM 病灶的18F-NaF PET/CT 影像特征,而对于有显像剂摄取异常的非MM 病灶未进行统计及分析,今后将进一步深入研究。
