两种不同模式鼻咽部放疗对人工耳蜗设备性能影响的短期观察
2020-07-27陈抗松虞幼军周道民赖彦冰张国义刘致滨何锦潮陈慧琴孙恺
陈抗松 虞幼军 周道民 赖彦冰 张国义 刘致滨 何锦潮 陈慧琴 孙恺
人工耳蜗植入是目前成人和儿童双侧重度感音神经性聋听觉补偿的最有效手段,自1984年美国药品与食物管理局(FDI)正式批准 3M/House植入投入临床应用以来,迄今全球约40 万人植入了人工耳蜗[1]。 从 1995 年多通道人工耳蜗引进我国以来,截止2013年,我国约有3万例严重感音神经性聋患者接受了人工耳蜗植入[2]。由于植入人数的增加和设备的使用期限较长,相当数量的人工耳蜗植入者可能在植入后罹患与植入无关的的恶性肿瘤并且需要接受放射治疗。广东省是全世界鼻咽癌最高发的地区,尤其以中部和西部的肇庆、佛山和广州高发,最高发病率甚至达到25.12/10万[3]。鼻咽癌的治疗是以放疗为主的综合治疗,不少患者放疗后可能合并重度感音神经性聋需要植入人工耳蜗,而植入后的患者仍然面临复发风险需要行二次放疗。因此,广东地区人工耳蜗植入后接受放射治疗者将来可能会愈来愈多。由于人工耳蜗包含集成电路,有可能会因放射治疗而受损,因此,本研究拟通过对人工耳蜗植入后的模型模拟鼻咽癌放射方案进行照射,检测放疗后人工耳蜗电子元件的稳定性,探讨放疗对人工耳蜗设备的安全性,以指导人工耳蜗植入者放疗方案的制定。
1 材料与方法
1.1建立人工耳蜗植入模型 将已测试确定完好的3个CS-20A型人工耳蜗植入体(杭州诺尔康公司)在显微镜(Zeiss,V700)下按经典的开放乳突-面隐窝经圆窗入路分别植入3个成人尸头(非鼻咽癌患者),分别为模型A、B、C;植入成功后将尸头浸泡入生理盐水中测试人工耳蜗电极阻抗。
1.2鼻咽部放射治疗方案
1.2.1体位固定及CT扫描人工耳蜗 将尸头模型仰卧于头颈肩定位体架上,以热塑头颈模固定。每例模型均以1 mm 层厚进行定位CT扫描,扫描范围从头顶至C2下缘,再将CT扫描图像传入Ecilps 治疗计划系统(treatment planning system,TPS)进行图像处理及放疗计划设计。
1.2.2勾画放疗靶区和危及器官 模型A以人工耳蜗植入体作为照射中心靶区(图1);模型B模拟鼻咽癌照射模式,照射靶区包括鼻咽部、咽旁间隙、翼腭窝、鼻腔和上颌窦的后三分之一、蝶窦底壁、后组筛窦、颅底、斜坡等,人工耳蜗植入体作为危及器官勾画(图2);其他危及器官则包括脑干、视神经及视交叉、晶体、眼球、内耳、颞叶、脊髓、下颌骨、腮腺、颞颌关节等。
1.2.3复位确定照射中心并实施放疗 在X光模拟机下将模型A、模型B移位至照射靶区中心位置(图3),在头颈模上标线,标记为照射中心;模型A:放疗总剂量80 Gy,每周5次,每次2 Gy,分40次约8周完成;模型B:模拟鼻咽癌照射模式,以鼻咽部为照射中心靶区,放射总剂量70 Gy,每次2 Gy,每周5次,分33次,约6.5周完成;模型C:不做任何放疗处理。
1.3放疗后人工耳蜗性能检测 放疗方案完成后当天每个模型取出人工耳蜗植入体,用诺尔康检测系统软件测试植入体阻抗、输出电流幅度。
1.3.1打开诺尔康人工耳蜗植入体检测系统软件,设置参数为编码模式HR-I CS1,系统模式N-channel,调节临床值,以设置对应的理论值刺激电流,测量电极阻抗(Z)。
1.3.2用示波器采集卡在标准电阻上(1 kΩ)读出相应通道的刺激信号的电流幅度值(I),计算输出电流幅度的偏差百分比X:
Xi= ∣(I1-I2)/I1∣ × 100%
(公式1)
其中I1为照射开始之前测量植入体电极的输出电流幅度,I2为照射之后植入体电极的输出电流幅度,i=1,2,3…24 为电极通道序号。输出电流为幅度偏差的参考值,辐射剂量照射之后,测量植入体电极的输出电流,计算输出电流脉冲幅度与参考值的偏差百分比。如果输出电流与参考值的偏差百分比在±10%内(含10%和-10%),则植入体被认为功能正常。输出电流的测量和计算按照人工耳国内标准YY0989.7-2017和国际标准ISO14708-7中6.1-6.2节的要求进行。
2 结果
2.1实验前后人工耳蜗电极阻抗比较 实验前和实验完成后3个人工耳蜗植入体都能在正常条件下启动,电极阻抗测量结果均在正常范围内(表1)。
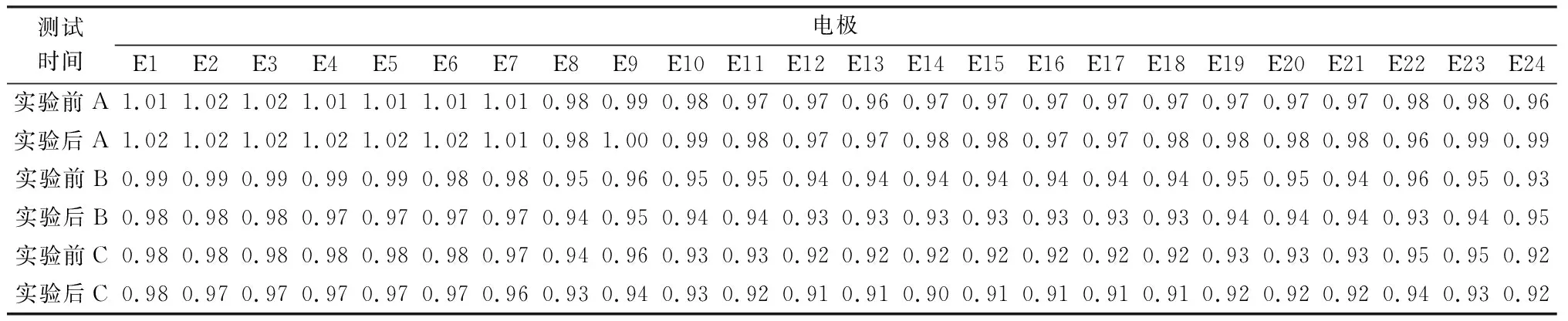
表1 模型A、B、C 3个人工耳蜗植入体实验前后各电极(MP1+2模式)阻抗值(kΩ)
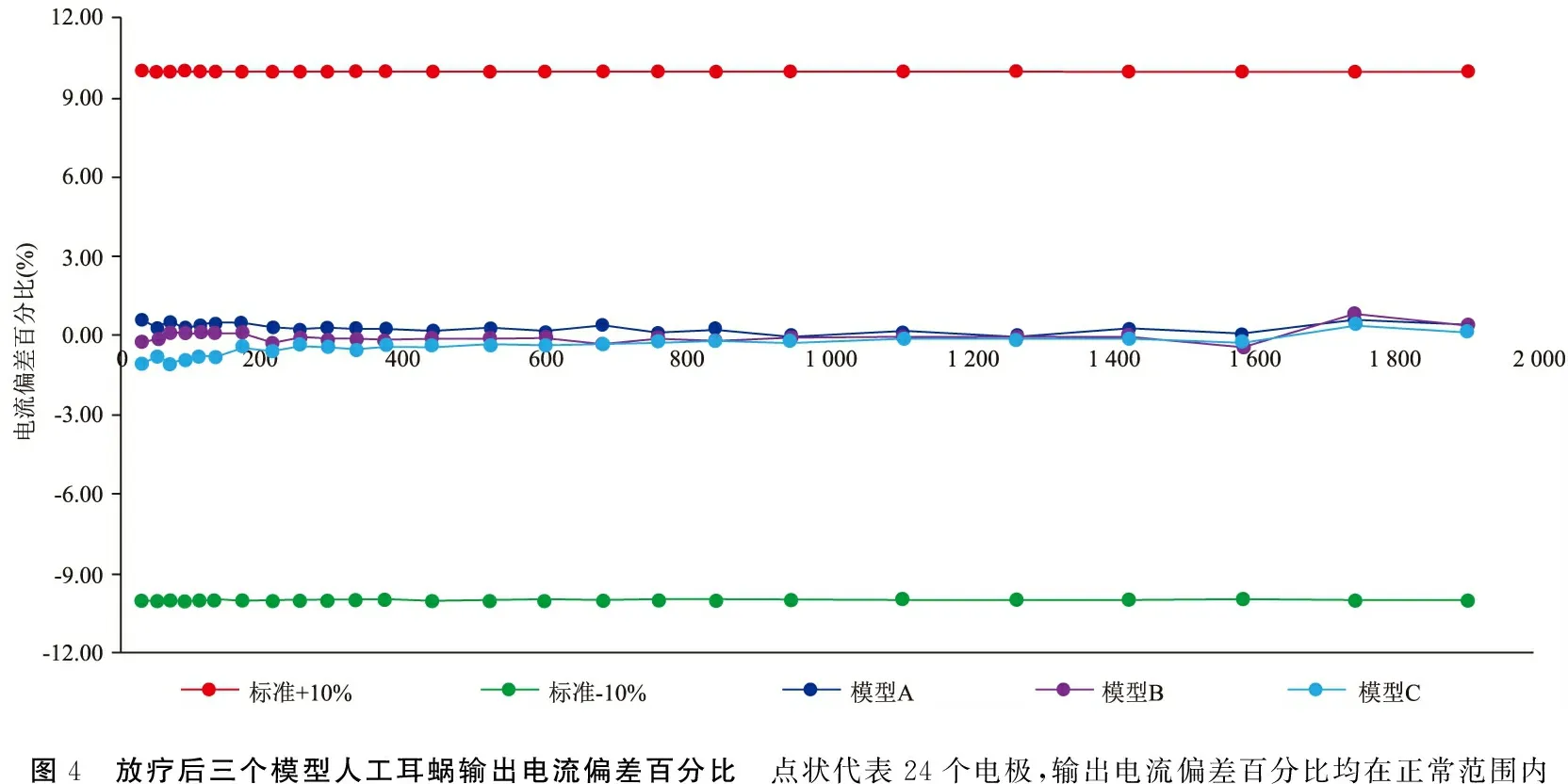
图4 放疗后三个模型人工耳蜗输出电流偏差百分比 点状代表24个电极,输出电流偏差百分比均在正常范围内
2.2实验前后人工耳蜗植入体输出电流幅度比较 完成放疗后,分别计算三个模型所有通道、刺激幅度、正负相位下的电流值与初始值的偏差,记录偏差的最大值、最小值、平均值和标准差。模型A和B完成计划剂量的放射后,与模型C比较,三者输出电流偏差百分比的绝对值均小于10%(图4,表2)。

表2 实验前后模型A、B、C人工耳蜗输出电流偏差比较(%)
3 讨论
人工耳蜗植入设备可以长期运转,术后3年植入体保存率超过99%,据估计术后11年只有2%的植入体会由于电极问题需要重新编程[4]。在人工耳蜗设备故障事件中,很少需要更换该设备,因此,预
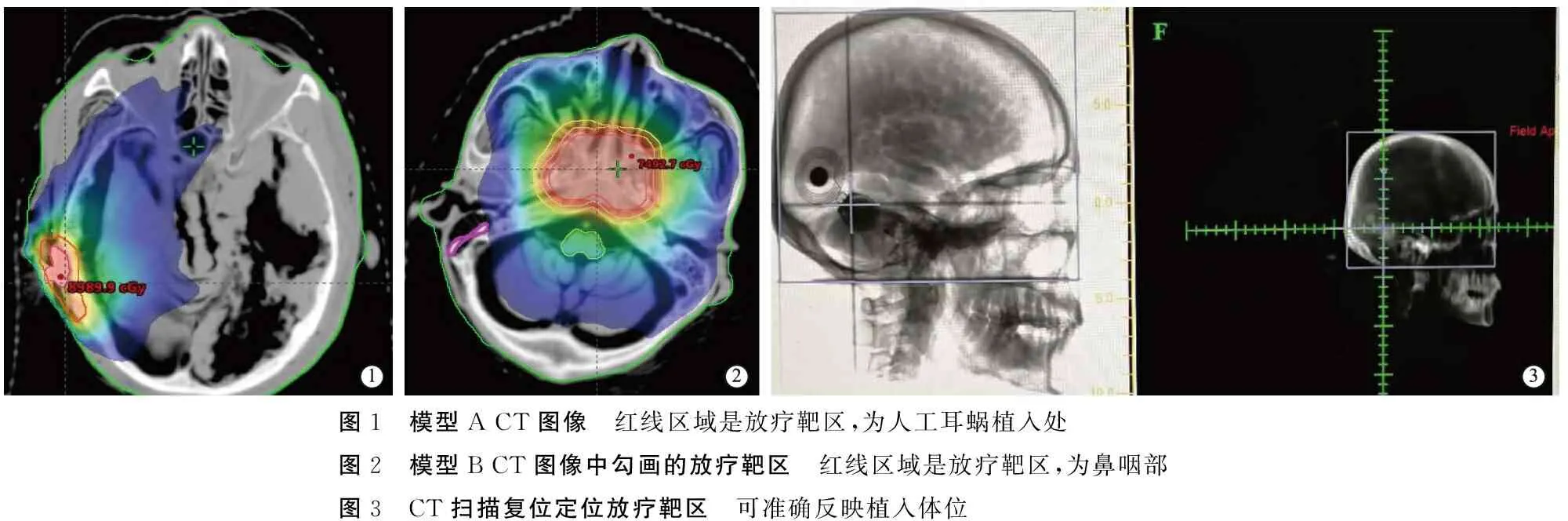
图1 模型A CT图像 红线区域是放疗靶区,为人工耳蜗植入处图2 模型B CT图像中勾画的放疗靶区 红线区域是放疗靶区,为鼻咽部图3 CT扫描复位定位放疗靶区 可准确反映植入体位
计植入体有数十年的使用期限。而现今肿瘤发病率增加,不排除人工耳蜗植入以后罹患肿瘤需要行放射治疗者。特别是广东地区鼻咽癌高发,而鼻咽癌患者预后好,生存期长,但放疗后常出现耳聋且肿瘤仍有复发可能,故此类患者人工耳蜗植入后需要放射治疗的病例将来更为常见。
鼻咽癌经调强放射治疗和/或化疗后5年生存率高,但仍有部分鼻咽癌患者出现局部、区域复发或远处转移[5],而以放疗为主的综合治疗仍是鼻咽癌复发后主要的治疗方法。值得注意的是,过度的放射剂量照射可能引起器官结构和功能的部分或全部丧失,Yilmaz等[6]统计19例头颈部肿瘤患者放射治疗后的并发症,有超过47%的患者在放疗后1年内出现了感音神经性听力损失。最近有研究认为在头颈部肿瘤的放疗过程中,即便是立体定位调强放疗,因为存在摆位误差的原因,耳蜗仍会受到不确定性的剂量照射,从而增加耳蜗受损的风险[7]。有报道对鼻咽癌放疗后出现重度感音神经性聋合并颞骨坏死的患者行颞骨次全切除术,同期植入人工耳蜗并封闭耳道,术后生活质量明显提高[8]。
人工耳蜗植入体是集成电路组成的复杂的电子装置,受到辐射后可能被损坏。目前文献检索国内没有发现电离辐射对人工耳蜗影响的相关研究报道,1995年国外文献报道[4],一例75岁的长期耳聋男性患者已植入人工耳蜗但被诊断为未知原发灶的腺癌,主要为孤立性脑转移,转诊至放射肿瘤科,全脑分12次接受了中剂量36 Gy的照射,人工耳蜗设备的内部组件包含在放疗靶区域中,放疗后患者反应良好,再生存了18个月,在此期间患者的听力仍然保持稳定,但没有对其植入体进行相关检测。之后国外有学者[9]对Cochlear公司提供的人工耳蜗植入体进行了电离辐射,并测试其功能故障和效用损失,发现放射总剂量小于80 Gy时,人工耳蜗电子元件功能正常;总剂量达106 Gy时出现输出电流幅值下降,总剂量达111 Gy时电极阻抗测不出。还有其它学者[10]针对Cochlear人工耳蜗进行研究,结果基本一致。诺尔康人工耳蜗是中国第一家规模性上市销售的人工耳蜗,越来越多的耳聋患者接受诺尔康人工耳蜗植入,截止于2017年,已有8 000多名患者植入诺尔康人工耳蜗。头颈部肿瘤术后需要行放射治疗的方案一般在常规分割( 每次1.8~2.0 Gy)的条件下,推荐GTVp和GTVln(指术后残留的原发病灶或淋巴结包膜外侵犯区域)给予66.0~70.0 Gy、CTV1(原发病灶高危亚临床区域)和CTV2(颈部淋巴结高危亚临床区域)给予60.0 Gy、CTV3(颈部淋巴结低危亚临床区域)给予50.0~55.0 Gy照射[11];而鼻咽癌无论常规分割还是超分割调强放疗方案,一般推荐每次1.2~2 Gy,总量70~80 Gy[12]。本研究模拟人体将诺尔康人工耳蜗植入体植入尸头,按目前临床上常见的鼻咽癌放疗方案对模型B进行调强放疗,模型A行延长性放疗,放疗完成后检测模型A、B的人工耳蜗电路性能均完好无损,表明人工耳蜗植入后罹患鼻咽癌的患者或鼻咽癌放疗后植入人工耳蜗复发的患者行放射治疗对人工耳蜗设备损伤小,安全性较高。
由于人工耳蜗植入体及尸头成本较高,本实验放疗例数少,但初步验证了一定剂量电离辐射对人工耳蜗植入体元件损伤较小,每次放疗剂量小于2 Gy,总剂量控制在80 Gy内,人工耳蜗植入体未见明显损坏。下一步将增加实验例数,并对人工耳蜗植入体进行直接放疗,延长观察时间,确定植入体对电离辐射的安全耐受范围和最大耐受剂量,进一步指导人工耳蜗植入者放疗方案的选择。
